5 червня, 2018
Метастатичний нирковоклітинний рак: особливості другої лінії терапії
 Одне з засідань ювілейної науково-практичної конференції «Від урології до онкоурології: досягнення та перспективи», що відбулася 19-20 квітня у м. Києві, було присвячене проблемним питанням нирковоклітинного раку (НКР). Метастатичний НКР (мНКР) характеризується поганим прогнозом, резистентність розвивається майже в усіх пацієнтів, яким призначається лікування інгібіторами тирозинкінази VEGFR, тому важливим є пошук найбільш ефективних опцій як першої, так і другої лінії терапії. Особливостям другої лінії терапії мНКР, останнім дослідженням, а також перспективним напрямам лікування пацієнтів з мНКР була присвячена доповідь кандидата медичних наук Олександра Едуардовича Стаховського (Національний інститут раку, м. Київ).
Одне з засідань ювілейної науково-практичної конференції «Від урології до онкоурології: досягнення та перспективи», що відбулася 19-20 квітня у м. Києві, було присвячене проблемним питанням нирковоклітинного раку (НКР). Метастатичний НКР (мНКР) характеризується поганим прогнозом, резистентність розвивається майже в усіх пацієнтів, яким призначається лікування інгібіторами тирозинкінази VEGFR, тому важливим є пошук найбільш ефективних опцій як першої, так і другої лінії терапії. Особливостям другої лінії терапії мНКР, останнім дослідженням, а також перспективним напрямам лікування пацієнтів з мНКР була присвячена доповідь кандидата медичних наук Олександра Едуардовича Стаховського (Національний інститут раку, м. Київ).
Як зазначив доповідач, НКР становить 2-3% усіх онкологічних захворювань. Найбільш висока захворюваність зареєстрована у країнах Східної Європи. Останніми роками спостерігається збільшення захворюваності приблизно на 2%. У 2012 р. у Європейському Союзі зафіксовано близько 84 000 нових випадків і 34 700 смертей внаслідок НКР (J. Ferlay et al., 2013).
У 2015 р. друга лінія терапії включала сунітиніб і пазопаніб у разі резистентності до імунотерапії, а також еверолімус та темсиролімус при резистентності до анти-VEGF-агентів. 2016 року відбулися істотні зміни, з’явилися нові терапевтичні опції, а саме ніволумаб, кабозантиніб та акситиніб.
Станом на 2016 р. впровадження таргетних препаратів у лікуванні НКР сприяло збільшенню медіани загальної виживаності (ЗВ) з 13-18 міс до 19-26 міс (R.J. Motzer et al., 2009), а в пацієнтів із низьким ризиком за критеріями IMDC медіана ЗВ може сягати 43,2 міс з показником 2-річної ЗВ – 75%.
Згідно з рекомендаціями Європейської асоціації урологів (EAU) від 2017 р. пацієнтам групи низького ризику за критеріями IMDC у другій лінії терапії рекомендовано призначати кабозантиніб або ніволумаб. Варто зазначити, що останній не зареєстрований в Україні. Пацієнтам групи проміжного та високого ризику за критеріями IMDC рекомендується лікування кабозантинібом, ніволумабом або анти-VEGF-терапія (T. Powles et al., 2017). Також доступними у другій лінії терапії опціями є акситиніб, еверолімус та сорафеніб.
Серед досліджень препаратів другої лінії терапії одним із вагомих було RECORD‑1, у якому відмічена перевага таргетного препарату над плацебо. У дослідженні було отримано достовірне збільшення медіани виживаності без прогресування (ВБП) на фоні терапії еверолімусом – 4,9 проти 1,9 міс.
У рандомізованому дослідженні AXIS порівнювалась ефективність акситинібу й сорафенібу в пацієнтів із гістологічно підтвердженим мНКР (світлоклітинна форма) при прогресуванні захворювання на фоні першої лінії терапії (сунітиніб, бевацизумаб в комбінації з інтерфероном-α, темсиролімус, цитокіни). На фоні терапії акситинібом показник ВБП був вищим у порівнянні з сорафенібом – 6,8 проти 4,7 міс. За більш детального аналізу після стратифікації пацієнтів майже в усіх підгрупах акситиніб також показав свою перевагу (B.I. Rini et al., 2011). За результатами досліджень AXIS і RECORD‑1 препарати акситиніб та еверолімус були включені в другу лінію терапії.
Першим схваленим препаратом у лікуванні у пацієнтів з мНКР, які раніше отримували таргетну терапію, став ніволумаб – моноклональне антитіло, дія якого спрямована проти рецептора PD‑1. Основою для схвалення ніволумабу в стандартах терапії мНКР стали результати рандомізованого дослідження ІІІ фази CheckMate 025, у якому взяв участь 821 пацієнт із метастатичним раком нирки з прогресуванням захворювання після однієї та більше ліній антиангіогенної терапії. Пацієнти були рандомізовані на 2 групи, одна з яких отримувала ніволумаб (3 мг/кг кожні 2 тижні), а друга – еверолімус (10 мг щодня).
Основним критерієм ефективності була ЗВ. Крім цього, проводили оцінку об’єктивної відповіді, ВБП і безпеки застосування препарату. Цікавим є те, що ВБП не є ключовим фактором, саме у ЗВ імунотерапія демонструє обнадійливі результати.
За результатами цього дослідження медіана тривалості життя в групі хворих, які отримували ніволумаб або еверолімус, склала 25 та 19,6 міс відповідно. Медіана ВБП у групі ніволумабу становила 4,6 міс. Частота об’єктивної відповіді (ЧОВ) була також задовільною – 21,5%, медіана тривалості відповіді – 23 міс (R.J. Motzer et al., 2015). Подальший аналіз показав, що найбільшу перевагу від застосування ніволумабу отримують пацієнти з поганим прогнозом за прогностичною шкалою Memorial Sloan Kettering Cancer Center (MSKCC), а також після терапії пазопанібом, що вказує на можливі зміни до рекомендацій (B. Escudier et al., 2017).
Сьогодні з’являється все більше доказів на користь того, що кожен препарат має певне місце в лікуванні мНКР. Одним із перших досліджень, у якому вивчали послідовність використання препаратів, було велике рандомізоване дослідження ІІ фази RECORD‑3. Його завданням було довести, що еверолімус є не менш ефективним за сунітиніб у хворих, які раніше не отримували лікування.
Медіана загальної ВБП (перша і друга лінії) склала 25,8 міс для послідовності сунітиніб–еверолімус і 21,1 міс для послідовності еверолімус–сунітиніб. Важливо зазначити, що в обох групах понад 40% пацієнтів змогли отримати другу лінію терапії. Медіана ЗВ склала 32 міс у групі сунітиніб–еверолімус і 22,4 міс у групі еверолімус–сунітиніб. Таким чином, еверолімус не виявив переваг у першій лінії терапії в порівнянні з сунітинібом. Це дослідження показало необхідність використання сунітинібу в першій лінії, а еверолімусу – у другій лінії.
Новою перспективною терапевтичною опцією в Україні є таргетний препарат кабозантиніб. Мішенями кабозантинібу є MET, AXL, VEGFR‑1, -2 та -3, які залучені у патофізіологію НКР, а також пов’язані з розвитком резистентності. У більшості випадків при НКР вміст білка von Hippel-Lindau у клітинах знижений, що призводить до збільшення рівнів MET, AXL та VEGF. Перекриваючи не тільки шлях VEGF, кабозантиніб може чинити багатоцільовий вплив на ниркову пухлину.
Кабозантиніб має унікальний механізм дії, що дозволяє подолати резистентність до інгібіторів тирозинкінази рецептора VEGF. Як показали результати дослідження ІІІ фази METEOR, кабозантиніб збільшує ЗВ, ЧОВ, ВБП у пацієнтів із НКР. У дослідженні взяли участь 658 пацієнтів із поширеним НКР, у яких попередня терапія інгібіторами тирозинкінази була неефективною. У рамках дослідження оцінювалася первинна кінцева точка – ВБП – у перших 375 рандомізованих пацієнтів. Вторинні кінцеві точки включали ЗВ і ЧОВ.
Пацієнти були рандомізовані у співвідношенні 1:1. У першій групі пацієнти отримували кабозантиніб (60 мг × 1 р/д), у другій – еверолімус (10 мг × 1 р/д). Пацієнти були стратифіковані залежно від кількості ліній терапії інгібіторами тирозинкінази рецептора VEGF, а також відповідно до критеріїв ризику MSKCC.
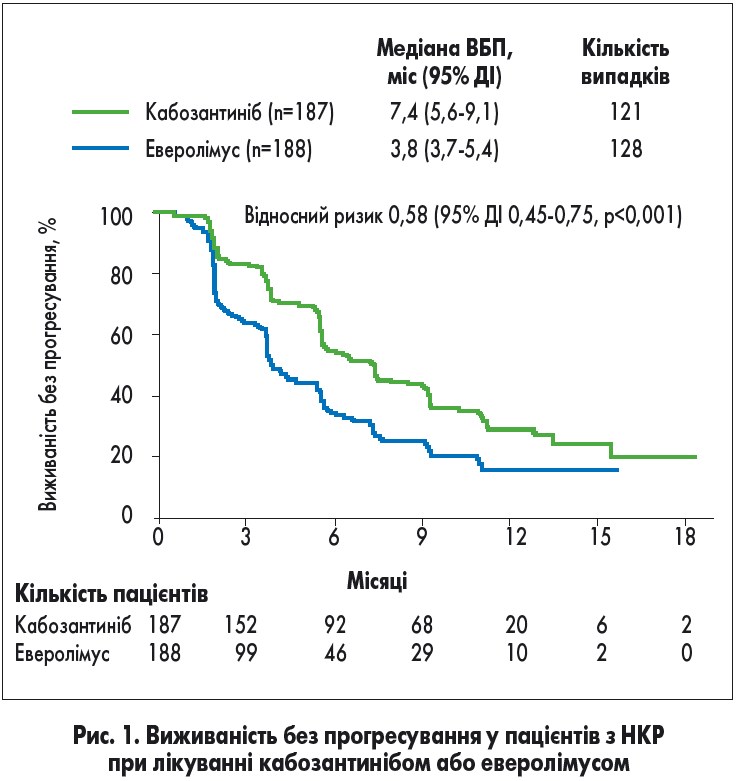
Лікування кабозантинібом було асоційоване з 42% зменшенням частоти прогресування або смерті порівнянно з еверолімусом. Медіана ВБП склала 7,4 і 3,8 міс для кабозантинібу та еверолімусу відповідно (рис. 1). Кабозантиніб також сприяв збільшенню ЧОВ при незалежній оцінці (17 проти 3%).
У ході дослідження кабозантиніб показав статистично значиме збільшення ЗВ: медіана ЗВ склала 21,4 і 16,5 міс для кабозантинібу та еверолімусу відповідно (рис. 2). На момент проведення аналізу середня тривалість терапії становила 8,3 і 4,4 міс для кабозантинібу та еверолімусу відповідно. У зв’язку з розвитком небажаних явищ лікування припинили 12 і 11% пацієнтів у групі кабозантинібу та еверолімусу відповідно. У ході стратифікації за видом попередньої терапії (сунітиніб, пазопаніб або анти-PD‑1/PD-L1-агенти) кабозантиніб продемонстрував перевагу незалежно від отримуваної раніше терапії (T. Powles et al., 2016; T.K. Choueri et al., 2016).
Постійні зміни у стандартах лікування підтверджують активну роботу в напрямку подолання резистентності до таргетних препаратів. Резистентність розвивається майже в усіх пацієнтів, які лікуються інгібіторами тирозинкінази VEGFR у першій лінії. Кабозантиніб, мішенями якого є MET, AXL, VEGFR‑1, -2 та -3, має унікальній механізм дії, що дозволяє подолати резистентність до інгібіторів тирозинкінази рецептора VEGF. Подальші дослідження щодо подолання резистентності, а також розробка нових терапевтичних опцій дозволять покращити клінічні результати пацієнтів із мНКР.
Підготувала Катерина Марушко
Тематичний номер «Онкологія» № 2 (53), травень 2018 р.