19 червня, 2018
Мометазону фуроат у щоденній клінічній практиці: ефективність та безпека сучасної терапії алергічного риніту
Алергічний риніт (АР) є найбільш поширеним алергічним захворюванням у світі, яке значно погіршує якість життя пацієнтів. Патогенетичну основу АР становить специфічне алергічне запалення, тому основним завданням терапії є досягнення 24-годинного контролю над симптомами за допомогою сучасних препаратів, які ефективно впливають на всі ланки запального процесу, не знижуючи при цьому прихильність пацієнтів до лікування.
Визначення та актуальність проблеми
АР є [імуноглобулін Е] IgE-зумовленим запальним захворюванням слизової оболонки носа, яке викликане дією сенсибілізуючого (патогенетично значущого) алергену і проявляється чханням, зудом, ринореєю та/або закладеністю носа (Akdis C.A., Agache I. Global atlas of allergic rhinitis and chronic rhinosinusitis. EAACI; 2017).
Актуальність проблеми АР визначається його широким розповсюдженням, яке має тенденцію до постійного зростання, особливо серед дітей та підлітків. У свій час результати дослідження, проведеного відповідно до протоколу Глобальної мережі з алергії та астми в Європі (Global Allergy and Asthma European Network, GA2LEN), показали, що поширеність АР серед підлітків 15-18 років становила 34,2% (Bousquet J. et al., 2008). За даними Міжнародного дослідження бронхіальної астми та алергії у дитячому віці (International Study of Asthma and Allergy in Childhood, ISAAC), АР спостерігається в середньому у 8,5% (1,8-20,4%) випадків у дітей віком 6-7 років і в 14% (1,4-33,3%) – у підлітків 13-14 років (Ait-Khaled N. et al., 2009). Сьогодні у світі від АР страждають до 30% населення (Akdis C.A., Agache I. Global atlas of allergic rhinitis and chronic rhinosinusitis. EAACI; 2017). Загалом дані щодо захворюваності на АР, засновані на зверненнях пацієнтів, не відображають реальної поширеності цієї патології, оскільки не враховують великої кількості осіб, котрі не звертаються за медичною допомогою, та хворих, в яких АР не було своєчасно і правильно діагностовано.
АР може виникати в будь-якому віці, навіть у дітей до 3 років, але в більшості пацієнтів симптоми розвиваються із досягненням 20-річного віку. Це захворювання являє собою неабияку медико-соціальну проблему не тільки в сенсі вартості медикаментозного лікування, але й через зниження щоденної активності пацієнтів, яких турбують, окрім назальних, і загальні симптоми: головний біль, втомлюваність, порушення сну, низька здатність до навчання та праці. Окрім того, хворі на АР часто мають супутню патологію: кон’юнктивіт, синусит і середній отит внаслідок анатомічних і функціональних зв’язків з очами, приносовими пазухами, середнім вухом, верхніми та нижніми дихальними шляхами тощо. При цьому додаткові симптоми розвиваються, у тому числі, внаслідок великої кількості назального секрету, порушення прохідності слухових труб та дренування приносових пазух.
Слід також зазначити, що останнім часом особливу увагу клініцистів привертає локальний АР (ЛАР), який характеризується типовими симптомами та даними анамнезу поряд із від’ємними результатами шкірних проб і відсутністю специфічних IgE у сироватці крові.
Патогенетичну основу ЛАР становить місцева (у слизовій облонці носа) гіперпродукція IgE-антитіл до значущих алергенів (сезонних або цілорічних), що призводить до розвитку локального алергічного запалення та типових клінічних проявів АР (Rondon C. et al., 2012; Papadopulos M.G. et al., 2015).
АР часто асоціюється із бронхіальною астмою (БА), яка виявляється у 15-38% пацієнтів; назальні симптоми турбують 6-85% хворих на БА; неконтрольований і тяжкий перебіг АР негативно впливає на контроль БА (Brozek J.L. et al., 2017). При цьому щорічні непрямі витрати на лікування АР, пов’язані із втратою працездатності, є вищими за ті, що виникають при БА (Haahtela T. et al., 2015; Yoi K.H. et al., 2016). Зв’язок між АР та БА підтримується низкою патофізіологічних механізмів. Обидва захворювання характеризуються ранньою та пізньою фазами запальної реакції, при яких у процес залучаються однакові ефекторні клітини із вивільненням ідентичних медіаторів запалення (прозапальні цитокіни, гістамін, протеази тощо). Медіатори впливають на клітини ендотелію судин і нейрорецептори слизової оболонки носа, внаслідок чого розвиваються клінічні симптоми АР. На тлі запалення слизової оболонки носа назальні симптоми можуть персистувати впродовж декількох годин після контакту з патогенетично значущим алергеном. При цьому розвивається так званий «ефект праймінгу», коли сама слизова оболонка стає більш реактивною по відношенню до інших алергенів та неалергічних тригерів (різкий запах, холодне повітря та ін.).
Сучасна класифікація АР базується на тяжкості та тривалості симптомів. За останньою ознакою виділяють персистуючий (≥4 тиж на рік або ≥4 дні на тиждень) та інтермітуючий (менша тривалість симптомів) АР. За ступенем тяжкості зберігається класифікація на тяжкий, середньотяжкий (за наявністю хоча б однієї з ознак: порушення сну, щоденної активності, обмеження занять спортом, важкість у досягненні контролю) та легкий АР. За стадією перебігу захворювання розрізняють загострення та ремісію АР.
Поділ АР на сезонний та цілорічний здебільшого відображає не тривалість симптомів, а спектр сенсибілізації. Незважаючи на те що такий поділ понад 15 років не застосовується в клінічній практиці, він дозволяє спеціалістам інтерпретувати деякі дані, що публікуються в науковій літературі (Brozek J.L. et al., 2017).
З огляду на вищенаведені факти можна зробити висновок, що навіть при легкому перебігу АР не може розглядатися як захворювання, яке не обтяжує пацієнта і його оточення. Відповідно, адекватна терапія АР покращує не тільки назальні симптоми, але й контроль над супутніми захворюваннями, працездатність та успішність у навчанні.
Менеджмент АР
Настанови та рекомендації щодо менеджменту АР, які постійно оновлюються впродовж останніх 20 років, мають на меті покращення клінічних результатів та якості життя пацієнтів (Padjas A. et al., 2014). Ефективними є заходи, що включають у себе мінімізацію або припинення контакту з алергенами, фармакотерапію, специфічну імунотерапію, навчання пацієнтів. Оскільки елімінація алергенів або повне припинення контакту з ними за реальних умов є практично неможливими, на перший план виступає фармакотерапія АР.
В оновлених консенсусах EAACI (European Academy of Allergy and Clinical Immunology), AAACI (American Academy of Allergy and Clinical Immunology), PRACTALL (Practical Allergology Pediatric Asthma Group), ARIA (Allergic Rhinitis and its Impact on Asthma) прийнято покроковий підхід до лікування АР, подібний до терапевтичної тактики при БА і заснований на досягненні контролю над алергічним запаленням. Критеріями контролю є відсутність назальних симптомів, порушень сну та щоденної активності, а також об’єктивні дані: нормалізація показників назальної пікової швидкості вдиху, тесту «дихання із закритим ротом» і тестів оцінки нормальної назальної прохідності.
Фармакотерапія: місце інтраназальних кортикостероїдів (ІКС) у лікуванні АР
У покроковій фармакотерапії АР варіанти лікування залежать від тяжкості та тривалості його симптомів (Papadopulos M.G. et al., 2015).
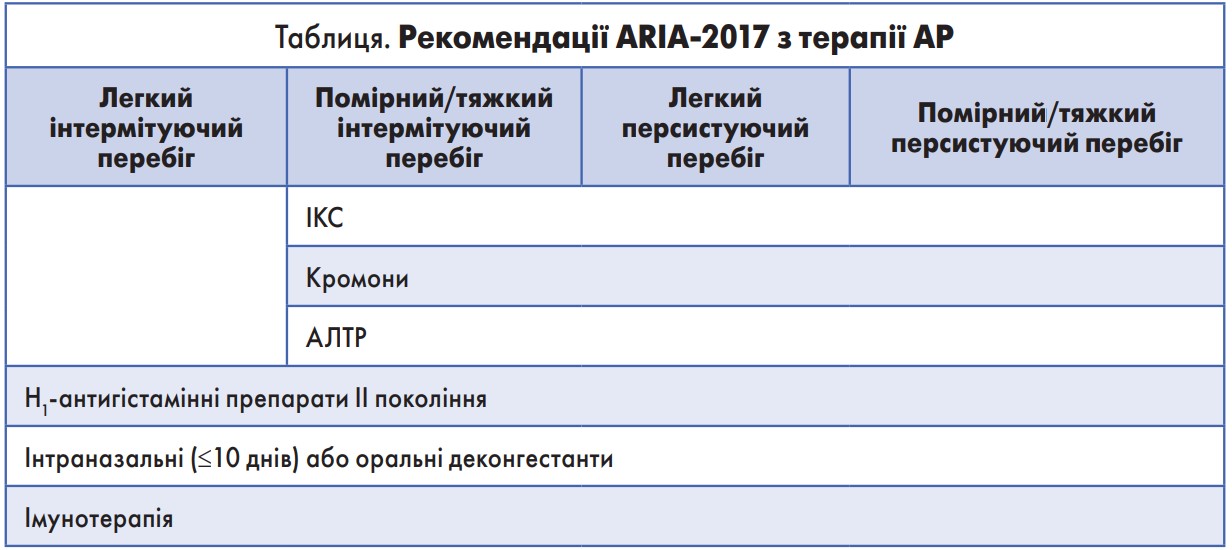
Разом із тим першочерговою метою фармакотерапії є ефективний контроль алергічного запалення слизової оболонки носа та запобігання ускладненням захворювання. Фармакологічні варіанти покрокової терапії АР представлено в таблиці.
Для пацієнтів із сезонним та цілорічним АР у загальні рекомендації ARIA‑2017 було внесено наступні зміни:
- перевага терапії ІКС перед уведенням інтраназального блокатора Н1-гістамінових рецепторів;
- рекомендовано комбінацію ІКС / інтраназальний блокатор Н1-гістамінових рецепторів;
- рекомендовано введення або інтраназального, або перорального блокатора Н1-гістамінових рецепторів.
У чинних міжнародних рекомендаціях підкреслюється, що ІКС є основою протизапальної терапії АР. Метааналізи, проведені в різні роки J.M. Weiner і співавт. (1998) та A.M. Wilson і співавт. (2004), продемонстрували, що ІКС є ефективнішими за пероральні антигістамінні препарати або антагоністи лейкотрієнових рецепторів (АГП або АЛТР) у разі монотерапії АР (рівень доказовості ІА). Окрім того, на відміну від інших методів лікування ІКС зменшують закладеність носа. Відповідно, ІКС використовуються як препарати першої лінії в пацієнтів з помірними та тяжкими проявами АР, а також із скаргою на закладеність носа. Тривалість дії цих препаратів становить від 3 до 36 год після інгаляції першої дози, при цьому постійне використання є більш ефективним, аніж періодичне (Blair Sarbacker G., 2016).
Свого часу J. Zhou і співавт. (2008) довели вплив глюкокортикостероїдів (ГКС) на усі ланки патогенезу при алергічному запаленні.
Ліпофільні молекули ГКС легко проникають крізь клітинну мембрану у цитоплазму, зв’язуються з ГКС-рецепторами і потрапляють у ядро, утворюючи гомодимери. Ті, у свою чергу, з’єднуються із специфічними послідовностями ДНК-стероїдчутливими елементами, розташованими в ділянці промотора генів білків, котрі пригнічують активність прозапальних факторів транскрипції. У результаті знижується експресія генів, що кодують синтез цитокінів, хемокінів, та рецепторних білків, причетних до патогенезу алергічного запалення. При цьому знижується чутливість слизової оболонки носа до гістаміну та механічних подразників. Таким чином, ГКС проявляють протиалергійний, протинабряковий і протизапальний ефекти.
ІКС відрізняються від системних ГКС більшою ліпофільністю, низькою біодоступністю, швидкою інактивацією, коротким періодом напіввиведення з плазми крові. Сучасні молекули ІКС характеризуються мінімальною (0,1-8%) абсорбцією із шлунково-кишкового тракту і майже повною (понад 90%) біотрансформацією до неактивних метаболітів при першому проходженні крізь печінку. Ці особливості фармакокінетики ІКС дозволяють тривало використовувати їх без ризику розвитку системних ефектів.
Ефективність і безпека застосування ІКС: мометазону фуроат
У рутинній клінічній практиці перевага віддається тим ІКС, які мають оптимальне співідношення «ефективність – безпека» й сприятливі фармакоекономічні аспекти (Bielory B. et al., 2014). Одним із таких препаратів є мометазону фуроат, що являє собою високоактивний 1,7-гетероциклічний ГКС місцевої дії.
Препарат є одним з найбільш вивчених ІКС, що застосовуються для терапії АР; у міжнародній медичній літературі опубліковано 256 науково-дослідних робіт, які доводять високу клінічну ефективність та безпеку мометазону фуроату – інтраназального спрею із рівнем доказовості ІА (Penagos M. et al., 2008; Baldwin C.M. et al., 2008). Мометазону фуроат внесено до переліку ІКС, рекомендованих для терапії АР як міжнародними, так і адаптованими вітчизняними клінічними документами, а також до оновленого відповідно до наказу МОЗ України від 26.04.2018 р. № 803 переліку лікарських засобів, що пройшли державну реєстрацію.
Клінічні ефекти мометазону фуроату забезпечуються його сприятливими фармакологічними властивостями. Раніше B.J. Lipworth і співавт. (2000) встановили, що ступінь біотрансформації мометазону фуроату при першому пасажі крізь печінку становить 99%. А мінімальна системна біодоступність забезпечується високою ліпофільністю і афінністю до ГКС-рецепторів. Це спричиняє потужну протизапальну й протиалергійну дію препарату, зумовлену пригніченням синтезу прозапальних цитокінів і продуктів метаболізму арахідонової кислоти (Samolinski B. et al., 2014). Як результат – гальмується міграція макрофагів, еозинофілів і нейтрофілів у вогнище запалення, зменшуються інфільтрація, набряк і грануляція слизової оболонки носа, пригнічуються рання та пізня фази алергічної реакції.
Найбільша серед ІКС кінцева в’язкість мометазону фуроату забезпечує його тривалу експозицію у вогнищі запалення; препарат не стікає по задній стінці глотки і не витікає з носа. Тому застосування мометазону фуроату 1 раз на добу дозволяє контролювати усі симптоми АР протягом 24 годин. Інтраназальний спрей мометазону фуроату починає діяти вже протягом 12 год після прийому першої дози із досягненням максимального ефекту на 2-гу добу.
Значною перевагою мометазону фуроату є доведена ефективність застосування при отоларингологічних ускладненнях АР (Cengel S. і співавт., 2006; European position paper on rhinosinusitis and nasal polyps, 2012). Інтраназальний спрей мометазону фуроату є ефективним у лікуванні не тільки АР, але й неалергічного риніту, гіпертрофії аденоїдів і неускладненого риносинуситу.
Щодо можливих місцевих небажаних ефектів, які можуть супроводжувати тривале застосування ІКС, проведені у різні роки дослідження продемонстрували сприятливий вплив інтраназального флютиказону фуроату на слизову оболонку носа. Так, H. Aksoy і співавт. (2011) та D. Passali і співавт. (2016) встановили, що мометазону фуроат не пригнічує назальну та назофарингеальну флору, не знижує мукоциліарну здатність епітелію слизової оболонки носа і не викликає його атрофію.
Терапія АР у дітей базується на тих самих принципах, що й у дорослих, проте клініцисти завжди враховують вік та потреби пацієнтів, сприйняття терапії не тільки дітьми, але й їхніми батьками, особливо щодо побоювань розвитку небажаних ефектів ІКС. Через те що системна абсорбція мометазону фуроату є незначною, йому віддають перевагу при застосуванні у педіатричній практиці (Derendorf H. et al., 2008). На сьогодні препарат вважається найбільш безпечним з ІКС (Papadopulos M.G. et al., 2015; Petersen T.H., 2016).
Підтверджено, що мометазону фуроат не впливає на ріст, не змінює добовий рівень кортизолу плазми та не призводить до підвищення внутрішньоочного тиску в дітей навіть у разі тривалого застосування.
В Україні інтраназальний мометазону фуроат представлений новим препаратом Саномен («Sandoz») у формі назального спрею в контейнерах по 60, 120 та 140 доз. Препарат застосовується для терапії АР у дітей віком від 3 років та дорослих.
Оптимальне дозування (50 мкг/доза) дозволяє використовувати Саномен 1 раз на добу, а зручність застосування та сприятливі фармакоекономічні аспекти додатково підвищують прихильність пацієнтів до терапії.
Підготувала Наталія Позднякова
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (43), травень 2018 р.