22 червня, 2018
Биластин при длительном лечении аллергического ринита и крапивницы: сочетание эффективности и безопасности
17-19 апреля в Днепре состоялся III Национальный конгресс по иммунологии, аллергологии и иммунореабилитации. Он был приурочен к 50-летию организации в Днепропетровской области специализированной аллергологической службы. В форуме принимали участие ведущие отечественные эксперты и их зарубежные коллеги; в рамках программы мероприятия были озвучены данные выполненных научных исследований, проведены мастер-классы, сделаны разборы клинических случаев, а также представлены международные рекомендации по лечению наиболее распространенных аллергических заболеваний (АЗ), в частности крапивницы и аллергического ринита (АР).
Учитывая, что частота случаев АЗ во всем мире за последние десятилетия увеличилась в среднем в 2 раза и продолжает расти, проблема диагностики и лечения АЗ по-прежнему остается актуальной. Именно своевременное установление диагноза и аспекты правильного лечения стали темой многих интересных выступлений. С некоторыми из них мы хотим познакомить наших читателей.
 Лечению аллергического риноконъюнктивита и выбору оптимального антигистаминного препарата был посвящен доклад заместителя руководителя Центра аллергических заболеваний верхних дыхательных путей и уха ГУ «Институт отоларингологии им. А. И. Коломийченко НАМН Украины» (г. Киев), доктора медицинских наук Инны Владимировны Гогунской.
Лечению аллергического риноконъюнктивита и выбору оптимального антигистаминного препарата был посвящен доклад заместителя руководителя Центра аллергических заболеваний верхних дыхательных путей и уха ГУ «Институт отоларингологии им. А. И. Коломийченко НАМН Украины» (г. Киев), доктора медицинских наук Инны Владимировны Гогунской.
– Частота АР достигает 30% в мировой популяции, и первая линия терапии этого состояния, а также крапивницы, пищевой и лекарственной аллергии – это антигистаминные препараты (АГП) 1-го и 2-го поколения. Особенностью 1-го (старого) поколения АГП является их способность свободно проникать через гематоэнцефалический барьер (ГЭБ), заполняя Н1-рецепторы, расположенные на постсинаптических мембранах гистаминергических нейронов по всей центральной нервной системе (ЦНС), что и обусловливает высокую частоту побочных эффектов.
Нежелательные явления Н1-АГП 1-го поколения, связанные с влиянием на различные рецепторы
- Н1-гистаминовые в ЦНС: снижение внимания, познавательной способности, обучения, памяти и психомоторных функций; повышение частоты нарушений с/без седации.
- Мускариновые: сухость во рту, задержка мочи, синусовая тахикардия.
- Серотониновые: повышение аппетита и прибавка массы тела.
- α-Адренорецепторы: головокружение и постуральная гипотензия.
- Ионные каналы в сердце: удлинение интервала QT, появление или повышение частоты желудочковых аритмий.
Но, несмотря на указанные нежелательные явления, Н1-АГП 1-го поколения продолжают широко применяться. А ведь пациенты с АЗ, как правило, нуждаются в длительной терапии, поэтому им необходимо обеспечить не только эффективное, но и безопасное лечение, которое не будет ухудшать качество их жизни. С этой точки зрения, Н1-АГП 2-го (нового) поколения являются наиболее предпочтительными и рекомендуемыми. Они не могут свободно проникать через ГЭБ и характеризуются низкой частотой побочных эффектов. Тем не менее не все препараты 2-го поколения имеют сопоставимую проницаемость, и это нужно учитывать.
Показания к назначению АГП с сильной доказательной базой: АР, аллергический конъюнктивит и крапивница. Все остальные состояния, для лечения которых часто применяются АГП, имеют слабую доказательную базу.
С учетом длительного течения АЗ и необходимости продолжительного лечения препараты для терапии этих состояний должны соответствовать неким оптимальным исходным данным:
- Фармакологические свойства: мощный и селективный блокатор Н1-рецепторов с дополнительным антиаллергическим действием; отсутствие токсических эффектов и взаимодействия с цитохромом Р4503А, пищей, транспортными белками кишечника, лекарствами.
- Эффективность: в отношении интермиттирующего и персистирующего АР, а также всех назальных симптомов (включая обструкцию); ослабление глазных аллергических симптомов; наличие исследований эффективности и безопасности у детей, беременных и больных преклонного возраста.
- Отсутствие побочных эффектов: седативного действия, нарушения когнитивных или психомоторных функций, антихолинергических и кардиотоксических эффектов, прибавки веса.
- Фармакодинамика: быстрое начало действия с быстрым клиническим эффектом, продолжительное действие (не менее 24 ч) с возможностью однократного приема в день, маловероятное развитие тахифилаксии (привыкания).
Сегодня самым новым АГП является биластин. Это АГП 2-го поколения, используемый в клинической практике под торговым названием Никсар®. Его действие начинается спустя 1,3 ч после приема и продолжается более 24 часов. Он обладает самой высокой среди всех АГП способностью к оккупации гистаминовых рецепторов. Является наиболее рекомендуемым препаратом во всех руководствах по лечению АЗ.
Следует отметить, что у 52% пациентов с АР отмечаются глазные симптомы, негативно влияющие на дневную активность и снижающие качество жизни. Однако не все АГП показаны для лечения аллергического риноконъюнктивита. Могут быть использованы только биластин и, частично, цетиризин. При этом эффективность биластина значительно выше в устранении таких симптомов, как зуд, слезотечение и покраснение кожи.
Согласно исследованию, проведенному К. Okubo и соавт., длительный (52 нед) прием биластина показал безопасность, хорошую переносимость и эффективность препарата у пациентов с сезонным и круглогодичным АР (САР и КАР). Наблюдаемое улучшение в отношении как глазных, так и назальных симптомов поддерживалось на протяжении всего исследования без потери эффективности. Более того, чем дольше длился курс приема, тем более успешным было лечение.
Никсар® – современный эффективный и безопасный препарат. Такими были вывод и рекомендации консенсус-группы по вопросам АГП нового поколения CONGA (Consensus Group on New-Generation Antihistamines), созданной при поддержке Британского общества аллергологии и клинической иммунологии (BSACI). Ими были определены три «предварительных условия» в качестве основных составляющих для нового класса АГП: отсутствие кардиотоксичности, лекарственных взаимодействий и побочных эффектов со стороны ЦНС.
Критерии исследований CONGA и их результаты
CONGA 1: частота случаев субъективной сонливости. По данным двойного слепого исследования, частота случаев субъективной сонливости на фоне лечения биластином не отличалась от таковой при приеме плацебо. Вывод: биластин не приводит к появлению случаев субъективной сонливости.
CONGA 2: объективные когнитивные и психомоторные функции. При сравнении плацебо, гидроксизина и биластина в дозах 20 мг, 40 мг и 80 мг соответственно было показано, что объективные когнитивные и психомоторные функции даже на фоне приема высоких доз биластина не отличаются от таковых при применении плацебо.
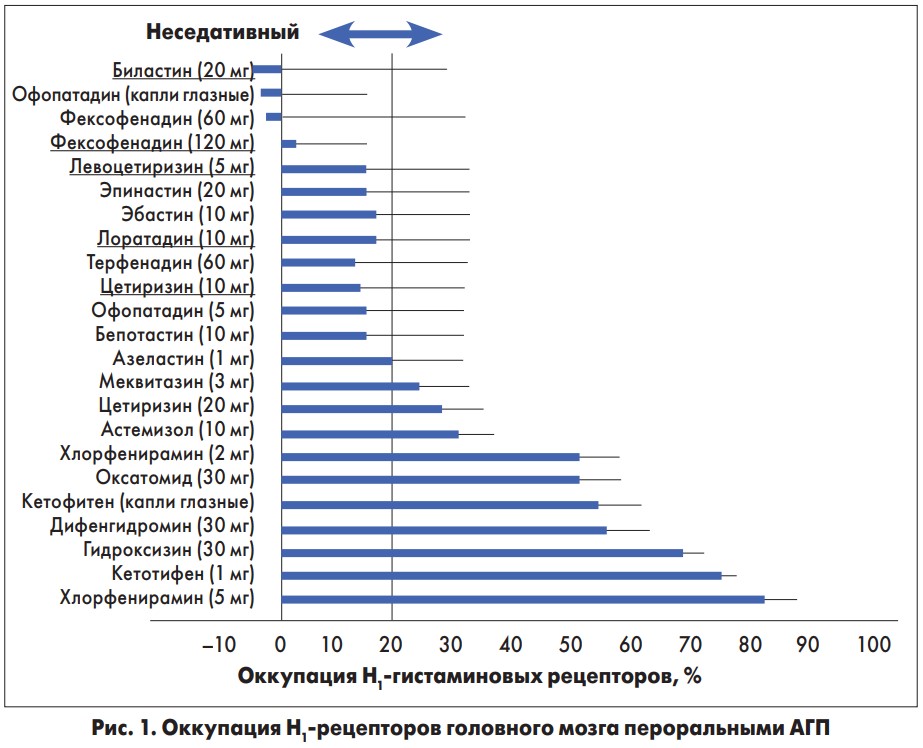
CONGA 3: оценка оккупации Н1-рецепторов в головном мозге при помощи позитронно-эмиссионной томографии (ПЭТ), поскольку именно этот фактор является ключевым в развитии побочных эффектов со стороны ЦНС.
Биластин – субстрат гликопротеина-Р, который может снижать его способность к проникновению через ГЭБ и связываться с Н1-гистаминовыми рецепторами в ЦНС. Проведенное двойное слепое перекрестное исследование с ПЭТ показало, что не было отмечено разницы в оккупации Н1-рецепторов ЦНС между группами биластина и плацебо. В данном исследовании было продемонстрировано, что Никсар® в дозе 20 мг абсолютно не оккупирует Н1-рецепторы головного мозга по сравнению с АГП 1-го поколения, где доля связанных рецепторов достигала 80% (рис. 1).
Кроме этого применение биластина в дозах 20 мг и 100 мг не оказывало клинически важного влияния на интервал QTc. Не было также обнаружено его взаимодействия с лоразепамом и алкоголем – в дозе 20 мг биластин не потенцировал их седативного воздействия на ЦНС при одновременном приеме.
Также было оценено влияние биластина 20 мг на когнитивную функцию пилотов в течение 6-часового полета на высоте 8 тыс. футов; это дало основания сделать вывод, что препарат не вызывает сонливости или нарушения производительности при выполнении задач, связанных с управлением самолетом. А следовательно, Никсар® может стать безопасной альтернативой для пилотов, страдающих АР или крапивницей. Полученные результаты могут быть применены к лечению АР у персонала, работающего на небезопасном производстве.
По мнению экспертов ARIA (Allergic Rhinitis and its Impact on Asthma/Аллергический ринит и его влияние на астму), благодаря фармакологическим особенностям и фармакодинамическим свойствам, эффективности и безопасности биластин отвечает критериям, рекомендованным [Европейской академией аллергологии и клинической иммунологии] EAACI/ ARIA в отношении лекарственных средств, применяемых для лечения АР.
 Руководитель Киевского городского аллергоцентра, доктор медицинских наук, профессор Лилия Ивановна Романюк представила в своем докладе опубликованные в прошлом году новые международные рекомендации по диагностике и лечению крапивницы.
Руководитель Киевского городского аллергоцентра, доктор медицинских наук, профессор Лилия Ивановна Романюк представила в своем докладе опубликованные в прошлом году новые международные рекомендации по диагностике и лечению крапивницы.
– В 2017 году были разработаны рекомендации по определению, классификации, диагностике и лечению крапивницы. В консенсусе приняли участие EAACI, Европейское сообщество по аллергии и астме, Европейский дерматологический форум и Всемирная организация по аллергии. Разработка этих рекомендаций была крайне необходима, потому что частота хронической крапивницы (ХК) продолжает стремительно расти, сталкиваются с ней врачи разных специальностей, а лечение при этом не всегда бывает эффективным. При этом влияние ХК на жизнь пациента оказывается значительно шире и тяжелее внешних проявлений на коже. Это тревожные и депрессивные состояния, проблемы со сном, снижение качества жизни и работоспособности.
С учетом новых рекомендаций классификация крапивницы основана на ее продолжительности и релевантности провоцирующих факторов, поскольку спектр клинических проявлений очень широк, а у одного и того же пациента может наблюдаться сочетание двух и более подтипов. Итак, крапивница бывает (в зависимости от продолжительности и наличия провоцирующего фактора):
- острой – продолжительность ≤6 недель;
- хронической – >6 недель;
- спонтанной – провоцирующий фактор не определен;
- индуцированной – провоцирующий фактор определен (холод, тепло, механическое или химическое воздействие и т. д.).
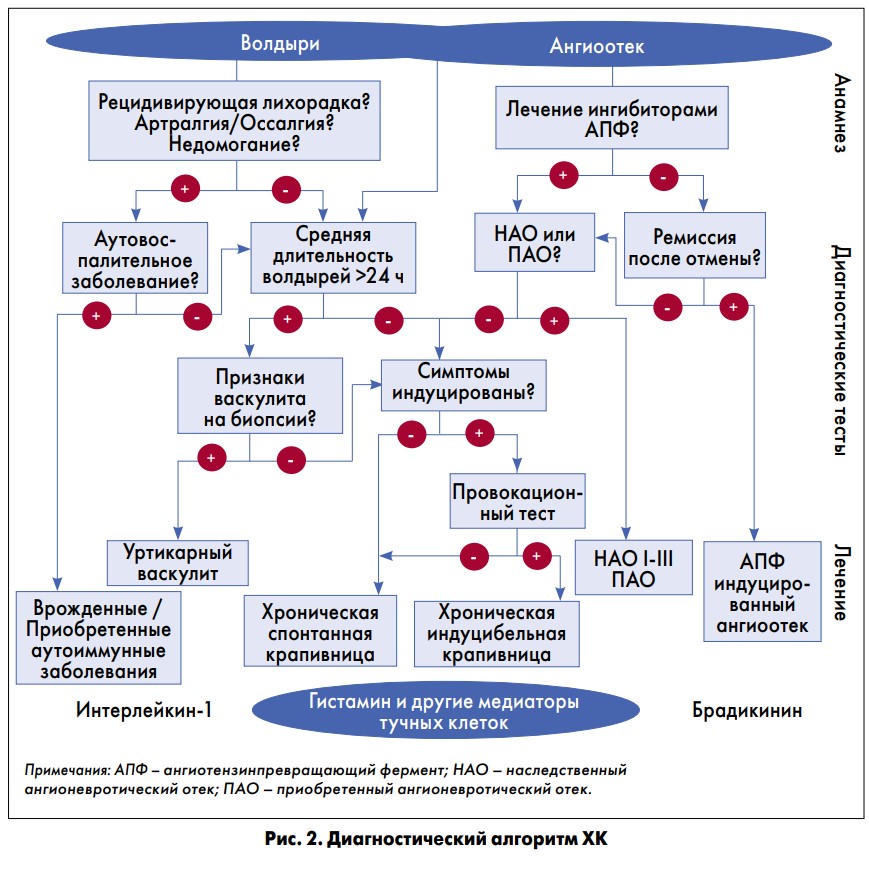
Диагностический алгоритм ХК построен на принципиальных отличиях между волдырями и ангиоотеком (рис. 2).
Для определения активности спонтанной ХК используется индекс активности крапивницы (urticarial activity score 7 – UAS7).
В течение недели проводится ежедневная балльная оценка волдырей и зуда (их наличие и выраженность), после чего баллы суммируют.
Базовые принципы ведения пациентов с ХК
- Лечить болезнь до полного исчезновения симптомов.
- Выявить и устранить причины; избегать провоцирующих факторов; индуцировать толерантность и/или предотвратить высвобождение и влияние медиаторов тучных клеток.
- Лечение должно длиться ровно столько, сколько необходимо до полного выздоровления пациента, но по возможности как можно меньше.
Алгоритм лечения ХК
Рекомендации по лечению крапивницы более чем в 90% консенсусов имеют лишь незначительные отличия.
- Первая линия терапии – Н1-АГП 2-го поколения.
- У пациентов без ответа на однократную дозу Н1-АГП 2-го поколения ее можно увеличить вплоть до 4-кратного уровня.
- При отсутствии ответа на увеличенную дозу Н1-АГП 2-го поколения рекомендуется добавить омализумаб (3-я линия терапии). Препарат эффективен и безопасен. Рекомендуемая доза – 300 мг каждые 4 недели.
- К 3-й линии терапии относится добавление циклоспорина А к Н1-АГП 2-го поколения в случае рефрактерности к высоким дозам АГП и омализумабу. Препарат эффективен, но из-за побочных эффектов должен применяться только в тяжелых, рецидивирующих случаях ХК. Рекомендуемая стартовая доза 3 мг/кг/сутки.
- В ряде случаев к АГП 2-го поколения могут быть добавлены антагонисты лейкотриеновых рецепторов (ЛТР) (монтелукаст), но не у всех пациентов. К выбору данной терапии необходимо подходить индивидуально.
- В лечении ХК не рекомендованы длительные курсы системных глюкокортикостероидов (ГКС). Они могут рассматриваться в рамках коротких курсов лечения у пациентов с тяжелым обострением.
- Указанный алгоритм лечения с осторожностью может быть использован для лечения детей, беременных и кормящих женщин.
Биластин (Никсар®) – самый современный, эффективный и безопасный АГП
Сравнительное исследование эффективности увеличенных доз неседативных АГП у пациентов с ХК (биластин, левоцетиризин, дезлоратадин), показало, что только биластин при 4-кратном увеличении дозировки продемонстрировал повышение эффективности на 60%, тогда как у двух других препаратов – чуть более чем на 20% (Sanchez-Borges M. et al.).
Другое перекрестное рандомизированное двойное слепое плацебо-контролируемое клиническое исследование, в котором сравнивалась эффективность биластина, дезлоратадина и рупатадина в отношении гистамин-индуцированной крапивницы, также продемонстрировало преимущества биластина. Никсар® способствовал наибольшему уменьшению площади волдыря и значительному уменьшению зуда по сравнению с другими препаратами и начинал действовать уже через час (Antonijoan R. et al.).
По данным исследования Martin K. Church, биластин в дозе 20 мг и цетиризин в дозе 10 мг продемонстрировали сопоставимую эффективность в отношении уменьшения вызванных гистамином волдырей и эритемы, однако скорость развития эффекта была выше в группе биластина.
K. Krause и соавт. в своем исследовании показали, что биластин был эффективен в уменьшении симптомов у пациентов с контактной холодовой крапивницей. А повышение эффективности биластина с увеличением дозы до 4-кратного уровня не сопровождалось выраженными нежелательными явлениями.
Длительное лечение биластином 20 мг 1 раз в день в течение 52 нед безопасно и хорошо переносится у пациентов с хронической идиопатической крапивницей (ХИК) или зудом, связанным с кожными заболеваниями. Биластин улучшал симптомы заболевания обоих состояний на ранней стадии терапии, и этот результат поддерживался на протяжении всего лечения.
В сравнении с опубликованными данными по другим АГП 1-го и 2-го поколений биластин в дозе 20 мг демонстрирует наименьшую способность связываться с церебральными Н1-рецепторами (по данным ПЭТ). Это говорит о том, что биластин является неседативным препаратом и не приводит к нарушению когнитивных и психомоторных функций. Кроме этого у него отсутствует кардиотоксический эффект, препарат также может быть использован у пожилых больных и/или у пациентов с нарушениями функции печени и почек без коррекции дозы.
Никсар® не продемонстрировал потенцирования депрессантного воздействия алкоголя и лоразепама на ЦНС.
Н1-АГП 2-го поколения рекомендуется в качестве 1-й линии терапии!
 Заслуживающую внимания информацию об инновационном препарате биластин (Никсар®) и его роли в лечении АР и ХК сообщил профессор медицинского факультета Университета г. Кельна Ralph Mоsges (Германия).
Заслуживающую внимания информацию об инновационном препарате биластин (Никсар®) и его роли в лечении АР и ХК сообщил профессор медицинского факультета Университета г. Кельна Ralph Mоsges (Германия).
– Одной из важнейших медицинских проблем является сегодня низкая обеспеченность населения квалифицированными аллергологами при высокой распространенности АЗ – с 1970 года их частота возросла вдвое. Так, по данным различных исследований, чувствительность по меньшей мере к одному ингаляционному аллергену превышает 50% в общей популяции. Наиболее высокая сенситизация отмечается к пылевым клещам (в Сингапуре достигает 80% среди населения), и это доминирующая причина АЗ дыхательных путей у городских жителей. В Европе каждый 4-й ребенок страдает той или иной формой аллергии. И если частота встречаемости экземы прогрессивно снижается c возрастом, то уровень заболеваемости АР остается практически неизменным, и это состояние сопровождает пациента всю его дальнейшую жизнь.
Несмотря на то что АР не относится к тяжелым заболеваниям, он значимо снижает качество жизни пациентов, негативно влияя на повседневную активность, профессиональную деятельность, учебу, сон. АР становится причиной головных болей, нервного раздражения, снижения концентрации и хронической усталости. Кроме этого была отмечена связь между АР и повышенным риском развития эректильной дисфункции у мужчин. Поэтому АР стоит рассматривать как системное заболевание и назначать соответствующую системную терапию с высоким профилем эффективности и безопасности.
АР – это хроническое респираторное заболевание, которое характеризуется наличием глазных и/или назальных симптомов. Согласно последним рекомендациям ARIA АР классифицируют как интермиттирующий и персистирующий, с легкой, среднетяжелой и тяжелой выраженностью симптомов.
В зависимости от типа АР и степени тяжести могут быть использованы разные группы препаратов: деконгестанты, кромоны, ингибиторы ЛТР, ГКС и, безусловно, АГП, которые являются 1-й линией терапии всех форм АР согласно рекомендациям ARIA. И при их эффективности они должны быть использованы в качестве монотерапии длительно.
Биластин – новый АГП или лучший из них?
Согласно результатам различных исследований биластин in vitro и in vivo показал свою высокую эффективность и безопасность, а также преимущество перед другими АГП, поэтому по праву может считаться лучшим из них.
In vitro: высокая избирательная тропность к Н1-рецепторам, антигистаминная и противовоспалительная активность, отсутствие аффинности к другим гистаминовым рецепторам или их подтипам.
In vivo: подавляет синтез гистамина, действует на уровне Н1-рецепторов, демонстрирует выраженный противоаллергический эффект, который влияет на все проявления аллергии.
Оптимальная доза биластина – 20 мг/сут, что было показано в сравнительном исследовании с различными дозами препарата у пациентов с АР и ХИК.
P. Kuna и соавт. (2009) сравнивали эффективность и безопасность биластина 20 мг/сут и цетиризина 10 мг/сут у больных с САР. В рандомизированном плацебо-контролируемом исследовании принимали участие почти 700 пациентов в возрасте от 12 до 70 лет.
Эффективность биластина и цетиризина оказалась сопоставимой и значительно превышала таковую плацебо. Однако, с точки зрения безопасности, биластин имел преимущества – на его фоне частота таких побочных эффектов, как сонливость и усталость, была достоверно ниже, чем при использовании цетиризина.
Более быстрое и продолжительное действие биластина по сравнению с другими АГП было продемонстрировано в многоцентровом рандомизированном двойном слепом исследовании F. Horak и соавт. (2010) с участием 75 пациентов с САР. Его обострение было спровоцировано искусственно: больные подвергались действию аллергена в течение 6 ч в 1-й день и в течение 4 ч во 2-й день.
Оценивалась эффективность биластина 20 мг, цетиризина 10 мг и фексофенадина 120 мг, которые были назначены однократно спустя 2 ч от начала провокации. Назальные симптомы оценивались по шкале TSS (Total Score Symptomes) у всех пациентов в 1-й и во 2-й день.
Биластин был эффективен уже спустя час, и его действие продолжалось более 26 часов. По этим критериям биластин и цетиризин отличались несущественно, а фексофенадин значительно уступал в эффективности.
Аналогичные результаты были получены К. Hashiguchi и соавт., оценивавшими терапевтическую эффективность биластина 20 мг и фексофенадина 60 мг у пациентов с АР, спровоцированным пыльцой японского кедра. По результатам исследования эффективность биластина была выше таковой фексофенадина, начинал он действовать раньше, а результат сохранялся дольше 24 часов.
Термином «крапивница» обозначают несколько состояний: уртикарии, острую крапивницу, ХИК и уртикарный васкулит, проявляющийся спонтанными волдырями и/или ангионевротическим отеком (рис.2).
Согласно рекомендациям большинства консенсусов (EAACI/GA2LEN/EDF/WAO) при лечении крапивницы следует избегать воздействия аллергических факторов и использовать в качестве 1-й линии терапии АГП 2-го поколения. При их неэффективности допускается даже 4-кратное увеличение дозы. Резистентность к АГП предусматривает применение омализумаба, циклоспорина А или монтелукаста в качестве 3-й линии терапии. При наличии выраженных симптомов могут быть назначены ГКС коротким курсом.
Важно, что повышение дозы АГП более эффективны по сравнению с комбинацией нескольких АГП в стандартных дозах. Так, результативность биластина увеличивается на 60%. Это максимальный результат по сравнению с другими препаратами этой группы.
С учетом того, что лечение АР и крапивницы обычно длится достаточно долго, важна не только эффективность терапии, но и ее безопасность. В отличие от подавляющего большинства АГП, которые метаболизируются в печени, биластин выводится в неизмененном виде с калом (67%) и мочой (33%), что делает его абсолютно безопасным.
Был проведен также целый ряд исследований оценки безопасности биластина, и в первую очередь его седативного действия.
Так, прием биластина в дозах 20, 40 и 80 мг в течение 7 дней в сравнении с гидроксизином 25 мг и плацебо показал, что наименьшее влияние на когнитивные функции оказывал биластин 20 мг и 40 мг. То есть даже в высоких дозах биластин не оказывает седативного эффекта, не влияет на психомоторные функции и скорость реакции у водителей и пилотов. Препарат не взаимодействует с алкоголем и лоразепамом, не усиливает их угнетающего действия на ЦНС при одновременном приеме.
Отсутствие седативного эффекта объясняется тем, что биластин не связывается с Н1-рецепторами в головном мозге, по сравнению, например, с гидроксизином, который оккупирует порядка 50% Н1-рецепторов ЦНС. Это было доказано в рандомизированном двойном слепом плацебо-контролируемом исследовании с применением ПЭТ.
Все отмеченные особенности делают биластин лучшим АГП с высоким профилем эффективности и безопасности.
Никсар® – это идеальный АГП, обладающий целым рядом преимуществ
- Отсутствие седативного эффекта.
- Быстрое и продолжительное действие.
- Побочные эффекты на уровне плацебо.
- Отсутствие клинически значимого удлинения интервала QTc или других сердечно-сосудистых эффектов.
- Отсутствие метаболизма через CYP450 и значимого взаимодействия с другими препаратами.
- Возможность применения у пациентов пожилого возраста, больных с нарушениями функции печени или почек без корректировки дозы.
- Возможность применения у пациентов, работающих на опасных производствах.
Никсар® рекомендуется в качестве 1-й линии терапии для длительного, эффективного и безопасного лечения АР и крапивницы.
Подготовила Ирина Чумак
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (43), травень 2018 р.