29 серпня, 2018
Контроль частоты сердечных сокращений при фибрилляции предсердий: место бета-блокаторов
По материалам VIII Научно-практической конференции Ассоциации аритмологов Украины (17-18 мая, г. Киев)
Фибрилляция предсердий (ФП) – наиболее частое нарушение сердечного ритма, с которым приходится сталкиваться врачам, оказывающим неотложную медицинскую помощь кардиологическим больным. Важнейшей задачей при этом является эффективный контроль частоты сердечных сокращений (ЧСС) и ритма.

О резервах терапии ФП, в частности о месте бета-блокаторов в длительном контроле ЧСС и в неотложной помощи при пароксизмах ФП, рассказал сопредседатель Ассоциации аритмологов Украины, заведующий отделом аритмий сердца ГУ «Национальный научный центр «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины» (г. Киев), доктор медицинских наук, профессор Олег Сергеевич Сычев.
ФП – самое распространенное нарушение ритма сердца, характеризующееся некоординированной электрической активностью предсердий с последующим ухудшением их сократительной функции. ФП увеличивает риск развития инсульта и других тромбоэмболических осложнений, сердечной недостаточности, дисфункции левого желудочка и ассоциирована с повышением частоты госпитализаций, ухудшением качества жизни, снижением переносимости физических нагрузок.
Учитывая широкий спектр негативных последствий, ФП рассматривают как потенциально опасную аритмию: уровень смертности у больных с ФП превышает таковой в общей популяции в 2 раза, независимо от наличия других известных предикторов смерти.
По данным популяционного исследования, проведенного сотрудниками ННЦ «Институт кардиологии им. Н. Д. Стражеско» (2007), установлено, что распространенность ФП / трепетания предсердий (ТП) среди городского населения составляет 2,4%.
ФП – хроническое прогрессирующее заболевание, при котором происходит постепенная эволюция от пароксизмальной (обычно проходит самостоятельно в течение 48 ч) до персистирующей (самостоятельно не проходит или необходима электрическая или медикаментозная кардиоверсия), длительной персистирующей (сохраняется более 1 года) и в конечном итоге постоянной формы ФП.
Впервые выявленная пароксизмальная ФП часто купируется спонтанно, но затем может рецидивировать (примерно у половины больных – в течение 1 мес), причем частота и длительность пароксизмов со временем увеличиваются.
Выделяют пять основных целей лечения больных с ФП: профилактика тромбоэмболий, купирование симптомов, оптимальное лечение сопутствующих сердечно-сосудистых заболеваний, контроль ЧСС и контроль ритма сердца.
Профессор О. С. Сычев остановился на проблеме контроля ЧСС и роли бета-блокаторов в долгосрочном контроле этого показателя и в неотложной помощи.
Как известно, основные эффекты бета-блокаторов реализуются блокадой β1- и β2-адренорецепторов. β1-адренорецепторы доминируют в структурах сердца, поэтому препараты, которые связываются с ними, не блокируя β2-адренорецепторы, называют кардиоселективными. Они препятствуют действию на адренорецепторы норадреналина, адреналина, снижают активность аденилатциклазы, что, в свою очередь, приводит к уменьшению синтеза циклического аденозинмонофосфата (цАМФ) и угнетению поступления ионов Са2+ в кардиомиоциты. Т
аким образом реализуются основные эффекты β1-адреноблокаторов: уменьшается сила и частота сердечных сокращений; подавляется проводимость; уменьшается автоматизм. Эти эффекты снижают потребность миокарда в кислороде, а также обеспечивают антиаритмическое действие.
Блокада β1-адренорецепторов в клетках юкстагломерулярного аппарата почек ведет к уменьшению содержания Са2+, угнетению секреции ренина и, соответственно, уменьшению образования ангиотензина II, что обусловливает антигипертензивный эффект бета-блокаторов. Согласно результатам крупных рандомизированных многоцентровых исследований бета-блокаторы достоверно снижают риск внезапной сердечной смерти.
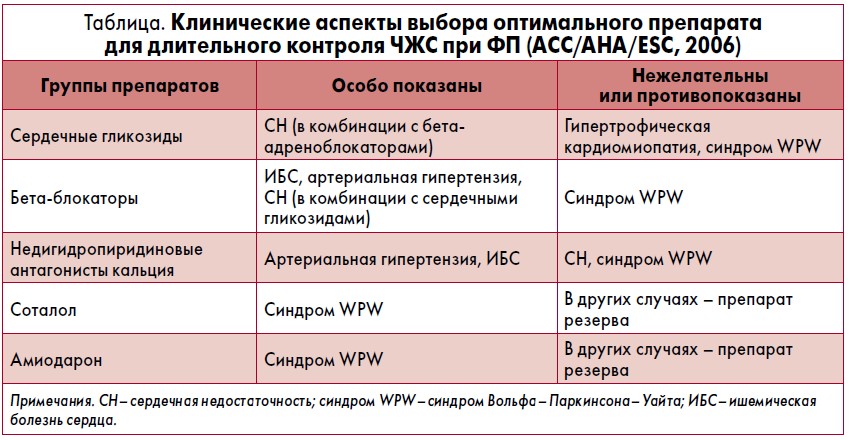 В консенсусном руководстве Европейского общества кардиологов (ESC), Американской коллегии кардиологов (ACC) и Американского общества сердца (АНА) 2006 г. даны рекомендации по выбору оптимального препарата для длительного контроля частоты желудочковых сокращений (ЧЖС) при ФП в зависимости от основного заболевания или сопутствующих синдромов (табл.). Очевидно, что бета-блокаторы являются препаратами выбора во многих клинических ситуациях.
В консенсусном руководстве Европейского общества кардиологов (ESC), Американской коллегии кардиологов (ACC) и Американского общества сердца (АНА) 2006 г. даны рекомендации по выбору оптимального препарата для длительного контроля частоты желудочковых сокращений (ЧЖС) при ФП в зависимости от основного заболевания или сопутствующих синдромов (табл.). Очевидно, что бета-блокаторы являются препаратами выбора во многих клинических ситуациях.
При сохранении симптомов, особенно если они связаны с высокой частотой или нерегулярностью желудочкового ритма, целесообразно обеспечить жесткий контроль ЧЖС. ЧСС следует снижать до тех пор, пока симптомы не исчезнут или существенно не уменьшатся, либо выяснится, что они преимущественно связаны с основным заболеванием, а не нарушением ритма.
Докладчик подчеркнул, что, помимо обеспечения длительного контроля ЧСС, при ведении пациентов с ФП существует еще одна важная задача: быстрое и безопасное влияние на этот показатель во время приступа, поскольку высокая ЧЖС на фоне пароксизма ФП приводит к развитию острой СН, острой ишемии миокарда, гипотензии, вплоть до аритмического шока.
Распространенной практикой является применение парентеральных бета-блокаторов в остром периоде ФП для контроля ЧЖС. При этом главное требование к используемым препаратам состоит в том, чтобы их эффект был легко управляемым в разных клинических ситуациях.
С целью достижения быстрого и контролируемого ЧСС-снижающего эффекта в неотложной помощи при ФП применяют кардиоселективный бета-блокатор ультракороткого действия эсмолол (Библок).
Эсмолол начинает действовать быстро – через 1-2 мин после начала внутривенного введения, а период его полувыведения составляет всего 9 мин (для сравнения: у метопролола период полувыведения составляет до 3,5 ч, у пропранолола – до 2,5 ч). Уникальная фармакокинетика препарата дает возможность длительного капельного введения и индивидуального титрования его дозировок, а также обеспечивает быструю (в течение 20 мин) обратимость эффекта.
Кардиоселективность и отсутствие внутренней симпатомиметической активности позволяют использовать эсмолол при наличии относительных противопоказаний к применению других бета-блокаторов.
Парентеральное применение эсмолола рекомендовано при суправентрикулярных тахиаритмиях для контроля ЧСС, замедления частоты ритма желудочков в остром периоде ФП и ТП для всех пациентов без наличия синдрома WPW, которым не противопоказано применение бета-адреноблокаторов.
Эсмолол (Библок) выпускается в форме раствора с концентрацией 10 мг/мл.
Схема введения эсмолола
Шаг 1. Введение нагрузочной дозы 500 мкг/кг/мин в течение 1 мин, затем введение поддерживающей дозы 50 мкг/кг/мин в течение 4 мин. При положительном результате: введение поддерживающей дозы 50 мкг/кг/мин.
Шаг 2. При необходимости в течение 5 мин: повторить введение с дозировкой 500 мкг/кг/ мин в течение 1 мин. Повысить поддерживающую дозу до 100 мкг/кг/мин в течение 4 мин. При положительном результате: введение поддерживающей дозы 100 мкг/кг/мин.
Шаг 3. При необходимости в течение 5 мин: повторить введение с дозировкой 500 мкг/кг/мин в течение 1 мин. Повысить поддерживающую дозу до 150 мкг/ кг/мин в течение 4 мин. При положительном результате: введение поддерживающей дозы
150 мкг/кг/мин.
Шаг 4. При необходимости: повторить введение с дозировкой 500 мкг/кг/мин в течение 1 мин. Повысить поддерживающую дозу до 200 мкг/кг/мин и оставить на этом уровне.
В экстренных ситуациях для контроля тахиаритмии и/или гипертензии возможно болюсное применение эсмолола 80 мг в течение 15-30 с, а затем следует продолжить инфузию в дозе 150 мкг/ кг/ мин, при необходимости титруя до 300 мкг/кг/мин.
Подготовила Екатерина Ткаченко
Справка «ЗУ»
- Доступный парентеральный кардиоселективный бета-блокатор эсмолол обладает широкими терапевтическими возможностями у пациентов с ФП и другими различными неотложными кардиологическими состояниями. В руководстве по оказанию экстренной помощи Rosens Emergency Medicine Concepts and Clinical Practice (2017) эсмолол рекомендован к применению на раннем догоспитальном этапе для контроля ЧСС и артериального давления у пациентов с острым коронарным синдромом, острой СН, диссекцией аорты, гипертоническим кризом, ишемическим инфарктом головного мозга, интрацеребральными гематомами. Эсмолол может использоваться у больных с синусовой тахикардией некомпенсаторного характера (R. Walls et al., 2017).
- Эсмолол часто используют для обеспечения контролируемой гипотонии и уменьшения кровопотери при микрохирургических, лапароскопических, челюстно-лицевых, ортопедических, нейрохирургических операциях; для предупреждения синдрома отмены пероральных бета-блокаторов длительного действия в периоперационном периоде и других ситуациях, когда продолжение их приема per os невозможно.
- Эсмолол также нашел применение с целью подавления рефлекторной гиперактивации симпатоадреналовой системы, купирования тахиаритмий и гипертензии при проведении кардиохирургических операций (во время стернотомии, при манипуляциях на трахее, сердце и корне аорты), диагностических процедур (ангиография, катетеризация полостей сердца, ларингоскопия, стресс-эхокардиография и др.). Подобная тактика позволяет минимизировать риск развития постоперационных кардиальных и церебральных осложнений, сократить длительность восстановительного периода, снизить летальность среди пациентов (E. J. Bakker, N. J. Ravensbergen, 2011; K. E. Raby, S. J. Brull et al., 1999).
- Эсмолол оказался значительно эффективнее дилтиазема при экстренной терапии ФП, осложняющей кардиохирургические операции: введение эсмолола позволило точнее контролировать ЧЖС и способствовало более быстрому возвращению к нормальному ритму, а также отличалось меньшей частотой побочных эффектов, включая те, которые приводили к отмене препарата (A. N. Mooss, R. L. Wurdeman et al.; D. E. Hilleman, A. P. Reyes et al., 2003).
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (58) червень 2018 р.


