29 листопада, 2018
Трансплантация фекальной микробиоты: европейские клинические рекомендации и первый украинский опыт

Одним из самых значительных прорывов в медицине, произошедших за последнее десятилетие, стало установление роли кишечной микробиоты (КМ) в понимании патогенеза многих заболеваний, особенно гастроэнтерологических и метаболических, а также появление новых возможностей их лечения при помощи модификации КМ. Число клинических исследований и публикаций, посвященных данному вопросу, за последнее десятилетие исчисляется сотнями. И все это – серьезные научные работы. Интерес к КМ особенно возрос после первых сообщений о великолепной терапевтической эффективности трансплантации фекальной микробиоты (ТФМ) при Clostridium difficile-ассоциированном колите, а также других заболеваниях кишечника, трудно поддающихся лечению традиционными методами.
ТФМ представляет собой одномоментную терапевтическую процедуру, которая позволяет быстро восстановить нормальный состав бактериальной флоры в толстой кишке. В октябре 2013 г. на ХХI Европейской объединенной гастроэнтерологической неделе ТФМ была представлена как одно из 3 самых весомых достижений гастроэнтерологии года. На протяжении нескольких десятилетий ТФМ во всем мире проводилась только в единичных центрах и, как правило, лишь в качестве крайней меры для пациентов с рецидивирующей инфекцией C. difficile. На сегодняшний день имеется уже несколько сотен публикаций с описанием как клинических случаев, так и рандомизированных клинических исследований (РКИ), продемонстрировавших приблизительно 90% кумулятивную эффективность ТФМ в лечении рецидивирующей инфекции C. difficile без каких-либо клинически значимых побочных эффектов.
Во всем мире успешно проведено тысячи процедур ТФМ, показавших свою эффективность при тяжелой рецидивирующей инфекции C. difficile, воспалительных заболеваниях кишечника (ВЗК), кишечном дисбиозе и синдроме раздраженного кишечника (СРК). Кроме того, в последние годы появились работы, свидетельствующие об эффективности ТФМ и при негастроэнтерологических заболеваниях – сахарном диабете (СД) и инсулинорезистентности, ожирении, рассеянном склерозе, идиопатической аутоиммунной пурпуре и другой патологии. В течение последних 3 лет ТФМ системно проводится и в нашей стране – в Украинском научно-практическом центре эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины, где выполнено уже 46 таких процедур.
Несмотря на то что широкое распространение ТФМ ограничено из-за многих бюрократических вопросов (в основном связанных с подбором доноров и контролем безопасности), сама практика использования ТФМ за рубежом процветает. Поскольку этот метод лечения приобрел необычайную популярность, возникла необходимость разработки официальных клинических рекомендаций, основанных на данных доказательной медицины. На специально созванной европейской конференции, состоявшейся в конце 2016 г., 28 экспертов из 10 стран Европы обсуждали ключевые вопросы ТФМ, в частности показания для ее проведения, выбор доноров, подготовку фекального материала и клиническое мониторирование. В результате был принят Европейский консенсус по проведению ТФМ в виде клинического руководства для врачей, основные положения которого приведены ниже.
Сегодня основным и единственным официально утвержденным показанием для проведения ТФМ по-прежнему является псевдомембранозный колит (ПМК), вызванный инфекцией C. difficile. В рекомендациях подчеркивается, что использование фекальной микрофлоры от здорового донора к реципиенту при ПМК способно восстанавливать здоровую микробную флору в пораженной толстой кишке, приводя к полному купированию симптоматики. В нескольких открытых РКИ трансплантация фекальной микробиоты при ПМК дала значительно более высокие показатели излечения по сравнению с ванкомицином (94 и 90% против 31 и 26% соответственно), в связи с чем эти исследования даже были приостановлены. В нескольких систематических обзорах и метаанализах излечение от ПМК после ТФМ варьировало от 85 до 89,7%. Во всех исследованиях ТФМ продемонстрировала отличную безопасность как минимум в краткосрочной перспективе, поскольку лишь несколько раз сообщалось о незначительных побочных эффектах. Хотя теоретически при ТФМ возможна передача потенциально опасных микроорганизмов, которые в течение десятилетий не проявляли свою активность, эту возможность следует рассматривать в контексте благоприятного соотношения «риск – польза», поскольку ТФМ является самым эффективным методом лечения ПМК и представляет собой жизненно важную терапию для данной категории больных. В связи с этим рекомендуется широкое внедрение ТФМ в клиническую практику для лечения как тяжелой, так и легкой формы ТФМ.
 Ключевым вопросом, касающимся ТФМ, является отбор доноров. При этом главная цель – уменьшение и предупреждение нежелательных событий, связанных с введением фекального трансплантата. В рекомендациях предлагается несколько шагов по выбору доноров для ТФМ независимо от показаний. Прежде всего, эксперты рекомендуют общие критерии исключения для доноров перед проведением ТФМ. Первым шагом является письменный опрос, сфокусированный на анамнезе заболеваний и привычках потенциального донора, с целью выявления вероятных факторов риска (табл. 1). Это чрезвычайно важно для исключения проблем, которые невозможно обнаружить при анализе крови и кала. Чтобы уменьшить вероятность сопутствующих заболеваний, предпочтение следует отдавать лицам младше 60 лет. Скринированные доноры также должны проходить дополнительное собеседование в день сдачи материала, чтобы исключить любую недавно возникшую и потенциально опасную проблему. Альтернативный способ, без использования анкеты, состоит в том, чтобы собирать донорские пробы сразу после результатов исследований, а также замораживать и хранить их, если центр имеет опыт работы с замороженными материалами и располагает доступными средствами для их хранения.
Ключевым вопросом, касающимся ТФМ, является отбор доноров. При этом главная цель – уменьшение и предупреждение нежелательных событий, связанных с введением фекального трансплантата. В рекомендациях предлагается несколько шагов по выбору доноров для ТФМ независимо от показаний. Прежде всего, эксперты рекомендуют общие критерии исключения для доноров перед проведением ТФМ. Первым шагом является письменный опрос, сфокусированный на анамнезе заболеваний и привычках потенциального донора, с целью выявления вероятных факторов риска (табл. 1). Это чрезвычайно важно для исключения проблем, которые невозможно обнаружить при анализе крови и кала. Чтобы уменьшить вероятность сопутствующих заболеваний, предпочтение следует отдавать лицам младше 60 лет. Скринированные доноры также должны проходить дополнительное собеседование в день сдачи материала, чтобы исключить любую недавно возникшую и потенциально опасную проблему. Альтернативный способ, без использования анкеты, состоит в том, чтобы собирать донорские пробы сразу после результатов исследований, а также замораживать и хранить их, если центр имеет опыт работы с замороженными материалами и располагает доступными средствами для их хранения.
Следующим ключевым вопросом является тестирование доноров. Согласно рекомендациям, подходящим для ТФМ донорам должны быть выполнены анализы крови и кала не более чем за 4 недели до сдачи материала (табл. 2). Если нет изменений в состоянии здоровья донора, тестирование может быть повторено через 8 недель.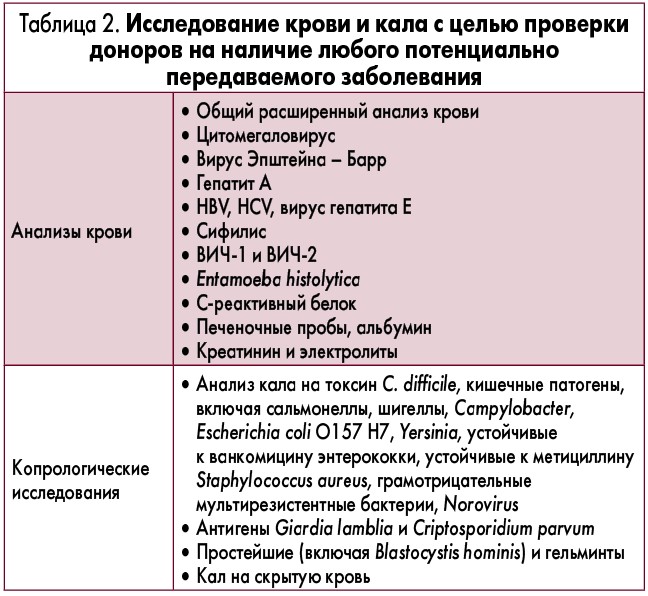
Согласно данным проведенного метаанализа, с точки зрения результатов ТФМ при лечении ПМК существенной разницы между выбранным пациентом и анонимными здоровыми донорами нет. Использование как родственных, так и неродственных доноров для ТФМ обеспечило отличные показатели в излечении ПМК в нескольких РКИ и больших сериях «случай – контроль». Тем не менее рандомизированные исследования, в которых сравнивались бы непосредственно эти категории доноров, пока еще отсутствуют. Использование неродственных здоровых доноров может быть полезно в центрах ТФМ с большим объемом пациентов для удовлетворения потребности в этом виде лечения. Доступность банка кала в этих центрах имеет первостепенное значение.
Ключевым практическим вопросом при проведении ТФМ является подготовка фекального материала. Хотя протоколы, используемые в разных исследованиях, схожи между собой, для приготовления взвеси свежих фекалий необходимо соблюдать определенную этапность, представленную в таблице 3. Количество использованного фекального материала варьирует от исследования к исследованию, при этом в большинстве исследований используется от 30 до 50 г фекалий. Вес кала является очень несовершенной мерой количества КМ, существует широкая изменчивость в микробном содержании в кале между отдельными лицами и даже различными пробами. Эксперты рекомендует использовать фекальный материал и стерильный солевой раствор (0,9%) в соотношении 1:5 (30 г фекалий, которые должны быть разбавлены в 150 мл физиологического раствора). После гомогенизации твердые вещества должны быть извлечены с использованием марли, чайного фильтра или аналогичного устройства, а суспензию желательно вылить в стерильный контейнер.
Сравнительные РКИ показали аналогичную эффективность ТФМ в лечении ПМК, проведенную со свежими и замороженными фекальными образцами. Перед замораживанием в свежие фекалии добавляют глицерин до конечной концентрации 10%, что защищает микробные клетки от повреждений, вызванных замораживанием. Конечная суспензия должна быть четко маркирована (с использованием кодов, аналогичных трансплантации крови и ткани) и храниться при –80 °C. Хранение при –20 °C также может быть осуществимо, но его следует избегать, поскольку это позволяет некоторым ферментам сохранять свою активность, что способно привести к деградации чувствительных микробных популяций. В день фекальной инфузии фекальную суспензию размораживают на теплой (37 °C) водяной бане. После разморозки для получения желаемого объема суспензии добавляется солевой раствор, а размороженный фекальный материал следует вводить в течение 6 ч. Поскольку микробные клетки чувствительны к размораживанию, следует избегать повторных разморозок и заморозок, а замороженные образцы должны быть приготовлены в дозах, необходимых для каждой процедуры ТФМ.
В клинической практике применяются различные пути доставки фекалий – путем колоноскопии, при помощи клизмы либо введение через верхние отделы ЖКТ (через рабочий канал гастроскопа, назогастральный или назоеюнальный зонд). Многие систематические обзоры и метаанализы показали, что наиболее эффективным и безопасным методом введения фекального трансплантата является колоноскопия. В зависимости от общего состояния реципиента донорский кал в количестве 200-500 мл фекальной суспензии, полученной из 20-100 г фекалий, может быть безопасно доставлен через рабочий канал колоноскопа как в правые (преимущественно), так и левые отделы толстой кишки. При использовании колоноскопа как средства доставки материала реципиенты получают обычную подготовку полиэтиленгликолем, как для колоноскопии.
ТФМ может проводиться с помощью клизмы. При этом пациентам следует удерживать полученный материал в течение не менее 30 мин и оставаться в положении на спине, чтобы свести к минимуму возможную дефекацию. Фекальная суспензия также может быть доставлена через рабочий канал гастроскопа, через назогастральную, назоеюнальную или гастростомическую трубку. После этого пациенты должны находиться в вертикальном положении в течение 4 ч после инфузии, чтобы предотвратить аспирацию.
ТФМ является безопасной процедурой даже у пациентов с ослабленным иммунитетом и у критически больных пациентов независимо от пути доставки. В случае тяжелых состояний предпочтение следует отдавать клизме. Частота серьезных побочных эффектов у реципиентов, получавших фекальный трансплантат через верхние отделы ЖКТ, несколько выше. Так, сообщалось о развитии у некоторых пациентов лихорадки и аспирационной пневмонии из-за тошноты и рвоты. В исследовании Moayyedi и соавт. 15 пациентов с язвенным колитом (ЯК) сообщили о 15 ректальных абсцессах после введения инфузии при помощи клизмы.
При необходимости ТФМ можно проводить повторно, особенно в случае неудачного лечения или клинического рецидива ПМК. Успех ТФМ также может зависеть от количества доставленной фекальной суспензии, что решается за счет множественных повторных инфузий. Факторами, отрицательно влияющими на результат ТФМ, могут быть малый объем донорского кала, тяжелый колит и/или продолжающееся лечение антибиотиками. В случае неудачного или неполного клинического ответа рекомендуется использовать фекальный материал от другого донора. Считается, что помимо ПМК, повторное применение ТФМ при ВЗК повышает вероятность успеха, однако убедительные подтверждающие данные пока отсутствуют.
При удовлетворительном состоянии пациента ТФМ обычно проводится в амбулаторных условиях. Продолжительность периода наблюдения после ТФМ еще не определена, поскольку она зависит от пути доставки, сопутствующей патологии и общего состояния пациента. Наиболее распространенными кратковременными побочными эффектами после ТФМ при ПМК были диарея, спазмы в животе, отрыжка, запор, лихорадка, а также грамотрицательная бактериемия и перфорация. При ВЗК часто отмечалась диарея, вздутие живота и спазмы, лихорадка и ухудшение течения заболевания. Один пациент умер после срыгивания фекального материала, введенного в двенадцатиперстную кишку под общим наркозом. У другого пациента развился септический шок и токсический мегаколон после доставки донорского кала через предварительно установленную назогастральную трубку. У одного пациента был септический шок из-за фекальной аспирации после ТФМ, проведенной при гастроскопии.
Периодичность и продолжительность наблюдения за долгосрочными неблагоприятными событиями после ТФМ пока не определены, поскольку для этого нужны дополнительные клинические и аналитические данные. На сегодняшний день имеются сообщения о единичных случаях увеличения массы тела, развитии периферической нейропатии, болезни Шегрена, идиопатической тромбоцитопенической пурпуры и ревматоидного артрита. В то же время имеется много сообщений об улучшении состояния пациентов на фоне течения других заболеваний ЖКТ после ТФМ, а именно СРК, ВЗК, хронического запора, антибиотикассоциированной диареи (ААД). В частности, по данным систематического обзора с метаанализом (S.P. Costello et al., 2017), проведение ТФМ способствовало индукции ремиссии ЯК у 24-32% больных против 5-20% при традиционной терапии, а клиническая ремиссия отмечалась у 39-55% больных против 20-24% при классической терапии. Имеется также много данных об эффективности ТФМ при некоторых внекишечных заболеваниях, таких как болезнь Паркинсона, рассеянный склероз, идиопатическая тромбоцитопеническая пурпура, метаболические нарушения (ожирение, СД) и заболевания детского возраста.
Согласно рекомендациям, пациенты, которым проведена ТФМ, должны находиться под наблюдением не менее 8 недель. Ответ на лечение подразумевает клиническое улучшение, а именно снижение частоты дефекации и улучшение консистенции кала, улучшение других параметров тяжести заболевания (лабораторных параметров, радиологических и/или эндоскопических данных). Повторение теста на C. difficile обычно не рекомендуется, так как токсины могут сохраняться еще в течение нескольких недель.
Как и в случае с другими техническими медицинскими процедурами, перед выполнением ТФМ требуется определенный период специального обучения. Поэтому врачи, которые собираются внедрить ТФМ в своем центре, должны пройти предварительную подготовку, состоящую обычно из нескольких этапов: клинической подготовки, включающей выбор доноров и пациентов, микробиологической подготовки (подготовка свежего и замороженного фекального материала), проведения самой процедуры при помощи различных путей доставки (клизма, колоноскопия, назодуоденальный/назоеюнальный зонд), мониторинга пациентов после ТФМ.
Как уже указывалось выше, пока ТФМ в нашей стране системно проводится только в Украинском научно-практическом центре эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины, где с конца 2015 г. по настоящее время проведено 46 однократных процедур ТФМ, из них 22 – со свежим материалом и 24 – с замороженными образцами. Спектр патологии, при которой выполнялась ТФМ, а также ее эффективность представлены в таблице 4.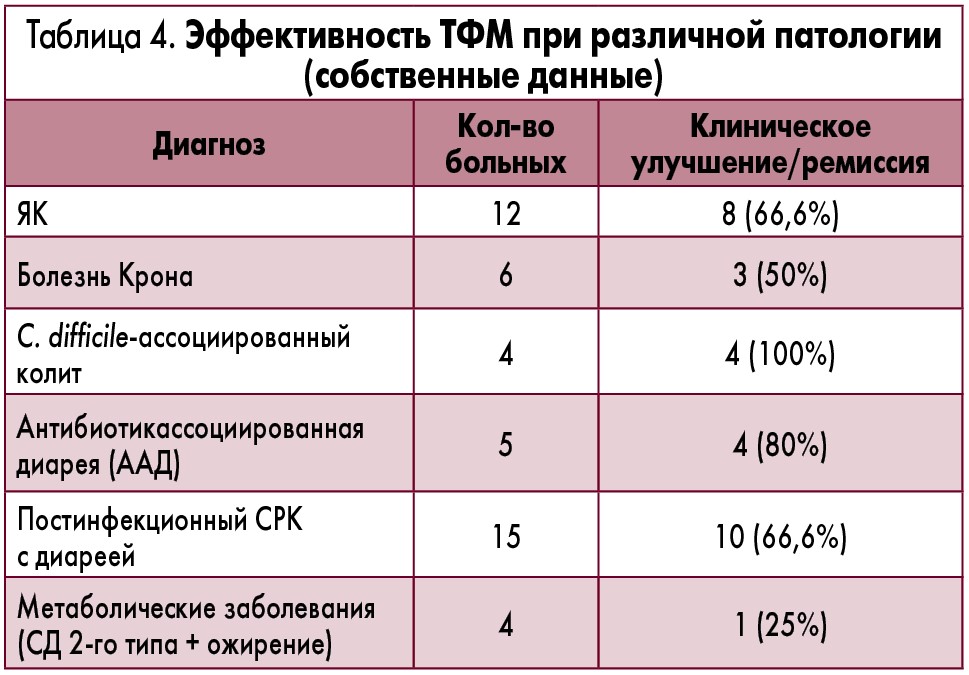
Как видно из приведенных данных, у всех пациентов с С. difficile-ассоциированным ПМК после однократной ТФМ было отмечено клиническое улучшение и наступление глубокой ремиссии, причем до настоящего времени рецидивов ПМК не отмечалось. Высокая эффективность ТФМ отмечена также при ААД (клиническое улучшение у 80% больных), постинфекционном СРК с диареей и ЯК (66,6%). У пациентов с болезнью Крона эффективность ТФМ была меньше (50%), причем у 1 пациента отмечались ближайшие побочные эффекты в виде повышения температуры и усиления абдоминальной боли в течение 3 дней после процедуры, которые в течение 1 недели разрешились. Каких-либо других существенных, клинически значимых побочных эффектов ТФМ в наших наблюдениях не отмечалось. Небольшое количество больных (4 пациента) и сравнительно малый срок наблюдения пока не позволяют нам сделать достоверные выводы об эффективности ТФМ при метаболических заболеваниях, таких как СД 2-го типа и ожирение.
Таким образом, на основании принятого Европейского консенсуса и собственного опыта мы можем сделать вывод о том, что фекальная трансплантация является важным и эффективным терапевтическим методом в лечении инфекции C. difficile и ассоциированного ПМК. Кроме того, последние данные показывают, что ТФМ является перспективным и эффективным методом лечения других расстройств, ассоциированных с изменением кишечной микрофлоры, в частности ВЗК, СРК, ААД. Эффективность ТФМ при внекишечных заболеваниях, продемонстрированная в эксперименте и отдельных клинических наблюдениях, нуждается в дальнейшем изучении. Для широкого внедрения ТФМ в клиническую практику в Украине необходимы создание специализированных центров ТФМ и соответствующая подготовка специалистов, использующих клинические рекомендации, основанные на достоверных данных.
Литература
- Baxter M., Colville A. Adverse events in faecal microbiota transplant: a review of theliterature. J Hosp Infect. 2016; 92: 117-27.
- Cammarota G., Ianiro G., Tilg H. et al. European consensus conference on faecal microbiota transplantation in clinical practice. Gut. 2017; 66: 569-580.
- Cammarota G., Masucci L., Ianiro G. et al. Randomised clinical trial: faecal microbiota transplantation by colonoscopy vs. vancomycin for the treatment of recurrent Clostridium difficile infection. Aliment Pharmacol Ther. 2015; 41: 835-43.
- Cui B., Feng Q., Wang H. et al. Fecal microbiota transplantation through mid-gut for refractory Crohn’s disease: safety, feasibility, and efficacy trial results. J Gastroenterol Hepatol. 2015; 30: 51-8.
- Debast S.B., Bauer M.P., Kuijper E.J. European Society of Clinical Microbiology and Infectious Diseases. European Society of Clinical Microbiology and Infectious Diseases: update of the treatment guidance document for Clostridium difficile infection. Clin Microbiol Infect. 2014; 20 (Suppl 2): 1-26.
- Drekonja D., Reich J., Gezahegn S. et al. Fecal microbiota transplantation for Clostridium difficile infection: a systematic review. Ann Intern Med. 2015; 162: 630-8.
- Kassam Z., Lee C.H., Yuan Y. et al. Fecal microbiota transplantation for Clostridium difficile infection: systematic review and meta-analysis. Am J Gastroenterol. 2013; 108: 500-8.
- Kelly C.R., Khorutz A., Staley C. et al. Effect of fecal microbiota transplantation on recurrence in multiply recurrent Clostridium difficile infection. Ann Intern Med. 2016; 165: 609-16.
- Kump P.K., Krause R., Steininger C. et al. Recommendations for the use of faecal microbiota transplantation «stool transplantation»: consensus of the Austrian Society of Gastroenterology and Hepatology (GGH) in cooperation with the Austrian Society of Infectious Diseases and Tropical Medicine. Z Gastroenterol. 2014; 52: 1485-92.
- Lee C.H., Steiner T., Petrof E.O. et al. Frozen vs fresh fecal microbiota transplantation and clinical resolution of diarrhea in patients with recurrent Clostridium difficile infection: a randomized clinical trial. JAMA. 2016; 315: 142-9.
- Moayyedi P., Surette M.G., Kim P.T. et al. Fecal microbiota transplantation induces remission in patients with active ulcerative colitis in a randomized controlled trial. Gastroenterology. 2015; 149: 102-9.
- Rossen N.G., Fuentes S., van der Spek M.J. et al. Findings from a randomized controlled trial of fecal transplantation for patients with ulcerative colitis. Gastroenterology. 2015; 149: 110-18.
- Satokari R., Mattila E., Kainulainen V. et al. Simple faecal preparation and efficacy of frozen inoculum in faecal microbiota transplantation for recurrent Clostridium difficile infection – an observational cohort study. Aliment Pharmacol Ther. 2015; 41: 46-53.
- Satokari R., Fuentes S., Mattila E. et al. Fecal transplantation treatment of antibiotic-induced, noninfectious colitis and long-term microbiota follow-up. Case Rep Med. 2014; 2014: 913867.
- Trubiano J.A., Cheng A.C., Korman T.M. et al. Australasian Society of Infectious Diseases updated guidelines for the management of Clostridium difficile infection in adults and children in Australia and New Zealand. Intern Med J. 2016; 46: 479-93.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (49), жовтень 2018 р.


