7 грудня, 2018
Вплив атезолізумабу на довготривалу виживаність пацієнтів із недрібноклітинним раком легені
Рак легені є провідною причиною онкологічної смертності у світі, причому частка недрібноклітинного раку легені (НДКРЛ) становить близько 85% [1]. Незважаючи на заходи, спрямовані на раннє виявлення, у більшості пацієнтів при первинній діагностиці раку легені фіксують поширену або метастатичну форму захворювання. Прогноз у таких пацієнтів залишається невтішним: за деякими оцінками, 5-річна загальна виживаність (ЗВ) становить лише 16%. Близько 30% пацієнтів не відповідають на лікування першої лінії, а у пацієнтів, які були чутливі до лікування спочатку, у середньому через 5 міс розвивається резистентність до протипухлинних препаратів [2]. Проте останніми роками відбулися значні зрушення у лікуванні НДКРЛ у другій лінії – в арсеналі терапевтичних опцій з’явилися нові варіанти, включаючи інгібітори імунних контрольних точок та антиангіогенні засоби [3].
На XVIII Міжнародній конференції з раку легені IASLC, яка відбулась у Японії (2017 р.), були представлені дані довготривалої виживаності на фоні терапії другої/третьої лінії атезолізумабом у хворих на НДКРЛ. Атезолізумаб – гуманізоване, модифіковане моноклональне антитіло IgG1, що діє на програмований ліганд смерті клітин 1 (PD-L1), блокуючи його взаємодію з PD‑1 і B7.1. Він продемонстрував перевагу у ЗВ над доцетакселом у рандомізованому дослідженні II фази POPLAR у пацієнтів із поширеним НДКРЛ. У дослідження були включені пацієнти з НДКРЛ, у яких прогресування відбулося після застосування платиновмісних комбінацій. Пацієнти були рандомізовані на групи атезолізумабу (1200 мг внутрішньовенно кожні 3 тижні) та доцетакселу (75 мг/м2 внутрішньовенно кожні 3 тижні), лікування тривало до прогресування захворювання або виникнення неприйнятної токсичності. Пацієнти були стратифіковані залежно від експресії PD-L1 пухлинними клітинами (TC), гістологічного типу, а також кількості ліній попередньої хіміотерапії. Імуногістохімічно визначали кількість пухлинних клітин (TC0 <1%, TC1 – 1-5%, TC2 – 5-50% і TC3 >50%) та лімфоцитів, що інфільтрують пухлину, – IC (IC0 <1%, IC1 >1-5%, IC2 – 5-10%, IC3 <10%), які експресують PD-L1.
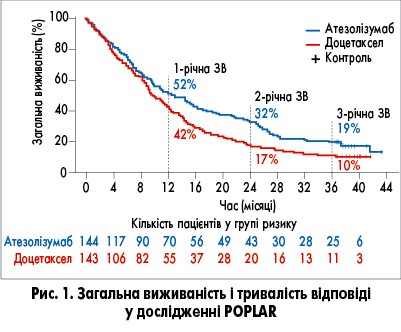 У дослідження були включені 287 пацієнтів, у 34% з яких був плоскоклітинний рак; 66% отримали тільки одну лінію хіміотерапії. За даними аналізу дослідження POPLAR, 2- та 3-річна виживаність пацієнтів, які отримували атезолізумаб або доцетаксел, становила 32% проти 17% і 19% проти 10,0% відповідно (рис. 1). Довгострокові переваги щодо ЗВ на фоні терапії атезолізумабом спостерігались у всіх підгрупах пацієнтів. Хоча найбільший показник ЗВ на фоні терапії атезолізумабом зареєстрований у підгрупі TC3 або IC3 (2-річна ЗВ – 41,7% проти 19,9%; 3-річна ЗВ – 37,5% проти 14,9%), у підгрупі TC0 та IC0 також спостерігалося збільшення довготривалої ЗВ на фоні прийому атезолізумабу порівняно з доцетакселом (2-річна ЗВ – 25,0% проти 6,8%; 3-річна ЗВ – 20,5% проти 6,8%). Для плоскоклітинного раку (2-річна ЗВ – 32,7% проти 7,8%; p=0,002; 3-річна ЗВ – 9,4% проти 5,2%) та неплоскоклітинного гістологічного типу (2-річна ЗВ – 32,2% проти 21,1%; 3-річна ЗВ – 23,3% проти 12,4%) атезолізумаб однаково продемонстрував покращення результатів. У популяції ІТТ частота загальної відповіді в обох групах становила 15%, однак середня тривалість відповіді була втричі довшою у групі атезолізумабу: 22,3 міс (95% довірчий інтервал – ДІ – 11,6‑31,1) проти 7,2 міс (95% ДІ 5,8-12,2). Сім із 11 пацієнтів, які перейшли поріг 3-річної виживаності у групі доцетакселу, у подальшому отримували терапію анти-PD-L1/PD‑1 агентами за межами протоколу.
У дослідження були включені 287 пацієнтів, у 34% з яких був плоскоклітинний рак; 66% отримали тільки одну лінію хіміотерапії. За даними аналізу дослідження POPLAR, 2- та 3-річна виживаність пацієнтів, які отримували атезолізумаб або доцетаксел, становила 32% проти 17% і 19% проти 10,0% відповідно (рис. 1). Довгострокові переваги щодо ЗВ на фоні терапії атезолізумабом спостерігались у всіх підгрупах пацієнтів. Хоча найбільший показник ЗВ на фоні терапії атезолізумабом зареєстрований у підгрупі TC3 або IC3 (2-річна ЗВ – 41,7% проти 19,9%; 3-річна ЗВ – 37,5% проти 14,9%), у підгрупі TC0 та IC0 також спостерігалося збільшення довготривалої ЗВ на фоні прийому атезолізумабу порівняно з доцетакселом (2-річна ЗВ – 25,0% проти 6,8%; 3-річна ЗВ – 20,5% проти 6,8%). Для плоскоклітинного раку (2-річна ЗВ – 32,7% проти 7,8%; p=0,002; 3-річна ЗВ – 9,4% проти 5,2%) та неплоскоклітинного гістологічного типу (2-річна ЗВ – 32,2% проти 21,1%; 3-річна ЗВ – 23,3% проти 12,4%) атезолізумаб однаково продемонстрував покращення результатів. У популяції ІТТ частота загальної відповіді в обох групах становила 15%, однак середня тривалість відповіді була втричі довшою у групі атезолізумабу: 22,3 міс (95% довірчий інтервал – ДІ – 11,6‑31,1) проти 7,2 міс (95% ДІ 5,8-12,2). Сім із 11 пацієнтів, які перейшли поріг 3-річної виживаності у групі доцетакселу, у подальшому отримували терапію анти-PD-L1/PD‑1 агентами за межами протоколу.
Порівняно з доцетакселом атезолізумаб демонструє істотне збільшення показників 2- та 3-річної виживаності хворих на НДКРЛ, у яких прогресування відбулося на фоні цисплатинвмісної хіміотерапії незалежно від експресії PD-L1 [4]. Ефект від застосування атезолізумабу корелює з експресією PD-L1 пухлинними клітинами та лімфоцитами, які інфільтрують пухлину, і є довготривалим. Ці результати узгоджуються з показниками довготривалої ЗВ у дослідженні ІІІ фази ОАК (Satouchi, WCLC‑2017).
OAK являє собою відкрите багатоцентрове рандомізоване дослідження ІІІ фази з оцінювання ефективності та безпечності застосування атезолізумабу порівняно з доцетакселом. У дослідженні брали участь 1225 пацієнтів із плоскоклітинним і неплоскоклітинним НДКРЛ, які були рандомізовані у співвідношенні 1:1 незалежно від PD-L1-статусу. У першій групі пацієнти отримували атезолізумаб (1200 мг внутрішньовенно кожні 3 тижні) до прогресування захворювання або втрати клінічної користі, у другій групі – доцетаксел (75 мг/м2 внутрішньовенно кожні 3 тижні) до прогресування захворювання або розвитку неприйнятної токсичності. Комбінована кінцева точка дослідження включала показники ЗВ перших 850 пацієнтів (популяція ITT) та в підгрупі, відібраної для первинного аналізу за PD-L1-статусом. Аналіз, проведений M. Satouchi та співавт., включав тільки пацієнтів, які досягли довготривалої виживаності – більше 24 міс.
Так, показники 2-річної виживаності були вищими у групі атезолізумабу порівняно з доцетакселом – 31% проти 21% відповідно. Після спостереження протягом 26 міс у групі атезолізумабу 119 пацієнтів досягли 2-річної виживаності та 279 пацієнтів її не досягли, тоді як у групі доцетакселу ці показники становили 77 проти 299 відповідно.
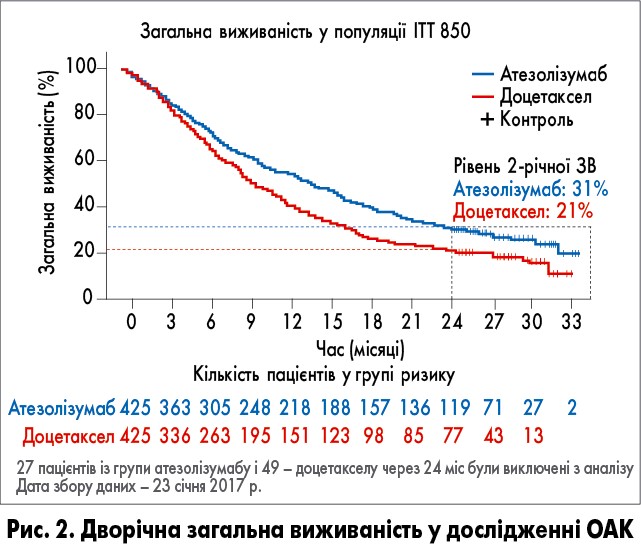 У групі атезолізумабу пацієнти, які досягли довготривалої виживаності, мали переважно неплоскоклітинний НДКРЛ, а також високу експресію PD-L1. У групі атезолізумабу серед пацієнтів, які досягли 2-річної виживаності, частота об’єктивної відповіді була вищою – 39,5% проти 5% (рис. 2). Пацієнти, які досягли довготривалої виживаності, отримували атезолізумаб у середньому протягом 18,0 міс [5].
У групі атезолізумабу пацієнти, які досягли довготривалої виживаності, мали переважно неплоскоклітинний НДКРЛ, а також високу експресію PD-L1. У групі атезолізумабу серед пацієнтів, які досягли 2-річної виживаності, частота об’єктивної відповіді була вищою – 39,5% проти 5% (рис. 2). Пацієнти, які досягли довготривалої виживаності, отримували атезолізумаб у середньому протягом 18,0 міс [5].
Ці результати ще раз підтверджують перевагу у довготривалій виживаності на фоні терапії атезолізумабом порівняно з доцетакселом. Окрім відомих прогностичних факторів (неплоскоклітинний гістологічний тип, жіноча стать, функціональний статус за шкалою ECOG 0), подальше використання атезолізумабу після прогресування також сприяло довготривалій виживаності [6].
У 20-40% пацієнтів із раком легені відбувається метастазування у головний мозок (ГМ), що істотно погіршує прогноз. Оскільки виживаність пацієнтів на фоні терапії атезолізумабом незалежно від PD-L1-статусу значно зростає, постає питання щодо безпечності та ефективності імунотерапії у пацієнтів із раком легені та метастазами у ГМ. Проведено великий аналіз даних досліджень PCD4989g, BIRCH, FIR, POPLAR та OAK, у яких оцінювали ефективність і безпеку застосування атезолізумабу у другій лінії терапії НДКРЛ серед пацієнтів із метастазами у ГМ і без них.
Загальна когорта включала 1452 пацієнти, 79 (5%) з яких мали метастази у ГМ. Частота всіх небажаних реакцій, у тому числі тяжкого ступеня, була подібною у хворих з/без метастазів у ГМ. Неврологічні небажані реакції реєструвалися частіше у пацієнтів із метастазами. Про неврологічні небажані явища 4-5 ступеня, пов’язані з лікуванням, у пацієнтів із метастазами у ГМ не повідомлялося. Найбільш поширеним неврологічним небажаним явищем, пов’язаним із лікуванням, був головний біль (8% пацієнтів із метастазами та 3% пацієнтів без метастазів у ГМ).
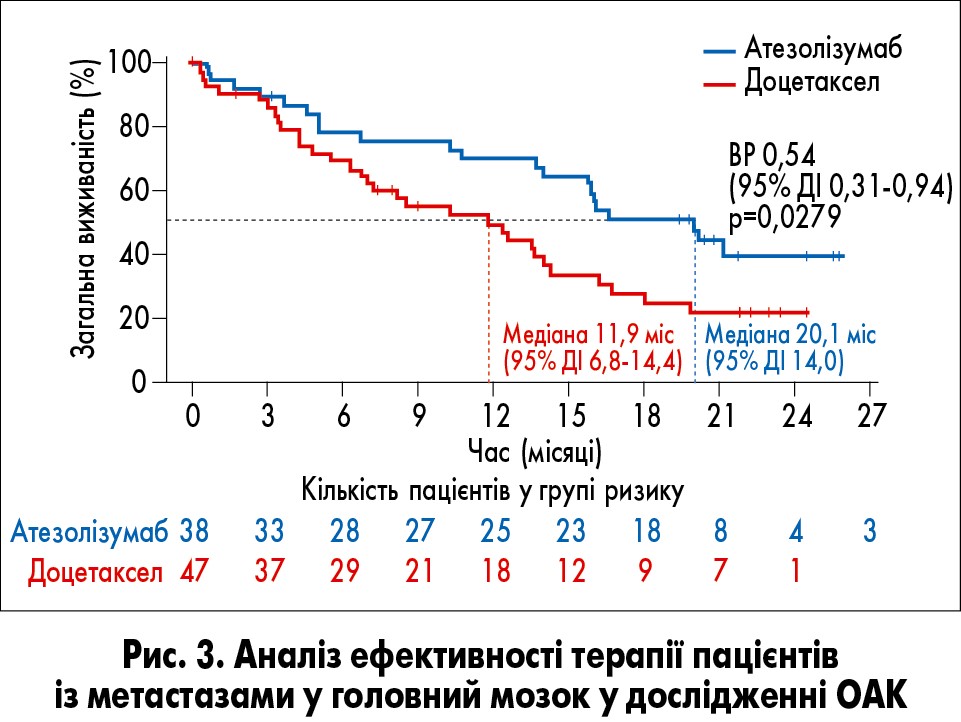 Субаналіз ефективності лікування проводили у популяції пацієнтів ITT (n=850) дослідження ОАК. Згідно з його результатами в пацієнтів із метастазами у ГМ, які отримували атезолізумаб, ЗВ була майже вдвічі вищою порівняно з пацієнтами, котрі отримували доцетаксел. Атезолізумаб показав перевагу у виживаності порівняно з доцетакселом при метастазах у ГМ (рис. 3): відносний ризик (ВР) 0,54; 95% ДІ 0,31-0,94; медіана ЗВ – 20,1 міс (n=38) проти 11,9 міс (n=47). Ризик виникнення нових уражень центральної нервової системи (ЦНС) був нижчим при застосуванні атезолізумабу (ВР 0,42; 95% ДІ 0,15-1,18; середній час до розвитку нового ураження ЦНС – не досягнуто проти 9,5 міс) у пацієнтів із наявними метастазами [7].
Субаналіз ефективності лікування проводили у популяції пацієнтів ITT (n=850) дослідження ОАК. Згідно з його результатами в пацієнтів із метастазами у ГМ, які отримували атезолізумаб, ЗВ була майже вдвічі вищою порівняно з пацієнтами, котрі отримували доцетаксел. Атезолізумаб показав перевагу у виживаності порівняно з доцетакселом при метастазах у ГМ (рис. 3): відносний ризик (ВР) 0,54; 95% ДІ 0,31-0,94; медіана ЗВ – 20,1 міс (n=38) проти 11,9 міс (n=47). Ризик виникнення нових уражень центральної нервової системи (ЦНС) був нижчим при застосуванні атезолізумабу (ВР 0,42; 95% ДІ 0,15-1,18; середній час до розвитку нового ураження ЦНС – не досягнуто проти 9,5 міс) у пацієнтів із наявними метастазами [7].
Таким чином, атезолізумаб демонструє прийнятний профіль безпеки та ефективність у пацієнтів із НДКРЛ порівняно з доцетакселом навіть у разі метастазування в ГМ, що робить його оптимальною опцією другої лінії терапії.
Література
- Torre L.A. et al. Global cancer incidence and mortality rates and trends – an update. Cancer Epidemiol Biomarkers Prev. 2016.
- Azzoli C.G. et al. American society of clinical oncology clinical practice guideline update on chemotherapy for stage IV non-small-cell lung cancer. J Clin Oncol. 2009.
- Lazzari C. Historical Evolution of Second-Line Therapy in Non-Small Cell Lung Cancer. Front Med (Lausanne). 2017.
- Maziеres J. et al. 3-year survival and duration of response in randomized phase II study of atezolizumab (atezo) vs docetaxel (doc) in 2L+ NSCLC (POPLAR). 2018.
- Satouchi et al. Long-Term Survival in Atezolizumab-Treated Patients with 2L+ NSCLC from Ph III Randomized OAK Study. Journal of Thoracic Oncology. 2017.
- Park et al. WCLC, 2017.
- Lukas R.V. et al. Safety and efficacy analyses of atezolizumab in advanced non-small cell lung cancer (NSCLC) patients with or without baseline brain metastases. Annals of Oncology. 2018.
Підготувала Катерина Марушко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (55), жовтень 2018 р


