22 грудня, 2018
Крушение парадигмы безопасности «золотого стандарта» НПВП: стратегия защиты от НПВП-индуцированных гастропатий с использованием ИПП
 Существует огромная доказательная база по вопросу необходимости и эффективности гастропротекции в условиях приема нестероидных противовоспалительных препаратов (НПВП) пациентами повышенного гастроинтестинального риска. Вместо с тем обсервационное исследование показало, что в реальной клинической практике >58% пациентов, принимающих НПВП, не используют гастропротекторных препаратов (Valkhoff V. et al., 2012). Можно предположить, что в отечественных клинических условиях эта цифра еще больше.
Существует огромная доказательная база по вопросу необходимости и эффективности гастропротекции в условиях приема нестероидных противовоспалительных препаратов (НПВП) пациентами повышенного гастроинтестинального риска. Вместо с тем обсервационное исследование показало, что в реальной клинической практике >58% пациентов, принимающих НПВП, не используют гастропротекторных препаратов (Valkhoff V. et al., 2012). Можно предположить, что в отечественных клинических условиях эта цифра еще больше.
Сердечно-сосудистый риск в условиях приема НПВП также часто становится предметом дискуссий. Датские исследователи M. Schmidt и соавт. (2018) изучили взаимосвязь кардиоваскулярного риска с приемом диклофенака по сравнению с другими НПВП, парацетамолом и отсутствием терапии как таковой. Были проанализированы данные датских национальных регистров (1996-2016), в которые вошли 252 когортных исследования с участием около 6,9 млн пациентов. В результате было установлено, что частота кардиоваскулярных событий у пациентов, получавших диклофенак, была выше на 50% по сравнению с теми, кто не принимал аналгетиков, и на 30% выше по сравнению с группой напроксена. Важно отметить, что повышение кардиоваскулярного риска было зафиксировано и для низких доз диклофенака. Кроме того, назначение диклофенака и напроксена ассоциировалось с повышением риска кровотечений в верхних отделах ЖКТ в 4,5 раза по сравнению с отсутствием терапии и в 2,5 раза по сравнению с терапией ибупрофеном и парацетамолом.
Необходимо обратить внимание на то, что НПВП вызывают повреждение слизистой оболочки ЖКТ несколькими путями (Ivey K. J., 1988). Одним из них является непосредственное токсическое воздействие, усиливаемое наличием кислоты, поскольку высокая кислотность среды улучшает всасывание НПВП в неионизированной форме (Hogben C. et al.,1957). Еще один механизм развития НПВП‑индуцированных гастропатий – нарушение простагландин-зависимых защитных реакций. Поверхностные клетки слизистой оболочки ЖКТ повреждаются тем или иным способом, а далее возникает вторая волна повреждения с развитием глубоких язвенных поражений (Elliott S. L. et al.,1996).
Частота эндоскопически выявленных язв среди пациентов, принимающих НПВП, составляет 14-44%. У 1,46-1,90% больных, длительно употребляющих данные противовоспалительные медикаменты, развиваются тяжелые поражения ЖКТ (кровотечения, обструкции, перфорации язв). В США ежегодно регистрируется 107 тыс. госпитализаций и 16,5 тыс. смертей, ассоциированных с использованием неселективных НПВП. Ситуация усугубляется тем, что данные язвенные осложнения терапии НПВП зачастую не сопровождаются симптомами или диспепсическими явлениями, что приводит к поздней диагностике. Этот факт обусловливает важность защиты желудка и кишечника, рекомендованной пациентам с повышенным и высоким гастроинтестинальным риском. К этой категории принадлежат лица с анамнезом язвенной болезни или кровотечений из ЖКТ, пациенты преклонного/старческого возраста, употребляющие кортикостероиды, а также применяющие высокие дозы НПВП или несколько препаратов этого класса одновременно (Goldstein J. L., 2000).
Основным этапом устранения какой-либо лекарственной токсичности является прекращение употребления причинного медикамента, что, однако, не всегда возможно. Это обусловило потребность в создании менее токсичных НПВП, а также в поиске дополнительных фармакопрепаратов, способных противодействовать нежелательным побочным воздействиям (Scheiman J. M., 2013).
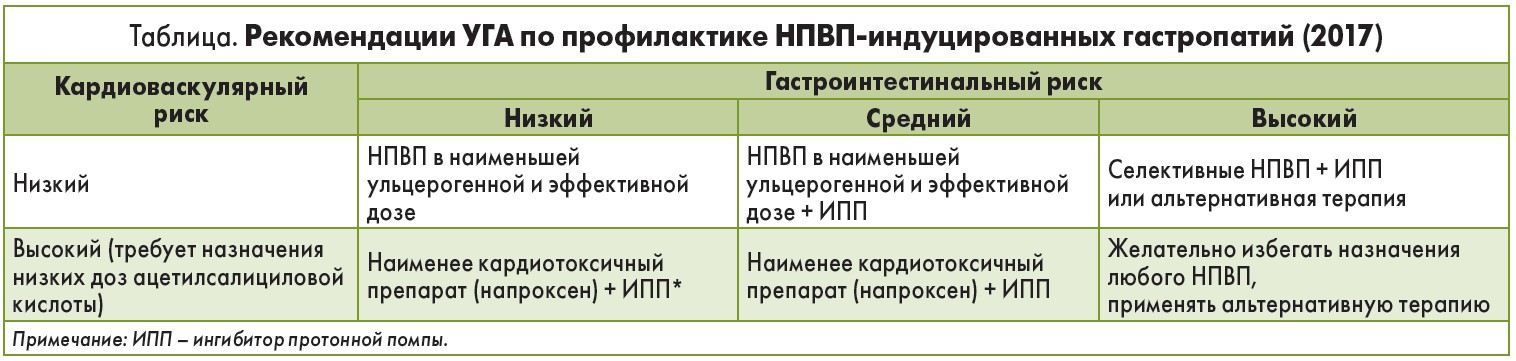
В 2017 г. в Украине были приняты Рекомендации Украинской гастроэнтерологической ассоциации (УГА) по профилактике и лечению гастропатий, индуцированных приемом НПВП, специально разработанные экспертной международной группой Gastrosphere 2.0.
Основные положения принятого консенсуса включают шесть ключевых практических рекомендаций, кратко представленных далее.
- До назначения НПВП следует определить индивидуальный риск НПВП-гастропатии каждого пациента (табл.). К группе высокого риска относят больных с осложненной пептической язвой в анамнезе, наличием ≥2 факторов риска. В группу умеренного риска входят пациенты >65 лет, с неосложненной пептической язвой в анамнезе, >7 дней принимающие высокие дозы НПВП, одновременно получающие антикоагулянты, кортикостероиды, несколько НПВП (включая низкие дозы ацетилсалициловой кислоты), с сопутствующими хроническими инвалидизирующими заболеваниями (сердечная/печеночная/почечная недостаточность, сахарный диабет). Больные без перечисленных факторов относятся к группе низкого риска.
- Диагностика НПВП-индуцированных гастропатий должна быть своевременной и включать определение группы риска, анализ клинической картины, лабораторные тесты (определение гематокрита, уровня гемоглобина, инфицирования хеликобактером) и эндоскопическое исследование.
- Всем пациентам, принимающим любые НПВП (в т. ч. селективные ингибиторы ЦОГ-2, безрецептурные формы традиционных НПВП в небольших дозах, низкие дозы ацетилсалициловой кислоты) рекомендовано дополнительное назначение гастропротектора (в первую очередь ИПП).
- У пациентов группы высокого риска гастропротекторная терапия ИПП должна быть длительной (≥6 мес).
- Врачам следует вести активную просветительскую работу среди пациентов с высоким риском развития НПВП-гастропатии, объясняя целесообразность модификации образа жизни, отказа от курения и злоупотребления алкоголем. Данная рекомендация также акцентирует внимание на взвешенном приеме НПВП, отказе от бесконтрольного применения НПВП и противоревматических препаратов, желательном переходе на использование селективных ингибиторов ЦОГ-2 и регулярном врачебном наблюдении при наличии факторов высокого риска.
- Пациентам с инфекцией H. pylori, которым впервые планируется назначить длительный курс НПВП, рекомендована антихеликобактерная терапия.
Таким образом, главной современной стратегией противодействия возникновению НПВП‑индуцированных поражений является назначение ИПП. При их совместном употреблении с НПВП риск развития симптоматических язв ЖКТ значительно снижается, в т. ч. у больных с факторами риска гастроинтестинальных осложнений и длительно принимающих НПВП (Hooper L. et al., 2004; Rostom A. et al., 2002; Jarupongprapa S. et al., 2013). Метаанализ X. Wang и соавт. (2011) продемонстрировал, что при использовании неселективных НПВП в сочетании с ИПП риск гастроинтестинальной токсичности лечения соответствует показателю терапии селективным ингибитором ЦОГ‑2. Тем не менее сочетание последних с ИПП также выступает стратегией снижения риска осложнений лечения со стороны ЖКТ (Barkun A. N. et al., 2010; Chan F. K.L. et al., 2007; Scheiman J. M. et al., 2006). M. Bakhriansyah и соавт. (2017) показали, что назначение селективных ингибиторов ЦОГ‑2 в совокупности с ИПП характеризуется меньшим риском перфораций, язвообразования или кровотечний из ЖКТ по сравнению с монотерапией этими препаратами во всех изученных подгруппах участников.
Критериями выбора оптимального ИПП выступают достаточный клинический опыт использования, подтвержденное качество и приемлемая цена (логично, что защита от побочных эффектов не должна быть дороже основного лечения). Этим критериям в полной мере соответствует омепразол (Омез, «Др. Реддис Лабораторис Лимитед», Индия). Омепразол препятствует образованию эрозий и других повреждений слизистой оболочки желудка, опосредованных воздействием ацетилсалициловой кислоты (Daneshmend T. K. et al., 1990; Scheiman J. M. et al., 1994). Омепразол быстро заживляет язвы, выступая одинаково эффективным при поражениях желудка и двенадцатиперстной кишки при условии лечения НПВП или его отсутствия (Walan A. et al., 1989; Lauritsen K. et al., 1992). Немаловажно, что омепразол оказывает благоприятное влияние на заживление язв всех этиологических типов. S. Kajura и соавт. (2015) показали, что назначение пероральных препаратов омепразола (20 мг/ сут) на протяжении всего лишь одной недели ускоряет заживление ран после эндоскопической резекции слизистой оболочки желудка при лечении ранних форм рака. Кроме кислотосупрессивного действия, омепразол осуществляет гастропротекцию путем антиоксидантного и антиапоптотического вплияния (Biswas K. et al., 2003).
Омепразол является первым представителем класса ИПП. При этом на сегодняшний день в лечении кислотозависимых заболеваний омепразол столь же эффективен, как и другие ИПП, которые были синтезированы позже. В крупном метаанализе W. Asghar и соавт. (2015) было доказано, что омепразол и эзомепразол в эквивалентных дозах характеризуются одинаковой эффективностью в составе тройной терапии при лечении язв желудка и двенадцатиперстной кишки, а также в суточном контроле интрагастрального pH. Большинство различий, продемонстрированных в исследованиях, не достигли уровня достоверности или были крайне незначительными. Метаанализ L. Chen и соавт. (2016), включавший 15 исследований, установил, что 20 мг омепразола 1 р/сут представляет собой оптимальное лечение неэрозивной гастроэзофагеальной рефлюксной болезни, вызывая наиболее выраженное облегчение симптомов. Кроме того, омепразолу свойственно более быстрое начало действия (30 мин), чем некоторым другим ИПП (5 ч). Исследование Е. С. Klinkenberg-Knol и соавт. (2000) указывает на безопасность длительного применения омепразола. Анализ почти 1500 пациенто-лет наблюдения не обнаружил каких-либо серьезных побочных эффектов этого препарата. Также было установлено, что омепразол не вызывает воспаления, атрофии или гиперплазии аргирофильных клеток у хеликобактер-негативных пациентов. Таким образом, омепразол выступает золотым стандартом ИПП.
Омез является медикаментом с огромным клиническим опытом применения в 19 странах мира (в том числе в США), одобрен FDA и включен в Orange Book. Назначение омепразола (Омез) в дозе 20 мг 1 р/сут на протяжении всего курса лечения НПВП позволяет уменьшить количество НПВП‑индуцированных гастропатий примерно в 4 раза (Cullen D. et al., 1998). Применение ИПП (препарата Омез), является обязательным методом защиты от НПВП‑гастропатий и связанных с ними патологических явлений (повышенной секреторной активности желудка, гипермоторики верхних отделов пищеварительной системы, микрокровотечений).
Таким образом, назначение НПВП, в т. ч. достаточно популярного среди отечественных специалистов диклофенака, должно проводиться после оценки потенциального риска развития НПВП-гастропатий в соответствии с такими факторами, как анамнез язвы/кровотечения из ЖКТ, старческий возраст, прием нескольких НПВП, употребление НПВП в высоких дозах (включая низкие дозы ацетилсалициловой кислоты) и др. При наличии хотя бы одного из перечисленных факторов обязательно параллельное назначение ИПП (Омез по 20 мг 1 р/сут) на протяжении всего приема НПВП. Омезу свойственно целевое действие – защита слизистой оболочки ЖКТ от повреждающего влияния НПВП.
Медична газета «Здоров’я України 21 сторіччя» № 23 (444), грудень 2018 р.