3 січня, 2019
Распространенность в украинской популяции солидных опухолей с микросателлитной нестабильностью и ее роль в иммунотерапии
 Иммунотерапия с применением антител, которые блокируют рецептор программируемой гибели 1 (PD‑1), его лиганд (PD-L1) или белок 4, ассоциированный с цитотоксическими T-лимфоцитами (CTLA‑4), может иметь хороший и продолжительный эффект при многих видах опухолей. Однако для большинства пациентов применение ингибиторов данных контрольных точек не будет эффективным. Так, наибольшая частота ответа на иммунотерапию наблюдается у пациентов с меланомой, немелкоклеточным раком легкого (НМРЛ) и раком почки и составляет 40, 25 и 19% соответственно. Это создает необходимость поиска предиктивных маркеров ответа на иммунотерапию. Первым таким маркером стал уровень экспрессии PD-L1, который позволил более точно отбирать пациентов с НМРЛ для иммунотерапии. Впоследствии определение экспрессии PD-L1 начало применяться для уротелиальных карцином, рака желудка. Сейчас предиктивное значение данного маркера изучается для многих видов рака.
Иммунотерапия с применением антител, которые блокируют рецептор программируемой гибели 1 (PD‑1), его лиганд (PD-L1) или белок 4, ассоциированный с цитотоксическими T-лимфоцитами (CTLA‑4), может иметь хороший и продолжительный эффект при многих видах опухолей. Однако для большинства пациентов применение ингибиторов данных контрольных точек не будет эффективным. Так, наибольшая частота ответа на иммунотерапию наблюдается у пациентов с меланомой, немелкоклеточным раком легкого (НМРЛ) и раком почки и составляет 40, 25 и 19% соответственно. Это создает необходимость поиска предиктивных маркеров ответа на иммунотерапию. Первым таким маркером стал уровень экспрессии PD-L1, который позволил более точно отбирать пациентов с НМРЛ для иммунотерапии. Впоследствии определение экспрессии PD-L1 начало применяться для уротелиальных карцином, рака желудка. Сейчас предиктивное значение данного маркера изучается для многих видов рака.
При любых локализациях логика тестирования одинакова: чем выше уровень экспрессии PD-L1 на клетках опухоли и ее микроокружении, тем выше вероятность ответа на иммунотерапию. В случае с таргетной терапией, где блокирование мишени непосредственно приводит к остановке роста опухоли, данный подход себя полностью оправдывает. Однако в случае с иммунотерапией ситуация гораздо сложнее. Именно поэтому около половины пациентов с высокой экспрессией PD-L1 не отвечают на терапию, при этом до 15% пациентов без экспрессии PD-L1 могут иметь хороший эффект от терапии.
Направленность иммунитета за или против опухоли зависит от многих факторов. Естественно, если опухоль в организме есть, это значит, что преобладают проопухолевые факторы. Одним из них действительно является экспрессия PD-L1. Общеизвестно, что активированные цитотоксические T-лимфоциты, инфильтрирующие опухоль, инактивируются в случае взаимодействия их рецептора PD‑1 с PD-L1 на клетке опухоли или ее микроокружения. Поэтому чем выше экспрессия PD‑L1, тем больше вклад этого фактора в супрессорную составляющую противоопухолевого иммунитета и, соответственно, выше шанс переключить иммунную систему применением анти-PD‑1/PD-L1-терапии. Тем не менее есть и множество других факторов, влияющих в итоге на направленность противоопухолевого иммунитета. Так, состав и пространственная организация стромы в опухолевом микроокружении также очень сильно влияет на потенциальную чувствительность к иммунотерапии. В то время как эффекторные Т-клетки опосредуют противоопухолевый ответ, другие клетки микроокружения, такие как опухоль-ассоциированные макрофаги, регуляторные Т-лимфоциты и дендритные клетки (ДК), а также некоторые другие стимулируют рост опухоли, продуцируя факторы роста и оказывая супрессорное действие на эффекторное звено иммунитета. Таким образом, если иммуносупрессия во многом обеспечивалась другими факторами кроме экспрессии PD-L1, то его блокады может оказаться недостаточно для переключения иммунитета в эффекторную фазу.
С другой стороны, если в опухолевом микроокружении преобладает эффекторный компонент, то даже при крайне низкой экспрессии PD-L1 эффекта от его блокады может оказаться достаточно, чтобы он начал реализовываться в противоопухолевую активность. Во многом преобладание в опухолевом микроокружении эффекторного или регуляторного звена иммунитета зависит от внутренних свойств конкретной опухоли.
Так, противоопухолевый иммунитет изначально запускается опухолевыми неоантигенами, которые захватываются резидентными ДК при гибели клеток опухоли. После этого ДК презентируют захваченные антигены наивным Т-лимфоцитам в регионарных лимфоузлах. Активированные Т-клетки возвращаются в опухолевое микроокружение, где уничтожают клетки, которые несут на себе данные антигены. Критическим моментом в формировании противоопухолевого иммунитета является присутствие на опухоли иммуногенных неоантигенов. Исследование различных мутаций показало, что только единичные из них являются неоантигенами, способными запускать противоопухолевый иммунитет. Так, например, исследование главного комплекса гистосовместимости опухоль-ассоциированных лимфоцитов выявило, что из ~400 мутаций-кандидатов только 2 пептида индуцировали образование антиген-специфических Т-лимфоцитов. Аналогичные результаты были получены и в других исследованиях. Таким образом, вероятность наличия на клетках опухоли иммуногенных антигенов растет с увеличением мутационной нагрузки опухоли.
Самой большой мутационной нагрузкой обладает меланома и НМРЛ, именно поэтому у пациентов с данными заболеваниями наблюдается наибольшая частота ответа. Однако высокая мутационная нагрузка может наблюдаться и в части опухолей, которые обычно не являются очень иммуногенными. В основном это связано с инактивацией систем репарации ошибок в ДНК. Одной из таких систем, нарушения в которой практически всегда приводят к высокой мутационной нагрузке опухоли, являются белки системы репарации ошибок комплементарности (MMR). В данную систему входит ряд белков, из которых чаще всего инактивируются MLH1, MSH2, MSH6 или PMS2. Кроме того, для этих опухолей характерна такая особенность, как микросателлитная нестабильность (MSI). Микросателлиты – это небольшие участки ДНК от 10 до 60 пар оснований, которые содержат множественные повторы мотивов от 1 до 5 пар оснований. Микросателлиты содержатся в особых локусах, разбросанных по всему геному. В нормальных клетках количество повторов в мотиве проверяется и поддерживается во время репликации MMR‑белками. Дефицит одного или нескольких белков из системы MMR приводит к невозможности контролировать длину микросателлитов во время репликации. Постепенно, в процессе размножения клеток с дефицитом MMR, возникают клоны с различной длиной данных повторов. Это явление называется MSI. Дефицит белков системы MMR обычно возникает путем соматической эпигенетической инактивации одного из белков (зачастую это гиперметилирование промотора гена MLH1) или наследственной мутации одного из генов (синдром Линча). Чаще всего MSI встречается у пациентов с колоректальным раком, раком эндометрия и желудка. Изначально основной целью определения MSI было выявление потенциально наследственно обусловленного рака, при подтверждении которого генетическому обследованию подлежали родственники пациента. Также было выявлено, что пациенты с II стадией колоректального рака с MSI имеют более благоприятный прогноз и им не показана адьювантная химиотерапия. Однако год назад клиническое значение MSI существенно возросло, после того как Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) 23 мая 2017 года одобрило данное показание к применению пембролизумаба. Решение было основано на результатах 5 клинических исследований Keynote с участием 149 пациентов с 15 формами рака, общей характеристикой которых было наличие MSI или дефицит MMR и прогрессия после предыдущей линии терапии. Общая частота ответа составила 39,6%, при этом продолжительность ответа – более 6 мес в 78% случаев. Регистрация нового показания для пембролизумаба спровоцировала всплеск исследований частоты встречаемости MSI практически при всех видах рака. На сегодняшний день уже накопились данные подобных многотысячных исследований. Так, в одной из работ MSI была выявлена в 27 из 39 исследуемых видов рака. При этом в 12 из них частота встречаемости MSI составила >1%. Наивысшая частота MSI наблюдается в опухолях правой половины кишечника, при раке тела матки и раке желудка. Похожие результаты были получены и в другом исследовании, которое выявило MSI в 23 из 26 видов рака. Характерной особенностью данного исследования было то, что кроме MSI исследовалась также мутационная нагрузка опухоли (МНО) и статус PD-L1. И если при колоректальном раке все пациенты с MSI имели высокую МНО, то для большинства других опухолей такое соответствие не наблюдалось. Более того, при раке из клеток Меркеля, раке мочевого пузыря, меланоме и НМРЛ MSI не была обнаружена, но при этом высокая МНО наблюдалась в 33,3; 16,8; 36,5 и 14,5% случаев. Высокая МНО в данных видах рака также часто не была связана с экспрессией PD-L1. Таким образом, актуальным является изучение эффективности иммунотерапии в опухолях, в которых присутствует либо PD‑L1, либо MSI, либо МНО, чтобы оценить независимое предиктивное значение каждого из данных маркеров.
Но на сегодняшний день универсальным показанием к применению пембролизумаба является наличие MSI, поэтому мы проанализировали собственные данные по частоте встречаемости MSI в украинской популяции пациентов с различными видами рака.
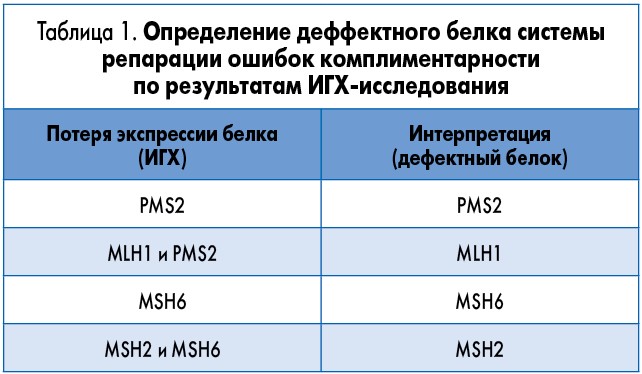 Существуют 2 основных метода определения статуса MSI. Во-первых, это определение непосредственно нестабильности в локусах микросателлитов методом ПЦР с последующим анализом длины фрагментов. Второй метод – определение дефицита белков системы репарации ДНК (MMR: MLH1, MSH2, MSH6, PMS2), потеря которых, в свою очередь, приводит к MSI. Принимая во внимание гетеродимерную природу белков MMR, следует учитывать, что потеря экспрессии одного из белков может по факту быть связана с дефектом его белка-партнера. Так, например, отсутствие экспрессии только PMS2 указывает на дефект самого PMS2, а потеря MLH1 и PMS2 связана с отсутствием MLH1, что приводит к нестабильности белка PMS2 и его деградации. То же относится к MSH6 и MSH2 соответственно (табл. 1).
Существуют 2 основных метода определения статуса MSI. Во-первых, это определение непосредственно нестабильности в локусах микросателлитов методом ПЦР с последующим анализом длины фрагментов. Второй метод – определение дефицита белков системы репарации ДНК (MMR: MLH1, MSH2, MSH6, PMS2), потеря которых, в свою очередь, приводит к MSI. Принимая во внимание гетеродимерную природу белков MMR, следует учитывать, что потеря экспрессии одного из белков может по факту быть связана с дефектом его белка-партнера. Так, например, отсутствие экспрессии только PMS2 указывает на дефект самого PMS2, а потеря MLH1 и PMS2 связана с отсутствием MLH1, что приводит к нестабильности белка PMS2 и его деградации. То же относится к MSH6 и MSH2 соответственно (табл. 1).
Цель – изучить частоту возникновения опухолей с MSI в украинской популяции пациентов с различными видами рака, проанализировать взаимосвязь статуса MSI с клиническими и биологическими характеристиками пациентов с колоректальным раком.
Материалы и методы
Всего в исследование было включено 445 пациентов с 13 видами онкологических заболеваний, которым проводилось определение MSI в лаборатории CSD Health Care (г. Киев) или в лаборатории OncoDNA в рамках молекулярного профилирования опухоли. Наибольшую группу составили пациенты с колоректальным раком, 40 из которых были обследованы в лаборатории OncoDNA и 311 – в лаборатории CSD Health Care. У остальных 94 пациентов были такие диагнозы, как рак молочной железы, желудка, эндометрия, простаты, яичников, поджелудочной железы, мочевого пузыря, почки, НМРЛ, адренокортикальный рак, гепатоцеллюлярная карцинома, глиобластома. Определение статуса MSI в лаборатории CSD Health Care проводилось с помощью иммуногистохимического (ИГХ) исследования MMR с применением антител против: MLH1 (Dako, Clone ES05), MSH2 (Dako, Clone FE11), MSH6 (Dako, Clone EP49) и PMS2 (Dako, Clone EP51). ИГХ-исследование проводили по стандартному протоколу с использованием системы детекции Dako FLEX. Опухоли с положительной ядерной реакцией со всеми 4 антителами классифицировались как микросателлитно-стабильные (MSS). При отсутствии реакции в клетках опухоли с одним или несколькими антителами и сохраненной их экспрессией в нормальных клетках (внутренний положительный контроль) классифицировали опухоль как MSI. В лаборатории OncoDNA определение статуса MSI проводилось ПЦР-методом с последующим фрагментным анализом с применением набора реактивов MSI Analysis System (Promega), который тестирует 5 мононуклеотидных (BAT‑25, BAT‑26, NR‑21, NR‑24 и MONO‑27) и 2 пентануклеотидных маркера (Penta Cand Penta D). При отрицательном результате по всем маркерам опухоль классифицировалась как MSS, при наличии нестабильности одного маркера – низкая MSI (MSI-low) и при наличии ≥2 нестабильных маркеров – высокая MSI (MSI-high). Для части пациентов с колоректальным раком также проводилось исследование мутаций в генах KRAS, NRAS, BRAF. В лаборатории CSD Health Care тестирование осуществлялось методом Real-time PCR с использованием соответствующих наборов реактивов фирмы Entrogen. В лаборатории OncoDNA тестирование проводилось методом секвенирования следующего поколения (NGS) в рамках генной панели молекулярного профилирования.
Результаты и их обсуждение
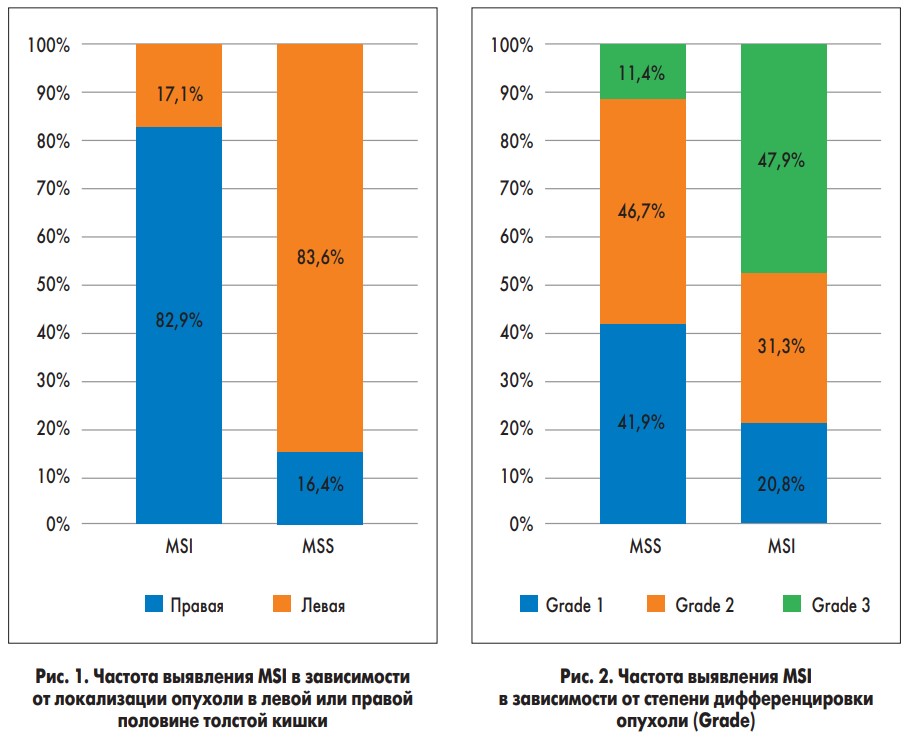
Из 351 пациента с колоректальным раком MSI была обнаружена в 50 случаях, что составило 14,2%. Клинические и биологические данные пациентов представлены в таблице 2. Пациенты с MSI были в среднем на 4 года моложе пациентов без нее (53,8 против 57,6, p=0,031), и локализация опухоли у них чаще была в правой половине кишечника (82,9% в MSI против 16,4% в MSS, p<0,001), как видно на рисунке 1.
Пациенты с MSI были в среднем на 4 года моложе пациентов без нее (53,8 против 57,6, p=0,031), и локализация опухоли у них чаще была в правой половине кишечника (82,9% в MSI против 16,4% в MSS, p<0,001), как видно на рисунке 1.
Также MSI-опухоли чаще были низкодифференцированными (Grade 3: 47,9% против 11,4%, p<0,001) (рис. 2) и имели муцинозную или медуллярную морфологию (22,4% против 7%, p<0,001).
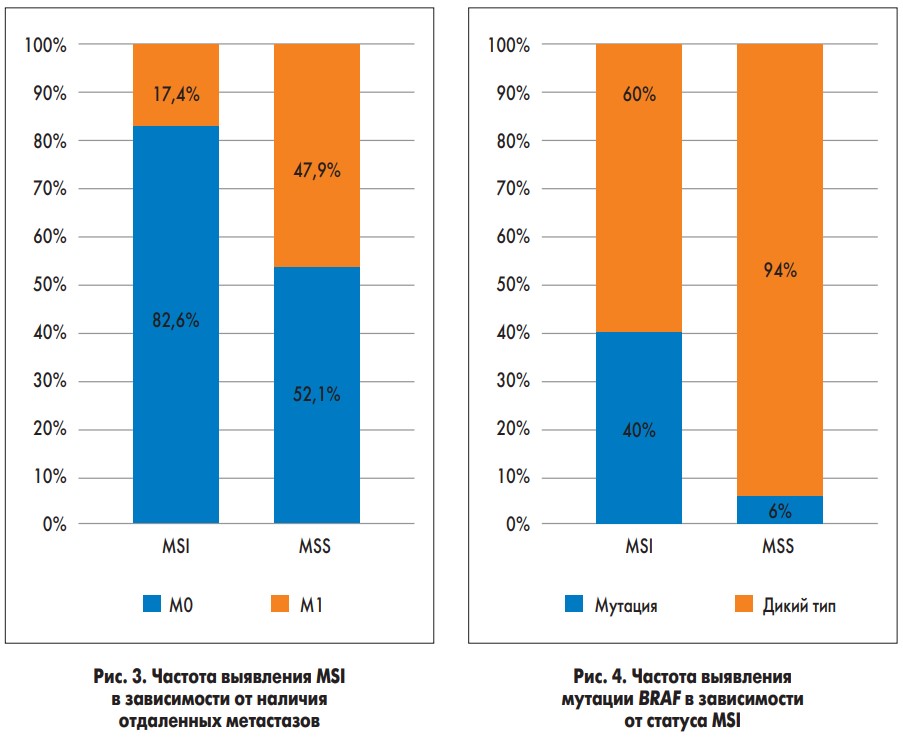
Несмотря на то, что почти половина MSI-опухолей были Grade 3 (рис. 3), эти пациенты значительно реже имели отдаленные метастазы (17,4% против 52,1%, p=0,001).
Корреляции статуса MSI с KRAS и NRAS не было обнаружено, в то время как мутация в гене BRAF существенно чаще обнаруживалась у пациентов с MSI: 40% против 6%, p=0,03 (рис. 4).
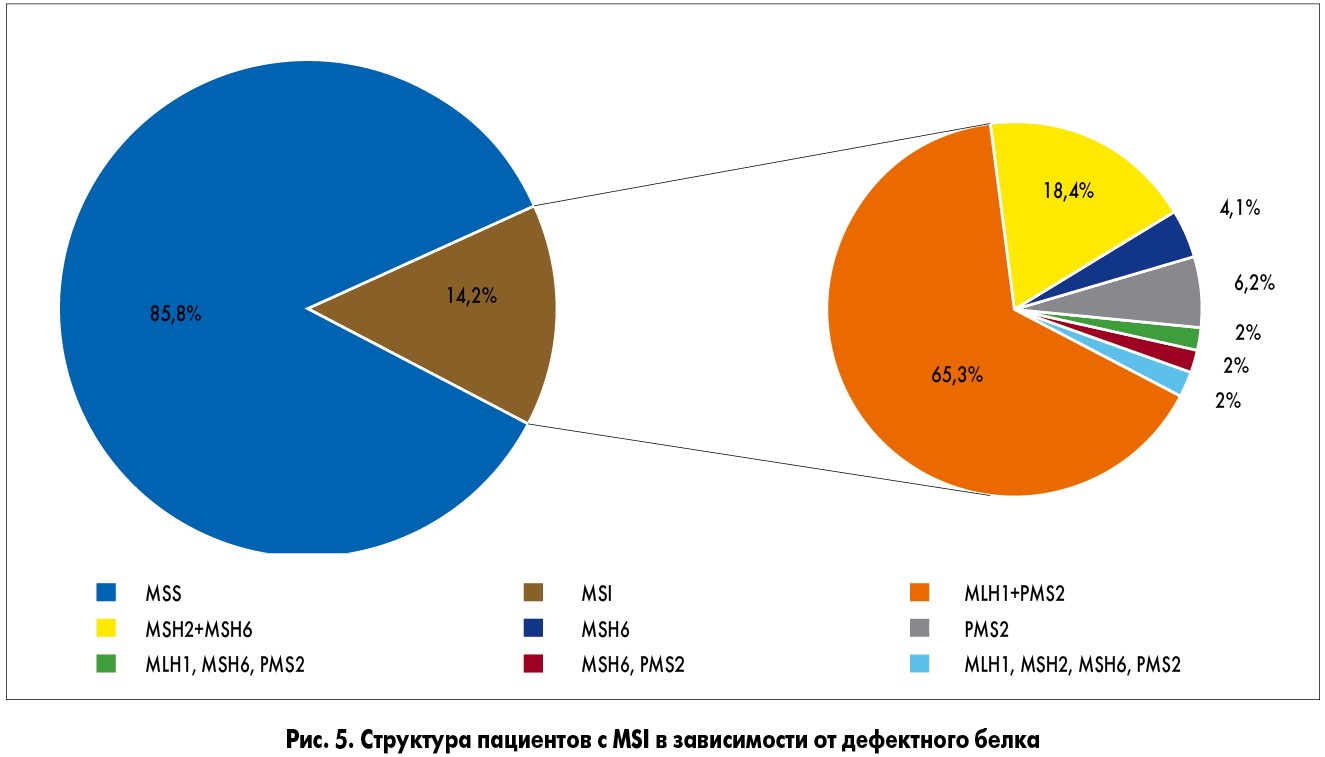
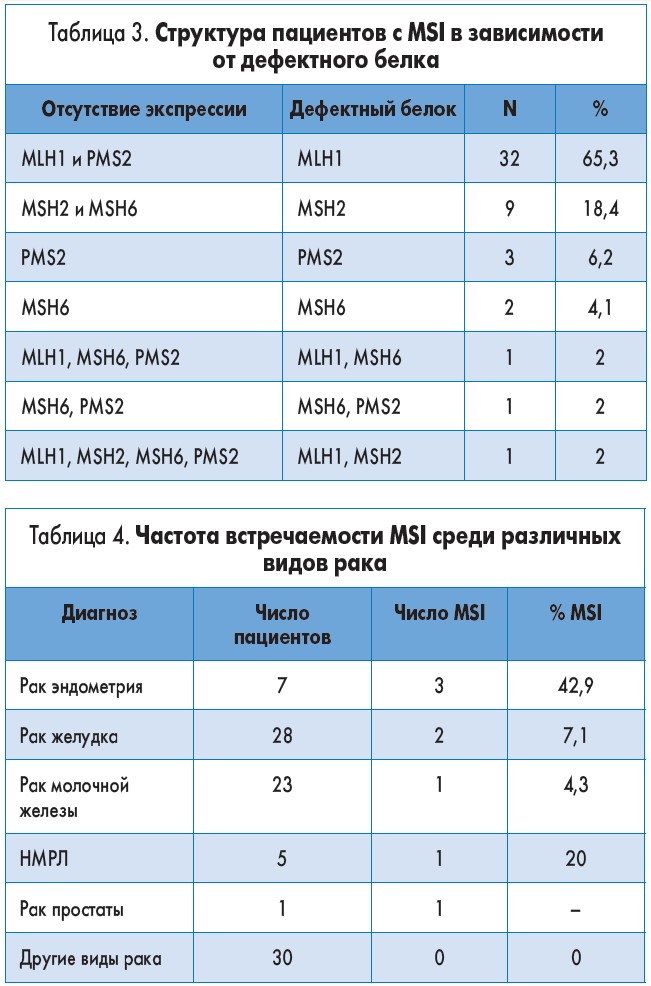
Чаще всего обнаруживался дефицит MLH1 (65,3%) и MSH2 (18,4%). Реже наблюдалась потеря PMS2 (6,2%) и MSH6 (4,1%). Структура пациентов с MSI в зависимости от дефектного белка представлена на рисунке 5. Интересно, что в трех случаях результаты ИГХ-исследования указывали на дефект сразу двух белков системы MMR (табл. 3).
Среди пациентов с другими диагнозами MSI обнаружена у 3 пациенток с раком эндометрия (42,9%), 2 с раком желудка (7,1%) и по 1 с раком молочной железы, НМРЛ и раком простаты (табл. 4).
 Среди протестированных пациентов с раком яичников, поджелудочной железы, мочевого пузыря, почки, печени, глиобластомой и адренокортикальной карциномой MSI не выявлено.
Среди протестированных пациентов с раком яичников, поджелудочной железы, мочевого пузыря, почки, печени, глиобластомой и адренокортикальной карциномой MSI не выявлено.
Полученные результаты свидетельствуют о высокой частоте MSI среди пациентов с колоректальным раком, раком эндометрия и желудка. Также данные, полученные нами в украинской популяции пациентов с колоректальным раком, согласуются с данными исследований в других популяциях: MSI чаще встречается в правой половине кишечника, данные опухоли в основном являются низкодифференцированными, однако преимущественно обнаруживаются на ранних стадиях, без отдаленных метастазов. Указанная группа опухолей зачастую имеет муцинозную или медуллярную морфологию и высокую частоту мутаций в гене BRAF. Среди других видов рака мы обнаружили MSI у пациентов с РМЖ, НМРЛ и раком простаты. Учитывая, что MSI обнаруживается, по данным литературы, более чем в 20 видах опухолей, а также то, что у этой категории пациентов независимо от локализации опухоли эффективно применение иммунотерапии пембролизумабом, актуальным является проведение тестирования пациентов с любым метастатическим раком, стандартные линии терапии которого были исчерпаны или неэффективны. Так, например, согласно данным Национального канцер-регистра, в 2016 году было выявлено 16 196 случаев рака прямой кишки. Это значит, что около 2300 пациентов имели MSI, из которых около 17%, по нашему мнению, должны быть с отдаленными метастазами. Таким образом, только среди пациентов с колоректальным раком в год в Украине появляется около 400 кандидатов на проведение иммунотерапии. А если охватить скринингом на MSI все новые случаи метастатического рака, которых в Украине в 2016 году было диагностировано около 23 000, и предположить, что MSI будет обнаружена хотя бы в 2% из них, то число кандидатов на иммунотерапию возрастает приблизительно до 860 в год только из первичных пациентов, без учета тех, у которых отмечено прогрессирование заболевания после выявления на более ранней стадии. Таким образом, актуальным является обязательное информирование пациентов о тестировании на MSI и его значении для определения возможности проведения иммунотерапии.
Выводы
- Частота выявления MSI в украинской популяции пациентов с колоректальным раком составила 14,2%.
- MSI чаще встречалась в низкодифференцированных опухолях правой половины кишечника, без отдаленных метастазов, и в таких опухолях чаще обнаруживалась мутация BRAF.
- Высокая частота MSI была также обнаружена при раке эндометрия (42,9%) и желудка (7,2%), единичные случаи – среди пациентов с РМЖ, НМРЛ, раком простаты.
- Для более точной оценки частоты MSI при онкологических заболеваниях, отличных от колоректального рака, требуется дальнейшее накопление статистических данных.
- Скрининг пациентов с метастатическими формами рака на MSI позволит выявить дополнительных кандидатов на проведение иммунотерапии и поможет повысить эффективность терапии.
Литература
- Robert C., Long G.V., Brady B., Dutriaux C., Maio M., Mortier L. et al. Nivolumab in previously untreated melanoma without BRAF mutation. N Engl J Med. 2015; 372: 320-30.
- Borghaei H., Paz-Ares L., Horn L., Spigel D.R., Steins M., Ready N.E. et al. Nivolumab versus Docetaxel in Advanced Nonsquamous Non-Small-Cell Lung Cancer. N Engl J Med. 2015; 373: 1627-39.
- Garon E.B., Rizvi N.A., Hui R., Leighl N., Balmanoukian A.S., Eder J.P. et al. Pembrolizumab for the treatment of non-small-cell lung cancer. N Engl J Med. 2015; 372: 2018-28.
- Motzer R.J., Escudier B., McDermott D.F., George S., Hammers H.J., Srinivas S. et al. Nivolumab versus Everolimus in Advanced Renal-Cell Carcinoma. N Engl J Med. 2015; 373: 1803-13.
- Hodi F.S., O’Day S.J., McDermott D.F., Weber R.W., Sosman J.A., Haanen J.B. et al. Improved Survival with Ipilimumab in Patients with Metastatic Melanoma. N Engl J Med. 2010; 363: 711-23.
- Atkins M.B., Kunkel L., Sznol M., Rosenberg S.A. High-dose recombinant interleukin‑2 therapy in patients with metastatic melanoma: long-term survival update. Cancer J Sci Am. 2000; 6 Suppl 1: S11-4.
- Fisher R.I., Rosenberg S.A., Fyfe G. Long-term survival update for high-dose recombinant interleukin‑2 in patients with renal cell carcinoma. Cancer J Sci Am. 2000; 6 Suppl 1: S55-7.
- Weber J.S., D’Angelo S.P., Minor D., Hodi F.S., Gutzmer R., Neyns B. et al. Nivolumab versus chemotherapy in patients with advanced melanoma who progressed after anti-CTLA‑4 treatment (CheckMate 037): a randomised, controlled, open-label, phase 3 trial. Lancet Oncol. 2015; 16: 375-84.
- Topalian S.L., Taube J.M., Anders R.A., Pardoll D.M. Mechanism-driven biomarkers to guide immune checkpoint blockade in cancer therapy. Nat Rev Cancer. 2016; 16: 275-87.
- Patel S.P., Kurzrock R. PD-L1 Expression as a Predictive Biomarker in Cancer Immunotherapy. Mol Cancer Ther. 2015; 14: 847-56.
- Zou W. Regulatory T cells, tumour immunity and immunotherapy. Nat Rev Immunol. 2006; 6: 295-307.
- Cohen C.J., Gartner J.J., Horovitz-Fried M., Shamalov K., Trebska-McGowan K., Bliskovsky V.V., Parkhurst M.R., Ankri C., Prickett T.D., Crystal J.S., Li Y.F., El-Gamil M., Rosenberg S.A., Robbins P.F., 2015 Oct 1. Isolation of neoantigen-specific T cells from tumor and peripheral lymphocytes. J. Clin. Invest. 125, (10) 3981-3991.
- Gros A., Robbins P.F., Yao X., Li Y.F., Turcotte S., Tran E., Wunderlich J.R., Mixon A., Farid S., Dudley M.E., Hanada K., Almeida J.R., Darko S., Douek D.C., Yang J.C., Rosenberg S.A., 2014.PD‑1 identifies the patient-specific CD8(+) tumor-reactive repertoire infiltrating human tumors. J Clin. Invest. 124, 2246-2259.
- Robbins P.F., Lu Y.C., El-Gamil M., Li Y.F., Gross C., Gartner J., Lin J.C., Teer J.K., Cliften P., Tycksen E., Samuels Y., Rosenberg S.A., 2013. Mining exomic sequencing data to identify mutated antigens recognized by adoptively transferred tumor-reactive T cells. Nat. Med. 19, 747-752.
- Tran E., Turcotte S., Gros A., Robbins P.F., Lu Y.C., Dudley M.E., Wunderlich J.R., Somerville R.P., Hogan K., Hinrichs C.S., Parkhurst M.R., Yang J.C., Rosenberg S.A., 2014. Cancer immunotherapy based on mutation-specific CD4+ T cells in a patient with epithelial cancer. Science. 344, 641‑645.
- Chen D.S., Mellman I., 2013. Oncology meets immunology: the cancer-immunity cycle. Immunity. 39, 1-10.
- van Rooij N., van Buuren M.M., Philips D., Velds A., Toebes M., Heemskerk B., van Dijk L.J., Behjati S., Hilkmann H., El Atmioui D., Nieuwland M., Stratton M.R., Kerkhoven R.M., Kesmir C., Haanen J.B., Kvistborg P., Schumacher T.N., 2013. Tumor exome analysis reveals neoantigen-specific T-cell reactivity in an ipilimumab-responsive melanoma. J. Clin. Oncol. 31, e439-e442.
- Linnemann C., van Buuren M.M., Bies L., Verdegaal E.M., Schotte R., Calis J.J., Behjati S., Velds A., Hilkmann H., Atmioui D.E., Visser M., Stratton M.R., Haanen J.B., Spits H., van der Burg S.H., Schumacher T.N., 2015. High-throughput epitope discovery reveals frequent recognition of neo-antigens by CD4+ T cells in human melanoma. Nat. Med. 21, 81-85.
- Rizvi N.A., Hellmann M.D., Snyder A., Kvistborg P., Makarov V., Havel J.J., Lee W., Yuan J., Wong P., Ho T.S., Miller M.L., Rekhtman N., Moreira A.L., Ibrahim F., Bruggeman C., Gasmi B., Zappasodi R., Maeda Y., Sander C., Garon E.B., Merghoub T., Wolchok J.D., Schumacher T.N., Chan T.A., 2015. Cancer immunology. Mutational landscape determines sensitivity to PD‑1 blockade in non-small cell lung cancer. Science. 348, 124-128.
- Snyder A., Makarov V., Merghoub T., Yuan J., Zaretsky J.M., Desrichard A., Walsh L.A., Postow M.A., Wong P., Ho T.S., Hollmann T.J., Bruggeman C., Kannan K., Li Y., Elipenahli C., Liu C., Harbison C.T., Wang L., Ribas A., Wolchok J.D., Chan T.A., 2014. Genetic basis for clinical response to CTLA‑4 blockade in melanoma. New Engl. J. Med. 371, 2189-2199.
- Schlotterer C. Genome evolution: Are microsatellites really simple sequences? Curr Biol 8: R132-R134, 1998.
- Shia J. Evolving approach and clinical significance of detecting DNA mismatch repair deficiency in colorectal carcinoma. Semin Diagn Pathol 2015; 32: 352-361.
- Strand M., Prolla T.A., Liskay R.M. et al. Destabilization of tracts of simple repetitive DNA in yeast by mutations affecting DNA mismatch repair. Nature 1993; 365: 274-276 [Erratum: Nature 368: 569, 1994].
- Armaghany T., Wilson J.D., Chu Q. et al. Genetic alterations in colorectal cancer. Gastrointest Cancer Res 2012; 5: 19-27.
- Kane M.F., Loda M., Gaida G.M. et al. Methylation of the hMLH1 promoter correlates with lack of expression of hMLH1 in sporadic colon tumors and mismatch repair-defective human tumor cell lines. Cancer Res 1997; 57: 808-811.
- Aaltonen L.A., Peltomaki P., Leach F.S. et al. Clues to the pathogenesis of familial colorectal cancer. Science 1993; 260: 812-816.
- Lynch H.T., Shaw M.W., Magnuson C.W. et al. Hereditary factors in cancer. Study of two large midwestern kindreds. Arch Intern Med 1966; 117: 206-212.
- Imai K., Yamamoto H. Carcinogenesis and microsatellite instability: The interrelationship between genetics and epigenetics. Carcinogenesis 2008; 29: 673-680.
- Watson P., Lynch H.T. The tumor spectrum in HNPCC. Anticancer Res 1994; 14: 1635-1639.
- Buckowitz A., Knaebel H.P., Benner A. et al. Microsatellite instability in colorectal cancer is associated with local lymphocyte infiltration and low frequency of distant metastases. Br J Cancer 2005; 92: 1746-1753.
- Benatti P., Gafa R., Barana D. et al. Microsatellite instability and colorectal cancer prognosis. Clin Cancer Res 2005; 11: 8332-8340.
- Le D.T., Durham J.N., Smith K.N., Wang H., Bartlett B.R., Aulakh L.K., Lu S., Kemberling H., Wilt C., Luber B.S. et al. Mismatch repair deficiency predicts response of solid tumors to PD‑1 blockade. Science. 2017; 357(6349): 409-13.
- Russell Bonneville, Melanie A. Krook, Esko A. Kautto, Jharna Miya, Michele R. Wing, Hui-Zi Chen, Julie W. Reeser, Lianbo Yu, Sameek Roychowdhury JCO Precision Oncology. 2017; 1: 1-15.
- Vanderwalde A., Spetzler D., Xiao N., Gatalica Z., Marshall J. Microsatellite instability status determined by next-generation sequencing and compared with PD-L1 and tumor mutational burden in 11,348 patients. Cancer Med. 2018 Mar; 7(3): 746-756.
- Richman S. Deficient mismatch repair: Read all about it (Review). International Journal of Oncology, 2015; 47: 1189-1202. https://doi.org/10.3892/ijo.2015.3119.
Настоящая публикация издана при поддержке компании MSD.
Информация предоставлена компанией MSD для профессиональной поддержки специалистов сферы здравоохранения. Информация, относящаяся к любому продукту(-ам), может не совпадать с инструкцией по применению препарата. Пожалуйста, ознакомьтесь с полным текстом инструкции для получения точной информации или данных по продуктам, рассматриваемым в настоящей публикации, до назначения.
ONCO-1278477-0000
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 5 (56), грудень 2018 р