6 січня, 2019
Эффективность энзалутамида в лечении пациентов с неметастатическим кастрационно-резистентным раком предстательной железы
Больные неметастатическим кастрационно-резистентным раком предстательной железы (КРРПЖ) c быстрым повышением уровня простатспецифического антигена (ПСА) относятся к группе высокого риска метастазирования. Известно, что применение энзалутамида способствует продлению общей выживаемости пациентов с метастатическим КРРПЖ. Ученые высказали предположение, что указанный препарат способен предотвратить развитие метастазов у мужчин с неметастатической формой КРРПЖ. Предлагаем обзор статьи международной группы экспертов M. Hussain, K. Fizazi, F. Saad и соавт., опубликованной в The New England Journal of Medicine в июне этого года. В ней представлены результаты мультицентрового рандомизированного исследования PROSPER.
Медиана выживаемости без костных метастазов у мужчин с неметастатическим КРРПЖ колеблется от 25 до 30 мес. Риск метастазирования связан с повышением уровня ПСА и временем его удвоения ≤10 мес. Метастатический КРРПЖ – неизлечимое заболевание с медианой выживаемости около 3 лет. Отсрочка образования метастазов клинически значима, поскольку способствует более позднему развитию связанных с онкопатологией осложнений и продлению выживаемости пациентов. В соответствии с действующим гайдлайном Национальной комплексной онкологической сети США (NCCN) по ведению пациентов с раком предстательной железы рекомендуется наблюдение, если время удвоения ПСА равно ≥10 мес, и лечение с применением второй линии гормональной терапии, если этот показатель составляет <10 мес. В Европе наблюдение в сочетании с непрерывной андрогенной депривацией считается стандартом лечения пациентов с неметастатическим КРРПЖ независимо от времени удвоения ПСА.
Энзалутамид конкурентно ингибирует связывание андрогенов с андрогенными рецепторами, угнетает ядерную транслокацию активированных рецепторов и ингибирует связывание активированных рецепторов андрогенов с ДНК. Его влияние на общую выживаемость было показано в двух международных исследованиях ІІІ фазы с участием пациентов с метастатическим КРРПЖ до и после приема доцетаксела. Кроме того, в рандомизированном исследовании II фазы STRIVE (сравнение эффективности энзалутамида и бикалутамида у больных неметастатическим и метастатическим КРРПЖ, ранее не получавших химиотерапию) было продемонстрировано, что лечение энзалутамидом способствует продлению выживаемости без признаков радиологического прогрессирования в подгруппе пациентов с неметастатическим КРРПЖ (относительный риск – ОР – радиологического прогрессирования или смерти от рака 0,24; 95% доверительный интервал – ДИ – 0,14-0,42).
Материал и методы исследования
Дизайн и участники
Рандомизированное двойное слепое плацебо-контролируемое исследование III фазы PROSPER было проведено более чем в 300 центрах в 32 странах. В исследование включали пациентов с гистологически подтвержденной аденокарциномой предстательной железы без нейроэндокринной дифференцировки, признаков перстневидноклеточной или мелкоклеточной карциномы; с повышенным уровнем ПСА, несмотря на кастрационный уровень тестостерона (1,73 нмоль/л, или 0,50 нг/мл); наличием трех повышенных значений уровня ПСА, определявшихся с интервалом не менее 1 недели; исходным уровем ПСА ≥2 нг/мл и временем удвоения ПСА ≤10 мес. Кроме того, к участию в исследовании допускались пациенты, получавшие андрогендепривационную терапию с применением агониста или антагониста гонадотропин-рилизинг-гормона или подвергшиеся двусторонней орхиэктомии. Одним из критериев включения также было отсутствие отдаленных метастазов по данным компьютерной или магнитно-резонансной томографии мягких тканей и сцинтиграфии скелета.
Критериями исключения из исследования стали: подозрение на метастазы в мозге; наличие заболевания оболочек мозга; судороги или предрасположенность к таковым в анамнезе.
Пациенты были стратифицированы в зависимости от времени удвоения уровня ПСА (<6 и ≥6 мес) и наличия/отсутствия в анамнезе применения остеомодифицирующих препаратов. Больных рандомизировали в 2 группы в соотношении 2:1. Пациенты первой группы принимали энзалутамид в дозе 160 мг, второй – плацебо. Лечение в обеих группах проводили до появления признаков прогрессирования, зафиксированного методами лучевой диагностики. Рост уровня ПСА без появления отдаленных метастазов не рассматривался как повод для прекращения терапии. Таковое допускалось при появлении признаков клинического прогрессирования или развитии токсических реакций.
Конечные точки
Первичной конечной точкой была выживаемость без метастазирования, которая определялась как время от рандомизации до радиологического прогрессирования или до смерти больного по любой причине (в течение периода от рандомизации до 112 дней после прекращения приема исследуемого препарата) в отсутствие признаков радиологического прогрессирования, в зависимости от того, что произошло раньше.
Вторичные конечные точки включали период до прогрессирования, определяемого по уровню ПСА, частоту ответа по уровню ПСА (снижение на 50% от исходного), время до начала другой противоопухолевой терапии, оценку качества жизни, общую выживаемость и безопасность.
Результаты
В общей сложности в исследование был включен 1401 пациент: 933 пациента – в группу энзалутамида и 468 – в группу плацебо. Группы были равнозначными по исходным клиническим и демографическим характеристикам участников (табл. 1). Медиана периода удвоения уровня ПСА у всех пациентов составила 3,7 мес. Всего 1395 рандомизированных больных получили хотя бы одну дозу энзалутамида или плацебо. Медиана длительности терапии составила 18,4 мес в группе энзалутамида и 11,1 мес в группе плацебо. На момент окончания сбора данных 810 пациентов продолжали лечение (634 – в группе энзалутамида и 176 – в группе плацебо). Наиболее частыми причинами прекращения терапии были прогрессирование заболевания у участников 1 и 2-й групп (15 и 44% соответственно) и развитие побочных эффектов (10 и 6% больных соответственно).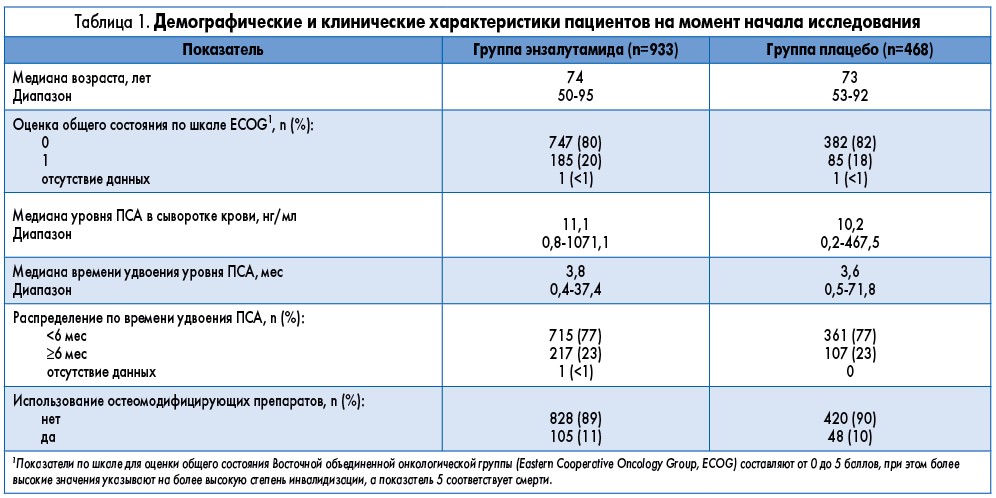
Первичная конечная точка
На момент анализа данных события, соответствующие первичной конечной точке, были зафиксированы у 219 (23%) больных в группе энзалутамида и у 228 (49%) в группе плацебо. Медиана выживаемости без метастазирования в группе энзалутамида составила 36,6 мес, в группе плацебо – 14,7 мес (табл. 2; рис. 1). Таким образом, терапия энзалутамидом приводила к снижению риска радиологического прогрессирования или летального исхода на 71% по сравнению с плацебо (ОР 0,29; 95% ДИ 0,24-0,35; р<0,001).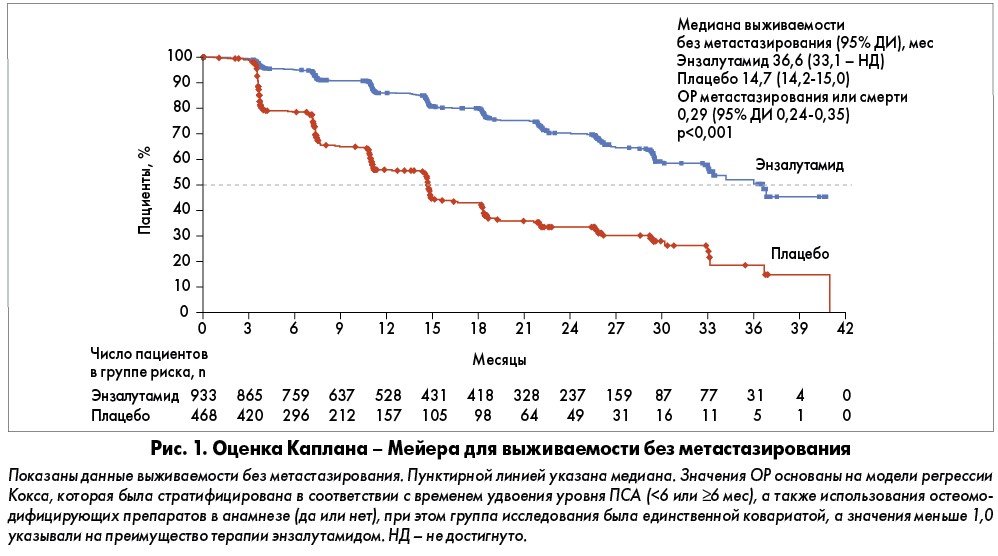
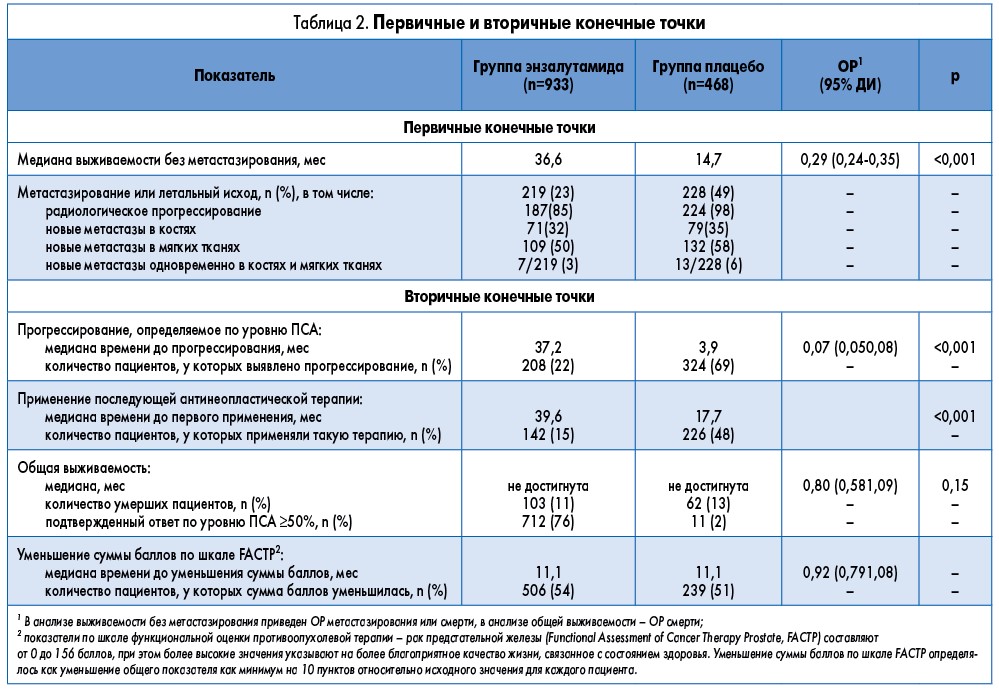 Из 219 пациентов группы энзалутамида у 187 (85%) было отмечено радиологическое прогрессирование, 32 (15%) пациента умерли при отсутствии признаков такового. Из 228 участников из группы плацебо, у которых возникло явление, рассматриваемое как первичная конечная точка, у 224 (98%) было отмечено радиологическое прогрессирование, 4 (2%) пациента умерли при отсутствии признаков такового. Более половины случаев радиологического прогрессирования в группе энзалутамида и группе плацебо приходилось на поражение мягких тканей (58 и 59% соответственно).
Из 219 пациентов группы энзалутамида у 187 (85%) было отмечено радиологическое прогрессирование, 32 (15%) пациента умерли при отсутствии признаков такового. Из 228 участников из группы плацебо, у которых возникло явление, рассматриваемое как первичная конечная точка, у 224 (98%) было отмечено радиологическое прогрессирование, 4 (2%) пациента умерли при отсутствии признаков такового. Более половины случаев радиологического прогрессирования в группе энзалутамида и группе плацебо приходилось на поражение мягких тканей (58 и 59% соответственно).
Вторичные конечные точки
Терапия с применением энзалутамида была более эффективной по сравнению с плацебо в отношении ключевых вторичных конечных точек: времени до прогрессирования, определяемого по уровню ПСА, и времени до первого применения последующей противоопухолевой терапии (табл. 2; рис. 2). Средний период между прекращением исследуемого лечения и назначением другой терапии составил 25 дней в группе энзалутамида и 18 – в группе плацебо. В общей сложности у 138 (15%) пациентов в группе энзалутамида и у 222 (48%) в группе плацебо было прекращено лечение в рамках исследования и начата последующая противоопухолевая терапия. Наиболее часто с этой целью применялся абиратерона ацетат (38% в группе энзалутамида и 36% в группе плацебо).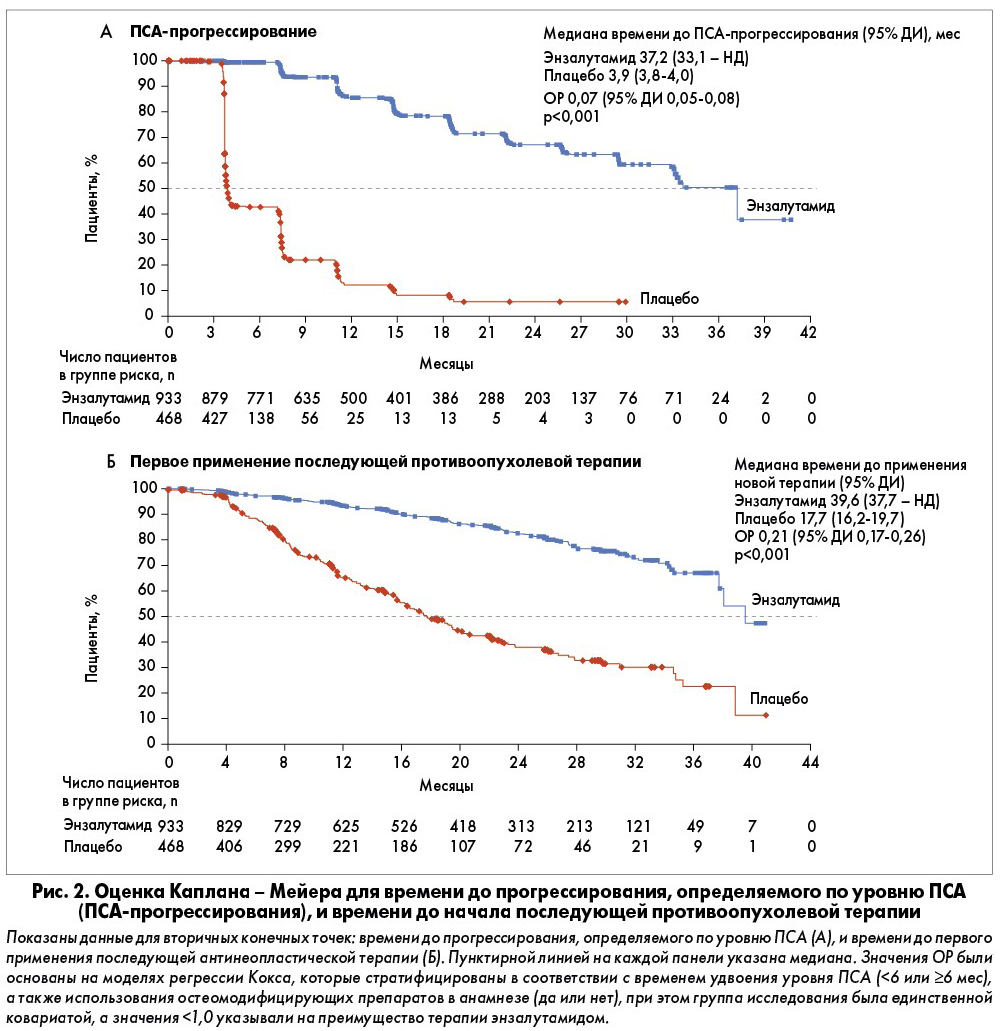
На момент первого промежуточного анализа общей выживаемости умерли 103 (11%) пациента в группе энзалутамида и 62 (13%) в группе плацебо (табл. 2). Ни в одной из групп не была достигнута медиана общей выживаемости. Частота достижения ответа уровня ПСА ≥50% была выше в группе энзалутамида по сравнению с группой плацебо.
Безопасность
Наиболее часто отмечавшимся нежелательным явлением у пациентов, получавших энзалутамид, была утомляемость. Нежелательными явлениями, вызывающими особую обеспокоенность, которые возникали чаще (на ≥2%) в группе энзалутамида, чем в группе плацебо, независимо от их связи с исследуемым режимом терапии, были гипертензия (12 против 5% соответственно), значительные нарушения сердечно-сосудистой системы (5 против 3% соответственно) и психической деятельности (5 против 2% соответственно). У 3 пациентов, получавших энзалутамид, возникли судороги, которые были оценены как серьезное нежелательное явление, вызванное применением лекарственного препарата и развившееся в течение 180 дней после начала приема энзалутамида. Один пациент с судорогами прекратил терапию энзалутамидом, у другого возникло осложнение, приведшее к летальному исходу. Больший процент участников из группы энзалутамида сообщили о случаях падения и непатологических переломов по сравнению с группой плацебо (17 против 8% соответственно).
Наиболее частыми нежелательными явлениями, вызвавшими смерть пациентов, были сердечно-сосудистые события – у 9 (1%) пациентов, принимавших энзалутамид, и у 2 (<1%) – получавших плацебо. В группе энзалутамида у 6 больных развился острый инфаркт миокарда и наблюдалось по одному случаю сердечной недостаточности, остановки сердца и желудочковой аритмии. В группе плацебо зарегистрировано по одному случаю остановки сердца и левожелудочковой недостаточности. В каждой группе частота серьезных неблагоприятных кардиальных событий была выше у пациентов, изначально имевших в анамнезе сердечно-сосудистые заболевания, артериальную гипертензию, сахарный диабет или гиперлипидемию либо возраст ≥75 лет.
Обсуждение
У пациентов с неметастатическим КРРПЖ и быстрым повышением уровня ПСА, получавших энзалутамид, наблюдался значительный рост выживаемости без метастазирования, увеличение времени до прогрессирования, определяемого по уровню ПСА, а также периода до назначения другой противоопухолевой терапии. Лечение энзалутамидом способствует снижению риска метастазирования или летального исхода на 71% по сравнению с плацебо. В процессе лечения не обнаружено ухудшения качества жизни пациентов в связи с приемом энзалутамида.
Несмотря на то что в обеих исследуемых группах медиана общей выживаемости не была достигнута, риск смерти оказался ниже на 20% при применении энзалутамида. Общий показатель смертности по любой причине был ниже в группе энзалутамида (11 против 13% в группе плацебо). Не отмечено какой-либо закономерности относительно причины смерти у умерших пациентов без признаков радиологического прогрессирования. Только в двух случаях исследователи оценили летальный исход как связанный с применением энзалутамида. В большинстве случаев смерть наступила в результате острого нарушения жизнедеятельности у пациентов преклонного возраста, состояние которых было отягощено сопутствующими заболеваниями.
Результаты изучения профиля безопасности энзалутамида согласовывались с таковыми, полученными в предыдущих клинических исследованиях с участием пациентов с КРРПЖ. В группе энзалутамида отмечено более частое развитие нежелательных явлений. Дальнейший анализ безопасности данного препарата с целью оценки риска развития побочных эффектов у этой категории больных продолжается.
Традиционно ведение пациентов с неметастатическим КРРПЖ включает динамическое наблюдение или использование препаратов, имеющих умеренную активность и не продемонстрировавших преимуществ в отношении общей выживаемости. Целью лечения является отсрочка прогрессирования заболевания, уменьшение ассоциированных с раком симптомов и продление общей выживаемости. В предыдущих исследованиях III фазы, в которых оценивали эффективность экспериментальных лекарственных средств, в качестве первичной конечной точки использовался показатель выживаемости без метастазирования в кости или метастазирования в целом. В этих исследованиях продемонстрировано незначительное увеличение периода до прогрессирования процесса.
Таким образом, у пациентов с неметастатическим КРРПЖ и быстрым повышением уровня ПСА лечение энзалутамидом приводит к значительному увеличению периода до развития метастазов, а также времени до прогрессирования, определяющегося по уровню ПСА, и до первого использования последующей противоопухолевой терапии. При этом не наблюдается различий в качестве жизни больных, получающих энзалутамид или плацебо.
По материалам: M. Hussain, K. Fizazi, F. Saad et al. Enzalutamide in Men with Nonmetastatic, CastrationResistant Prostate Cancer. N Engl J Med. 2018; 378: 24652474.
Подготовила Виктория Лисица
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 5 (56), грудень 2018 р


