23 січня, 2019
Вплив аеробних вправ та вітаміну С на симптоматику в пацієнтів з алергійним ринітом
Алергійний риніт (АР) – поширена хвороба, спричинена порушенням функціонування імунної системи у відповідь на реакцію гіперчутливості до алергенів, що надходять до слизової оболонки носа. Клінічними проявами АР є свербіння, закладеність носа, чхання, ринорея [1].
У порожнині носа алергени підлягають впливу специфічного імуноглобуліну Е (IgE), який зв’язується з відповідними рецепторами на поверхні мастоцитів і базофілів, стимулюючи вивільнення таких хімічних медіаторів, як гістамін, лейкотрієни, цитокіни. Ці медіатори запускають процеси появи симптомів АР [2]. Велика кількість нещодавніх досліджень продемонструвала зростання рівня інтерлейкіну (ІЛ)-4 у пацієнтів з АР. Інший цитокін – ІЛ‑2 – навпаки індукує активацію макрофагів, яка дозволяє контролювати інфекцію, у т. ч. викликану внутрішньоклітинними патогенами.
Пацієнти з АР відчувають неабиякий дискомфорт, несуть чималі фінансові витрати, пов’язані з прийомом місцевих та системних ліків, страждають проявами побічних ефектів лікування та мають погіршену якість життя [3]. Аеробні вправи були рекомендовані як дієве ад’ювантне лікування симптомів у пацієнтів з низкою патологічних станів [4-7]. Однак попередні дослідження продемонстрували, що стрімкий початок високоінтенсивних фізичних вправ може спричинити погіршення симптомів риніту [8]. Крім того, доведено, що високоінтенсивне навантаження здатне знижувати об’єм форсованого видиху за 1-у секунду [9] та підвищувати рівень IgE [10] у пацієнтів з АР. Нещодавно Tongtako і співавт. [11] повідомили, що і виснажливе, і помірно інтенсивне фізичне навантаження зменшують вираженість симптомів АР. Але після тренування помірної інтенсивності було зафіксовано значне підвищення співвідношення ІЛ‑2/ІЛ‑4. Слід зазначити, що ІЛ‑2 є критично важливим для підтримки активації T-лімфоцитів, запобігання аутоімунним процесам та контролю інфекції, саме тоді ІЛ‑4 діє як координатор запальних процесів дихальних шляхів за умов алергічних захворювань. Тобто з цих результатів випливає, що помірно інтенсивне аеробне навантаження є більш ефективним для контролю над симптомами АР [11-12]. Silva і співавт. [12] стверджують, що аеробне тренування збільшує рівень плазмових IgE; знижує кількість еозинофілів та концентрації ІЛ‑4, -5, -13; мінімізує ремоделювання дихальних шляхів; зменшує синтез слизу та товщину непосмугованого м’язового шару у моделі алергійного захворювання дихальних шляхів на тваринах.
Результати досліджень продемонстрували, що вітамін C (аскорбінова кислота) є важливим антиоксидантом, який застосовується для профілактики та лікування різноманітних хвороб [13-15]. Вважається, що дефіцит вітаміну С спричиняє імуносупресію, а сам вітамін може діяти як протизапальний агент, пригнічуючи секрецію цитокінів [16]. Але дані стосовно впливу вітаміну С на симптоми АР досі є суперечливими. Однак Helms та Miller стверджують, що аерозольне нанесення вітаміну C на слизову оболонку носа знижує вираженість симптомів, зменшуючи кількість агентів, які стимулюють закладеність та набряк носової порожнини [17]. Доведено також, що призначення щонайменше 2 г вітаміну С на день запобігає вивільненню гістаміну з лейкоцитів. Цей факт може слугувати певним підґрунтям для створення інноваційного лікування АР [18]. На противагу цьому, деякі дослідження виявили відсутність впливу вітаміну С на сенсибілізацію до алергенів та АР [19, 20].
Оскільки помірне аеробне навантаження виявилося дієвим засобом покращення стану здоров’я пацієнтів з АР [11-12], а наявна на цей час інформація стосовно вітаміну С є неоднозначною, виникло питання, чи здатне поєднання цих засобів чинити більш виражений протективний ефект за умов АР, ніж тільки аеробне тренування. Первинною ціллю даного дослідження стала оцінка ефективності аеробного фізичного навантаження помірної інтенсивності у вигляді монотерапії та в поєднанні з вживанням вітаміну С на симптоми риніту, секрецію цитокінів слизовою оболонкою порожнини носа, назальний кровотік (НК) та піковий назальний інспіраторний потік (ПНІП). Згідно з гіпотезою авторів, помірне аеробне навантаження у поєднанні з прийомом вітаміну C може бути більш дієвим засобом зниження алергійної відповіді у пацієнтів з АР.
Матеріали та методи. У дослідженні взяли участь 33 пацієнти з симптоматичним АР віком 18-45 р. Критеріями АР вважалися закладеність носа, чхання, свербіж носа, ринорея більше 4 днів на тиждень та позитивний шкірний прік-тест (діаметром >3 мм) на антигени побутового пилового кліща (D. pteronyssimus). Особи з астмою, хронічним риносинуситом, артеріальною гіпертензією чи іншими кардіоваскулярними захворюваннями, а також курці залишили дослідження. Для виключення анатомічних аномалій проводилася передня риноскопія. Учасників просили утриматися від вживання антигістамінних засобів упродовж щонайменше 3 днів до проведення обстежень і від пероральних та інтраназальних кортикостероїдів – упродовж щонайменше 2 тиж до початку дослідження. Також учасники припиняли прийом антагоністів рецепторів лейкотрієну щонайменше за 1 тиж до проведення обстежень; не займалися регулярними фізичними навантаженнями щонайменше 6 міс до початку дослідження і уникали прийому будь-яких дієтичних добавок під час іспитів. Учасників було рандомізовано в 3 групи: група контролю (без фізичного навантаження та прийому вітаміну С), група аеробних вправ у поєднанні з прийомом плацебо та група комбінації аеробних вправ та прийому вітаміну С. Дослідження тривало 8 тиж.
Фізичне навантаження учасників передбачало розминку/розтяжку (5 хв), ходьбу/біг на біговій доріжці з інтенсивністю 65-70% резерву частоти серцевих скорочень (приблизно 40 хв), заминку (5 хв) 3 рази на тиждень. Вітамін С учасники вживали двічі на день у дозі 1000 мг (зранку та ввечері) упродовж 2 міс. Дослідники оцінювали показники роботи серця відповідно до даних електрокардіографії, складу тіла за даними імпедансометрії, легеневої функції за допомогою пневмотахографічного спірометра. Також було проведено біохімічний аналіз крові з визначенням вмісту IgE, плазмової концентрації вітаміну С, малонового діальдегіду. Під час виконання фізичного навантаження постійно проводилися контроль частоти серцевих скорочень та аналіз видихуваних газів. Симптоми риніту оцінювалися за опитувальником TNSS (Total Nasal Symptom Score) [22] до та після кожного виконання вправ. Оцінка за TNSS розраховувалась як сума рівнів чотирьох окремих симптомів: закладеність носа, свербіння, чхання, ринорея. Бали варіювалися від 0 до 3 (0 – симптом відсутній, 1 – незначно виражений, 2 – помірно виражений, 3 – тяжкий). Крім вимірювання ПНІП та НК, пацієнтам проводилася провокаційна проба (вдихання алергенів пилового кліща) з вимірюванням рівнів ІЛ‑2 та ІЛ‑4 (стартово і через 5 хв після проби). Проби виділень з носа отримувалися за допомогою фільтрувального паперу.
Дослідження завершили 27 пацієнтів (8 – у групі контролю, 9 – у групі вправ, 10 – у групі вправ та вітаміну С). Групи суттєво не відрізнялися за рівнем артеріального тиску, функції легень, загального та специфічного IgE. І в групі аеробного навантаження, і в групі аеробного навантаження в поєднанні з прийомом вітаміну С через 8 тиж спостерігались достовірне підвищення пікового об’єму O2, а також достовірне зниження частоти серцевих скорочень у спокої та малонового діальдегіду плазми (всі р<0,05). Ці результати також достовірно відрізнялися від показників групи контролю. Концентрація та застосування вітаміну С у групі аеробного навантаження були достовірно вищими, ніж до початку дослідження (p=0,012) та у групі контролю (p=0,022) і групі фізичних вправ (p=0,027). Відмінностей у рівнях загального та специфічного IgE виявлено не було. Щодо симптомів риніту, через 8 тиж вони істотно зменшились як у групі аеробних вправ, так і в групі комбінації даних засобів. Зниження вираженості ознак захворювання було достовірним для закладеності носа (p=0,015, p=0,002), свербежу (p=0,009, p=0,004), чхання (p=0,013, p=0,005), ринореї (p=0,012, p=0,014), а також сукупної оцінки симптомів (p=0,001, p=0,002). Загальний рівень симптомів риніту за TRSS був достовірно нижчим у групі аеробного навантаження та вітаміну С проти вихідного рівня та групи контролю. У групі вправ результат був також кращим за показники контрольної групи. Після провокаційної проби у групі контролю не спостерігалося жодних змін у порівнянні з вихідними показниками, однак у обох групах хворих показники симптомів риніту істотно знизилися при вимірюванні на 15, 30, 45 та 60 хвилинах проти вихідних вимірів.
У обох групах втручання (вправи / вправи + вітамін С) також достовірно збільшився ПНІП (p=0,000; p=0,016 відповідно) та знизився НК (p=0,002; p=0,018) у порівнянні з результатами вихідних вимірів. Показники групи контролю не змінилися. Подібна тенденція була виявлена при оцінці ПНІП та НК після провокаційної проби.
Під час стартових вимірів між трьома групами не було виявлено різниці в рівнях цитокінів (ІЛ‑2, ІЛ‑4) у виділеннях з носової порожнини. Однак через 8 тиж і в групі аеробного навантаження, і в групі аеробних вправ та прийому вітаміну С визначалися достовірно вищі (p=0,024, p=0,019 відповідно) показники ІЛ‑2 та достовірно нижчі (p=0,012, p=0,025) показники ІЛ‑4, ніж у групі контролю. ІЛ‑4 також знизився у порівнянні з вихідним показником. Такі ж результати були зафіксовані після проведення провокаційної проби.
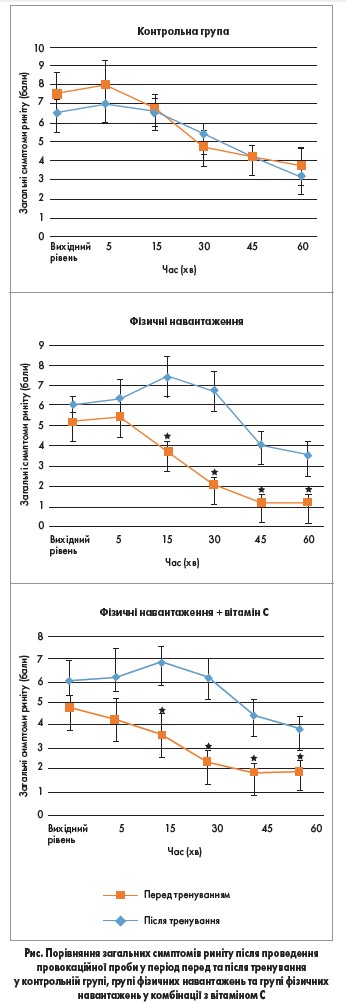 Отже, головне відкриття даного дослідження полягає в тому, що фізичні вправи як самостійно, так і в поєднанні з вживанням вітаміну С зменшують вираженість симптомів риніту у пацієнтів з АР (рис.). Покращення клінічної картини супроводжувалося зменшенням НК та ПНІП, а також зростанням ІЛ‑2 на тлі зниження ІЛ‑4. Рівні загального та специфічного IgE до пилового кліща після дослідження не змінилися. Зменшення симптомів риніту після аеробного фізичного навантаження може бути результатом зниження загального носового опору внаслідок падіння інтенсивності симпатичної вазоконстрикції у слизовій оболонці носа [23]. Зниження носового опору також може бути спричинене зниженням кровотоку [24], яке веде до зменшення закладеності носа [25]. Виявлене зростання ПНІП після аеробного навантаження відповідає результатам Marioni і співавт. [26], які довели чутливість та надійність ПНІП як показника прохідності носа, яка покращується після фізичних вправ.
Отже, головне відкриття даного дослідження полягає в тому, що фізичні вправи як самостійно, так і в поєднанні з вживанням вітаміну С зменшують вираженість симптомів риніту у пацієнтів з АР (рис.). Покращення клінічної картини супроводжувалося зменшенням НК та ПНІП, а також зростанням ІЛ‑2 на тлі зниження ІЛ‑4. Рівні загального та специфічного IgE до пилового кліща після дослідження не змінилися. Зменшення симптомів риніту після аеробного фізичного навантаження може бути результатом зниження загального носового опору внаслідок падіння інтенсивності симпатичної вазоконстрикції у слизовій оболонці носа [23]. Зниження носового опору також може бути спричинене зниженням кровотоку [24], яке веде до зменшення закладеності носа [25]. Виявлене зростання ПНІП після аеробного навантаження відповідає результатам Marioni і співавт. [26], які довели чутливість та надійність ПНІП як показника прохідності носа, яка покращується після фізичних вправ.
Алергійне запалення асоціюється з продукцією ІЛ‑4, -13 та -5, відповідальних за продукцію B-клітинами IgE, активацію еозинофілів, виробіток слизу [2]. Нещодавнє дослідження виявило, що у назальному слизі пацієнтів з АР відзначаються вищі рівні ІЛ‑4, ніж у групі контролю без алергії [27]. На противагу цьому, диференційовані Th1-клітини секретують інтерферон-γ та ІЛ‑2, що беруть участь у внутрішньоклітинному руйнуванні фагоцитованих мікробів [28]. У даному експерименті 8 тиж аеробного навантаження не призводили до змін загального та специфічного IgE до пилового кліща, однак рівні ІЛ‑4 істотно зменшилися порівняно з вихідними показниками (як у звичайних умовах, так і після провокаційної проби). Існує думка, що аеробне навантаження здатне призводити до зниження рівня ІЛ‑4 [29-30], хоча Shimizu і співавт. [31] продемонстрували, що помірно інтенсивні тренування 5 днів/тиж упродовж 6 міс не забезпечували жодних змін у концентрації цього цитокіну.
Вищезгадане дослідження також виявило зростання ІЛ‑2 у назальному секреті після аеробних тренувань порівняно з групою контролю. Arai та співавт. [32] вказують, що тривале тренування здатне підвищувати виробіток ІЛ‑2 до рівнів, які можна зіставити з показниками молодих осіб чоловічої статі, тобто запобігати імуностарінню. Автори даного дослідження вважають, що клінічне покращення у пацієнтів з АР може бути наслідком змін цитокінового профілю після регулярних фізичних навантажень. Попередні досліди показали, що протизапальні ефекти аеробних тренувань можуть бути спричинені зниженням рівнів ІЛ‑4, -5, IgE та паралельним зростанням протизапальних цитокінів [29-30]. Механізм модуляції цитокінової відповіді аеробним навантаженням точно не встановлені. Імовірно, зокрема, що зростання пікового об’єму O2 після вправ знижує вираженість оксидативного стресу, що зі свого боку міняє патерн експресії запальних цитокінів [34]. Також покращення запального статусу організму під впливом помірних аеробних вправ може спричинятися зменшенням міграції антиген-специфічних T-хелперів через зниження функції хемокінових рецепторів у цих осіб [34]. Оскільки після 8 тиж аеробних тренувань знизився рівень малонового діальдегіду плазми, автори вважають, що помірні аеробні тренування послаблюють оксидативний стрес, можливо, внаслідок змін цитокінової відповіді носової секреції після навантаження.
Даний експеримент довів, що носові симптоми, ПНІП та НК у обох групах втручання суттєво покращилися порівняно з вихідними показниками, на відміну від групи контролю. Між групами аеробного навантаження та навантаження в поєднанні з вживанням вітаміну С істотної різниці не відзначалось. На думку авторів, оскільки в учасників спостерігався нормальний рівень вітаміну С до експерименту (0,6-2,0 мг/дл) [35], призначення цього вітаміну під час дослідження не забезпечило жодних додаткових покращень клінічної картини. Однак існує потреба в подальших дослідженнях з визначенням різних доз аскорбінової кислоти.
Дане спостереження має низку недоліків. Зокрема, не було передбачено контрольної групи без аеробних вправ, яка б приймала тільки вітамін С. До того ж кількість учасників була досить невеликою та контрольна група не отримувала плацебо.
Висновки
Це дослідження показало, що аеробне фізичне навантаження як самостійне, так і в поєднанні з вживанням вітаміну С сприятливо впливало на клінічну картину пацієнтів з АР, зменшуючи вираженість симптомів риніту. Позитивними ефектами обох засобів було також покращення імунної функції (зростання ІЛ‑2 та зниження ІЛ‑4). Автори відзначили, що аеробне навантаження покращує кардіореспіраторні показники, ПНІП та НК; зменшує оксидативний стрес. Загалом, аеробні вправи достовірно поліпшують клінічний стан хворих з АР і їхій цитокіновий профіль. Внаслідок наявності певних обмежень дане дослідження не дозволяє встановити переваги застосування вітаміну С як доповнення до аеробного навантаження, що обумовлює потребу в подальшому вивченні цього питання.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 19 (440), жовтень 2018 р.


