23 січня, 2019
Лізоцим як ензибіотик: потенційне рішення глобальної проблеми антибіотикорезистентності
Відкриття антибіотиків стало одним з найбільших досягнень медицини у ХХ ст. Проте через широке і часто нераціональне застосування цих препаратів людство стикнулося з новою проблемою – зростанням розповсюдженості антибіотикорезистентних штамів, зокрема бактерій з мульти- і панрезистентністю. Цю загрозливу ситуацію погіршує той факт, що нині практично відсутні нові класи антибіотиків з іншим механізмом дії, необхідні для стримування поширеності резистентних патогенів. Деякі експерти навіть висловлюють побоювання, що незабаром ми можемо повернутися в доантибіотичну еру. Отже, існує нагальна потреба в розробці інноваційних антибактеріальних агентів, активних проти мультирезистентних бактерій. Одним з перспективних класів нових, принаймні в аспекті клінічного застосування, протимікробних засобів є ензибіотики.
Термін «ензибіотик» (ензим + антибіотик) увійшов у наукову літературу у 2001 р. після публікації статті групи американських учених під керівництвом Вінсента Фішетті [1]. Професор В. Фішетті вивчав ферменти класу лізинів, які можуть руйнувати більшість грампозитивних і грамнегативних патогенів. Ці ферменти виявилися дуже потужними: лише декілька мікрограмів знищували мільйони мікроорганізмів за лічені секунди.
За сучасним визначенням, ензибіотики – це ферменти будь-якого походження, що мають антибактеріальну та/або протигрибкову і противірусну активність. Важливими перевагами ензибіотиків є унікальний механізм дії, активність проти мультирезистентних штамів, специфічність (відсутність негативного впливу на коменсальну мікрофлору) і низька імовірність розвитку резистентності. Сьогодні у відкритих базах даних EnzyBase та PhiBIOTICS [2, 3] містяться дослідження понад тисячі різних ензибіотиків, з-поміж яких найбільш вивченим щодо клінічного застосування є лізоцим.
Лізоцим як ензибіотик
 Лізоцим, також відомий як мурамідаза, або N-ацетилмурамідглікангідролаза, – це антимікробний фермент тваринного світу, що функціонує в складі вродженої імунної системи. В організмі людини лізоцим у високих концентраціях міститься в секретах, зокрема в сльозах, слині, слизі та грудному молоці, а також у цитоплазматичних гранулах макрофагів і поліморфноядерних нейтрофілів.
Лізоцим, також відомий як мурамідаза, або N-ацетилмурамідглікангідролаза, – це антимікробний фермент тваринного світу, що функціонує в складі вродженої імунної системи. В організмі людини лізоцим у високих концентраціях міститься в секретах, зокрема в сльозах, слині, слизі та грудному молоці, а також у цитоплазматичних гранулах макрофагів і поліморфноядерних нейтрофілів.
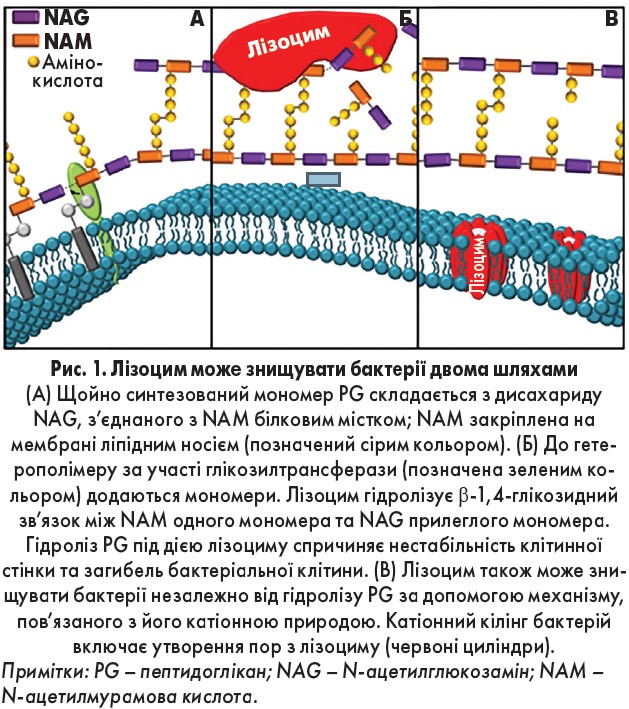
Лізоцим каталізує гідроліз глікозидних зв’язків пептидоглікану та хітину – основних компонентів клітинної стінки бактерій і грибів відповідно – з подальшим руйнуванням клітинної стінки і загибеллю мікроорганізмів (рис. 1). Мурамідазна активність вважається головним механізмом антибактеріальної дії лізоциму, проте є також докази неферментативних ефектів [4]. Наприклад, блокування каталітичної активності лізоциму шляхом мутації критичної амінокислоти в активному сайті (52-Асп → 52-Сер) не позбавляє його антимікробної активності. Лізоцим взаємодіє з антитілами і рецепторами Т-лімфоцитів, а також має лектиноподібну здатність розпізнавати бактеріальні вуглеводні антигени без літичної активності. Крім антибактеріальної і протигрибкової активності, лізоцим демонструє противірусну, протинабрякову, антиоксидантну та регенеративну дію [5].
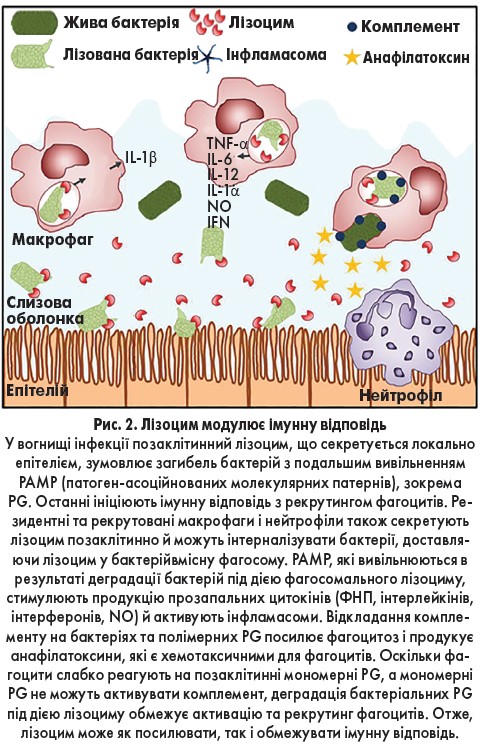 За допомогою сучасних молекулярних методів була встановлена унікальна властивість лізоциму модулювати запалення на різних етапах (рис. 2) [4]. На початку інфекції руйнування бактеріальних пептидогліканів, опосередковане лізоцимом, ініціює активацію численних імунних рецепторів, які стимулюють прозапальну відповідь. Бактерії під дією лізоциму стають більш чутливими до деградації макрофагами, що корелює з підвищенням продукції запальних цитокінів (фактора некрозу пухлини (ФНП), інтерлейкінів 1β і 6, інтерферонів та ін.). Лізоцим також стимулює прозапальну активність імунних клітин шляхом підвищення активації інфламасом NLRP1, NLRP3 та AIM2.
За допомогою сучасних молекулярних методів була встановлена унікальна властивість лізоциму модулювати запалення на різних етапах (рис. 2) [4]. На початку інфекції руйнування бактеріальних пептидогліканів, опосередковане лізоцимом, ініціює активацію численних імунних рецепторів, які стимулюють прозапальну відповідь. Бактерії під дією лізоциму стають більш чутливими до деградації макрофагами, що корелює з підвищенням продукції запальних цитокінів (фактора некрозу пухлини (ФНП), інтерлейкінів 1β і 6, інтерферонів та ін.). Лізоцим також стимулює прозапальну активність імунних клітин шляхом підвищення активації інфламасом NLRP1, NLRP3 та AIM2.
Натомість після реалізації адекватної імунної відповіді лізоциму належить важлива роль в обмеженні системного запалення і попередженні запальної патології. Механізми такої захисної дії включають підтримання цілісності епітеліальних бар’єрів; кліренс полімерних пептидогліканів, здатних викликати гіперактивацію резидентних макрофагів; зниження хемотаксису й окислювального «вибуху» нейтрофілів; нейтралізацію позаклітинних прозапальних біореактивних продуктів та ін.
! Завдяки антимікробним та імуномодулювальним властивостям лізоцим у формі льодяників широко застосовується для місцевого лікування запальних процесів слизової оболонки рота і горла – стоматиту, гострого та хронічного тонзиліту (ангіни), тонзилофарингіту. Для підвищення термостабільності та посилення біологічної активності лізоциму його комбінують з піридоксином (вітаміном В6). Піридоксин сприяє більш швидкій та повній репарації слизової оболонки, запобігає утворенню афт і позитивно впливає на імунітет. В Україні комбінація лізоциму та піридоксину представлена препаратом Лісобакт®. Порівняно з іншими подібними засобами Лісобакт® містить найвищу дозу лізоциму в одному льодянику.
Клінічні дослідження
Клінічна ефективність і безпека Лісобакту в лікуванні інфекційно-запальних захворювань ротоглотки добре продемонстровані в дослідженнях за участю дітей і дорослих пацієнтів.
У дітей, які часто і тривало хворіють на гострі респіраторні захворювання, включення Лісобакту в комплексну терапію забезпечило більш швидке зникнення інтоксикаційного синдрому, зменшення тривалості катаральних проявів, відновлення емоційного статусу, сну й апетиту, а також удвічі скоротило вірогідність бактеріальних ускладнень [6].
В іншому дослідженні в педіатричній популяції на тлі застосування препарату Лісобакт® відзначалися позитивні зміни мікробіоценозу порожнини рота і глотки, що проявлялися в підвищенні чисельності й активності облігатної мікрофлори, зниженні активності факультативних та залишкових мікроорганізмів, нормалізації балансу аеробно-анаеробних популяцій мікроорганізмів і відновленні процесів протеолізу і муциноутворення [7].
У дослідженні за участю дорослих пацієнтів з гострим тонзилітом або загостренням хронічного тонзиліту Лісобакт® порівнювали з топічним антисептиптиком (амілметакрезол + 2,4-дихлорбензиловий спирт) [8]. Результати показали, що в усіх пацієнтів на тлі лікування досягнуто клінічне одужання. Динаміка зміни симптомів в обох групах була зіставною, проте вираженість дискомфорту і відчуття чужорідного тіла в глотці, інтенсивність сухого кашлю в пацієнтів після курсу лікування препаратом Лісобакт® були значно меншими, ніж у групі порівняння. Ці результати можна пояснити стимулюванням репаративних процесів у слизовій оболонці і захисною дією на останню піридоксину, що є компонентом зазначеного лікарського засобу. Лісобакт® також продемонстрував імунозберігаючий ефект, який проявлявся в попередженні бактеріального суперінфікування – появи нових патогенів через добу після завершення терапії.
T. Catic і співавт. вивчали симптоматичну ефективність і переносимість препарату на основі лізоциму в дорослих пацієнтів із тонзилофарингітом [9]. У період з грудня 2014 по березень 2015 року в дослідження були включені 1727 пацієнтів з 93 клінічних центрів Європи. Пацієнти зверталися по медичну допомогу з приводу тонзилофарингіту, асоційованого із застудою, у перші 2 дні після появи симптомів. Найчастішими проявами захворювання були біль у горлі (34% пацієнтів), біль під час ковтання (22%), відчуття печіння або подразнення в горлі (18%), відчуття сухості у горлі (10%) і кашель (16%). У половини пацієнтів спостерігали два або більше симптомів. У 45% учасників тонзилофарингіт був пов’язаний з вірусною інфекцією, у 23% – з поганим імунітетом, у 18% – зі змінами кліматичних умов, у 9% – з носінням не відповідного погоді одягу та в 5% – з тривалим перебуванням у погано вентильованих приміщеннях.
Загалом 95% пацієнтів характеризували ефективність досліджуваного препарату як добру, дуже добру або відмінну. Третина хворих відчули значний симптоматичний ефект, зокрема полегшення болю в горлі, вже через 10 хв після першого застосування. У 71% пацієнтів симптоми захворювання повністю зникли протягом 3 днів від початку лікування.
Ефективність препарату корелювала з кількістю епізодів застуди за останній рік: повне зникнення болю в горлі після 2 днів лікування відзначили 73% пацієнтів з ≤2 епізодами (n=1122) та 67% хворих з >2 епізодами (n=605) (р=0,01).
Лікування добре переносилося; незначні побічні ефекти, такі як шкірний висип, спостерігалися лише в 7 пацієнтів (0,004%). Загалом 97% хворих характеризували переносимість препарату як добру, дуже добру або відмінну.
Стрімке зростання стійкості мікроорганізмів до антибактеріальних препаратів загрожує підірвати основи охорони здоров’я, закладені за останні 50 років. Як результат, Всесвітня організація охорони здоров’я визначила антибіотикорезистентність як одну з головних загроз людству. У цій ситуації ензибіотики, такі як лізоцим, можуть стати потужною зброєю в боротьбі зі стійкими патогенами і поширенням резистентних штамів.
Список літератури знаходиться в редакції.
Підготувала Марина Симінська


