12 лютого, 2019
Склеродермічний нирковий криз: клініко-діагностичні акценти
 Системна склеродермія (ССД), або прогресуючий системний склероз – це стадійне поліорганне захворювання із характерними вазоспастичними судинними реакціями за типом синдрому Рейно та облітераційною судинною патологією з ішемічними порушеннями, при яких розвиваються специфічні автоімунні розлади, що супроводжуються активацією фіброзоутворення та надлишковим відкладанням колагену в тканинах [10].
Системна склеродермія (ССД), або прогресуючий системний склероз – це стадійне поліорганне захворювання із характерними вазоспастичними судинними реакціями за типом синдрому Рейно та облітераційною судинною патологією з ішемічними порушеннями, при яких розвиваються специфічні автоімунні розлади, що супроводжуються активацією фіброзоутворення та надлишковим відкладанням колагену в тканинах [10].
Ураження нирок – надважливий і прогноз-визначальний клінічний прояв системного склерозу. Зокрема, склеродермічний нирковий криз (СНК) є критичним клінічним виявом ураження нирок при ССД і переважною причиною смерті у таких пацієнтів. Проте варто зазначити, що показники виживання осіб із СНК за останні роки значно покращилися [12]. Безсумнівно, рутинне застосування інгібіторів ангіотензинперетворювального ферменту (іАПФ) сумісно з іншими сучасними методами лікування СНК суттєво модифікувало наслідки цього стану, що є одним із найважливіших досягнень у терапії ССД. Однак, попри явне зменшення ранньої смертності через СНК, довгостроковий прогноз для цих пацієнтів вельми несприятливий, зважаючи на супутні ускладнення та наслідки ураження життєво важливих органів та органів-мішеней при ССД, неухильне прогресування патології, необхідність тривалого нирковозамісного лікування. Відтак СНК залишається зламним проявом хвороби, отже, необхідність раннього розпізнавання цього стану та призначення своєчасної відповідної терапії – актуальні проблеми ревматології та нефрології на сьогодні.
Ураження нирок при ССД
Незважаючи на те що СНК є найтяжчим і частим ускладненням ураження нирок при ССД, маніфестуючи, як правило, злоякісною артеріальною гіпертензією (АГ) і гострим ушкодженням нирок (ГУН), необхідно враховувати й інші проблеми, властиві ССД. До них відносять інтерстиціальний нефрит, гломерулонефрит, АНЦА-асоційований нирковий васкуліт [3], хронічну ниркову васкулопатію та нирковий паренхіматозний фіброз [2; 30]. Крім того, у хворих на ССД спостерігається висока частота мікроскопічної гломерулярної або тубулярної протеїнурії, довгострокове значення яких все ще остаточно не з’ясоване.
Визначення
Гостра склеродермічна нефропатія, або СНК характеризується вперше виявленою злоякісною АГ та/або швидко прогресуючим олігуричним варіантом ниркової недостатності на тлі встановленого діагнозу ССД. Злоякісна гіпертензія без уремії або інших проявів ураження нирок не є власне нирковим кризом [26]. Аналогічно зміни в аналізах сечі та/або помірна уремія у пацієнтів із ССД без АГ також не мають розглядатися як СНК. Існують деякі відмінності між критеріями, які використовували для визначення СНК у різних дослідженнях. Окрім того, СНК як відмітний прояв ССД не знайшов відображення в ACR/EULAR-2013 – класифікаційних критеріях щодо ССД, оскільки в цьому симптомокомплексі не було додано чутливості та специфічності діагностиці цього захворювання [33]. З іншого боку, в діагностичні критерії ССД були включені антитіла до РНК-полімерази III, які тісно асоційовані з СНК.
Епідеміологія
За даними різних джерел, для дифузної форми ССД (дССД) частота СНК становить у середньому 14%, для лімітованої (лССД) набагато менше – приблизно 3% [22]. Захворюваність на нирковий криз, мабуть, зменшилася відтоді, як почали застосовувати іАПФ, хоча в літературі немає прямих доказів того, що ця група препаратів запобігає СНК.
Нирковий криз найчастіше спостерігається у жінок та на ранній стадії ССД: до 75% випадків СНК маніфестує у період від 7,5 місяців до 4 років від першого прояву системного склерозу [33]. Також дослідження продемонстрували, що в афроамериканців СНК розвивається утричі частіше, аніж у європейців [22].
Патогенез
Основними ланками патогенезу ССД є взаємодія вродженої та адаптивної імунних систем, порушений метаболізм сполучної тканини й позаклітинного матриксу, васкулопатія мікроциркуляторного русла та порушення артеріального кровотоку в нирках [26]. Відповідно до теорії V.D. Steen і співавт. [28], у генетично схильних осіб внаслідок розвитку автоімунних реакцій, васкулопатії та фіброзу виникає специфічне ураження органів [9], зокрема й нирок. При СНК відбуваються пошкодження ендотелію, проліферація інтими та звуження ниркових артеріол, зумовлюючи зниження кровотоку, гіперплазію юкстагломерулярного апарату, гіперренiнемію та виникнення АГ [26]. На рисунку 1 схематично представлено послідовність патогенетичних механізмів, які зумовлюють розвиток СНК.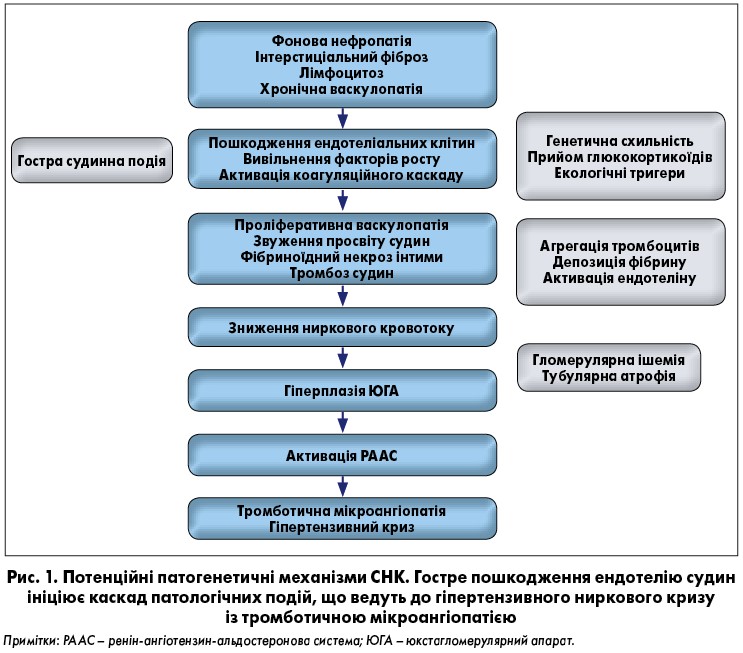
Тригером виникнення СНК є вазоспазм ниркових судин (нирковий синдром Рейно), що призводить до пошкодження ендотеліальних клітин, проліферативної васкулопатії переважно дугових та інтралобулярних ниркових артерій із фібриновими тромбами та фібриноїдним некрозом [26]. Надалі відбуваються фіброз і ущільнення екстрацелюлярного матриксу клубочків та канальцевого інтерстицію, мукоїдний набряк інтими судин і концентрична гіпертрофія інтралобулярних артерій за типом «цибулевого лушпиння» [25]. Адвентиціальний і періадвентиціальний фіброз – ознака хронічної васкулопатії, що спостерігається у пацієнтів із СНК. Цікаво, що на відміну від інших захворювань нирок, ступінь інтерстиціального склерозування не має прогностичної цінності, тоді як маркери гострого судинного ушкодження (включно із фібриноїдним некрозом і тромбозом судин) пророкують погані наслідки [25]. Ураження клубочків є вторинним і розвивається внаслідок розладнання внутрішньониркової гемодинаміки із прогресом ішемії ниркової тканини.
Кінцевим результатом СНК є ініціація самовідтвореного каскаду гломерулярної гіпоперфузії, активація прозапальних цитокінів і зростання вивільнення реніну з активованого ренін-ангіотензин-альдостеронового циклу за зворотним зв’язком [25]. Гіперпродукція реніну – це один із ключових моментів патогенезу СНК, що зумовлює спазм артеріол ниркових клубочків із наступним наростанням порушень внутришньониркової гемодинаміки, які посилюються зростанням системного артеріального тиску (АТ), додатково негативно впливаючи на гломерулярні капіляри. Водночас гіперренінемія рідко зустрічається перед гострим початком СНК і не може виступати предиктором його розвитку.
Окрім пошкодження ендотеліальних клітин і порушення бар’єрної функції, до розвитку і прогресування СНК залучена також їхня активація з експресією ними маркерів ендотелійзалежної ланки гемостазу та медіаторів фіброгенезу. У пацієнтів із СНК встановлене підвищення рівня вазоконстрикторних молекул – циркуляційного ендотеліну‑1 (ET‑1) та ангіотензину II, трансформувального фактора росту та розчинної молекули адгезії (sVCAM).
На рисунку 2 схематично зображено послідовність патогістологічних змін і патогенетичних подій, що лежать у підвалинах розвитку СНК.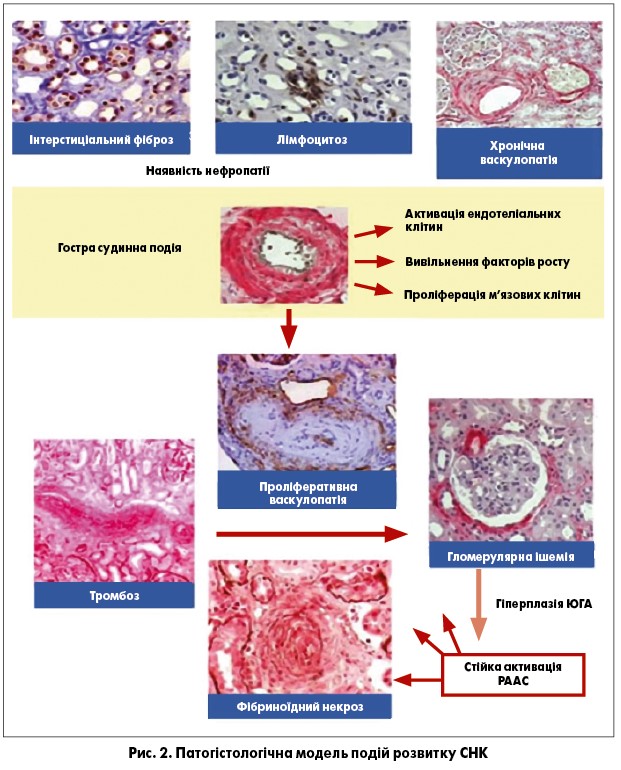
Фактори ризику розвитку СНК
Про характеристики типового пацієнта із СНК детально написано у науковій літературі. Багато з цих ознак або лабораторних показників можуть бути ідентифіковані до виникнення самого невідкладного стану, через те необхідний ретельний базовий аналіз усіх випадків ССД для ймовірної оцінки ризику розвитку ГУН. Один із основних предикторів СНК – дССД. У групі осіб із дССД у 20-25% розвивався СНК, що становить 75-80% усіх випадків хвороби [26]. Набагато менше пацієнтів із лімітованою (обмеженою) формою склеродермії (CREST-синдромом) мають ризик появи СНК. Ще менше проявів ниркового кризу задокументовані у хворих на лімітовану склеродермію з високими титрами антицентромірних антитіл [28]. Таким чином, переважна більшість випадків СНК (75-80%) припадає на пацієнтів із дифузним залученням шкіри, крім того, слід підкреслити, що швидке прогресування її потовщення пов’язане з більш високою ймовірністю розвитку СНК [28].
Існує кілька характерних ознак, які допомагають ідентифікувати осіб із ризиком розвитку СНК. Це пацієнти, які майже завжди мають короткий анамнез захворювання, часто менш ніж 1 рік, поліартрит/поліартралгії, подушкоподібний щільний набряк переважно проксимальних відділів кистей і стоп (puffy fingers), тунельний синдром зап’ясткового каналу [1, 5]. Наявність шуму тертя (крепітації) сухожиль, що визначається пальпаторно під час руху ліктьових, променево-зап’ясткових, колінних або гомілковостопних суглобів, у 65% хворих є надзвичайно корисним та важливим для прогнозу проявом дССД ще до розвитку дифузного шкірного ураження; до 5% пацієнтів із лССД мають таку ознаку [11]. Цей симптом пов’язаний із відкладенням фібринозних депозитів на поверхні сухожильних піхов і фасцій та нерідко передує змінам шкіри. Ураження сухожилків нерідко призводить до формування згинальних контрактур. У проспективному дослідженні EUSTAR, яке включало 1301 хворого на ССД із тривалістю патології ≤3 роки, підтверджено, що шум тертя сухожилків (відносний ризик 2,33; 95% довірчий інтервал 1,03; 6,19) є незалежним предиктором розвитку СНК [4].
Автоантитіла можуть бути корисними для оцінки прогнозу СНК. Антинуклеарні антитіла (АНА) спостерігаються у 95% пацієнтів зі склеродермією, тому їхнє виявлення в периферичній крові у пацієнтів зі злоякісною гіпертензією може бути важливою діагностичною ознакою. Антитіла до РНК-полімерази III – власне склеродермічне специфічне антитіло, яке визначається виключно при дССД; у понад 50% хворих із цим імунологічним показником розвивається СНК [21]. Отже, антитіла до РНК-полімерази III можна використовувати як надійний предиктор виникнення СНК. І навпаки, тільки у 10% пацієнтів з антитілами до топоізомерази І, що також пов’язані з дифузним захворюванням шкіри, розвивається нирковий криз [9]. Антицентромерні антитіла, які спостерігаються при класичній лімітованій формі склеродермії (або CREST-синдромі), так само рідко асоціюються з нирковим кризом [31].
Пацієнтам із ранньою дССД рекомендовано регулярно контролювати АТ і відразу ж повідомляли лікаря, коли той має тенденцію до зростання, оскільки у більшості осіб (до 75%) із дифузною формою системного склерозу СНК розвивається у термін від 7,5 місяців до 4 років [26]. Гіпертензія в анамнезі зазвичай не властива СНК, більш типовою ознакою є вперше виявлене раптове різке неконтрольоване підвищення (наростання в динаміці) АТ.
На додаток, деякі позаниркові ураження іноді передують СНК: це безсимптомний перикардіальний випіт, застійна серцева недостатність та/або аритмія [29]. Анемія – незвичний і нечастий прояв склеродермії, але вона також може бути ранньою ознакою ниркового кризу, особливо за наявності гемолізу та тромбоцитопенії [6].
У випробуваннях підтверджено, що раннє використання високих доз глюкокортикоїдів – ГК (>15 мг/добу в еквіваленті преднізолону) часто передує розвитку СНК [29; 32]. У дослідженні «випадок-контроль» було виявлено, що нирковий криз розвивався утричі частіше протягом наступних 6 місяців у пацієнтів із ССД, які отримували ГК (преднізолон) у дозі >15 мг/добу [29].
Деякі з найбільш надійних предикторів розвитку СНК, що перераховані вище, знайшли своє підтвердження у нещодавньому міжнародному дослідженні International Scleroderma Renal Crisis Survey [14]. Так, середня тривалість захворювання від початку перших симптомів ССД до діагнозу СНК становила 1,5 року, у 75% пацієнтів діагностовано дССД, майже у половини були виявлені антитіла, асоційовані з дифузним ураженням шкіри (АНА, анти-РНК-полімераза III). Крім того, у цьому випробуванні встановлено зв’язок між прийомом ГК і ризиком смерті від СНК: кожний міліграм преднізолону підвищував ризик смерті на 4% [14].
У таблиці 1 підсумовані предиктори розвитку СНК.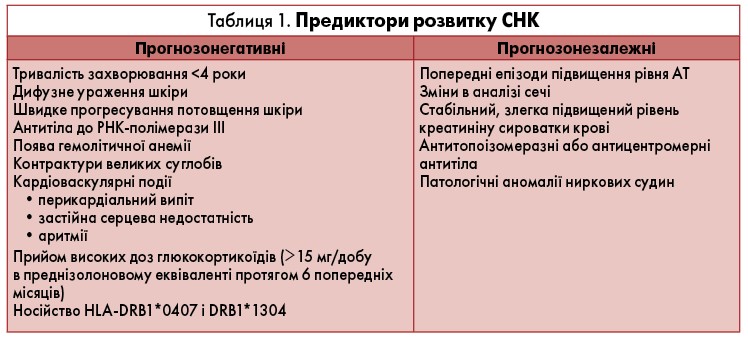
Діагностичні критерії СНК
Для діагностики СНК на даний час не існує золотого стандарту. У таблиці 2 представлені сучасні чинні критерії: обов’язкова наявність двох критеріїв злоякісної (гіперренінової) АГ і швидко прогресуючої ниркової недостатності, а також як мінімум одного клініко-інструментального критерію із третьої групи [13; 33].
Близько 10% випадків СНК можуть з’являтися при нормальному АТ. Повідомляється, що саме такі прояви нормотензивного СНК мають особливо поганий прогноз. Згідно з діагностичними критеріями треба звернути увагу, що в першій групі є не тільки фіксоване підвищення АТ >150/90 мм рт. ст., але й збільшення САТ та/або ДАТ на 30/20 мм рт. ст. відповідно від звичайних показників для кожного конкретного пацієнта, тобто в останньому випадку може мати місце нормотензивний варіант СНК.
Клінічна картина
Пацієнти можуть скаржитися на сильний головний біль, порушення зору або інші симптоми гіпертензивної енцефалопатії, пов’язані з різким підвищенням АТ. Так само характерна велика кількість неспецифічних симптомів: підвищена втома, кволість, задишка або загальне нездужання. Згідно з наявними факторами ризику (прогнозонегативними чинниками), осіб із ССД і високим ризиком розвитку СНК необхідно навчити пильно відстежувати ці симптоми та самостійно контролювати рівень АТ.
Більшість пацієнтів мають значне та раптове підвищення показників АТ як маніфестацію СНК: у 90% він становить >150/90 мм рт. ст., а у 30% спостерігається ДАТ >120 мм рт. ст. До 10% клінічних випадків СНК супроводжуються нормальним АТ, хоча «нормальне» значення має бути інтерпретоване в кожному конкретному випадку, як вже зазначалося вище. Таким чином, будь-яка раптова й неочікувана зміна АТ у бік підвищення повинна насторожити лікаря та пацієнта, спонукати до подальшого спостереження й моніторингу. Для діагностики нормотензивного ниркового кризу необхідна наявність інших ознак, насамперед швидко прогресуючої незрозумілої азотемії та/або гемолітичної анемії з тромбоцитопенією [19].
Достатньо часто у пацієнтів із СНК можна виявити клінічні ознаки застійної серцевої недостатності (задишку, зокрема пароксизмальну нічну, або навіть набряк легень), серйозні шлуночкові аритмії, включно із зупинкою серця, та/або масивний перикардіальний випіт, розвиток гострого кардіоренального синдрому (1, 3 або 5-го типу) [16; 34]. Безумовно, це спричинено, насамперед, стресовим впливом високого АТ на міокард, ефектами гиперренінемії та перевантаженням об’ємом внаслідок олігуричної стадії ниркової недостатності, але робить свій внесок у цей стан і залучення до патологічного процесу міокарда, властиве для ССД.
Лабораторні феномени
Лабораторне підтвердження ГУН при СНК є основним напрямком початкової діагностики. Як правило, у загальному аналізі сечі можна виявити протеїнурію та мікрогематурію. Протеїнурія є незначною або помірною (зазвичай <2 г/добу), при мікроскопії сечі кількість еритроцитів становить 5-100 у полі зору, можуть зустрічатися поодинокі гранулоцитарні циліндри [23]. Креатинін сироватки крові найчастіше становить не менш ніж 150% від початкового значення. Вищевказані ознаки є 1-ю стадією ГУН згідно з міжнародними консенсусними рекомендаціями щодо ведення таких пацієнтів [16]. Знову ж таки, «нормальну» функцію нирок слід інтерпретувати з обережністю, оскільки показник креатиніну може досягти відносного збільшення на 150%, не піднімаючись вище нормального абсолютного діапазону. Рівень креатиніну швидко зростає у перші кілька днів від початку ниркового кризу і, як правило, продовжує підвищуватися навіть після адекватного контролю АТ та становить 0,5-1,0 мг/дл на день.
Мікроангіопатична гемолітична анемія, яка характеризується нормохромними, фрагментованими еритроцитами, ретикулоцитозом і тромбоцитопенією, зустрічається майже у половини пацієнтів із СНК. Кількість тромбоцитів рідко буває нижчою за 20 000/мм3, і нормалізація рівня цих клітинних елементів є першою ознакою адекватної відповіді на терапію, навіть незважаючи на те, що триває зростання рівня креатиніну в сироватці крові. Тромбоцитопенія при СНК зазвичай малосимптомна, проте анемія може сприяти розвитку серцевої недостатності.
Лікування
Найважливішим аспектом ведення пацієнтів із нирковим кризом є рання діагностика цього стану. Надзвичайно важливо виявити хворих із високим ризиком розвитку такого ускладнення, навчити їх самостійно виконувати моніторинг АТ щонайменше двічі на день, і за появи гострих симптомів – головного болю, задишки, запаморочення або синкопе у сукупності із високим АТ – негайно звернутися до лікаря. Також необхідно проводити регулярну оцінку аналізів сечі та біохімічних показників крові щодо функції нирок. Це особливо важливо за тривалості анамнезу дССД менш ніж 4 роки. Якщо за станом здоров’я пацієнта із ССД спостерігає сімейний лікар, то при виникненні маніфестної АГ або інших відповідних симптомів, аномалій аналізу сечі або наростання ниркової недостатності необхідна негайна консультація у ревматолога та/або нефролога. Таким чином, можна своєчасно запідозрити розвиток СНК і розпочати лікування. У разі встановлення діагнозу СНК хворий має бути негайно госпіталізований. Метою лікування СНК є досягнення нормального АТ. Відповідно до сучасних рекомендацій [18], АГ при СНК слід корегувати шляхом призначення іАПФ або збільшення їхньої дози при попередньому прийомі. іАПФ короткої дії краще використовувати у гемодинамічно нестабільних ситуаціях. Зниження цифр АТ є головною метою терапії СНК, проте для цього може знадобитися кілька днів, протягом яких потрібно збільшити дози іАПФ до максимальних, можливо, подвоювати їх кожні 24 години. Необхідний також ретельний моніторинг пацієнта з щоденними оцінками загального аналізу крові та функції нирок. Потрібно пам’ятати, що ймовірне прогресивне погіршення останньої впродовж перших кількох діб, незважаючи на розпочате лікування. Це ключовий момент, оскільки лікар може необґрунтовано скасувати або зменшити дозу іАПФ з огляду на їхню неефективність або побічні ефекти, але не треба поспішати.
При збереженні високої АГ на тлі максимальної дози іАПФ до лікування СНК додають блокатори кальцієвих каналів, α-блокатори (доксазозин), моксонідин, нітропрусид натрію та клонідин. Антагоністи рецепторів ангіотензину ІІ при ізольованому прийомі є менш ефективними, аніж іАПФ, що, ймовірно, пов’язано з відсутністю ефекту на брадикінін. Бета-блокатори протипоказані при СНК через вплив на периферичний кровообіг. Зазвичай для терапії АГ при СНК немає необхідності у призначенні парентеральних антигіпертензивних засобів, хоча інфузія нітратів може знадобитися у разі виникнення гострої лівошлуночкової недостатності та набряку легень на тлі СНК.
Останніми роками з’явилися дані про використання антагоністів ендотелінових рецепторів (бозентану та ситаксентану) при СНК [15], що є обґрунтованим підходом, зважаючи на високі рівні циркулюючого ЕТ‑1, а також підвищену експресію рецепторів і лігандів ендотеліну [20].
У разі розвитку СНК додатково рекомендується використовувати ілопрост – стабільний аналог простацикліну, що має вазодилатуючі та антиагрегантні властивості. При внутрішньовенному використанні ілопрост збільшує нирковий плазмотік, розширюючи приносну та виносну артеріоли [7].
У випадках необхідності замісної ниркової терапії методами вибору є гемофільтрація або гемодіаліз. Результати останніх досліджень показують, що останній потрібний половині пацієнтів із СНК через перевантаження об’ємом внаслідок зниження ниркової функції або для контролю АТ при резистентній АГ. За оптимального лікування діаліз можливо перервати у 16-55% хворих на СНК. Іноді при повільно прогресуючому розвитку СНК можна скористатися перитонеальним діалізом як ініціальною терапією. Водночас при несприятливих варіантах перебігу СНК єдиним варіантом лікування є трансплантація нирки [35]. У зв’язку з наявною можливістю відновлення ниркової функції операцію слід проводити не раніше ніж через 18-24 місяці після появи СНК. Проте частота повторного розвитку СНК у нирковому трансплантаті сягає 20-50% [8].
Різні біологічні агенти, зокрема інгібітори TNF, анти-CD20 (ритуксимаб), моноклональні антитіла до інтерлейкіну‑6 (IL‑6), екулізумаб та інгібітори тирозинкінази, проходять дослідження для оцінки ефективності та безпеки при СПК.
Плазмаферез на сьогодні не розглядається як метод вибору при СНК, оскільки його ефективність вкрай низька. Однак він є провідним методом лікування при деяких асоційованих станах, як, наприклад, тромбоцитопенічна пурпура, тяжка мікроангіопатична гемолітична анемія та коагулопатія споживання [17].
Лікування ускладнень СНК у вигляді ураження життєво важливих органів, зокрема набряку легень і гіпертензивної енцефалопатії, слід проводити відповідно до чинних стандартів і рекомендацій для терапії цих станів. На рисунку 3 представлений узагальнений алгоритм ведення хворих на СНК.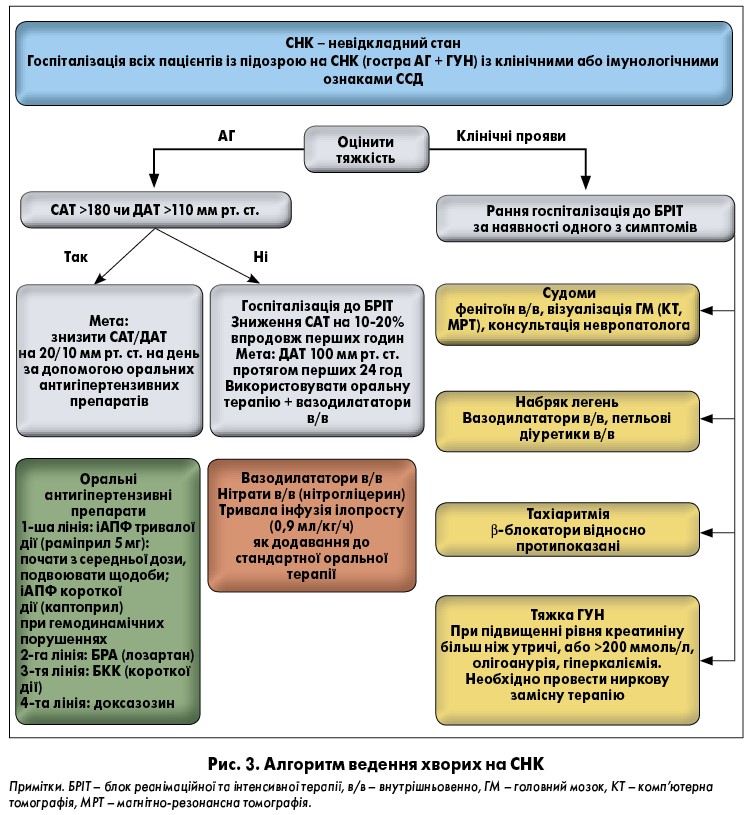
Профілактика
Навчання пацієнтів разом зі стратифікацією ризику та пильним моніторингом АТ, аналізів сечі та рівня креатиніну мають вирішальне значення у профілактиці СНК. Немає жодних доказів того, що іАПФ чинять профілактичний ефект.
Попри значне збільшення виживаності осіб із СНК із початком «ери іАПФ», гостра склеродермічна нефропатія є високофатальним проявом ССД. Пацієнти цієї групи потребують ретельного лікарського контролю, починаючи від виділення груп ризику, своєчасного та правильного встановлення діагнозу і проведення інтенсивної терапії з тісною міждисциплінарною взаємодією, до виконання нирковозамісної терапії та трансплантації нирки.
Література
- Нейко Є.М., Яцишин Р.І. Основні дебютні прояви системної склеродермії // Галицький лікарський вісник. – 2001. – Т. 8, № 2. – С. 45-47.
- Нейко Є.М., Яцишин Р.І. Патологія нирок при системній склеродермії // Галицький лікарський вісник. – 2001. – № 3. – С. 77-79.
- Arnaud L., Huart A., Plaisier E. et al. ANCA-related crescentic glomerulonephritis in systemic sclerosis: revisiting the “normotensive scleroderma renal crisis” // Clin Nephrol. – 2007. – Vol. 68, № 3. – P. 165-70.
- Avouac J., Walker U. A., Hachulla E. et al. Joint and tendon involvement predict disease progression in systemic sclerosis: a EUSTAR prospective study // Ann Rheum Dis. – 2016. – Vol. 75, № 1. – P. 103-109.
- Bellando-Randone S., Guiducci S., Matucci-Cerinic M. Very early diagnosis of systemic sclerosis // Pol Arch Med Wewn. – 2012. – Vol. 122, № 1. – P. 18-23.
- Bose N., Chiesa-Vottero A., Chatterjee S. Scleroderma renal crisis // Semin Arthritis Rheum. – 2015. – Vol. 44, № 6. – P. 687-694.
- Casigliani R.S., Della R.A., Pepe P. et al. Long-term cyclic intravenous iloprost in systemic sclerosis: clinical experience from a single center // Reumatismo. – 2012. – Vol. 64, № 3. – P. 158-165.
- Cheung W.Y., Gibson I.W., Rush D. et al. Late recurrence of scleroderma renal crisis in a renal transplant recipient despite angiotensin II blockade // Am J Kidney Dis. – 2005. – Vol. 45, № 5. – P. 930-934.
- Denton C.P. Renal manifestations of systemic sclerosis – clinical features and outcome assessment // Rheumatology. – 2008. – Vol. 47, № 5. – P. 54-56.
- Desbois A.C., Cacoub P. Systemic sclerosis: an update in 2016 // Autoimmun Rev. – 2016. – Vol. 15. – P. 417-426.
- Gabriele V., Vettori S., Cuomo G. et al. Early systemic sclerosis: short-term disease evolution and factors predicting the development of new manifestations of organ involvement // Arthritis Res Ther. – 2012. – Vol. 14, № 4. – P. 188.
- Guillevin L., Bеreznе A., Seror R. et al. Scleroderma renal crisis: a retrospective multicentre study on 91 patients and 427 controls // Rheumatology (Oxford). – 2012. – Vol. 51, № 3. – P. 460-467.
- Hoa S., Stern E.P., Denton C.P., Hudson M. Towards developing criteria for scleroderma renal crisis: A scoping review // Autoimmun Rev. – 2017. – Vol. 16, № 4. – P. 407-415.
- Hudson M., Baron M., Tatibouet S. et al. Exposure to ACE inhibitors prior to the onset of scleroderma renal crisis-results from the International Scleroderma Renal Crisis Survey // Semin Arthritis Rheum. – 2014. – Vol. 43, № 5. – P. 666-672.
- Izzedine H., Rouvier P., Deray G. Endotelin receptor antagonism- based treatment for scleroderma renal crisis // Am J Kidney Dis. – 2013. – Vol. 62 (2). – Р. 394-395.
- KDIGO. Clinical practice guideline for acute kidney injury (AKI) // Kidney Int Suppl. – 2012. – Vol. 2, № 1. – P. 4.
- Kfoury Baz E.M., Mahfouz R.A., Masri A.F., Jamaleddine G.W. Thrombotic thrombocytopenic purpura in a case of scleroderma renal crisis treated with twice-daily therapeutic plasma exchange // Ren Fail. – 2001. – Vol. 23, № 5. – P. 737-742.
- Kowal-Bielecka O., Landewe R., Avouac J. et al. EULAR recommendations for the treatment of systemic sclerosis: a report from the EULAR Scleroderma Trials and Research group (EUSTAR) // Ann Rheum Dis. – 2009. – Vol. 68, № 5. – P. 620-628.
- Manadan A.M., Harris C., Block J.A. Thrombotic thrombocytopenic purpura in the setting of systemic sclerosis // Semin Arthritis Rheum. – 2005.– Vol. 34, № 4. – P. 683-688.
- Mouthon L., Bussone G., Bereznе A. et al. Scleroderma renal crisis // J Rheumatol. – 2014. – Vol. 41. – P. 1040-1048.
- Nguyen B., Assassi S., Arnett F.C., Mayes M.D. Association of RNA polymerase III antibodies with scleroderma renal crisis // J Rheumatol. – 2010. – Vol. 37, № 5. – P. 1068.
- Nihtyanova S.I., Schreiber B.E., Ong V.H. et al. Prediction of pulmonary complications and long-term survival in systemic sclerosis // Arthritis Rheumatol. – 2014. – Vol. 66, № 6. – P. 1625-1635.
- Penn H., Denton C.P. Diagnosis, management and prevention of scleroderma renal disease // Curr Opin Rheumatol. – 2008. – Vol. 20, № 6. – P. 692-696.
- Penn H., Howie A.J., Kingdon E.J. et al. Scleroderma renal crisis: patient characteristics and long-term outcomes // QJM. – 2007. – Vol. 100, № 8 – Р. 485-494.
- Penn N., Quillinan N., Khan K. et al. Targeting the endothelin axis in scleroderma renal crisis: rational and feasibility // Q J Med. – 2013. – Vol. 106, № 9. – Р. 839-848.
- Shanmugam V.K., Steen V.D. Renal disease in scleroderma: an update on evaluation, risk stratification, pathogenesis and management // Curr Opin Rheumatol. – 2012. – Vol. 24, № 6. – P. 669-676.
- Steen V.D., Mayes M.D., Merkel P.A. Assessment of kidney involvement // Clin Exp Rheumatol. – 2003. – Vol. 21, № 3. – P. 29-31.
- Steen V.D., Medsger Jr T.A., Osial Jr T.A. et al. Factors predicting development of renal involvement in progressive systemic sclerosis // Am J Med. – 1984. – Vol. 76, № 5. – P. 779-786.
- Steen V.D., Medsger T.A. Case-control study of corticosteroids and other drugs that either precipitate or protect from the development of scleroderma renal crisis // Arthritis Rheum. – 1998. – Vol. 41. – Р. 1613-1619.
- Steen V.D., Syzd A., Johnson J.P. et al. Kidney disease other than renal crisis in patients with diffuse scleroderma // J Rheumatol. – 2005. – Vol. 32, № 4. – P. 649-655.
- Sugimoto T., Sanada M., Kashiwagi A. Is scleroderma renal crisis with anti-centromere antibody-positive limited cutaneous systemic sclerosis overlooked in patients with hypertension and/or renal dysfunction? // Nephrology (Carlton). – 2008. – Vol. 13, № 2. – P. 179-180.
- Trang G., Steele R., Baron M., Hudson M. Corticosteroids and the risk of scleroderma renal crisis: a systematic review // Rheumatol Int. – 2012. – Vol. 32(3). – Р. 645-653.
- Van den Hoogen F., Khanna D., Fransen J. et al. 2013. Сlassification criteria for systemic sclerosis: an American college of rheumatology / European league against rheumatism collaborative initiative // Ann Rheum Dis. – 2013. – Vol. 72, № 11. – P. 1747-1755.
- Wipff J., Gallier G., Dieude P. et al. Angiotensin-converting enzyme gene does not contribute to genetic susceptibility to systemic sclerosis in European Caucasians // J Rheumatol. – 2009. – Vol. 36, № 2. – P. 337-340.
- Woodworth T.G., Suliman Y.A., Furst D.E., Clements P. Scleroderma renal crisis and renal involvement in systemic sclerosis // Nat Rev Nephrol. – 2016. – Vol. 12. – P. 678-691.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (60) листопад 2018 р.


