13 лютого, 2019
Метформин: негликемические эффекты и потенциал для расширения показаний
Метформин является наиболее часто назначаемым лекарственным средством при сахарном диабете (СД) 2 типа в силу очевидных эффектов этого препарата в снижении сердечно-сосудистого риска. Масштабное британское проспективное исследование UKPDS (United Kingdom Prospective Diabetes Study) доказало, что метформин достоверно снижает риск развития инфаркта миокарда (ИМ), а более поздние исследования продемонстрировали связь между использованием метформина и снижением риска развития инсульта, мерцательной аритмии и смертности от всех причин.
Механизмы, объясняющие эти преимущества, пока до конца не выяснены и могут включать уменьшение энергетических затрат организма (с сопутствующей потерей веса), улучшение липидного профиля и снижение артериального давления (АД). При этом обзор научной литературы показывает, что метформин снижает только повышенное АД и нейтрален по отношению к нормальному. Препарат, по-видимому, безопасен для пациентов с хронической болезнью почек 3-й стадии (ХБП‑3). Более того, есть данные, что пациенты с ХБП‑3 и повышенным сердечно-сосудистым риском выигрывают от терапии метформином. Следует отметить, что риск развития лактоацидоза является весьма отдаленным, поэтому его можно избежать путем измерения уровня метформина в плазме и более частого мониторинга почечной функции у больных ХБП‑3, которые получают этот препарат. Наконец, есть доказательства того, что метформин безопасен для пациентов с сердечной недостаточностью (СН). Более того, терапия метформином ассоциируется с уменьшением числа новых эпизодов и смертности от СН.
Метформин и сердечно-сосудистые заболевания (ССЗ)
За последние 10 лет бигуанид метформин стал препаратом первой линии терапии СД 2 типа: Американская диабетическая ассоциация (АDА), Европейская ассоциация по изучению диабета (EASD) и Американская ассоциация клинических эндокринологв (AACE) одобрили метформин в своих гайдлайнах [1, 2].
Основным аргументом доминирования (и первенства в настоящее время) метформина в терапии СД 2 типа является доказанное снижение риска ССЗ [3], основанное главным образом на результатах исследования UKPDS [4, 5]. Учитывая то, что у большинства пациентов с диабетом в конечном итоге возникает сердечно-сосудистое событие [6], метформин сильно снижает этот риск, в то время как инсулинотерапия или применение препаратов сульфонилмочевины (ПСМ) оказывает меньшее влияние на риск развития ИМ [7].
Проспективное обсервационное исследование с участием почти 20 тыс пациентов с СД 2 типа и атеросклерозом показало, что применение метформина ассоциировалось со снижением смертности от всех причин на 24% по сравнению с пациентами, не получавшими этот препарат [8]. Кроме того, ретроспективное когортное исследование с участием более чем 250 тыс участников с СД 2 типа продемонстрировало, что частота комбинированной конечной точки смерти или госпитализации в результате ИМ или инсульта у пациентов, принимавших метформин, была на 40% ниже, чем у тех, кто получал ПСМ [9].
Недавнее ретроспективное исследование с участием почти 15 тыс пациентов с СД 2 типа показало, что риск инсульта в течение 4-летнего периода был на 60% ниже у тех, кто принимал метформин, по сравнению с теми, кто не принимал [10]. В другом ретроспективном 13-летнем исследовании с участием более чем 600 тыс пациентов выяснилось, что прием метформина снижает риск фибрилляции предсердий на 20% [11]. Наряду с этим было показано, что добавление инсулина при терапии метформином увеличивает риск сердечно-сосудистых событий и смертности от всех причин [12].
Исследования, проведенные на животных, демонстрируют уменьшение размера очага инфаркта у грызунов без диабета, получавших метформин незадолго до или во время реперфузии [14, 15]. Этот эффект опосредован активацией АМФ-киназы (АМФК) и киназы, спасающей от реперфузионного поражения миокарда (Reperfusion Injury Salvage Kinase, RISK). Однако сопоставимый эффект метформина у людей пока не был продемонстрирован [16].
Постоянная терапия метформином также оказывает благоприятное влияние на липидный профиль. В ряде исследований [17-20] было доказано снижение общего холестерина и триглицеридов (ТГ), в некоторых случаях сопровождаемое повышением уровня липопротеинов высокой плотности (ЛПВП) [21-23] на фоне терапии метформином. Кроме того, описано благоприятное воздействие препарата на уровень ЛПВП и размер частиц липопротеинов низкой плотности (ЛПНП) у людей без диабета [24]. В масштабном ретроспективном исследовании с участием почти 18 тыс пациентов с СД 2 типа, получавших метформин, уровень ТГ оказался значительно ниже, а уровень ЛПВП – значительно выше, чем у пациентов, получавших ПСМ [25].
Также было показано улучшение функции эндотелия на фоне терапии метформином, которое, возможно, опосредовано активацией АМФК и потенцированием действия инсулина [27]. Другие исследования [18] продемонстрировали уменьшение числа тромботических осложнений, часто сопровождающих диабет; данный эффект метформина, по-видимому, связан со снижением уровня фибриногена, активацией PAI‑1 и угнетением воспаления [28].
Влияние на энергетический баланс
Примечательно, что вначале применение метформина вызывает скромную потерю веса [4], но при постоянном приеме препарат снижает вес более значимо [5]. Возможно, это явление объясняется снижением всасывания всей принимаемой пищи и/или повышенным расходом энергии, однако в действительности некоторые авторы предполагают, что метформин уменьшает всасывание углеводов [29, 30]. Хотя тщательные исследования на людях не подтвердили данный факт, метформин, тем не менее, может задерживать всасывание углеводов [31]. Потеря веса, вызванная этим препаратом, вероятно, связана с возрастанием чувства насыщения; в одном из исследований терапия метформином показала снижение суточного потребления пищи на 250-300 ккал [32]. Абсолютная потеря веса на фоне приема метформина невелика отчасти потому, что снижение потребления энергии при СД 2 типа приводит к улучшению гликемического контроля, который, в свою очередь, оказывает антиглюкозурический эффект и также приводит к снижению энергетических расходов. Комбинация этих двух эффектов замедляет потерю веса и даже может привести к его увеличению [32].
В проспективном обсервационном исследовании с участием почти 5 тыс пациентов с СД 2 типа индуцированная потеря веса ассоциировалась со снижением смертности от ССЗ на 28% [33]. Пока не известно, связано ли улучшение сердечно-сосудистых исходов у людей, принимающих метформин, со скромной потерей веса или оно обусловлено прямым действием препарата, однако известно, что инсулинотерапия обычно вызывает увеличение веса [32].
Влияние на артериальное давление
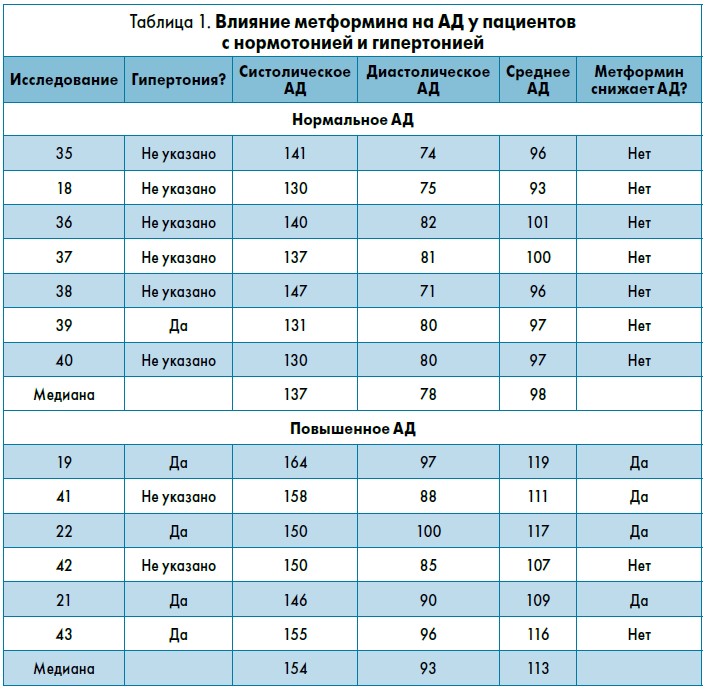
Обычно из обзоров литературы следует вывод о том, что метформин не влияет на АД [26, 30]. Так, в исследовании Программы по профилактике диабета, в котором 70% пациентов имели нормотонию, метформин не оказывал заметного влияния на АД или увеличение частоты новых случаев гипертонии по сравнению с плацебо [34]. Поэтому логично было бы разделить и проанализировать исследования, участники которых имели нормальное АД и в группах с гипертонией. Мы включили в анализ только те исследования, в которых было указано базовое АД в популяции, и подробно рассмотрели 13 исследований, соответствующих этим критериям [18, 19, 21, 22, 35-43]. Поскольку во многих исследованиях не указывалось, была ли у пациентов изначальная гипертония, мы рассчитали среднее АД для всех исследований с помощью онлайн-калькулятора (http://www.physiologyweb.com/calculators./mean_arterial_pressure_calculator.html), а затем разделили исследования на две группы: нормальное АД (<107 мм рт. ст.) и повышенное АД (≥107 мм рт. ст.). Результаты показаны в таблице 1.
Хотя критерии разделения на группы АД являются произвольными, в отношении систолического, диастолического и среднего АД существует четкое разделение. В группе пациентов с нормальным АД в 7 исследованиях изучаемый эффект метформина не наблюдался, в то время как препарат снижал АД в 4 из 6 исследований у пациентов с гипертонией. Из двух исследований в группе с повышенным АД и отрицательными результатами в одном [43] метформин назначался в дозе 500 мг/сут, а в другом показатель среднего АД был самым низким [42]. Таким образом, полученные результаты свидетельствуют о том, что метформин снижает повышенное АД и не влияет на нормальное. Кроме того, в ретроспективном сравнительном когортном исследовании с участием около 3500 пациентов с СД 2 типа было показано, что группа, получавшая метформин, имела более низкое АД по сравнению с группой, получавшей ПСМ [45]. Аналогичные результаты были получены в проспективных исследованиях, сравнивающих влияние метформина и глибурида на АД у пациентов с СД 2 типа, как с нормотонией [23], так и с гипертонией [46]. Суммарно все эти данные указывают на то, что метформин может снижать АД у лиц с гипертонией, но большинство доказательств показывает, что этого не происходит у людей с нормальным АД.
Механизм снижения АД в популяции с артериальной гипертензией может заключаться в уменьшении активности симпатической нервной системы. В одном исследовании было показано значительное снижение плазменных уровней норадреналина в ответ на терапию метформином [22]. В другом сравнительном плацебо-контролируемом исследовании метформин в суточной дозе 1700 мг в течение 4 мес назначали 120 пациентам с СД 2 типа и нормотонией, которые показали значительное увеличение вариабельности интервала R-R, что свидетельствует о снижении тонуса симпатической нервной системы [47].
Применение у пациентов с болезнями почек
Практически 100% метформина, всасываемого из желудочно-кишечного тракта, выводится с мочой в неизмененном виде [49]. И хотя при СД 2 типа, который связан с высоким риском развития ССЗ [50], часто встречается ХБП, нарушение почечной функции может ограничивать использование метформина. Обновленные руководства AACE/ACE не рекомендуют назначать препарат при СКФ≤45 мл/мин/1,73 м2 [2]. Широко распространенное мнение о том, что метформин не используют при снижении почечной функции [53], в значительной степени основано на опасениях по поводу развития лактоацидоза, вызванного применением фенформина [52, 54, 55]. Следует отметить, что лактоацидоз встречается и у пациентов, принимающих метформин, и сопровождается гипоксией (лактоацидоз типа А), однако не в большинстве случаев [56]. В литературе описаны редкие случаи развития «нормоксического» лактоацидоза типа В, включая передозировку метформина [52]. Однако в больших популяциях пациентов (≥100 000 пациенто-лет), принимающих метформин, доказательств повышенного риска лактоацидоза получено не было [55, 57, 58].
В отличие от ситуации с фенформином, объяснение крайней редкости возникновения лактоацидоза у пациентов, получавших метформин, заключается в различиях химического состава этих двух соединений. Фенформин является липофильным веществом, которое активно связывается с митохондриальными мембранами и гидроксилируется в печени, тогда как метформин является гидрофильным, с митохондриями активно не связывается и в тканях не метаболизируется [49]. Таким образом, существует серьезное обоснование для расширения применения метформина у некоторых пациентов с ХБП‑3 [52, 55, 59, 60]. Кроме того, пациенты с высоким риском ССЗ получают дополнительные преимущества на фоне терапии метформином, так же как и пациенты с нормальной функцией почек [50]. Так, в шведском исследовании метформин хорошо переносился пациентами с ХБП‑3 и его применение ассоциировалось с более низкой (на 13%) смертностью от всех причин в данной группе [54].
Также установлено, что использование метформина связано с достоверно меньшим риском снижения функции почек по сравнению с ПСМ [61]. На необходимость расширения применения метформина у пациентов с ХБП‑3 указывают и ADA/EASD [59].
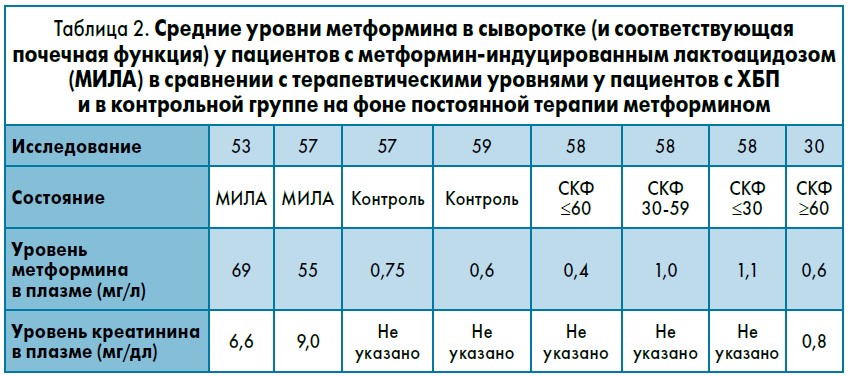
Следует также подчеркнуть, что безопасность препарата была подтверждена в крупных исследованиях [55, 57, 58]. Однако необходимо учитывать потенциальную возможность развития лактоацидоза типа В у пациентов. При использовании метформина в терапевтических дозах у пациентов с нормальной функцией почек и у больных ХБП уровень препарата в плазме должен поддерживаться ниже 3,0 мг/л [52, 62-64], в среднем <1,0 мг/л (табл. 2).
Лабораторный мониторинг уровня метформина в плазме позволяет безопасно использовать этот препарат у пациентов с ХБП‑3 [52, 55]. У отдельных пациентов (СКФ 30-44 мл/ мин/1,73 м2) дополнительную безопасность применения метформина можно обеспечить путем мониторинга его минимальных уровней в плазме. В рутинной практике избирательный подход к клинически доступному мониторингу метформина в плазме с возможностью корректировки дозы препарата позволил бы увереннее назначать его пациентам с ХБП‑3. Следует также заметить, что в первые часы острого повреждения почек уровень креатинина сыворотки может не отражать СКФ, поэтому у отдельных пациентов (СКФ 30-44 мл/мин/1,73 м2) необходимо более тщательно проводить мониторинг почечной функции (например, ежеквартально измерять уровни креатинина).
Применение у пациентов с сердечной недостаточностью
Распространенность СН (как и СД 2 типа) увеличивается с возрастом. Вероятность развития СН у пациентов с диабетом гораздо выше, чем у людей без него: 30,9 и 12,4 на 1000 человеко-лет, ОР=25 [52, 55].
В ряде исследований по изучению возможной взаимосвязи между использованием сахароснижающих препаратов и риском развития СН было показано, что начало инсулинотерапии ассоциировалось с удвоением риска новых эпизодов СН [68], а очевидный риск СН при использовании тиазолидиндионов связан с задержкой натрия [69]. Что касается метформина, то в начале его использования в США в аннотации в качестве противопоказания также была отмечена СН [70]. Однако при этом метформин часто использовался у пациентов с СН [71]. По мере получения новых данных о безопасности применения препарата у таких пациентов FDA впоследствии отозвала противопоказания [71]. Дальнейшие исследования по изучению взаимосвязи между терапией метформином и сердечно-сосудистыми исходами показали снижение новых эпизодов СН у пациентов с СД 2 типа [73, 74]. Учитывая, что у пациентов, получавших метформин, АД оказалось ниже, чем у пациентов, принимавших ПСМ [23, 45, 46], смертность от СН в первой группе также снижалась [75]. Когортное исследование более чем 15 тыс пациентов с диабетом, получавших метформин, показало снижение смертности от СН почти на треть по сравнению с людьми, которые этот препарат не принимали [71]. Подобные результаты продемонстрировало и недавнее проспективное обсервационное исследование с участием почти 20 тыс человек с СД 2 типа [8].
Как упоминалось выше, метформин вызывает снижение потребления пищи на 250-300 ккал/день [32]. При этом даже небольшая потеря веса, достижимая и при модификации образа жизни, оказывает благоприятное влияние на фракцию выброса и функциональный класс у пациентов с СН [79]. Потеря веса снижает потребность миокарда в кислороде (mVO2) по тому же механизму, который объясняет его увеличение с повышением ИМТ [80]. При этом спонтанная потеря веса является прогностически неблагоприятной в терминальной стадии СН [76]. Терапия метформином уменьшает перекисное окисление свободных жирных кислот [48], что приводит к снижению mVO2 и оказывает благоприятное влияние на фракцию выброса и функциональный класс у пациентов с СН [79].
Установлено, что у пациентов с СН наблюдается повышенная симпатическая активность [84]. Терапия метформином у пациентов с СД 2 типа и ожирением приводит к увеличению вариабельности сердечного ритма, что свидетельствует о снижении симпатического тонуса [47]. Кроме того, метформин снижает концентрацию норадреналина в плазме [22], которая увеличивается с приемом пищи и уменьшается с потерей веса [87]. Метформин также снижает постпрандиальную концентрацию инсулина [17], который, как известно, активирует симпатическую нервную систему [88]. Таким образом, благоприятное влияние метформина на СН, возможно, достигается путем снижения симпатической активности и потери веса в комбинации.
Механизмы действия
Метформин резко снижает гликемию, подавляя глюконеогенез в печени посредством ингибирования митохондриального комплекса дыхательной цепи, что приводит к активации пути АМФК-FOX03, снижению перекисного окисления жирных кислот и уменьшению синтеза активных форм кислорода [89, 90]. В результате улучшаются биодоступность оксида азота, функция эндотелия и сосудистый кровоток [91]. При постоянном использовании препарат улучшает чувствительность тканей к инсулину [52].
Существуют и другие эффекты, которые являются более важными в обеспечении очевидных долгосрочных преимуществ использования метформина. Хотя препарат, который всасывается в кровоток, оказывает существенное влияние на метаболизм глюкозы, это не объясняет потерю веса на фоне терапии метформином. Так, было установлено, что более половины перорального метформина не попадает в кровоток [49], а доставляется в терминальный отдел подвздошной кишки, где может вызвать нарушения всасывания желчных кислот [93]. При этом мальабсорбированные желчные кислоты обладают свойством стимулировать высвобождение инкретинов в L-клетках, во множестве присутствующих в тонкой кишке. В результате задерживается опорожнение желудка, что в конечном итоге вызывает ощущение сытости [52, 93]. Этими эффектами также может объясняться снижение энергетических затрат на фоне терапии метформином [32].
Большой интерес представляет и влияние метформина на постпрандиальную гликемию, которое может быть связано с инкретин-опосредованным действием на моторику желудочно-кишечного тракта, вызывающим задержку всасывания углеводов [52, 93, 94].
Клиническое применение
В США чаще всего метформин назначают дважды в день, при этом максимальная эффективная суточная доза составляет 2000 мг [95]. Однако эта рекомендация относится к гликемическому действию препарата; по отношению к воздействию на сердечно-сосудистые исходы эффективная суточная доза не определена. В единственном проспективном рандомизированном исследовании, продемонстрировавшем явную пользу метформина для сердечно-сосудистой системы, препарат назначался в суточной дозе 2550 мг, разделенной на 3 приема [4].
Наиболее частыми побочными эффектами, связанными с метформином, являются симптомы со стороны желудочно-кишечного тракта, особенно диарея. Этот симптом встречается у приблизительно 30% пациентов, принимающих метформин [96]. Как правило, желудочно-кишечные расстройства носят легкий характер и быстро проходят; тяжелая диарея возникает вследствие неправильного дозирования (высокая начальная доза) или применения препарата натощак. Также установлено, что около 5% пациентов не переносят метформин из-за развития у них побочных эффектов [97]. Дефицит витамина В12 биохимически определяется у приблизительно 6% пациентов [98], однако его клиническая значимость не выявлена [99].
Выводы
Метформин заслуженно занимает доминирующую позицию в терапии СД 2 типа вследствие сильного благоприятного воздействия на сердечно-сосудистый риск.
Механизмы, ответственные за это преимущество, пока не ясны и включают улучшение липидного профиля и снижение повышенного АД. Данные эффекты могут быть частично связаны с уменьшением потребления энергии и умеренной потерей веса.
Метформин, по-видимому, безопасен для применения у пациентов с ХБП‑3, поэтому рекомендации по расширению его использования у этой группы являются оправданными. Мониторинг уровня метформина в плазме наряду с более частым мониторингом почечной функции необходим для некоторых категорий пациентов и позволяет безопасно корректировать дозу препарата.
Для пациентов с СН метформин не только безопасен, но и оказывает благоприятное влияние на сердечную функцию.
A. Anabtawi, MD; J.M. Miles, MD.
Адаптированный перевод
DOI:10.4158/EP151145.RAR © 2016 AACE.
Список литературы находится в редакции.
Подготовила Наталия Позднякова
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (44) грудень 2018 р.