22 лютого, 2019
Мігрень: нові дані щодо патогенезу, соціально-економічні наслідки та сучасні підходи до лікування
За матеріалами 12-го Конгресу Європейської федерації головного болю (EHF) спільно з 32-м Національним конгресом Італійського товариства з вивчення головного болю (SISC), 28-30 вересня, м. Флоренція, Італія
Гормональні контрацептиви в жінок з мігренню
Багато пацієнток з мігренню застосовують гормональні контрацептиви, оскільки зазначена патологія найчастіше зустрічається в жінок репродуктивного віку. Враховуючи те, що деякі препарати для лікування мігрені, зокрема триптани, протипоказані під час вагітності, важливо бути впевненим в ефективності контрацепції та відсутності в протизаплідних засобах негативного впливу на мігрень. При цьому деякі контрацептивні стратегії можуть позитивно впливати на перебіг мігрені, особливо в жінок, у яких захворювання загострюється перименструально.
Менструація асоціюється з двома незалежними тригерами мігрені: різким зниженням рівнів естрогенів перед менструацією та вивільненням простагландинів, яке часто супроводжує менорагію та/або дисменорею. Розуміння того, яким чином різні методи гормональної контрацепції впливають на ці механізми, дозволяє більш ефективно лікувати мігрень.
 Гормональні методи є найпопулярнішими в попередженні небажаної вагітності й включають застосування комбінованих гормональних контрацептивів (комбіновані оральні контрацептиви, контрацептивне вагінальне кільце, комбінований трансдермальний пластир) та контрацептивів, що містять лише прогестоген (таблетки, підшкірні імплантати, внутрішньом’язове/підшкірне депо медроксипрогестерону ацетату, внутрішньоматкова система з левоноргестрелом).
Гормональні методи є найпопулярнішими в попередженні небажаної вагітності й включають застосування комбінованих гормональних контрацептивів (комбіновані оральні контрацептиви, контрацептивне вагінальне кільце, комбінований трансдермальний пластир) та контрацептивів, що містять лише прогестоген (таблетки, підшкірні імплантати, внутрішньом’язове/підшкірне депо медроксипрогестерону ацетату, внутрішньоматкова система з левоноргестрелом).
Комбіновані оральні контрацептиви містять естроген (зазвичай синтетичний етинілестрадіол) і прогестоген. Додавання етинілестрадіолу забезпечує більшу оваріальну супресію та кращий контроль циклу порівняно з лише прогестогенними контрацептивами. Зі зменшенням дози етинілестрадіолу підвищується імовірність проривних кровотеч. Прогестогени першого та другого покоління, отримані з тестостерону, чинять андрогенні ефекти, що врівноважує дію естрогенів. Більш нові прогестини третього та четвертого покоління мають нейтральний андрогенний ефект.
Гормональні контрацептиви, призначені для застосування в безперервному режимі або з більш коротким інтервалом без прийому гормонів, дозволяють зменшити частоту та тяжкість проявів різкого зниження рівнів естрогенів, а отже, можуть позитивно вливати на перебіг мігрені. Натомість міні-пілі та імплантати з дезоноргестрелом пригнічують овуляцію, проте не можуть передбачувано інгібувати активність яєчників. Це може призводити до коливань рівнів естрогенів і проривних кровотеч (MacGregor E. A. Abstract S18).
Мігрень з початком у дитячому віці є епігенетичним захворюванням
 За визначенням C. Waddington (1942), епігенетика – це фактори та події зовнішнього середовища, які можуть впливати на експресію генів і структуру хроматину шляхом посттрансляційних змін хвостів гістонових білків, метилювання або сайленсингу ДНК, що призводить до змін структури ДНК без порушення генетичного коду. Останнім часом з’являється все більше доказів того, що епігенетичні механізми можуть пояснювати вплив ендогенних та екзогенних негенетичних факторів на частоту, тяжкість і генез мігрені.
За визначенням C. Waddington (1942), епігенетика – це фактори та події зовнішнього середовища, які можуть впливати на експресію генів і структуру хроматину шляхом посттрансляційних змін хвостів гістонових білків, метилювання або сайленсингу ДНК, що призводить до змін структури ДНК без порушення генетичного коду. Останнім часом з’являється все більше доказів того, що епігенетичні механізми можуть пояснювати вплив ендогенних та екзогенних негенетичних факторів на частоту, тяжкість і генез мігрені.
У деяких дослідженнях встановлено, що гормональні зміни, особливо в жінок, недостатній сон, пропуск прийомів їжі та стрес суттєво впливають на прояви мігренозних нападів. Завдяки епігенетичним механізмам жіночі гормони можуть змінювати баланс між інгібіторною та збудливою нейротрансмісією, підвищуючи збудливу нейрональну активність.
Іншим важливим епігенетичним фактором є ранній стресовий досвід. Так, висока розповсюдженість головного болю та мігрені спостерігається в дорослих, які в дитячому віці зазнавали сексуального, емоційного, фізичного або домашнього насильства. Ранній негативний досвід шляхом епігенетичних змін може мати віддалений шкідливий вплив на функціонування гіпоталамо-гіпофізарно-надниркової вісі й активність імунної системи, що асоціюється з більш тяжкими й резистентними до лікування нападами мігрені (Natalucci G. et al. Abstract S32).
Мігрень і метаболічний синдром
 Мігрень вважають неврологічним захворюванням, що характеризується підвищенням периферичної трійчасто-судинної активації у відповідь на процеси центральної сенситизації. Проте патогенез мігрені є складним і залучає, зокрема, метаболічні порушення.
Мігрень вважають неврологічним захворюванням, що характеризується підвищенням периферичної трійчасто-судинної активації у відповідь на процеси центральної сенситизації. Проте патогенез мігрені є складним і залучає, зокрема, метаболічні порушення.
Огляд літератури показав, що метаболічний синдром (МС) частіше зустрічається в пацієнтів з мігренню (21,8% з аурою, 16,8% без аури) порівняно з контролем (14,5%) та асоціюється з розвитком хронічної форми головного болю, зумовленої зловживанням лікарськими препаратами. Ці дані узгоджуються з результатами епідеміологічних досліджень, які вказують на підвищений ризик цереброваскулярних захворювань у пацієнтів з мігренню.
Добре відомо, що ожиріння й артеріальна гіпертензія є факторами ризику розвитку та хронізації мігрені, натомість зниження маси тіла та контроль артеріального тиску можуть зменшувати тяжкість мігрені. У пацієнтів з мігренню проба з навантаженням глюкозою (тест на толерантність до глюкози) спричиняє значне підвищення плазмових рівнів інсуліну та глюкози порівняно з контролем. Крім того, в багатьох пацієнтів з мігренню спостерігається дуже пізня гіпоглікемічна відповідь, що муже бути тригером нападу мігрені. Роль гіпоглікемії, однієї з ранніх ознак інсулінорезистентності, опосередковано підтверджується тим, що розвиток діабету, для якого характерний стан постійної гіперглікемії, ймовірно, є захисним механізмом проти нападів мігрені. Інсулінорезистентність та інші метаболічні порушення зумовлюють хронічне низькорівневе запалення з вивільненням прозапальних цитокінів (зокрема, CGRP – пептиду, асоційованого з геном прокальцитоніну), що, своєю чергою, призводить до нападу мігрені.
Одним з можливих пояснень високої розповсюдженості мігрені серед пацієнтів з МС є так звана теорія ощадливих генів. Відповідно до цієї теорії, високий рівень життя в західній популяції пов’язаний з підвищеним надходженням нутрієнтів, що є стресом для метаболізму людини, генетично пристосованої до голоду, з подальшим розвитком МС. Якщо мігрень і МС мають спільний генетичний і біологічний фон, це може пояснювати високу розповсюдженість мігрені в загальній популяції (Di Lorenzo С. et al. Abstract S46).
Мігрень і кетогенна дієта
 Кетогенна дієта (КД) – це режим харчування, що характеризується дуже низьким вживанням вуглеводів з метою індукції метаболічного кетозу (фізіологічної ендогенної продукції кетонових тіл) і, відповідно, заміщенням глюкози як енергетичного субстрату для головного мозку. Кетони є дуже ефективним джерелом енергії для мозку, оскільки вони підвищують синтез АТФ зі зниженням окислювального стресу, пов’язаного з активністю мітохондрій. Крім того, кетони мають протизапальний вплив і здатні модулювати збудливість кори завдяки прямому й опосередкованому ГАМК‑ергічному ефекту. На сьогодні розроблено декілька різних типів КД, проте всі вони відрізняються низьким вмістом вуглеводів. Є нормокалорійні (збагачені жирами для компенсації вуглеводів) та гіпокалорійні КД (з нижчим умістом жирів для посилення метаболізму ліпідів у жировій тканині).
Кетогенна дієта (КД) – це режим харчування, що характеризується дуже низьким вживанням вуглеводів з метою індукції метаболічного кетозу (фізіологічної ендогенної продукції кетонових тіл) і, відповідно, заміщенням глюкози як енергетичного субстрату для головного мозку. Кетони є дуже ефективним джерелом енергії для мозку, оскільки вони підвищують синтез АТФ зі зниженням окислювального стресу, пов’язаного з активністю мітохондрій. Крім того, кетони мають протизапальний вплив і здатні модулювати збудливість кори завдяки прямому й опосередкованому ГАМК‑ергічному ефекту. На сьогодні розроблено декілька різних типів КД, проте всі вони відрізняються низьким вмістом вуглеводів. Є нормокалорійні (збагачені жирами для компенсації вуглеводів) та гіпокалорійні КД (з нижчим умістом жирів для посилення метаболізму ліпідів у жировій тканині).
З 1921 р. КД використовують для лікування резистентної епілепсії в дітей. У 1928 р. і 1930 р. з’явилися перші повідомлення про ефективність КД у пацієнтів з мігренню, проте в ті часи вже почали використовувати різні протимігренозні препарати, тому КД не набула популярності. І лише нещодавно, з огляду на те що багато пацієнтів зловживають симптоматичними засобами, а також на велику кількість резистентних до лікування випадків мігрені, увага дослідників знову зосередилася на КД.
У дослідженні, представленому на конгресі EFH, італійські вчені повідомили про 9-річний досвід застосування КД у пацієнтів з головним болем. Вибір дієти (нормо- чи гіпокалорійна) здійснювали залежно від індивідуальних потреб хворих, зокрема з урахуванням надмірної маси тіла. Було встановлено, що КД є корисним інструментом у лікуванні пацієнтів з мігренню (епізодичною та хронічною), а також у хворих з кластерним головним болем. Водночас КД виявилася неефективною в пацієнтів з головним болем напруги та цервікогенним головним болем.
Важливою перевагою КД є її здатність покращувати якість життя пацієнтів. Так, КД може застосовуватися з метою зниження надмірної ваги, що, власне, може покращувати перебіг мігрені. На думку дослідників, перспективним є вивчення екзогенних кетонів, так званої кетогенної таблетки (Pierelli F. et al. Abstract S47).
Номігрен Босналек® – ефективне лікування мігрені без аури
Мігрень без аури (МБА) – це найпоширеніший тип мігренозного болю, частка якого становить 70-90% усіх випадків захворювання. За відсутності лікування напади МБА тривають від 4 до 72 год і часто супроводжуються іншими симптомами, такими як блювання, підвищена чутливість до світла (фотофобія) та/або звуків (фонофобія).
Триптани, ерготамін і дигідроерготамін вважаються дієвими засобами лікування МБА. Проте розвиток цього захворювання є складним і включає цілу низку патогенетичних механізмів, тому монопрепарати в багатьох випадках не здатні забезпечити ефективне переривання нападу.
Номігрен Босналек® – комбінований препарат, який містить раціональне поєднання 5 високоспецифічних компонентів із синергічною дією та в оптимальних дозах: ерготамін тартрат, меклоксамін цитрат, камілофін гідрохлорид, кофеїн та пропіфеназон.
На конгресі EHF було представлено європейське дослідження, метою якого було вивчити ефективність препарату Номігрен Босналек® порівняно із суматриптаном у лікуванні МБА.
За дизайном дослідження було рандомізованим подвійним сліпим плацебо-контрольованим у паралельних групах. У 5 медичних центрах було залучено жінок (n=168) і чоловіків (n=33) з МБА, яких випадковим чином розподілили на дві рівні групи для лікування препаратом Номігрен Босналек® або суматриптаном. Ефективність досліджуваних лікарських засобів оцінювали на підставі зникнення болю через 2 год після прийому, здатності попереджувати повторні напади та за впливом на інші симптоми.
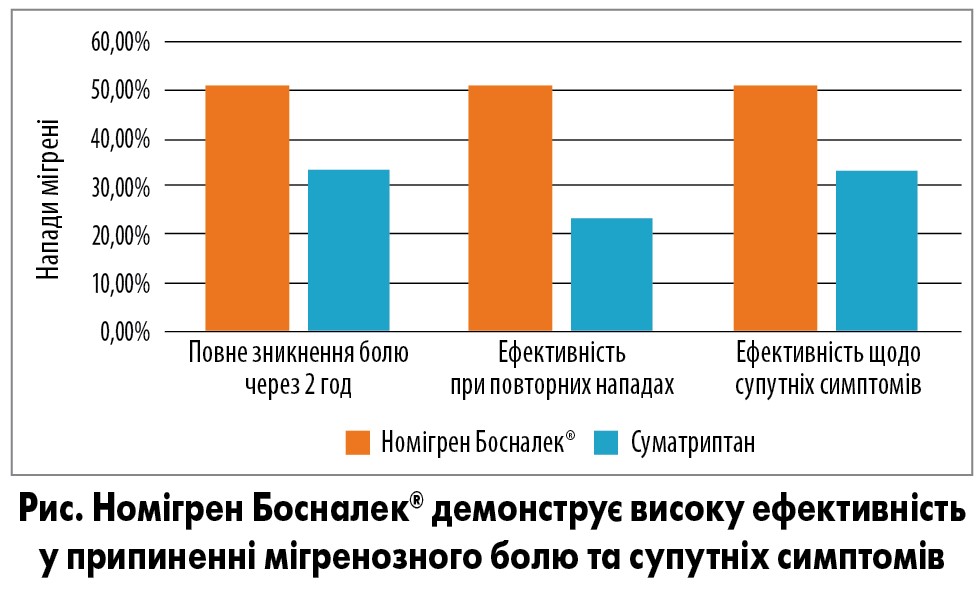 Згідно з отриманими результатами, повне зникнення болю через 2 год було зафіксовано для 51,12% нападів МБА у групі Номігрену Босналек та 33,70% нападів у групі суматриптану (р=0,0015). Так само Номігрен Босналек® продемонстрував високу ефективність під час повторних нападів: відповідний показник становив 50,91% порівняно з 23,73% для суматриптану (р=0,005). У пацієнтів, які отримували Номігрен Босналек®, значно частіше вдавалося позбутися фото-, фоно- та осмофобії (51,12% нападів vs 33,70% при застосуванні суматриптану) (рис.). Про повну неефективність лікування повідомили 9 хворих у групі суматриптану та лише 2 пацієнти в групі Номігрену.
Згідно з отриманими результатами, повне зникнення болю через 2 год було зафіксовано для 51,12% нападів МБА у групі Номігрену Босналек та 33,70% нападів у групі суматриптану (р=0,0015). Так само Номігрен Босналек® продемонстрував високу ефективність під час повторних нападів: відповідний показник становив 50,91% порівняно з 23,73% для суматриптану (р=0,005). У пацієнтів, які отримували Номігрен Босналек®, значно частіше вдавалося позбутися фото-, фоно- та осмофобії (51,12% нападів vs 33,70% при застосуванні суматриптану) (рис.). Про повну неефективність лікування повідомили 9 хворих у групі суматриптану та лише 2 пацієнти в групі Номігрену.
Отже, у проведеному дослідженні Номігрен Босналек® продемонстрував значно кращу ефективність у припиненні головного болю та супутніх симптомів порівняно з суматриптаном у пацієнтів з МБА (Miljkovic S. et al. Abstract P130).
Що відбувається з пацієнтами в різні фази мігрені?
My Migraine Voice – глобальне зрізове дослідження із залученням 11 266 пацієнтів з 31 країни Європи, Америки, Азії та Африки. У дослідження включали дорослих пацієнтів з мігренню за критеріями Міжнародної класифікації головного болю 3-го перегляду (ICHD‑3), які мали принаймні 4 дні з мігренню на місяць протягом останніх 3 міс.
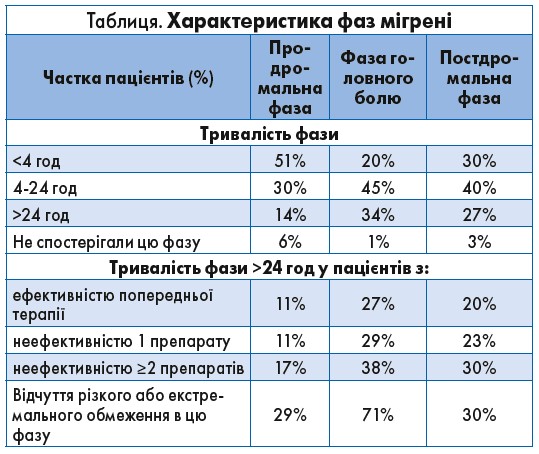 Як показали результати, пацієнти страждали від нападів мігрені в середньому 9,8 дня на місяць; у 37% хворих анамнез мігрені перевищував 15 років. У 44% опитаних напад мігрені тривав ≥1 дня (у 19% – понад 3 дні). Половина пацієнтів (49%) почувалися значно обмеженими в професійній та іншій діяльності протягом усіх трьох фаз мігрені. Майже третина хворих (29%) повідомили про різке або екстремальне обмеження під час продромальної фази, 71% – у фазі головного болю та 30% – протягом постдромальної фази (табл.).
Як показали результати, пацієнти страждали від нападів мігрені в середньому 9,8 дня на місяць; у 37% хворих анамнез мігрені перевищував 15 років. У 44% опитаних напад мігрені тривав ≥1 дня (у 19% – понад 3 дні). Половина пацієнтів (49%) почувалися значно обмеженими в професійній та іншій діяльності протягом усіх трьох фаз мігрені. Майже третина хворих (29%) повідомили про різке або екстремальне обмеження під час продромальної фази, 71% – у фазі головного болю та 30% – протягом постдромальної фази (табл.).
Отже, дослідження My Migraine Voice уперше дозволило кількісно оцінити тягар мігрені під час різних фаз. Власне напад мігрені спричиняє найтяжчі порушення, проте цей тягар значною мірою також поширюється на продромальну та постдромальну фази, особливо в пацієнтів з неефективністю ≥1 симптоматичного препарату (Lanteri-Minet M. et al. Abstract P65).
Економічний та соціальний тягар мігрені у Європі
Мігрень – це тяжке неврологічне захворювання з високою розповсюдженістю у європейській популяції. На конгресі EHF міжнародна група вчених представила новий аналіз клінічних, людських та економічних втрат, асоційованих з епізодичною та хронічною мігренню у Європі.
 Аналіз 68 публікацій і останній звіт Всесвітньої організації охорони здоров’я свідчать, що у Європі тягар мігрені є вищим порівняно з таким епілепсії, розсіяного склерозу та хвороби Паркінсона. Понад 57% пацієнтів з мігренню мають тяжке порушення професійних і соціальних функцій, при цьому в багатьох випадках лікування є неефективним. Нудота та/або блювання супроводжують напади мігрені в 74% хворих. Депресія та/або тривога розвиваються втричі частіше в пацієнтів з мігренню порівняно із загальною популяцією. У пацієнтів з мігренню різко погіршується якість життя, і це погіршення корелює з частотою нападів. Європейці, які страждають на мігрень, відчувають, що захворювання чинить негативний вплив на професійні можливості (76% хворих), ситуацію в сім’ї, вільний час, навчання, сексуальне життя, реалізацію в соціумі, кохання, фінансову ситуацію, кар’єру та дружбу.
Аналіз 68 публікацій і останній звіт Всесвітньої організації охорони здоров’я свідчать, що у Європі тягар мігрені є вищим порівняно з таким епілепсії, розсіяного склерозу та хвороби Паркінсона. Понад 57% пацієнтів з мігренню мають тяжке порушення професійних і соціальних функцій, при цьому в багатьох випадках лікування є неефективним. Нудота та/або блювання супроводжують напади мігрені в 74% хворих. Депресія та/або тривога розвиваються втричі частіше в пацієнтів з мігренню порівняно із загальною популяцією. У пацієнтів з мігренню різко погіршується якість життя, і це погіршення корелює з частотою нападів. Європейці, які страждають на мігрень, відчувають, що захворювання чинить негативний вплив на професійні можливості (76% хворих), ситуацію в сім’ї, вільний час, навчання, сексуальне життя, реалізацію в соціумі, кохання, фінансову ситуацію, кар’єру та дружбу.
Розповсюдженість є найвищою серед жінок і чоловіків на піку їх економічної активності (у віковому періоді 25-55 років). У Європі загальні втрати від мігрені перевищують 110 млрд євро на рік, з них 72-98% – це непрямі втрати (дві третини непрямих втрат – через знижену продуктивність). Щорічні прямі втрати внаслідок хронічної мігрені в 4 рази перевищують такі від епізодичної мігрені (Benhaddi H. et al. Abstract O24).
12th European Headache Federation Congress jointly with 32nd National Congress of the Italian Society for the Study of Headaches. Meeting Abstracts. The Journal of Headache and Pain, 2018; 19 (Suppl 1): 80.
Підготував Андрон Буряк
Медична газета «Здоров’я України 21 сторіччя» № 23 (444), грудень 2018 р.


