23 лютого, 2019
Високоінтенсивні та невисокоінтенсивні статини в пацієнтів, які досягли цільових показників холестерину ліпопротеїнів низької щільності після черезшкірного коронарного втручання
Вступ
У кількох рандомізованих дослідженнях високоінтенсивна терапія статинами (ВІТС) продемонструвала переваги у вторинній профілактиці кардіоваскулярних подій порівняно з терапією статинами помірної інтенсивності дії. У зв’язку з цим рекомендації Американської колегії кардіологів та Американської асоціації серця (ACC/AHA) з контролю холестерину (2013) радять призначати пацієнтам із кардіоваскулярними захворюваннями атеросклеротичного генезу високоінтенсивну терапію, а саме аторвастатин у дозі 40 чи 80 мг або розувастатин у дозі 20 чи 40 мг. Однак лишається невідомим, чи сприятливі ефекти ВІТС зумовлені саме їх призначенням чи виключно досягненням нижчих показників холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) при застосуванні цих препаратів. Відомо, що зниження ХС ЛПНЩ за допомогою статинотерапії сприяє зменшенню кількості основних кардіоваскулярних подій незалежно від типу й інтенсивності препарату. З огляду на це рекомендації Європейського товариства кардіологів та Європейського товариства атеросклерозу (ESC/EAS) із лікування дисліпідемій пропонують вважати цільовим показник ХС ЛПНЩ <1,8 ммоль/л (70 мг/дл) або прагнути до зменшення ХС ЛПНЩ щонайменше на 50% від вихідного рівня для осіб дуже високого ризику, не вказуючи вид чи інтенсивність статину. Відмінності між згаданими рекомендаціями спричинили дискусії та плутанину в щоденній практиці. Питання різниці наслідків у пацієнтів з однаковим рівнем ХС ЛПНЩ залежно від інтенсивності застосовуваного статину залишається суперечливим. Тому метою цього дослідження стало вивчення зв’язку між інтенсивністю дії статину та довготривалим прогнозом у пацієнтів, які підлягали черезшкірним коронарним втручанням (ЧКВ) і досягали цільових показників ХС ЛПНЩ.
Методи
Популяція учасників дослідження була вибрана з реєстру ЧКВ медичного центру Samsung (м. Сеул, Корея). Протягом лютого 2003 – грудня 2014 року ЧКВ зі встановленням драг-елютинг стентів підлягали 8148 осіб. До остаточного аналізу було включено 1746 пацієнтів, які досягли усереднених за часом цільових показників ХС ЛПНЩ протягом періоду спостереження. Далі цих пацієнтів було класифіковано на дві групи відповідно до інтенсивності призначеного при виписці після ЧКВ статину: групу ВІТС (n=372) та групу невисокоінтенсивної терапії статинами – НВІТС (n=1374). Визначення інтенсивності статинів ґрунтувалося на рекомендаціях ACC/AHA. Статинами високої інтенсивності вважалися аторвастатин (40 та 80 мг) і розувастатин (20 мг), невисокої – всі інші статини. Розувастатин 40 мг у Кореї не зареєстрований.
Пацієнти підлягали обстеженню через 1, 6 та 12 міс після первинної процедури ЧКВ, далі – щорічно. Необхідна інформація була отримана з електронних реєстрів пацієнтів, додаткова – з карт пацієнтів або за телефоном. Окрім того, аналізувався усереднений за часом показник високочутливого С‑реактивного білка (вчСРБ).
Як первинна кінцева точка розглядалися великі кардіоваскулярні події (сумарна частота кардіоваскулярної смерті, інфаркту міокарда (ІМ), інсульту) протягом періоду спостереження. Кардіоваскулярною смертю вважалася та, для якої не було підтверджено іншої етіології. Вторинними кінцевими точками були смерть від усіх причин, повторна реваскуляризація й окремі події – компоненти первинної кінцевої точки.
Результати
У групі ВІТС спостерігалася більша частота цукрового діабету, випадків цереброваскулярних катастроф у анамнезі, гострого коронарного синдрому при госпіталізації, була більша кількість курців. Ацетилсаліцилова кислота, інгібітори P2Y12, β-блокатори, інгібітори ангіотензинперетворювального ферменту та блокатори рецепторів ангіотензину ІІ однаково часто призначалися під час виписки в обох групах. У групі НВІТС при первинному ЧКВ частіше встановлювалися стенти першого покоління, але загальна кількість стентів, їх середній діаметр і місце розташування між групами не відрізнялися. Після проведення псевдорандомізації до аналізу було включено 367 пацієнтів групи ВІТС і 798 – НВІТС. Ці групи значущо не відрізнялися за основними характеристиками, призначеними ліками й особливостями проведених ЧКВ.
Загальна популяція
Прихильність до статинотерапії
У групі ВІТС прихильність до лікування статинами становила 98,5% через 2 роки та 87,3% через 3 роки після проведення ЧКВ. У групі НВІТС прихильність до статинотерапії становила 99,2 та 94,8% відповідно. Отже, через 3 роки спостереження прихильність до прийому статинів у групі ВІТС була достовірно нижча, ніж у групі НВІТС (87,3 проти 94,8%; p<0,01).
Зміни в показниках ХС ЛПНЩ і вчСРБ
У групі ВІТС визначався вищий вихідний рівень ХС ЛПНЩ, аніж у групі НВІТС (126±41 проти 112±41 мг/дл; р<0,01); вихідні показники холестерину ліпопротеїнів високої щільності та тригліцеридів не відрізнялися. Відмінність за усередненим за часом показником ХС ЛПНЩ після статинотерапії була хоч і незначною, але достовірною (59±13 мг/дл у групі ВІТС проти 61±12 мг/дл у групі НВІТС; р=0,04). ВІТС знижували ХС ЛПНЩ більш виражено – приблизно на 0,4 ммоль/л більше, ніж НВІТС. Різниця у відсотковому зниженні показника ХС ЛПНЩ від вихідного рівня між цими групами становила 8,6% на користь ВІТС (48,0 проти 39,4%; р<0,01). Зниження вчСРБ також було достовірно більшим у групі ВІТС (6,6±34,8 проти 2,1±24,6 мг/л у групі НВІТС; р=0,04).
Стандартизована популяція
Вихідний рівень ХС ЛПНЩ був однаковим в обох групах (125±41 проти 123±41 мг/дл; р=0,54). Після статинотерапії в групі ВІТС усереднений за часом показник ХС ЛПНЩ став достовірно нижчим, аніж у групі НВІТС (59±13 проти 62±13 мг/дл; р=0,03). ВІТС знижували ХС ЛПНЩ на приблизно 0,1 ммоль/л більше за НВІТС. Різниця між групами у відсотковому зниженні ХС ЛПНЩ від вихідного рівня становила 5,0% (47,9 проти 42,9%; р<0,01). Зниження вчСРБ від вихідного рівня було достовірно більшим у групі ВІТС (6,7±35,1 проти 2,1±19,0 мг/л; р=0,04).
Клінічні наслідки
Загальна популяція
Медіана тривалості періоду спостереження становила 4,2 року (міжквартильний розмах – 2,2-5,0). Клінічні наслідки представлені в таблиці. Великі кардіоваскулярні події трапилися в 110 пацієнтів, у тому числі 53 кардіальні смерті, 30 ІМ та 51 інсульт. Частота великих кардіоваскулярних подій була достовірно нижчою в групі ВІТС, аніж у групі НВІТС (4,1 проти 9,9%; стандартизоване ВР 0,42; 95% ДІ 0,23-0,79; р<0,01). Серцеві смерті також рідше спостерігалися в групі ВІТС (0,8 проти 4,8%; стандартизоване ВР 0,29; 95% ДІ 0,09-0,94; р=0,04). Однак за умови визнання кардіоваскулярними смертями лише тих смертей, для яких була точно встановлена кардіальна етіологія, кардіоваскулярна смертність між групами достовірно не відрізнялася (0,6 проти 2,8%; стандартизоване ВР 0,31; 95% ДІ 0,07-1,34; р=0,12). Хоча в групі ВІТС спостерігалася тенденція до меншої частоти смерті від усіх причин та інсультів порівняно з групою НВІТС, різниця не досягла рівня достовірності.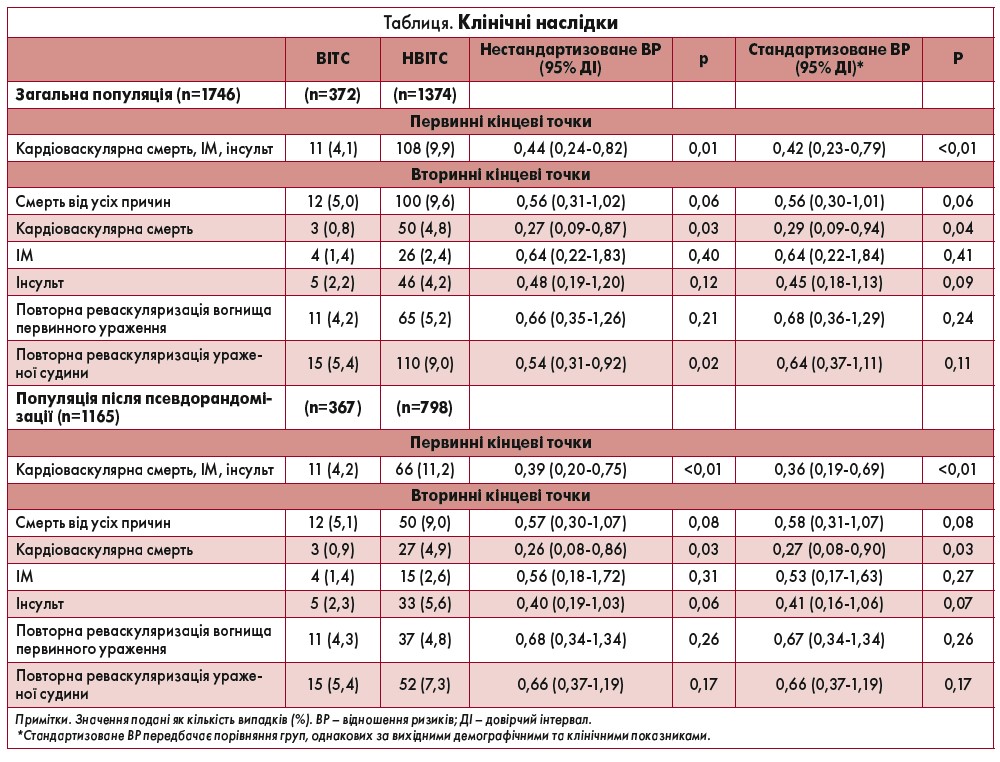
Стандартизована популяція
У стандартизованій популяції медіана тривалості періоду спостереження становила 4,1 року (міжквартильний розмах – 2,1-5,0). Протягом цього часу сталося 77 великих кардіоваскулярних подій. Їх частота була достовірно нижче в групі ВІТС, аніж у групі НВІТС (4,2 проти 11,2%; стандартизоване ВР 0,36; 95% ДІ 0,19-0,69; р<0,01). Серцева смерть також рідше спостерігалася в групі ВІТС, аніж у групі НВІТС (0,9 проти 4,9%; стандартизоване ВР 0,27; 95% ДІ 0,08-0,90; р=0,03). Хоча стосовно смерті від усіх причин та інсульту відзначалася тенденція до меншої частоти в групі ВІТС, аніж у групі НВІТС, різниця не досягла рівня достовірності.
Аналіз окремих підгруп
Для визначення того, чи переваги ВІТС спостерігаються стало в усій популяції дослідження, було підраховано нестандартизоване ВР для великих кардіоваскулярних подій у різних підгрупах учасників (рис.). Переваги ВІТС виявлялися в усіх проаналізованих підгрупах.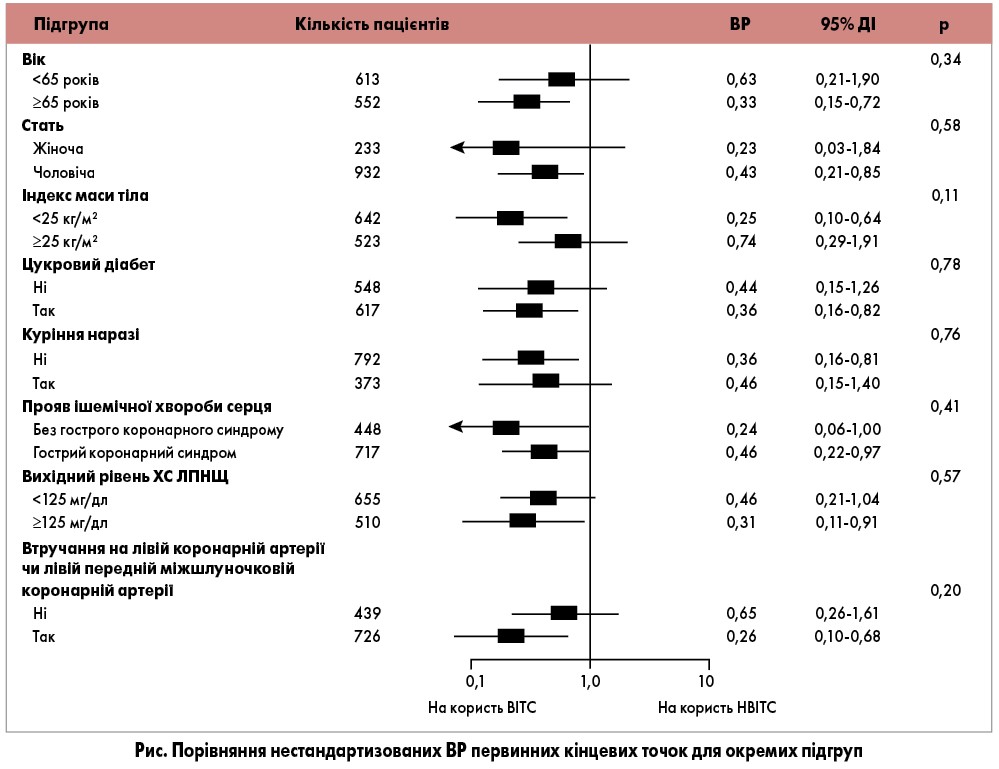
Обговорення
У дослідженні було порівняно довготривалі клінічні наслідки залежно від інтенсивності дії призначеного статину в пацієнтів, які досягали цільових показників ХС ЛПНЩ після ЧКВ. Основні висновки є такими:
- у пацієнтів групи ВІТС відзначалася достовірно менша частота великих кардіоваскулярних подій, аніж у групі НВІТС;
- цей феномен фіксувався в стандартизованій популяції та окремих підгрупах дослідження;
- усереднений за часом показник ХС ЛПНЩ, розрахований за кількома значеннями ХС ЛПНЩ після ЧКВ, був достовірно нижчим у групі ВІТС, аніж у групі НВІТС, хоча різниця була невеликою;
- зниження вчСРБ від вихідного рівня було достовірно більшим у групі ВІТС, аніж у групі НВІТС.
Обмежені дані стосовно порівняння різних стратегій статинотерапії в пацієнтів після ЧКВ
У всіх пацієнтів, які підлягають коронарній реваскуляризації з приводу ішемічної хвороби серця, слід якомога раніше розпочинати статинотерапію незалежно від вихідного рівня холестерину. Однак провідні американські та європейські організації рекомендують застосовувати різні ліпідознижувальні стратегії для вторинної профілактики в пацієнтів із ЧКВ. Тоді як рекомендації ESC/EAS концентруються на зниженні ХС ЛПНЩ до специфічних цільових показників, рекомендації ACC/AHA вказують на потребу обирати лікування залежно від інтенсивності дії статину без специфічного цільового значення ХС ЛПНЩ. Така різниця між наявними рекомендаціями призводить до плутанини в клінічних умовах.
Під час періоду дослідження ВІТС призначалася 14,2% пацієнтів, щодо яких у проаналізованому реєстрі наявні дані про тип і дозування статину. Хоча частка призначення ВІТС зросла до 41,9% після виходу згаданих американських рекомендацій у листопаді 2013 р., НВІТС і надалі часто застосовують для вторинної профілактики в пацієнтів, які підлягають ЧКВ. Ці спостереження свідчать про відсутність згоди стосовно контролю ХС ЛПНЩ із метою вторинної профілактики. У метааналізі Cholesterol Treatment Trialists’ Collabolation зниження ХС ЛПНЩ на 1 ммоль/л (близько 40 мг/дл) супроводжувалося зменшенням ризику великих кардіоваскулярних подій приблизно на 22% незалежно від типу та дози статину. Крім того, нещодавні дослідження продемонстрували, що нестатинові ліпідознижувальні засоби (езетиміб, інгібітори білка – переносника ефірів холестерину) за умови додавання до статинів здатні сприяти ще більшому зниженню ХС ЛПНЩ і покращувати наслідки для пацієнта. Ці результати підтримують стратегію, засновану на встановленні цільового показника ХС ЛПНЩ. Однак кілька ключових досліджень статинотерапії у вторинній профілактиці, котрі порівнювали ВІТС і статинотерапію помірної інтенсивності, виявили, що ВІТС переважала в зниженні частоти великих кардіоваскулярних подій. Отже, порівнювати стратегії, що ґрунтуються на інтенсивності дії статинів і цільових показниках ХС ЛПНЩ, надзвичайно складно, особливо в пацієнтів з однаковими рівнями ХС ЛПНЩ. У зв’язку з цим у дослідженні було порівняно довготермінові клінічні наслідки прийому ВІТС та НВІТС пацієнтами, що досягли цільових рівнів ХС ЛПНЩ після ЧКВ.
Імовірні пояснення переваг ВІТС
У дослідженні ВІТС була дієвішою в запобіганні великим кардіоваскулярним подіям у пацієнтів після ЧКВ, аніж НВІТС. Існує кілька ймовірних пояснень цьому феномену. По-перше, в групі ВІТС було досягнуто нижчих показників усередненого за часом ХС ЛПНЩ, аніж у групі НВІТС, а за даними метааналізів і рандомізованих контрольованих досліджень більш виражене зниження ХС ЛПНЩ супроводжується більш значним зменшенням частоти великих кардіоваскулярних подій. По-друге, відсоткова частка зниження ХС ЛПНЩ була вищою в групі ВІТС, аніж у групі НВІТС. В узагальненому аналізі трьох великих досліджень статинів S. Bangalore та співавт. (2016) повідомили, що серед пацієнтів із досягнутим рівнем ХС ЛПНЩ ≤70 мг/дл особи зі зменшенням цього показника на <50% мали істотно вищий ризик кардіоваскулярних подій, аніж представники групи зі зниженням ХС ЛПНЩ на ≥50%. Більша відсоткова частка зниження ХС ЛПНЩ у групі ВІТС порівняно з групою НВІТС може частково пояснювати відмінності в ризику великих кардіоваскулярних подій. По-третє, виявлені переваги групи ВІТС є більшими, ніж очікувані переваги від подібного зниження ХС ЛПНЩ відповідно до попередніх даних. Це свідчить, що вказані переваги ВІТС можуть бути пояснені не лише ліпідознижувальним впливом статинів, а й неліпідозалежними механізмами їхньої дії та плейотропними ефектами.
Показано, що статини чинять різноманітні протективні впливи на серцево-судинну систему: покращують ендотеліальну функцію; модулюють запальну відповідь і тромбогенез; стабілізують атеросклеротичні бляшки. Деякі дослідження продемонстрували, що плейотропні ефекти ВІТС є більш потужними, ніж такі НВІТС.
У дослідженні був також проаналізований рівень вчСРБ учасників із метою порівняння протизапальної дії призначених статинів. У періоді спостереження вчСРБ був достовірно нижчим, а зменшення цього показника порівняно з вихідним рівнем – достовірно більш вираженим у групі ВІТС, що є підтвердженням неліпідозалежних сприятливих ефектів цього підкласу статинів. Додатково автори провели порівняння клінічних наслідків серед усіх пацієнтів, яким призначали ВІТС (n=618) та НВІТС (n=3517), у тому числі учасників, які не досягли цільових показників ХС ЛПНЩ. На відміну від результатів пацієнтів, які досягли цільових показників ХС ЛПНЩ, у останній когорті частота первинних кінцевих точок у двох групах не відрізнялася (7,3 проти 10,0%; стандартизоване ВР 0,80; 95% ДІ 0,55-1,16; р=0,24).
Хоча точні причини встановити неможливо, до виразної різниці між двома проаналізованими групами могли призвести відносно невеликий розмір вибірки, особливо групи ВІТС, і нерандомізований дизайн дослідження.
Обмеження
Дослідження має декілька обмежень – передусім нерандомізований обсерваційний дизайн. Питання призначення ВІТС або НВІТС вирішувалося закріпленим лікарем, тому на прийняття рішення могли впливати певні чинники (демографічні фактори, клінічний стан під час госпіталізації, вихідні рівні ліпідів, особисті вподобання лікаря). Хоча авторами з метою уникнення небажаних впливів на результат дослідження були проведені псевдорандомізація та стандартизація, деякі невраховані чинники все ж могли модифікувати отримані результати. По-друге, хоча початково було відібрано 8148 учасників, 3622 пацієнти були виключені з дослідження через відсутність інформації стосовно призначення статинів і рівня ХС ЛПНЩ під час періоду спостереження. Цей своєрідний відбір також міг вплинути на отримані результати. По-третє, прихильність пацієнтів до статинотерапії оцінювалася непрямими методами й могла бути визначена неточно. Оскільки до аналізу було включено лише пацієнтів, які досягли цільових рівнів ХС ЛПНЩ, автори схильні вважати, що більшість учасників мали високий рівень прихильності до статинотерапії. Тому головною причиною зниження прихильності через 3 роки спостереження може бути заміна ВІТС на терапію статинами помірної інтенсивності у зв’язку з досягненням та утриманням цільових показників ХС ЛПНЩ. По-четверте, дані стосовно вчСРБ були наявними лише для 69,6% загальної популяції дослідження (1216 із 1746 осіб). По-п’яте, медіана тривалості спостереження за групою ВІТС була меншою, ніж у групі НВІТС: 3,1 (1,4-4,9) проти 4,5 (2,5-5,0) року. З метою виявлення впливу тривалості спостереження на результат автори провели окрему оцінку клінічних наслідків, скоротивши проаналізований період спостереження в обох групах до 3 років. При такому аналізі частота первинних точок була достовірно нижчою в групі ВІТС, аніж у групі НВІТС (2,4 проти 6,1%; стандартизоване ВР 0,41; 95% ДІ 0,20-0,86; р=0,02). Стандартизоване ВР за 3 роки виявилося аналогічним такому за 5 років. Зважаючи на це, автори зробили висновок, що відмінність у тривалості спостереження за групами значуще не впливала на клінічний результат. І наостанок, деякі ІМ та інсульти могли бути недіагностовані, оскільки це не було рандомізоване контрольоване дослідження з ретельним спостереженням. Утім, співвідношення ІМ та інсультів до кардіоваскулярних смертей або смертей від усіх причин було зіставне чи перевищувало таке згідно з результатами проведених раніше рандомізованих контрольованих досліджень. Окрім того, малоймовірно, що гіподіагностика ІМ та інсультів була виключно в групі ВІТС, а не в обох групах.
Висновки
У пацієнтів, які досягли цільового рівня ХС ЛПНЩ, рекомендованого ESC/EAS для вторинної профілактики після ЧКВ, ВІТС супроводжувалася достовірно меншою частотою великих кардіоваскулярних подій, аніж НВІТС. Ці дані свідчать, що слід розглянути призначення ВІТС навіть у пацієнтів, які можуть досягти цільових показників ХС ЛПНЩ за допомогою НВІТС.
Стаття друкується в скороченні.
Kim J., Park K. T., Jang M. J. et al. High-intensity versus non-high-intensity statins in patients achieving low-density lipoproteins cholesterol goals after percutaneous coronary intervention. J. Am. Heart. Assoc. 2018; 7: e009517.
Переклала з англ. Лариса Стрільчук
ДОВІДКА «ЗУ»
Препарати аторвастатину Аторис (10, 20, 30, 40 мг) і розувастатину Роксера (5, 10, 15, 20, 30, 40 мг) виробництва компанії KRKA (Словенія) завоювали заслужену популярність серед лікарів України. Ефективність і безпечність Аторису та Роксери доведені результатами численних клінічних досліджень. Застосування цих препаратів дає змогу не тільки досягти цільових показників ХС ЛПНЩ при зменшенні ризику кардіоваскулярних катастроф, а й реалізувати їхні плейотропні ефекти: знизити запалення, стабілізувати атеросклеротичні бляшки, покращити функцію ендотелію, зменшити тромбогенез. Багатогранна кардіопротективна дія Аторису та Роксери зумовлює доцільність їх призначення, особливо пацієнтам високого та дуже високого ризику, в тому числі для вторинної профілактики.
Медична газета «Здоров’я України 21 сторіччя» № 23 (444), грудень 2018 р.


