2 квітня, 2019
Эффективность и переносимость лейпрорелина ацетата (Элигард) в повседневной клинической практике в Германии
Обобщенные данные двух проспективных неинтервенционных исследований 3- и 6-месячной депо-формы препарата у пациентов с распространенным раком предстательной железы
В Германии рак предстательной железы (РПЖ) является наиболее распространенной онкопатологией у мужчин (26%). В 2016 г. частота новых случаев заболевания составила 66 900 [1]. В рейтинге причин смертности от злокачественных новообразований среди мужского населения РПЖ занимает третье место (10%) [1].
Поскольку РПЖ является гормонозависимым заболеванием [2-4], андрогенная депривационная терапия (АДТ), направленная на снижение уровня сывороточного тестостерона, является стандартной опцией в лечении распространенного гормончувствительного рака и также применяется при развитии кастрационной резистентности [5, 6]. Медикаментозная кастрация также используется у пациентов с более ранними стадиями РПЖ и у больных с биохимическим рецидивом (повышение уровня простатспецифического антигена [ПСА]) после радикальной простатэктомии или лучевой терапии. АДТ может назначаться как монотерапия, а также в составе мультимодального лечения [5, 6].
В качестве препаратов, вызывающих андрогенную депривацию, используют депо-формы агонистов лютеинизирующего гормона рилизинг-гормона (ЛГРГ), такие как лейпрорелина ацетат, бусерелина ацетат, гозерелина ацетат или трипторелина ацетат [5, 6].
Синтетические аналоги ЛГРГ оказывают стимулирующее действие на ЛГРГ-рецепторы гипофиза, что индуцирует секрецию лютеинизирующего (ЛГ) и фолликулостимулирующего гормона (ФСГ). В свою очередь, ЛГ и ФСГ стимулируют выработку тестостерона в яичках, что может приводить к временному повышению уровня тестостерона (феномен вспышки). Однако длительное воздействие агонистов ЛГРГ обусловливает реализацию механизма отрицательной обратной связи, снижение стимуляции экспрессии рецепторов ЛГРГ с последующим уменьшением выработки ЛГ, ФСГ и, как следствие, тестостерона. В течение 2-4 недель после начала лечения у большинства пациентов концентрация тестостерона в крови снижается до уровня кастрационных значений (традиционно определяется как <50 нг/дл, хотя в последнее время этот показатель пересмотрен и составляет <20 нг/дл), что соответствует уровню этого гормона после двусторонней орхиэктомии [5, 6].
Изначально разработанные формы препаратов агонистов ЛГРГ были предназначены для ежедневного подкожного введения. В последующем появились 1-, 2-, 3-, 4-, 6- и 12-месячные депо-формы для подкожного введения. Препарат Элигард («Астеллас») представляет собой депо-форму, содержащую активный компонент лейпрорелина ацетат в комбинации с биоразлагаемым полимерным матриксом (система доставки Атригель). Депо-формы препарата, показанные для введения 1 раз в месяц (7,5 мг), каждые 3 мес (22,5 мг) и 6 мес (45 мг) были одобрены для применения в Германии в 2003, 2004 и 2006 году соответственно. По результатам клинических испытаний, применение всех трех форм препарата сопровождалось значимым снижением уровня тестостерона и ПСА, а также характеризовалось хорошей переносимостью [7-9]. Однако клинические испытания часто ограничены определенной категорией пациентов в связи со строгими критериями включения и исключения, поэтому существует потребность в «реальных» данных, полученных в условиях обычной клинической практики. С этой целью были обобщены данные двух неинтервенционных исследований, оценивающих эффективность и переносимость 3- и 6-месячных депо-форм лейпрорелина ацетата среди обширной гетерогенной популяции пациентов в Германии.
Всего в это исследование было включено 1906 больных, что делает его самым крупным из всех, в которых сообщалось об эффективности и безопасности лейпрорелина ацетата.
Методы
Дизайн исследования и пациенты
В данной статье представлены результаты двух проспективных открытых неинтервенционных исследований, проведенных в Германии с января 2007 года по декабрь 2009 года. Пациенты получали лейпрорелина ацетат либо один раз в 3 мес (n=633), либо один раз в 6 мес (n=1273) на протяжении одного года. В исследование были включены мужчины (в возрасте старше 18 лет) с распространенным гормончувствительным РПЖ, которым было показано проведение АДТ. При этом не было строгих критериев исключения, а также каких-либо ограничений касательно момента установления диагноза, степени злокачественности или стадии опухоли. Пациенты получали или 3-месячные (22,5 мг), или 6-месячные (45 мг) депо-формы лейпрорелина ацетата (Элигард) и находились под наблюдением в течение 12 месяцев. Доза препарата и кратность введения (1 раз каждые 3 мес [22,5 мг] или 1 раз каждые 6 мес [45 мг]) были единственным существенным различием между двумя исследованиями. Установление диагноза и назначение лечения, а именно выбор АДТ, формы препарата, дополнительных лекарственных средств, проводилось по усмотрению лечащего врача. Проведение данных исследований было одобрено Этическим комитетом Баден-Вюртемберга (Германия). Перед началом проведения исследования все участники подписали письменное информированное согласие.
Конечные точки исследования
Первичной конечной точкой для оценки эффективности лечения был уровень ПСА в сыворотке крови по прошествии 12 месяцев. Общий уровень ПСА определяли перед началом терапии, каждые 3 мес (22,5 мг) или 6 мес (45 мг) на протяжении года. Нежелательные явления фиксировали при каждом визите в клинику и оценивали в соответствии с классификацией MedDRA (версия 14.1). Лечащий врач также оценивал простоту (удобство) использования и выраженность реакций в месте введения препарата.
Результаты
Характеристика пациентов
Для проведения исследования были собраны данные о 1906 пациентах. Из них 633 получали 3-месячную депо-форму лейпрорелина ацетата и 1273 – 6-месячную. Исходные характеристики участников исследования представлены в табл. 1.
Средний возраст больных составил 75 лет, среднее время, прошедшее с момента постановки диагноза, – 11,2 месяца. При этом 46,1% (n=879) участников исследования диагноз РПЖ установлен ≤12 мес назад, а у 19,6% (n=374) больных с момента установления диагноза прошло более 4 лет. На момент включения в исследование костные метастазы диагностированы у 8% пациентов, отдаленные – у 1,3%, и у 2% участников отмечено метастазирование в лимфоузлы (неполная информация о стадии и локализации опухоли в различные временные точки объясняет разницу в количестве пациентов, получавших лечение по поводу отдаленных метастазов и метастазов в регионарные лимфатические узлы). Согласно медицинской документации, у 58,5% исследуемых отмечены сопутствующие заболевания, преимущественно патология сердечно-сосудистой системы (71,5% больных). В общей сложности 49,7% всех пациентов получали сопутствующее лечение.
Согласно анализу структуры предшествующего лечения, 43,2% (n=824) пациентов ранее получали гормональную терапию по поводу данного заболевания (см. табл. 1). Не было выявлено клинически значимых различий в структуре коморбидной патологии, стадии или степени злокачественности опухоли между ранее не леченными пациентами, больными, получавшими до момента включения в исследование лейпрорелина ацетат, и теми, кто получал другие препараты агонистов ЛГРГ.
Показания к назначению депо-форм лейпрорелина ацетата
Основным показанием к назначению терапии лейпрорелина ацетатом было наличие у пациента местно распространенного РПЖ (42,1%). Другими причинами были следующие: отсутствие показаний к проведению радикальной простатэктомии, лучевой терапии или отказ пациента от других методов лечения (28,2%); увеличение уровня ПСА после проведения радикальной простатэктомии (13,5%) или лучевой терапии (8,1%); наличие отдаленных метастазов (12,9%) или метастазирование в лимфоузлы (5,6%) (неполнота записей о стадии и локализации опухоли в различные временные точки объясняет разницу в количестве пациентов, получавших лечение по поводу отдаленных метастазов и метастазов в регионарные лимфатические узлы).
У 58,4% пациентов лейпрорелина ацетат назначали в качестве монотерапии, при этом 34,3% больных получали данный препарат в сочетании с антиандрогенами (бикалутамид – 14,7%, флутамид – 12,2%; ципротерона ацетат – 4,7%), золедроновой кислотой (8%) или химиотерапевтическими средствами (эстрамустин – 0,7%, доцетаксел – 0,4%). У 7,3% пациентов данные о наличии сочетанной терапии отсутствовали.
В целом 6,8% (n=129) пациентов не закончили 12-месячный курс лечения. Из них 28 больных умерли, 22 выбыли из-под наблюдения, у 15 был отмечен несущественный терапевтический эффект и 4 прекратили лечение по причине нежелательных явлений.
Эффективность
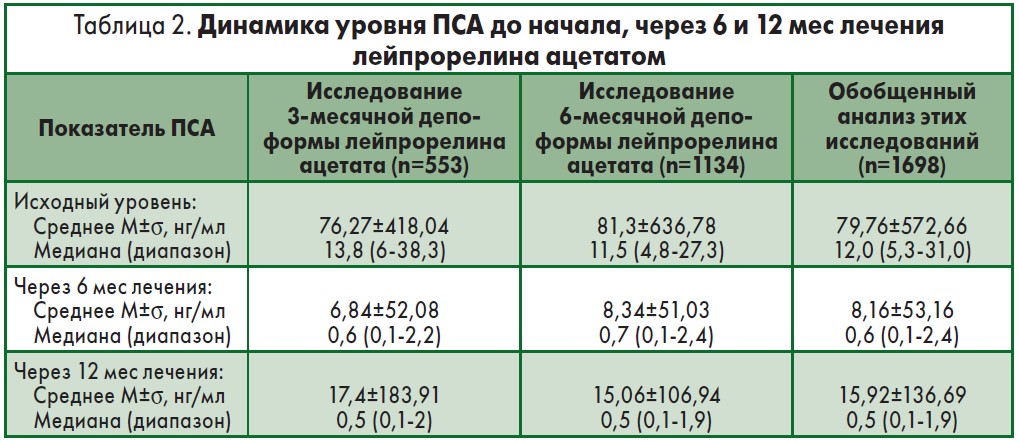
Полная информация касательно уровня ПСА была доступна для 1698 пациентов. В табл. 2 представлены средние значения и медиана концентрации ПСА до начала терапии и на протяжении 12 мес при приеме 3- и 6-месячных депо-форм лейпрорелина ацетата. Несоответствие между показателями среднего значения и медианы свидетельствует о значительной вариабельности данных. При этом более точным является значение медианы, на основании которого и был проведен последующий анализ.
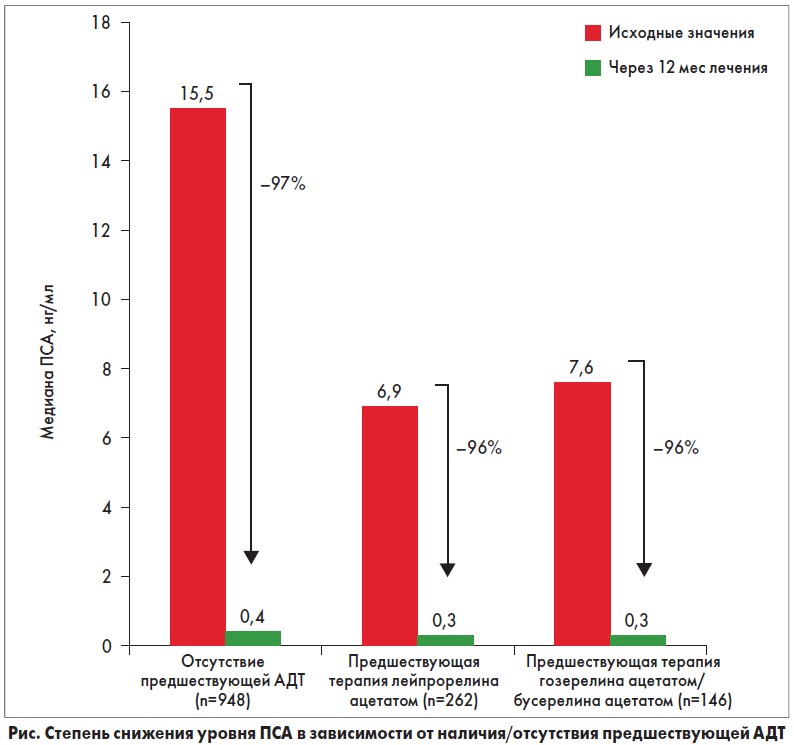
Через 12 мес лечения лейпрорелина ацетатом медиана уровня ПСА снизилась на 96%: с 12,0 до 0,5 нг/мл (см. табл. 2). Результаты были сопоставимы у пациентов, получавших 3- и 6-месячные депо-формы препарата. Показательным является тот факт, что терапия лейпрорелина ацетатом сопровождалась снижением концентрации ПСА на 96% в сравнении с исходным значением как у ранее не получавших АДТ пациентов, так и у тех, кому агонисты ЛГРГ ранее назначались (рис.).
В общей сложности у 8,8% (n=167) пациентов наблюдались нежелательные явления. Незначительные побочные реакции отметили 5,7% (n=109) участников исследования, среди которых наиболее часто встречались болезненность в месте инъекции (2,3%) и приливы (1,6%). В 1,3% случаев побочные эффекты были оценены клиницистами как определенно, вероятно или возможно связанные с приемом препарата. Серьезные нежелательные явления имели место у 3,0% (n=58) пациентов, включая 14 случаев смерти: вследствие полиорганной недостаточности (n=1); РПЖ, почечно-печеночной недостаточности и азотемии (n=1); РПЖ (n=5); анемии на фоне опухолевого процесса (n=1); из-за прогрессирования новообразования и легочной эмболии (n=1); карциномы поджелудочной железы (n=1); развития сердечной недостаточности (n=1); цереброваскулярной катастрофы (n=2); неустановленной причины (n=1). Неблагоприятные явления со стороны кардиоваскулярной системы включали цереброваскулярные события (n=6), сердечную недостаточность (n=5), коллапс (n=4), а также по одному случаю развития инсульта, ИБС, инфаркта миокарда и легочной эмболии. Другие серьезные неблагоприятные явления, выявленные более чем у одного участника, включали необходимость проведения радикальной простатэктомии или другого хирургического вмешательства, метастазирование РПЖ, приливы, опухолевую прогрессию. Лишь у одного пациента было зарегистрировано серьезное побочное явление с возможной причинной взаимосвязью с проводимой терапией (повышение уровня ПСА и метастазы в кости). Из общего количества участников исследования только 4 пациента преждевременно прекратили лечение из-за побочных явлений (сильные приливы, общая слабость, усталость, потливость и отечность в месте инъекции).
Мнение исследователей
Урологи отметили, что длительный интервал между инъекциями был основной причиной выбора назначения депо-формы лейпрорелина ацетата (77,8% случаев). Для пациентов преимуществами данной формы препарата были небольшой объем вводимой жидкости и короткая игла предварительно заполненного шприца (28,8 и 25,6% соответственно). Согласно обобщенному анализу, 67,8% врачей отметили наличие предварительно заполненного шприца депо-формы лейпрорелина ацетата очень удобным/удобным. По мнению 91% урологов, локальная переносимость препарата была оценена как хорошая или отличная.
Обсуждение
В данном исследовании представлены результаты самого крупномасштабного на сегодняшний день анализа эффективности и безопасности применения депо-форм лейпрорелина ацетата (препарат Элигард) у пациентов с распространенным РПЖ в реальной клинической практике. В анализ вошли обобщенные данные двух неинтервенционных исследований с общим количеством участников 1906 пациентов, получавших лечение по поводу РПЖ в условиях обычной клинической практики. С момента появления депо-форм лейпрорелина ацетата были опубликованы результаты трех неинтервенционных исследований по оценке эффективности, переносимости и/или влияния на качество жизни агонистов ЛГРГ в условиях повседневной клинической практики: французское исследование ELIRE (3- и 6-месячные депо-формы препарата) [11], бельгийское MANTA (1- и 3-месячные депо-формы) [12] и немецкое наблюдательное исследование (6-месячная депо-форма) [10].
Результаты данного обобщенного анализа двух исследований (3- и 6- месячные депо-формы лейпрорелина ацетата) продемонстрировали значительное снижение (96%) медианных уровней ПСА через 12 мес после начала лечения. Клинические испытания, в которых были показаны эффективность и переносимость исследуемых форм препарата, отличались гомогенностью участвующих в них пациентов, поскольку были ограничены строгими критериями включения и исключения. Однако исследования, оценивающие эффективность и переносимость препарата в условиях обычной клинической практики, такие как это, включают гораздо более широкий контингент пациентов.
По сравнению с участниками пилотных клинических испытаний лейпрорелина ацетата популяция пациентов в данном неинтервенционном исследовании была более гетерогенной, с различными стадиями опухолевого процесса, степенью злокачественности, показаниями к андрогенной депривации и сопутствующими заболеваниями на момент начала исследования. Многие из этих пациентов были бы исключены из интервенционных клинических испытаний. Это подтверждается, например, величиной диапазона исходного уровня ПСА в данном исследовании (0,02-17,300 нг/мл) по сравнению с таковым в пилотных испытаниях (3-месячная депо-форма препарата – 0,2-5,270 нг/мл; 6-месячная – 0,19-2,284 нг/мл) [7, 8]. Более того, в отличие от клинических испытаний, значительная часть пациентов получали лейпрорелина ацетат в сочетании с антиандрогенами, бисфосфонатами или химиотерапевтическими препаратами. Кроме того, не было никаких ограничений в отношении временного интервала между предшествующей гормональной терапией и началом применения депо-форм лейпрорелина ацетата, в то время как в клинических испытаниях был необходим как минимум 3-месячный промежуток [7, 8]. Таким образом, пациенты, получавшие ранее/принимающие препараты АДТ на момент начала исследования, также были включены в исследование. Более низкие исходные уровни ПСА у пациентов, ранее получавших препараты с целью медикаментозной кастрации, в сравнении с теми, кто не принимал таковые (см. рис.), свидетельствуют о том, что интервал между предшествующей АДТ и инициацией лечения депо-формой лейпрорелина ацетата был относительно коротким.
Как отмечалось выше, существуют расхождения между средними и медианными значениями показателя ПСА в данном исследовании, что указывает на его большую вариабельность. Поэтому более показательными являются значения медианы, а не среднего уровня ПСА.
Поскольку в опубликованных результатах исследований 3- и 6-месячных депо-форм лейпрорелина ацетата [7, 8] представлены только средние значения концентрации ПСА (без медианных), то это не позволяет напрямую сравнить их с выводами данного исследования. Однако в нем было продемонстрировано выраженное снижение уровня ПСА на фоне лечения лейпрорелина ацетатом у подавляющего большинства гетерогенной популяции пациентов с РПЖ в условиях рутинной клинической практики, независимо от предшествующего лечения агонистом ЛГРГ.
Неблагоприятные явления в данном исследовании отмечались реже, чем в клинических испытаниях [7, 8], в основном за счет меньшего количества жалоб на приливы или реакции в месте инъекций. Возможные причины, объясняющие эти несоответствия, могут быть следующими:
- сочетание АДТ с приемом антиандрогенов (примерно у трети пациентов), которые могут уменьшать частоту приливов [5, 6];
- использование другого препарата для гормональной терапии в одной из подгрупп пациентов на момент начала лечения депо-формой лейпрорелина ацетата;
- меньшее количество нежелательных явлений, о которых сообщали лечащие врачи (в повседневной клинической практике они могут рассматривать такие жалобы как «нормальные» реакции после инъекции агонистов ЛГРГ). Последнее согласуется с результатами данного исследования, в котором урологи оценили локальную переносимость депо-форм лейпрорелина ацетата как хорошую или отличную у более чем 90% пациентов.
Данные двух неинтервенционных исследований, используемых для обобщенного анализа, отличаются от таковых, полученных в более строгих рандомизированных контролируемых испытаниях. Однако практический опыт применения депо-форм лейпрорелина ацетата (по результатам обобщенного анализа) может лучше отражать реальную ситуацию касательно применения депо-форм исследуемого препарата в повседневной клинической практике.
Выводы
Результаты представленного исследования свидетельствуют о высокой эффективности и хорошей переносимости 3- и 6-месячных депо-форм лейпрорелина ацетата в широкой популяции пациентов (как получавших, так и не получавших ранее агонисты ЛГРГ) в условиях повседневной клинической практики.
Список литературы находится в редакции.
Реферативный перевод с англ. Марии Арефьевой
Carsten-Henning Ohlmann, Marco Gross-Langenhoff. Efficacy and Tolerability of Leuprorelin Acetate (Eligard®) in Daily Practice in Germany: Pooled Data from 2 Prospective,
Non-Interventional Studies with 3- or 6-Month Depot Formulations in Patients with Advanced Prostate Cancer. Urol Int; DOI: 10.1159/000479187.
Тематичний номер «Урологія. Нефрологія. Андрологія» №3 (14), листопад-грудень 2018 р.