2 квітня, 2019
Роль противовоспалительных и обезболивающих препаратов в хирургическом лечении полости рта
В рамках I Украинского стоматологического конгресса с международным участием «Интегрированная медицина и стоматология», который состоялся 8-9 февраля в Киеве, особое внимание было уделено проблемам ведения пациентов с болевым синдромом и воспалением.
 С докладом «Менеджмент боли и воспаления на этапах подготовки и проведения дентальной имплантации» выступил член координационного совета Ассоциации стоматологов Украины, вице-президент Ассоциации стоматологов-ортопедов и зубных техников Украины, профессор кафедры ортопедической стоматологии Института стоматологии Национальной медицинской академии последипломного образования им. П. Л. Шупика (г. Киев), доктор медицинских наук Павел Викторович Леоненко.
С докладом «Менеджмент боли и воспаления на этапах подготовки и проведения дентальной имплантации» выступил член координационного совета Ассоциации стоматологов Украины, вице-президент Ассоциации стоматологов-ортопедов и зубных техников Украины, профессор кафедры ортопедической стоматологии Института стоматологии Национальной медицинской академии последипломного образования им. П. Л. Шупика (г. Киев), доктор медицинских наук Павел Викторович Леоненко.
– Такие клинические признаки, как болевой синдром и развитие воспалительного процесса, являются характерными для многих стоматологических пациентов. Однако значение патогенетических механизмов боли и воспаления нередко недооценивается при проведении различных хирургических вмешательств в полости рта. При осуществлении операции по удалению одного или нескольких зубов и планировании последующей имплантации врач сталкивается с рядом проблем, которые могут быть косвенно или напрямую связаны с болевым синдромом и воспалительным процессом.
К одной из таких проблем относят резорбцию костной ткани альвеолярного отростка. В случае потери пациентом одного или нескольких зубов неминуемо происходит запуск катаболических процессов, которые приводят к уменьшению объема кости в области оперативного вмешательства. Чем травматичнее операция по удалению зуба, тем больше выражены процессы резорбции. Как следствие, значительная травматизация костной лунки при удалении зуба сопровождается выраженным воспалением и резорбцией костной ткани, а недооценка объема кости альвеолярного отростка перед проведением имплантации может приводить к отторжению имплантата. В худшем случае отторжение развивается уже после того, как опорные имплантаты получили нагрузку в виде ортопедической конструкции, что перечеркивает все усилия врачей, а также немалые финансовые затраты пациента.
Взаимосвязь воспалительного процесса и резорбции костной ткани
В исследовании H. K. Jung и соавт. (2009) было показано, что воспаление тканей пародонта всегда сопровождается резорбцией костной ткани. Повреждение тканей при удалении зуба приводит к развитию местных воспалительных реакций, в процессе которых происходит активация лейкоцитов, фибробластов, эндотелиоцитов и других клеток. Наблюдается также высвобождение медиаторов воспаления: интерлейкина (ИЛ) 1, ИЛ‑6, фактора некроза опухоли (ФНО), интерферона-γ. Помимо местных, развиваются реакции со стороны нервной, эндокринной, кроветворной и иммунной систем. Этот каскад событий приводит к активации процесса резорбции костной ткани. Таким образом, в контексте хирургических вмешательств в полости рта между понятиями «воспаление» и «резорбция» можно поставить знак равенства.
Методы превенции воспаления и потери костной ткани в области предполагаемой имплантации
К методам превенции воспаления относят снижение травматичности и длительности хирургического вмешательства в полости рта, консервацию лунки зуба после удаления и назначение нестероидных противовоспалительных препаратов (НПВП).
Отдельное внимание следует уделить противовоспалительной терапии, а именно выбору оптимального НПВП. Противовоспалительные препараты очень часто используют в стоматологической практике, поскольку они могут воздействовать непосредственно на воспалительный процесс, обеспечивая таким образом ингибирование механизмов запуска резорбции костной ткани. Первые НПВП были разработаны в середине прошлого века. Однако по мере появления новых данных о механизмах воспаления и резорбции костной ткани представления медицинского сообщества об эффективности и безопасности разных представителей этой фармакологической группы претерпели значительные изменения.
Различия в эффектах НПВП обусловлены главным образом воздействием на изоферменты циклооксигеназы (ЦОГ) 1 и 2 типа. Ранее существовала гипотеза, согласно которой ЦОГ‑1 является полезным агентом, что и привело к появлению селективных ингибиторов ЦОГ‑2. Однако в более поздних исследованиях было показано, что влияние ЦОГ‑1 сопровождается рядом негативных явлений: этот изофермент играет ключевую роль в патогенезе ревматоидного артрита и остеоартроза, является фактором продукции простагландинов при бурсите, принимает участие в любом воспалительном процессе в равной степени (продемонстрировано в эксперименте на животных). Выяснилось также, что ЦОГ‑2 обладает рядом ценных свойств, в частности участвует в регуляции овуляции, тонуса сосудов, функции поджелудочной железы, ремоделировании и регенерации костной ткани, заживлении дефектов слизистой оболочки кишечника. Стоит обратить внимание, что селективные ингибиторы ЦОГ‑2 повышают риск инсультов и инфарктов, эти препараты противопоказаны при наличии ишемической болезни сердца, цереброваскулярных и других сосудистых нарушений.
Важно подчеркнуть, что как ЦОГ‑1, так и ЦОГ‑2 оказывают позитивное и негативное влияние на метаболические процессы в организме. Функции всех типов ЦОГ взаимосвязаны. Ожидаемые пользу и вред от ингибирования ЦОГ‑1 и ЦОГ‑2 следует рассматривать комплексно с учетом конкретной клинической ситуации. Именно такой подход необходимо использовать при оценке соотношения польза/риск различных НПВП.
В качестве исключительно патологического агента рассматривается только 5-липооксигеназа (5-ЛОГ). Этот фермент содействует продукции лейкотриенов, ответственных за воспалительные и аллергические реакции, а также способствующих язвообразованию. Свободные радикалы также являются важными патогенетическими факторами при воспалительных процессах, поэтому их элиминация с помощью медикаментозной терапии может значительно усилить противовоспалительный эффект.
Какой НПВП является оптимальным для ингибирования индуцированной воспалением резорбции костной ткани?
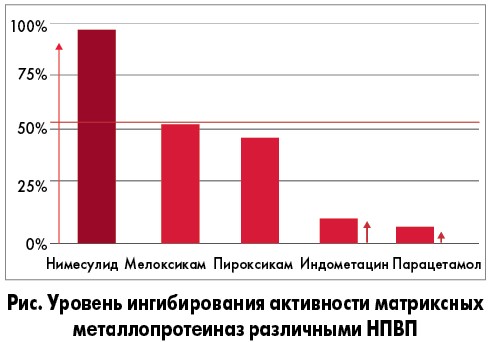 Единственным НПВП, который наряду с подавлением активности ЦОГ‑1 и ЦОГ‑2 проявляет также ингибирующее действие в отношении 5-ЛОГ, является нимесулид. Этот препарат был впервые синтезирован в качестве ловушки для супероксидных радикалов кислорода. В связи с этим нимесулид способен связывать свободные радикалы, противодействуя этому важному провоспалительному фактору. В исследовании A. Barracchini и соавт. (1998) было показано, что нимесулид оказывает более выраженное ингибирующее действие на матриксные металлопротеиназы по сравнению с мелоксикамом, пироксикамом, индометацином и парацетамолом (рис.).
Единственным НПВП, который наряду с подавлением активности ЦОГ‑1 и ЦОГ‑2 проявляет также ингибирующее действие в отношении 5-ЛОГ, является нимесулид. Этот препарат был впервые синтезирован в качестве ловушки для супероксидных радикалов кислорода. В связи с этим нимесулид способен связывать свободные радикалы, противодействуя этому важному провоспалительному фактору. В исследовании A. Barracchini и соавт. (1998) было показано, что нимесулид оказывает более выраженное ингибирующее действие на матриксные металлопротеиназы по сравнению с мелоксикамом, пироксикамом, индометацином и парацетамолом (рис.).
Нимесулид подавляет активность всех факторов резорбции костной ткани: ИЛ‑1 и ИЛ‑17, простагландина E2, ФНО, RANKL‑активированных остеокластов. Помимо системного противовоспалительного эффекта, назначение нимесулида в пред- и послеоперационный периоды обусловливает локальный эффект, а именно минимизацию резорбции костной ткани, риск которой максимально высок в участках альвеолярного отростка, где имели место хирургические вмешательства или травмы надкостницы. Указанные свойства делают нимесулид оптимальным противовоспалительным препаратом для противодействия потере костной ткани при хирургических вмешательствах в полости рта. На фармацевтическом рынке Украины нимесулид представлен широко известным и отлично зарекомендовавшим себя в клинической практике препаратом Нимесил.
При пероральном приеме Нимесила максимальная концентрация действующего вещества в крови достигается через 2 ч. При малоинвазивных методиках имплантации рекомендовано использование препарата Нимесил в дозе 100 мг за 1,5 ч до проведения хирургического лечения. В случае длительных хирургических вмешательств, особенно при проведении костной пластики с обширным отбрасыванием лоскута и его дальнейшей мобилизацией путем расщепления, первый прием Нимесила в дозе 100 мг следует осуществить накануне утром, а второй – за 1,5 ч до операции. После хирургического вмешательства Нимесил назначают в дозе 100 мг 2 р/сут в течение 5-10 дней.
Эффективное обезболивание как залог успешного восстановительного периода после оперативного вмешательства
Еще одной распространенной проблемой, связанной с хирургическими вмешательствами в полости рта, является болевой синдром. Несмотря на повсеместное внедрение методик интраоперационного обезболивания, фактор послеоперационной боли может недооцениваться при ведении больного, перенесшего хирургическое лечение в полости рта. Врачу необходимо помнить, что болевой синдром не сводится только к ощущениям пациента, он может оказывать существенное негативное влияние на послеоперационный восстановительный период.
Отсутствие адекватного обезболивания в послеоперационном периоде может приводить к страданию больного, нарушению сна, ограничениям в повседневной жизни, нарушению подвижности, страху и тревоге, частичной или полной потере производительности, значительному удлинению периода реабилитации, снижению качества жизни. У пациентов, не получающих адекватную послеоперационную аналгезию, может происходить задержка заживления раны, обусловленная повышением тонуса симпатической нервной системы. В связи с нарушением биомеханики дыхания на фоне болевого синдрома повышается риск развития легочных заболеваний, включая ателектазы и пневмонию. Увеличивается также риск тромбообразования, возникает устойчивая гиперадренергическая стрессовая реакция с развитием артериальной гипертензии (Behamou D. et al., 2008). Таким образом, эффективное послеоперационное обезболивание может оказывать значительное влияние на отдаленный результат хирургического лечения.
Какой аналгетик выбрать для быстрого и эффективного купирования болевого синдрома?
В настоящее время в странах Европы до 95% пациентов в послеоперационном периоде получают декскетапрофен как в монотерапии, так и в рамках мультимодальной аналгезии. На фармацевтическом рынке Украины декскетапрофен представлен препаратом Дексалгин.
Первый прием Дексалгина (1 таблетка, 25 мг) рекомендуется произвести за 30 мин до предполагаемого оперативного вмешательства, последующие – через каждые 8 ч при появлении болевых ощущений. В зависимости от выраженности последних допустимо уменьшение разовой дозы декскетапрофена до 12,5 мг (1/2 таблетки) каждые 4-6 ч. Суточная доза препарата не должна превышать 75 мг. Побочные реакции при использовании Дексалгина сводятся к минимуму за счет приема минимальных эффективных доз в течение как можно более короткого промежутка времени.
Подготовил Игорь Кравченко
Медична газета «Здоров’я України 21 сторіччя» № 5 (450), березень 2019 р.


