2 квітня, 2019
Периндоприл у лікуванні артеріальної гіпертензії та вторинній профілактиці серцево-судинних захворювань
Завдяки блокаді ключового ферменту ренін-ангіотензинової системи (РАС) інгібітори ангіотензинперетворювального ферменту (ІАПФ) є препаратами вибору в лікуванні не лише артеріальної гіпертензії (АГ), а й пов’язаних із нею ушкоджень органів-мішеней та серцево-судинних (СС) ускладнень (ESC, 2018).
Переваги периндоприлу над іншими ІАПФ
Насамперед це тривала дія та висока біодоступність (70%), що забезпечують надійний контроль артеріального тиску (АТ) упродовж 24 год після орального застосування. Для досягнення максимального ефекту не потрібне титрування дози. Відповідно до сучасних стандартів для тривалої терапії рекомендовані лише препарати із значенням «корито-пік» (показник, що відображає відсоток ефективності препарату через 24 год після одноразового прийому щодо максимальної ефективності на піку його концентрації в крові) >50%. Із цих позицій периндоприл має переваги над багатьма ІАПФ.
Терапія периндоприлом практично не зумовлює гіпотензії, а отже, і гіпоперфузії органів-мішеней, що дуже важливо при серцевій недостатності (СН), гострому інфаркті міокарда (ІМ), шоку, хронічній хворобі нирок (ХХН) та станах з високим ризиком ортостатичної гіпотензії чи синкопе (MacFadyen R. et al., 1991). Потужне пригнічення АПФ у плазмі та тканинах забезпечує високу специфічність до органів-мішеней (Zhuo J. et al., 2002; Ferrari R., 2004).
Незважаючи на високу селективність до зв’язувальних центрів брадикініну в АПФ, за даними досліджень PROGRESS та EUROPA, відсоток відміни через сухий кашель не перевищує 2. З іншого боку, брадикінін стимулює ендотеліальну NO-синтазу (еNOс) та пригнічує апоптоз клітин серця та ендотелію, тому периндоприл значно підвищує експресію й активність еNOс у порівнянні з трандолаприлом, квинаприлом, раміприлом, еналаприлом та має виражену антиапоптичну дію (Krysiak R. et al., 2010; Ceconi C. et al., 2007). Поліпшення функції великих і малих артерій зумовлене ще й зниженням їх жорсткості та ремоделювання (Nedogoda S. et al., 2013; Mancini M. et al., 2016).
Іншими плейотропними ефектами периндоприлу є зменшення прогресування некальцифікованих коронарних бляшок (Bruining N. et al., 2009); більш виражене зниження рівня резистину порівняно з еналаприлом як при ІХС, так і при гострому ішемічному інсульті (Krysiak R. et al., 2010; Perovic E. et al., 2017); поліпшення коронарного кровотоку (Pilote L. et al., 2004); потужний вплив на такі патогенетичні фактори ремоделювання, як трансформуючий фактор росту і колаген 3 типу; більш виражена протизапальна, антиоксидантна, антитромботична та профібринолітична дія в порівнянні з еналаприлом (Krysiak R. et al., 2008; Koz C. et al., 2009). Нефропротекторний вплив периндоприлу полягає в зменшенні мікроальбумінурії та сповільненні прогресування ушкодження клубочків (Davis B. et al., 2004).
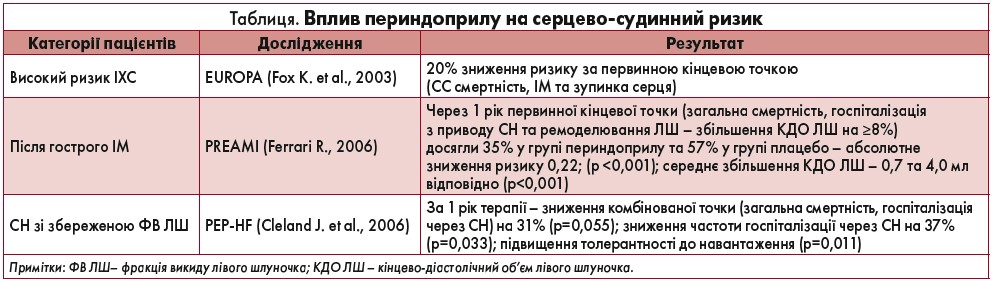
Отже, завдяки сильній зв’язувальній здатності з тканинним АПФ та вищій селективності до сайтів брадикініну плейотропні ефекти периндоприлу (NO‑стимулюючий, антиоксидантний, антиапоптичний, протизапальний, антитромботичний, профібринолітичний та антиатеросклеротичний) більш виражені, ніж у інших ІАПФ. Препарат має також добре виражені кардіо-, вазо- та ренопротекторні властивості. Крім того, у периндоприлу велика доказовість щодо здатності знижувати ризик СС ускладнень (табл.).
Є також декілька прямих порівнянь периндоприлу з іншими ІАПФ. Ретроспективне дослідження (15 622 хворих на АГ) продемонструвало значно нижчі рівні загальної та СС смертності внаслідок 5-річної терапії периндоприлом у порівнянні з лізиноприлом – 20 проти 22,2% та 5,6 проти 6,5% відповідно (обидва p<0,005; Tsoi K. et al., 2014). Згідно з результатами метааналізу 26 досліджень периндоприл знижує частоту ІМ на 28%, тоді як раміприл лише на 19% (Savarese G. et al., 2013). Метааналіз 20 досліджень, що загалом охоплював 158 998 пацієнтів і вивчав вплив різних блокаторів РАС, виявив, що периндоприл – це єдиний препарат з чіткими перевагами щодо виживання (van Vark L. et al., 2012).
Монотерапія при АГ показана кволим пацієнтам, особам віком >80 років та при АГ 1 ступеня з низьким ризиком (ESC, 2018). З цього погляду периндоприл – ідеальний препарат, особливо для осіб похилого віку, які найбільш схильні до гіпотензії, а одноразове застосування підвищує прихильність до терапії. Крім того, у цій когорті часто спостерігаються цереброваскулярні порушення чи гіпертензивна енцефалопатія, а периндоприл добре проникає в тканини, має антиатеросклеротичну та вазопротекторну дію.
Вторинна профілактика
СС ускладнення при стабільних формах ІХС, у тому числі при цукровому діабеті 2 типу
Дослідження EUROPA, учасниками якого були 12 218 хворих на стабільні форми ІХС з помірним СС ризиком, продемонструвало, що додавання 8 мг/добу периндоприлу до звичайної схеми лікування знижує СС смертність, ризик нефатального ІМ та зупинки серця (8 проти 10% у групі плацебо; р=0,003), що відповідає зниженню відносного ризику на 20% (р=0,0003). Ефект почав проявлятися вже через 1 рік, а за 3 роки досяг статистичної значущості. Виявлено вплив на всі вторинні кінцеві точки: сумарна частота виникнення ІМ, нестабільної стенокардії, зупинки серця, смерті від усіх причин зменшилася на 14% (р=0,0009); частота фатального і нефатального ІМ – на 24% (р <0,001), виникнення СН – на 39% (р=0,002), незалежно від віку, наявності чи відсутності АГ, проведення хірургічної реваскуляризації чи застосування статинів (Fox K. et al., 2003).
Аналогічне зниження ризику щодо комбінованої первинної кінцевої точки (19%) виявлено у хворих на цукровий діабет (ЦД) 2 типу в субдослідженні PERSUADE. Ризик фатального і нефатального ІМ був нижчим на 23%, кількість госпіталізацій унаслідок СН – на 46% (Daly C. A. et al., 2005). Оскільки зниження ризику було практично однаковим у пацієнтів з та без АГ, а середні показники АТ зменшилися лише на 5/2 мм рт. ст., це зумовлено плейотропною дією, а не антигіпертензивним ефектом, що підтверджено результатами субдослідження PERTINENT.
Регрес атеросклеротичних коронарних уражень при стабільних формах ІХС
У дослідженні PERSPECTIVE вивчали вплив периндоприлу 8 мг/добу на ремоделювання коронарних артерій у 118 пацієнтів методом внутрішньосудинного ультразвукового сканування. Регрес виявлено в 34,4% сегментів коронарних артерій у групі периндоприлу в порівнянні з 24,5% сегментів у групі плацебо (p=0,004), а позитивне ремоделювання – у 28,3 і 31,3% сегментів відповідно (p=0,001; Rodriguez-Granillo G.A., 2007).
Унаслідок однорічної терапії такою ж дозою знизилися рівень ангіотензину ІІ (-27%), апоптоз (-37%) і хронічне системне запалення (-13%) та підвищилися рівень брадикініну (+17%), експресія й активність еNOс (+19 і +27% відповідно), що не спостерігалося в групі плацебо (Ceconi C. et al., 2009). У хворих на ІХС із нормальним АТ після лікування периндоприлом суттєво знизилися концентрації окислених ліпопротеїнів низької щільності (ЛПНЩ), С‑реактивного протеїну, фібриногену, моноцитарного хемотаксичного білка-1 та інгібітора активатора плазміногену-1 (Krysiak R., Okopien B., 2008).
Виникнення СН і зменшення ризику СС ускладнень після перенесеного ІМ
Тривале лікування суттєво сповільнює ремоделювання серця, що продемонстровано результатами дослідження PREAMI, яке включало 1252 пацієнти віком ≥65 років без СН (середня ФВ ЛШ 59%). З 11-го дня до стандартної терапії половині пацієнтів додавали периндоприл, решті – плацебо. Первинна кінцева точка включала загальну смертність, госпіталізацію з приводу СН та ремоделювання серця за збільшенням КДО ЛШ на ≥8% від початкового значення. Вторинними кінцевими точками були СС смертність, госпіталізація через повторний ІМ або стенокардію та реваскуляризація. Через рік первинної кінцевої точки досягли 35% у групі периндоприлу та 57% у групі плацебо (абсолютне зниження ризику 0,22; p <0,001); середнє збільшення КДО ЛШ – 0,7 та 4,0 мл відповідно (p <0,001). Лікування периндоприлом не впливало на смертність і вторинні кінцеві точки, але зменшувало частоту госпіталізації з приводу СН (Ferrari R., 2006). Призначення периндоприлу після гострого коронарного синдрому зменшує апоптоз та поліпшує оновлення ендотелію (Cangiano E. et al., 2011).
Зменшення прогресування СН у пацієнтів з кардіопатіями зі збереженою/зниженою ФВ ЛШ
Периндоприл запобігає ремоделюванню міокарда, зменшує гіпертрофію та кількість субендокардіального колагену, відновлює відношення міозин/ізоензим, підвищує толерантність до навантаження та зменшує симптоми СН і частоту госпіталізацій з приводу декомпенсації (Cleland J. et al., 2006; Nicolosi G. et al., 2009). У дозі 2 мг/добу периндоприл рідше зумовлює гіпотензію та ліпше переноситься хворими на хронічну СН II-IV класів NYHA з ФВ ЛШ <40%, спричинену ІХС чи дилатаційною кардіоміопатією, ніж еналаприл у дозі 2,5 мг/добу (Vitovec J. et al., 2000).
Зменшення протеїнурії та прогресування ХХН при діабетичній нефропатії
У пацієнтів із ЦД 1 типу з початковими стадіями діабетичної нефропатії через 3-5 років терапії периндоприлом товщина базальної мембрани клубочків суттєво зменшилася (Ahmad J. et al., 2003). У хворих на ЦД 2 типу з альбумінурією через 2 роки об’єм інтерстицію кори нирок у групі периндоприлу був істотно меншим, ніж у групі плацебо (Cordonnier D. J. et al., 1999). Крім зменшення альбумінурії, тривала терапія периндоприлом сповільнює зниження швидкості клубочкової фільтрації у хворих на ЦД 2 типу (Jerums G. et al., 2004).
При порівнянні однорічної терапії периндоприлом (4 мг/добу) та кандесартаном (8-16 мг/добу) у хворих на ЦД 2 типу з хорошим глікемічним контролем та АГ 1 ступеня обидва препарати ефективно знижували АТ (р <0,01) та зменшували альбумінурію (р <0,05). Однак лише периндоприл зменшував рівні глікемії та інсулінемії натще, індекс НОМА, холестерин, ліпопротеїн (а) та холестерин ЛПНЩ (p <0,05 у порівнянні з початковими показниками); ліпідознижувальний ефект утримувався через місяць після відміни периндоприлу (Derosa G. et al., 2003).
Зменшення ризику СС ускладнень та смертності при термінальній стадії ниркової недостатності
У пацієнтів з термінальною стадією ниркової недостатності ризик загальної смертності знизився на 81%, СС – на 82% (Guerin A. P. et al., 2001).
Зменшення ризику інсульту в пацієнтів з перенесеним інсультом
За 4 роки спостереження в дослідженні PROGRESS, яке включало групу активної терапії (периндоприл 4 мг/добу + індапамід за потреби; n=3051) та групу плацебо (n=3054), під впливом монотерапії АТ знизився на 5/3 мм рт. ст., ризик інсульту – на 5%, тоді як у поєднанні з індапамідом ризик тяжких СС ускладнень знизився на 50%, інсульту – на 28% (PROGRESS Collaborative Group, 2001). У зв’язку з цим питання ефективності монотерапії периндоприлом у цієї категорії пацієнтів залишається відкритим. В осіб, які перенесли інсульт, периндоприл не зменшує кровоток у внутрішній сонній та середній мозковій артерії.
На сьогодні в Україні доступний препарат Періндопрес – перший вітчизняний генеричний периндоприл виробництва ПрАТ «Фармацевтична фірма «Дарниця» у дозах 4 та 8 мг по 30 таблеток в упаковці. Препарат є високоефективним і фінансово доступним, забезпечує надійний контроль АТ упродовж 24 год та всі інші плейотропні ефекти периндоприлу, зменшує ризик ускладнень, зокрема ІМ на 24%.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 5 (450), березень 2019 р.