6 травня, 2019
Настоящее и будущее терапии воспалительных заболеваний кишечника: 14-й конгресс ЕССО под руководством Обеликса

6-9 марта состоялся 14-й международный конгресс Европейской организации по изучению болезни Крона и колита (ECCO), который на этот раз прошел в чарующей и несколько чопорной столице Дании – Копенгагене. Волшебство этого города покорило организаторов конгресса, и, вдохновленные всемирно известными сказками Ганса Христиана Андерсена, они решили создать костюмированный комедийный фильм-легенду об ЕССО‑2019 в духе Астерикса и Обеликса.
 Главными героями этого фильма стали сами организаторы: Silvio Danese (президент ЕССО и председатель организационного комитета) предстал в образе сильного Обеликса, Laurent Peyrin-Biroulet (вновь избранный президент ЕССО, но пока еще не вступивший в должность) сыграл роль ловкого Астерикса, Willem Bemelman (секретарь ЕССО) убедительно исполнил роль друида Гетафикса, а Janneke van der Woude (член организационного комитета, соавтор многих руководств ЕССО) – незаменимой помощницы друида Майорикс.
Главными героями этого фильма стали сами организаторы: Silvio Danese (президент ЕССО и председатель организационного комитета) предстал в образе сильного Обеликса, Laurent Peyrin-Biroulet (вновь избранный президент ЕССО, но пока еще не вступивший в должность) сыграл роль ловкого Астерикса, Willem Bemelman (секретарь ЕССО) убедительно исполнил роль друида Гетафикса, а Janneke van der Woude (член организационного комитета, соавтор многих руководств ЕССО) – незаменимой помощницы друида Майорикс.
Сюжет фильма ЕССО‑2019 очень напоминает фабулу оригинала: римские легионеры окружили одну маленькую галльскую деревушку, жители которой не собираются покориться великой Римской империи. Два известных галльских воина – Астерикс и Обеликс – обратились к друиду Гетафиксу с просьбой сварить волшебное зелье, чтобы с легкостью одолеть скопище легионеров. Однако Гетафикс, как и остальные жители деревни, оказались тяжело больны: римляне наслали на них проклятье в виде воспалительных заболеваний кишечника (ВЗК). Майорикс, ухаживающая за Гетафиксом, отправляет Астерикса и Обеликса на волшебном самолете в современный Копенгаген – в Великий замок на конгресс ЕССО, где славные воины смогут найти лекарство от коварного недуга.
Вот так в Великом замке (крупнейшем выставочном центре Копенгагена Bella Center), на сцене во время торжественной церемонии открытия ЕССО‑2019 появились галлы (многочисленные члены организационного комитета), а вступительное слово произнес сам Обеликс (профессор S. Danese).
 Такое необычное начало международной конференции, проводимой под эгидой авторитетного научного общества, безусловно, заинтриговало участников ЕССО‑2019, которые с большим интересом слушали вступительную речь профессора S. Danese. Приветствуя участников конгресса, президент организации подчеркнул, что ЕССО‑2019 – это крупнейшее в мире мероприятие, посвященное ВЗК. В отличие от ранее проводившихся конгрессов, в работе ЕССО‑2019 приняли участие 7960 делегатов из 78 стран, в этом году опубликовано рекордное количество абстрактов – 1012. Такая высокая популярность в мировом медицинском сообществе, по мнению профессора S. Danese, свидетельствует о высоком уровне проведения данного научного мероприятия. Помимо основной научной работы ЕССО‑2019, в рамках конгресса предусматривалась дополнительная обучающая программа: состоялись 4-й ЕССО-форум, 4-й D-ЕССО-семинар, 1-й ЕССО-ESGAR-форум по базовой визуализации, 6-й ЕССО-ESGAR-форум по ультразвуковой диагностике, 1-й форум по методологии и разработке практических руководств, 8-й мастер-класс S-ЕССО по ВЗК. Президент организации представил участникам конгресса объединенный регистр для клинической оценки и исследований – UR-CARE (объемную базу данных, содержащую медицинские документы больных ВЗК и результаты исследований в этой области) и предложил активно использовать ее в своей практической деятельности. Не остался без внимания журнал, выпускаемый под эгидой ЕССО, – Journal of Crohn’s and Colitis (JCC), представляющий точную, корректную и объективную оценку проводимых исследований по ВЗК и входящий в топ‑3 мировых медицинских журналов.
Такое необычное начало международной конференции, проводимой под эгидой авторитетного научного общества, безусловно, заинтриговало участников ЕССО‑2019, которые с большим интересом слушали вступительную речь профессора S. Danese. Приветствуя участников конгресса, президент организации подчеркнул, что ЕССО‑2019 – это крупнейшее в мире мероприятие, посвященное ВЗК. В отличие от ранее проводившихся конгрессов, в работе ЕССО‑2019 приняли участие 7960 делегатов из 78 стран, в этом году опубликовано рекордное количество абстрактов – 1012. Такая высокая популярность в мировом медицинском сообществе, по мнению профессора S. Danese, свидетельствует о высоком уровне проведения данного научного мероприятия. Помимо основной научной работы ЕССО‑2019, в рамках конгресса предусматривалась дополнительная обучающая программа: состоялись 4-й ЕССО-форум, 4-й D-ЕССО-семинар, 1-й ЕССО-ESGAR-форум по базовой визуализации, 6-й ЕССО-ESGAR-форум по ультразвуковой диагностике, 1-й форум по методологии и разработке практических руководств, 8-й мастер-класс S-ЕССО по ВЗК. Президент организации представил участникам конгресса объединенный регистр для клинической оценки и исследований – UR-CARE (объемную базу данных, содержащую медицинские документы больных ВЗК и результаты исследований в этой области) и предложил активно использовать ее в своей практической деятельности. Не остался без внимания журнал, выпускаемый под эгидой ЕССО, – Journal of Crohn’s and Colitis (JCC), представляющий точную, корректную и объективную оценку проводимых исследований по ВЗК и входящий в топ‑3 мировых медицинских журналов.
 Анонсируя появление новых практических рекомендаций ЕССО, импозантный Обеликс отметил, что в этом году ожидается обновление четырех руководств: практических рекомендаций по лечению язвенного колита (ЯК) и болезни Крона (БК), терапии БК в педиатрической популяции, профилактике и лечению оппортунистических инфекций у больных ВЗК. Помимо активного научного общения, профессор S. Danese пригласил участников конгресса продолжить диалог в ходе генеральной ассамблеи и в менее формальной обстановке – в рамках ЕССО-вечеринки «Сердца и мысли». Завершая свою речь, президент организации пожелал участникам конгресса найти много нового, интересного, полезного для практической деятельности в ходе мероприятия.
Анонсируя появление новых практических рекомендаций ЕССО, импозантный Обеликс отметил, что в этом году ожидается обновление четырех руководств: практических рекомендаций по лечению язвенного колита (ЯК) и болезни Крона (БК), терапии БК в педиатрической популяции, профилактике и лечению оппортунистических инфекций у больных ВЗК. Помимо активного научного общения, профессор S. Danese пригласил участников конгресса продолжить диалог в ходе генеральной ассамблеи и в менее формальной обстановке – в рамках ЕССО-вечеринки «Сердца и мысли». Завершая свою речь, президент организации пожелал участникам конгресса найти много нового, интересного, полезного для практической деятельности в ходе мероприятия.
Помимо такого интригующего открытия, участников ЕССО‑2019 ожидали и другие замечательные новшества. Пристальное внимание делегаты конгресса уделили Е-терминалам. В рамках этой инициативы ЕССО на специальных станциях, оснащенных мощными компьютерными терминалами, участники конференции могли ознакомиться с обучающими программами, просмотреть видео с профессиональными советами по проведению диагностических и лечебных манипуляций у больных ВЗК, прослушать обучающие аудиоподкасты от ведущих мировых экспертов в области ВЗК. Е-терминалы предоставляли доступ к электронной библиотеке, содержащей результаты многочисленных клинических исследований и данные систематических обзоров, метаанализов, а также книгу абстрактов с лучшими рефератами, поданными в этом году, Е-справочник с открытым доступом к расширенной коллекции алгоритмов, сформированных на основе последних рекомендаций ЕССО. С помощью Е-терминалов делегаты могли оформить заявку на получение стипендий и грантов для финансирования своих научных исследований, ознакомиться с самыми популярными статьями и практическими рекомендациями, опубликованными в JCC, а также получить доступ в UR-CARE.
 Особой гордостью ЕССО‑2019 стало создание вебкастов, освещавших все выступления, прозвучавшие в ходе 12 научных сессий конгресса, а также 6-го ЕССО-ESGAR-форума по ультразвуковой диагностике, 8-го мастер-класса S-ЕССО по ВЗК, 1-й рабочей группы по методологии создания практических руководств. Вплоть до 30 апреля любые специалисты, состоявшиеся врачи и ученые, студенты вузов и молодые доктора, только начинающие свою практическую деятельность, имели возможность в любой точке земного шара получить бесплатный онлайн-доступ к этим бесценным обучающим материалам.
Особой гордостью ЕССО‑2019 стало создание вебкастов, освещавших все выступления, прозвучавшие в ходе 12 научных сессий конгресса, а также 6-го ЕССО-ESGAR-форума по ультразвуковой диагностике, 8-го мастер-класса S-ЕССО по ВЗК, 1-й рабочей группы по методологии создания практических руководств. Вплоть до 30 апреля любые специалисты, состоявшиеся врачи и ученые, студенты вузов и молодые доктора, только начинающие свою практическую деятельность, имели возможность в любой точке земного шара получить бесплатный онлайн-доступ к этим бесценным обучающим материалам.
Организаторы ЕССО‑2019 особо выделили семь докладов, которые, по их мнению, окажут большое влияние на последующее развитие фармакотерапии ВЗК. В частности, сообщение госпожи Salome Pinho (г. Порто, Португалия), сделанное от имени мультидисциплинарной команды ученых и посвященное гликанам – новым иммуномодуляторам, позволяющим влиять на иммунный ответ, опосредованный Т-клетками. Ранее португальские ученые показали, что Т-лимфоциты, располагающиеся в слизистой оболочке кишечника больных ВЗК, содержат малое количество разветвленных N-гликанов, что ассоциируется с тяжелым течением заболевания. В данной работе, выигравшей ЕССО-грант, использовался мультидисциплинарный подход с проведением исследований in vitro, ex vivo и с участием лабораторных животных. Исследователи доказали, что введение простого гликана N-ацетилглюкозамина в культуру Т-клеток слизистой оболочки кишечника, полученных у больных активным ЯК, сопровождалось усилением процессов N-гликозилирования в Т-клеточных рецепторах, что приводило к супрессии роста Т-клеток, ингибированию иммунного ответа Th1/Th17 и контролированию активности Т-клеток. Введение N-ацетилглюкозамина мышам, дефицитным по MGAT5-/-, MGAT5+/-, предрасположенным таким образом к раннему развитию и тяжелому течению ЯК, сопровождалось значительным снижением активности заболевания и позволило предупредить прогрессирование ЯК. Такого эффекта, по мнению исследований, удалось достичь за счет уменьшения активности иммунного ответа, опосредованного Т-клетками. Исследуя биоптаты толстой кишки, полученные у больных ЯК, исследователи доказали, что уровень экспрессии разветвленных N-гликанов ассоциируется с тяжестью заболевания и может использоваться для прогнозирования эффективности стандартной терапии. В заключение S. Pinho отметила, что гликаны можно рассматривать в качестве новых иммуномодуляторов для лечения ВЗК, а также как многообещающий прогностический гликобиомаркер ответа на проводимую терапию.
Доктор Geert R. D’Haens (г. Амстердам, Нидерланды) представил результаты II фазы рандомизированного контролированного исследования (РКИ), в котором изучалась эффективность индукционной и поддерживающей терапии с использованием нового моноклонального препарата – мирикизумаба, прицельно направленного р‑19 антитела к интерлейкину‑23. В исследовании приняли участие больные со среднетяжелым/тяжелым течением ЯК. Исследование проводилось в две фазы. Первоначально пациентов рандомизировали в соотношении 1:1:1:1 для внутривенного (в/в) введения плацебо (n=63), 50 мг (n=63) или 200 мг (n=62) мирикизумаба с предусмотренной возможностью увеличения дозировки препарата, фиксированной дозы мирикизумаба – 600 мг (n=61) каждые 4 нед. Оценку эффективности проводимой терапии проводили на 12-й неделе лечения. Пациентов, достигших клинической ремиссии на фоне приема мирикизумаба, к 12-й неделе повторно рандомизировали в соотношении 1:1 для проведения поддерживающей подкожной (п/к) терапии мирикизумабом (200 мг) каждые 4 нед (К4Н; n=47) или каждые 12 нед (К12Н; n=46) вплоть до достижения суммарной длительности лечения 52 нед.
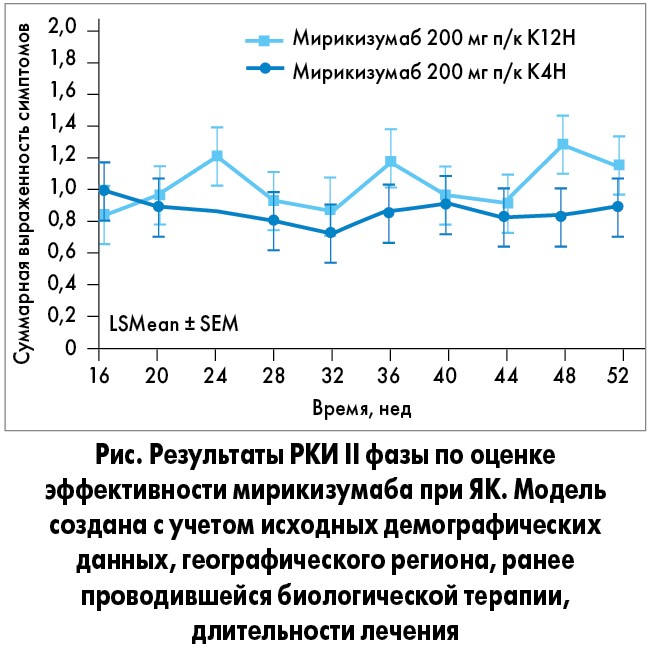 К 52-й неделе клинической ремиссии достигли 46,8 и 37,0% пациентов, получавших мирикизумаб К4Н и К12Н соответственно; клинический ответ зафиксирован у 80,9 и 76,1% больных из группы К4Н и К12Н. Среди участников исследования, достигших ремиссии к 12-й неделе терапии, течение заболевания у 61,1 и 38,5% пациентов, принимавших мирикизумаб по схеме К4Н и К12Н соответственно, расценивалось как клиническая ремиссия. В когорте больных, достигших клинического ответа (но не ремиссии) к 12-й неделе терапии, у 37,9 и 36,4% участников из групп К4Н и К12Н диагностирована клиническая ремиссия к 52-й неделе лечения (рис.).
К 52-й неделе клинической ремиссии достигли 46,8 и 37,0% пациентов, получавших мирикизумаб К4Н и К12Н соответственно; клинический ответ зафиксирован у 80,9 и 76,1% больных из группы К4Н и К12Н. Среди участников исследования, достигших ремиссии к 12-й неделе терапии, течение заболевания у 61,1 и 38,5% пациентов, принимавших мирикизумаб по схеме К4Н и К12Н соответственно, расценивалось как клиническая ремиссия. В когорте больных, достигших клинического ответа (но не ремиссии) к 12-й неделе терапии, у 37,9 и 36,4% участников из групп К4Н и К12Н диагностирована клиническая ремиссия к 52-й неделе лечения (рис.).
Результаты III фазы исследования UNIFI, анализировавшего эффективность и безопасность п/к введения другого моноклонального антитела – устекинумаба в поддерживающей терапии ЯК, представил W. Sandborn (г. Сан-Диего, США). В этом исследовании приняли участие больные со среднетяжелым/тяжелым течением ЯК, не ответившие на традиционную или биологическую терапию (включая антифактор некроза опухоли и/или ведолизумаб; n=523), но достигшие клинического ответа спустя 8 нед после в/в инфузии одной индукционной дозы устекинумаба. Пациентов рандомизировали в соотношении 1:1 для п/к введения плацебо, 90 мг устекинумаба К8Н или К12Н. Первичной конечной точкой являлось достижение клинической ремиссии к 44-й неделе терапии (52-й неделе после в/в инфузии устекинумаба); в качестве вторичных конечных точек выступали длительность поддержания клинического ответа, частота достижения эндоскопической ремиссии, поддержания ремиссии без использования кортикостероидов, а также поддержание клинической ремиссии в подгруппе пациентов, достигших клинической ремиссии первоначально.
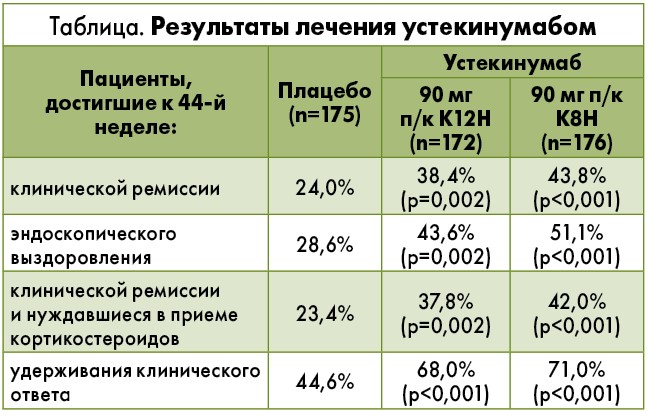 Введение устекинумаба К8Н и К12Н достоверно чаще позволяло достичь клинической ремиссии к 44-й неделе (43,8 и 38,4% соответственно) по сравнению с плацебо (24,0%; р<0,001 и р=0,002 соответственно). У значительно большей части пациентов, получавших устекинумаб К8Н и К12Н, оказалось возможным удержать клинический ответ к 44-й неделе и достичь эндоскопической ремиссии, а также клинической ремиссии без приема кортикостероидов, в отличие от группы плацебо (табл.).
Введение устекинумаба К8Н и К12Н достоверно чаще позволяло достичь клинической ремиссии к 44-й неделе (43,8 и 38,4% соответственно) по сравнению с плацебо (24,0%; р<0,001 и р=0,002 соответственно). У значительно большей части пациентов, получавших устекинумаб К8Н и К12Н, оказалось возможным удержать клинический ответ к 44-й неделе и достичь эндоскопической ремиссии, а также клинической ремиссии без приема кортикостероидов, в отличие от группы плацебо (табл.).
Профессор W. Sandborn подчеркнул хорошую переносимость устекинумаба: количество нежелательных явлений в основной группе оказалось сопоставимым с таковым в группе плацебо, а количество пациентов, завершивших исследование не в соответствии с протоколом, в группе плацебо значительно превышало таковое в группах К8Н и К12Н.
Таким образом, различные схемы п/к введения устекинумаба (К8Н и К12Н) позволяли достичь клинической ремиссии, удерживать клинический ответ, способствовали эндоскопическому выздоровлению и достижению ремиссии без применения кортикостероидов.
Профессор L. Peyrin-Biroulet (г. Нанси, Франция), недавно избранный президент ЕССО, который еще не успел вступить в свою должность, представил делегатам результаты II фазы исследования OASIS, в котором анализировалась эффективность этрасимода (перорального селективного модулятора сфингозин‑1-фосфатного рецептора) в лечении среднетяжелого/тяжелого ЯК. Согласно дизайну исследования, пациентов рандомизировали для приема 1 мг (n=52) или 2 мг (n=52; без титрации дозы) этрасимода либо плацебо (n=54). Эндоскопическую тяжесть заболевания оценивали исходно и спустя 12 нед терапии при помощи ректосигмоидоскопии со взятием биоптатов. В качестве конечных точек использовали частоту эндоскопического и гистологического улучшения, а также гистологической ремиссии.
 По сравнению с больными из группы плацебо, пациенты, принимавшие 2 мг этрасимода, достоверно чаще достигали эндоскопического улучшения (16,3 против 43,2%; р=0,003), гистологического улучшения (10,2 против 31,7%; р=0,006) и гистологической ремиссии (6,1 против 19,5%; р=0,027) к 12-й неделе терапии. Полное восстановление слизистой оболочки толстой кишки (одновременное наличие признаков эндоскопического улучшения и гистологической ремиссии) зафиксировано у 19,5% пациентов, получавших 2 мг этрасимода, и у 4,1% больных из группы плацебо (р=0,010). Назначение этрасимода в дозе 1 мг также превосходило плацебо по частоте достижения конечных точек, однако зарегистрированные различия не имели статистической значимости. Исходя из полученных данных, исследователи считают этрасимод (в дозе 2 мг) эффективным средством для лечения ЯК. Профессор L. Peyrin-Biroulet резюмировал: полное восстановление слизистой оболочки может считаться реально достижимым и объективным показателем эффективности лекарственных средств в исследованиях, посвященных индукции ремиссии.
По сравнению с больными из группы плацебо, пациенты, принимавшие 2 мг этрасимода, достоверно чаще достигали эндоскопического улучшения (16,3 против 43,2%; р=0,003), гистологического улучшения (10,2 против 31,7%; р=0,006) и гистологической ремиссии (6,1 против 19,5%; р=0,027) к 12-й неделе терапии. Полное восстановление слизистой оболочки толстой кишки (одновременное наличие признаков эндоскопического улучшения и гистологической ремиссии) зафиксировано у 19,5% пациентов, получавших 2 мг этрасимода, и у 4,1% больных из группы плацебо (р=0,010). Назначение этрасимода в дозе 1 мг также превосходило плацебо по частоте достижения конечных точек, однако зарегистрированные различия не имели статистической значимости. Исходя из полученных данных, исследователи считают этрасимод (в дозе 2 мг) эффективным средством для лечения ЯК. Профессор L. Peyrin-Biroulet резюмировал: полное восстановление слизистой оболочки может считаться реально достижимым и объективным показателем эффективности лекарственных средств в исследованиях, посвященных индукции ремиссии.
Результаты III фазы исследования VARSITY представил профессор Stefan Schreiber (г. Кельн, Германия). Дизайн этого РКИ предполагал сравнение эффективности ведолизумаба и адалимумаба в лечении ЯК. Больных ЯК распределяли на две группы. Пациенты 1-й группы получали в/в 300 мг ведолизумаба на 0-й, 2-й, 6-й неделе с последующим введением препарата каждые 8 нед до достижения общей длительности лечения 46 нед и п/к введением плацебо каждые 2 нед до достижения 50-й недели (n=385). Больным 2-й группы п/к вводили адалимумаб в дозе 160 мг на 0-й неделе, 80 мг на 2-й неделе, затем 40 мг каждые 2 нед до достижения общей длительности лечения 50 нед, а также в/в вводили плацебо на 0-й, 2-й, 6-й неделе, затем каждые 8 нед на протяжении 46 нед (n=385). Длительность тщательного медицинского наблюдения составляла 18 нед (50-68-я неделя терапии), последующее наблюдение за состоянием пациентов осуществляли на протяжении 6 мес посредством телефонной связи. Первичной конечной точкой являлось достижение клинической ремиссии; в качестве вторичных конечных точек использовали такие параметры, как полное восстановление слизистой оболочки толстой кишки, а также количество пациентов, принимавших пероральные кортикостероиды на момент включения в исследование, но отказавшихся от их приема к 52-й неделе.
 Первичной конечной точки достигли 22% пациентов, принимавших адалимумаб, и 31% больных, получавших ведолизумаб (средние различия, СР 8,8%; 95% доверительный интервал, ДИ 2,6-15,0%). Терапия адалимумабом способствовала полному восстановлению слизистой в 27% случаев, а применение ведолизумаба – в 39,7% случаев (СР 12,0%; 95% ДИ 5,3-18,6%). Частота возникновения нежелательных эффектов признана сопоставимой между группами. В группе ведолизумаба зафиксировано абсолютное уменьшение количества пациентов, нуждавшихся в приеме пероральных кортикостероидов, однако межгрупповые различия оказались статистически недостоверными. Таким образом, исследование VARSITY подтвердило превосходство ведолизумаба над адалимумабом в достижении клинической ремиссии и полном восстановлении слизистой кишечника у пациентов со среднетяжелым/тяжелым течением ЯК. Наилучшие результаты зафиксированы в когорте больных, ранее не получавших терапию. Завершая свое выступление, профессор S. Schreiber подчеркнул, что полученные результаты подтверждают целесообразность первоочередного назначения ведолизумаба, а не адалимумаба в лечении среднетяжелого/тяжелого ЯК.
Первичной конечной точки достигли 22% пациентов, принимавших адалимумаб, и 31% больных, получавших ведолизумаб (средние различия, СР 8,8%; 95% доверительный интервал, ДИ 2,6-15,0%). Терапия адалимумабом способствовала полному восстановлению слизистой в 27% случаев, а применение ведолизумаба – в 39,7% случаев (СР 12,0%; 95% ДИ 5,3-18,6%). Частота возникновения нежелательных эффектов признана сопоставимой между группами. В группе ведолизумаба зафиксировано абсолютное уменьшение количества пациентов, нуждавшихся в приеме пероральных кортикостероидов, однако межгрупповые различия оказались статистически недостоверными. Таким образом, исследование VARSITY подтвердило превосходство ведолизумаба над адалимумабом в достижении клинической ремиссии и полном восстановлении слизистой кишечника у пациентов со среднетяжелым/тяжелым течением ЯК. Наилучшие результаты зафиксированы в когорте больных, ранее не получавших терапию. Завершая свое выступление, профессор S. Schreiber подчеркнул, что полученные результаты подтверждают целесообразность первоочередного назначения ведолизумаба, а не адалимумаба в лечении среднетяжелого/тяжелого ЯК.
Пристальное внимание делегатов конгресса привлекло выступление S. Vermeire (г. Левен, Бельгия), представившего финальные результаты исследования GEMINI LTS, в котором изучалась безопасность длительного приема ведолизумаба – кишечно-селективного гуманизированного моноклонального антитела к α4β7-интегрину. Ведолизумаб одобрен регуляторными органами США и Европы для лечения больных среднетяжелым/тяжелым ЯК и БК еще в 2014 г., поэтому запланированная исследования GEMINI LTS длительность составляла 9 лет. В этом международном многоцентровом исследовании приняли участие 894 больных ЯК и 1349 пациентов с БК, получавшие в/в инъекции ведолизумаба каждые 4 нед в рамках II фазы исследования GEMINI (прием препарата продолжался вплоть до завершения исследования или отмены медикамента в силу различных причин). Появление нежелательных явлений отмечали 93 и 96% больных ЯК и БК соответственно. Наиболее часто пациентов беспокоили обострения ЯК (36%), рецидивы БК (35%) и назофарингиты (в группе ЯК – 28%, в группе БК – 25%). Никаких новых тенденций в отношении развития инфекционных заболеваний, неопластических трансформаций, постинфузионных осложнений, поражения печени исследователи не зафиксировали. Серьезные нежелательные явления отмечены у 31% пациентов с ЯК и 41% больных БК, при этом обострение заболевания было наиболее частым серьезным нежелательным явлением (ЯК – 13%; БК – 17%). Отменить прием ведолизумаба в связи с появлением побочных действий пришлось у 15 и 17% больных ЯК и БК соответственно. На протяжении всего исследования не зарегистрировано ни одного случая развития мультифокальной лейкоэнцефалопатии; констатировано 10 летальных случаев (в группе ЯК – 4; в группе БК – 6), однако они не были ассоциированы с приемом препарата. Таким образом, исследование GEMINI LTS предоставило убедительные данные о безопасности длительной терапии ведолизумабом как ЯК, так и БК.
 Анализируя данные, представленные в постерной сессии, делегаты ЕССО‑2019 уделили большое внимание работе F. Castiglione и соавт. (г. Неаполь, Италия), которые представили результаты систематического обзора и метаанализа, сравнивавших эффективность расширенной эндоскопии и эндоскопического осмотра в белом свете в диагностике дисплазии/неоплазии у больных ВЗК. Ученые тщательно изучили данные 27 публикаций, размещенных в электронных базах PubMed/MEDLINE, EMBASE, SCOPUS, Кокрейновской библиотеке. В ходе этих испытаний были обследованы 6167 больных ВЗК, у которых впоследствии диагностировали 2024 случая различных неоплазий.
Анализируя данные, представленные в постерной сессии, делегаты ЕССО‑2019 уделили большое внимание работе F. Castiglione и соавт. (г. Неаполь, Италия), которые представили результаты систематического обзора и метаанализа, сравнивавших эффективность расширенной эндоскопии и эндоскопического осмотра в белом свете в диагностике дисплазии/неоплазии у больных ВЗК. Ученые тщательно изучили данные 27 публикаций, размещенных в электронных базах PubMed/MEDLINE, EMBASE, SCOPUS, Кокрейновской библиотеке. В ходе этих испытаний были обследованы 6167 больных ВЗК, у которых впоследствии диагностировали 2024 случая различных неоплазий.
Оказалось, что расширенное эндоскопическое исследование превосходило эндоскопию с белым светом в выявлении участков дисплазии (19,3 против 8,5%; отношение рисков, ОР 2,036). Вероятность обнаружения аденом при использовании хромоэндоскопии с контрастными красителями (ОР 2,605) и аутофлюоресцентного изображения (ОР 3,055) превосходила таковую при проведении эндоскопии с белым светом (ОР 1,096). Эндоскопия с использованием технологии I-SCAN (ОР 1,096), эндоскопия с использованием узкопольной оптики (ОР 0,650), полноспектровая эндоскопия (ОР 1,118) уступали в диагностической ценности эндоскопии с белым светом. Хромоэндоскопия с контрастными красителями превосходила эндоскопию с белым светом в обнаружении аденом, но уступала всем остальным методам исследования. Основываясь на полученных данных, эксперты настаивают на проведении расширенной эндоскопии больным ВЗК в ходе динамического наблюдения, т. к. вероятность диагностики неопластического поражения с помощью этого метода значительно превосходит эндоскопию с белым светом.
 Еще одним рекордом ЕССО‑2019 стала широкомасштабная выставка, проводившаяся на громадной площади (2350 м2); на этот раз экспозицию представляли 45 крупнейших медицинских компаний мира, в том числе AbbVie, Dr. Falk Pharma, Janssen, Pfizer, Roche, Sandoz, Takeda. Спонсоры конгресса традиционно организовали проведение интереснейших сателлитных симпозиумов. Представители компании Takeda репрезентовали сравнительные данные доказательной медицины, иллюстрирующие эффективность разнообразной фармакотерапии в лечении прогрессирующих ВЗК, а также рассказали об особенностях подготовки пациентов, страдающих ВЗК, к международным поездкам и длительным путешествиям. Симпозиум, прошедший под эгидой AbbVie, стал площадкой для обсуждения новых конечных точек в лечении ВЗК и возможного изменения целей консервативной терапии ВЗК. Компания Pfizer с гордостью представила практические рекомендации по применению тофацитиниба у больных ЯК; в рамках второго симпозиума, организованного этой фирмой, делегаты ЕССО‑2019 ознакомились с эффективными способами фармакотерапии депрессии у больных ВЗК. Захватывающее общение с лидерами фармацевтической индустрии, проходившее порой в игровой форме, увлекало делегатов ЕССО‑2019, погружая их в мир инноваций и новых возможностей.
Еще одним рекордом ЕССО‑2019 стала широкомасштабная выставка, проводившаяся на громадной площади (2350 м2); на этот раз экспозицию представляли 45 крупнейших медицинских компаний мира, в том числе AbbVie, Dr. Falk Pharma, Janssen, Pfizer, Roche, Sandoz, Takeda. Спонсоры конгресса традиционно организовали проведение интереснейших сателлитных симпозиумов. Представители компании Takeda репрезентовали сравнительные данные доказательной медицины, иллюстрирующие эффективность разнообразной фармакотерапии в лечении прогрессирующих ВЗК, а также рассказали об особенностях подготовки пациентов, страдающих ВЗК, к международным поездкам и длительным путешествиям. Симпозиум, прошедший под эгидой AbbVie, стал площадкой для обсуждения новых конечных точек в лечении ВЗК и возможного изменения целей консервативной терапии ВЗК. Компания Pfizer с гордостью представила практические рекомендации по применению тофацитиниба у больных ЯК; в рамках второго симпозиума, организованного этой фирмой, делегаты ЕССО‑2019 ознакомились с эффективными способами фармакотерапии депрессии у больных ВЗК. Захватывающее общение с лидерами фармацевтической индустрии, проходившее порой в игровой форме, увлекало делегатов ЕССО‑2019, погружая их в мир инноваций и новых возможностей.
Четыре дня насыщенной научной программы завершились торжественной церемонией закрытия, на которой делегаты 14-го конгресса увидели окончание ЕССО-фильма: Астерикс и Обеликс возвращаются в родную деревушку, найдя чудодейственный напиток в Великом замке ЕССО, исцеляют друида Гетафикса и всех своих односельчан от коварного недуга. Пополнив свой багаж теоретических знаний и насытившись яркими впечатлениями, участники конгресса покинули гостеприимные стены выставочного центра Bella Center. Организаторы ЕССО приступили к подготовке следующего масштабного конгресса, который состоится 12-15 февраля 2020 г. в Вене (Австрия): уже функционирует сайт ЕССО‑2020, разрабатывается предварительная научная программа, скоро начнется регистрация устных и постерных докладов.
Медична газета «Здоров’я України 21 сторіччя» № 7 (452), квітень 2019 р


