7 травня, 2019
Сахарный диабет и ожирение: актуальная проблема и эффективное решение
По материалам рекомендаций ADA (2019) и ADA/EASD (2018)
 Из года в год авторитетные международные сообщества (Всемирная организация здравоохранения (ВОЗ), Международная федерация диабета (International Diabetes Federation), Американская ассоциация клинических эндокринологов – American Association of Clinical Endocrinologists) неустанно подчеркивают важность проблемы сахарного диабета (СД), посвящая этому заболеванию многочисленные практические руководства. Так, Американская ассоциация диабетологов (American Diabetes Association, ADA) и Европейская ассоциация по изучению диабета (European Association for the Study of Diabetes, EASD) в 2019 и 2018 г. соответственно опубликовали обширные руководства по лечению СД, освещающие самые разнообразные аспекты лечения и профилактики данной метаболической патологии, а также сопутствующих ей заболеваний.
Из года в год авторитетные международные сообщества (Всемирная организация здравоохранения (ВОЗ), Международная федерация диабета (International Diabetes Federation), Американская ассоциация клинических эндокринологов – American Association of Clinical Endocrinologists) неустанно подчеркивают важность проблемы сахарного диабета (СД), посвящая этому заболеванию многочисленные практические руководства. Так, Американская ассоциация диабетологов (American Diabetes Association, ADA) и Европейская ассоциация по изучению диабета (European Association for the Study of Diabetes, EASD) в 2019 и 2018 г. соответственно опубликовали обширные руководства по лечению СД, освещающие самые разнообразные аспекты лечения и профилактики данной метаболической патологии, а также сопутствующих ей заболеваний.
Одним из таких недугов, распространенность которого в мире достигла масштабов эпидемии, является ожирение. По данным обновленного бюллетеня экспертов ВОЗ (2018), на протяжении 1975-2016 гг. распространенность ожирения во всем мире возросла в 3 раза; при этом в 2016 г. 13% взрослого населения земного шара страдали ожирением, что в абсолютных цифрах составляло 650 млн человек. Учитывая сохраняющиеся темпы роста заболеваемости, эксперты ВОЗ прогнозируют беспрецедентный рост уровня ожирения: к 2030 г. лишний вес / ожирение будут иметь более 65% населения Великобритании, а в Ирландии данный показатель достигнет небывалого уровня – 80%.
В связи с этим вопросы ведения больных СД с избыточной массой тела / ожирением являются чрезвычайно актуальными для врачей всего мира. Подчеркивая тот факт, что коррекция ожирения может затормозить прогрессирование предиабета в СД 2 типа, а нормализация массы тела у лиц, страдающих СД, способна улучшить степень компенсации гликемии и уменьшить потребность в гипогликемических препаратах (ГГП), эксперты ADA и EASD предлагают ряд эффективных мер, направленных на лечение ожирения. В данной статье будут рассмотрены основные способы коррекции массы тела у больных СД, рекомендованные ADA (2019) и ADA/EASD (2018).
Контроль ИМТ – обязательное условие
Опираясь на данные доказательной медицины, представители ADA предлагают целый спектр действий по оптимальному снижению массы тела у больных СД, включая коррекцию пищевого рациона и привычного образа жизни, фармакотерапию и оперативные вмешательства.
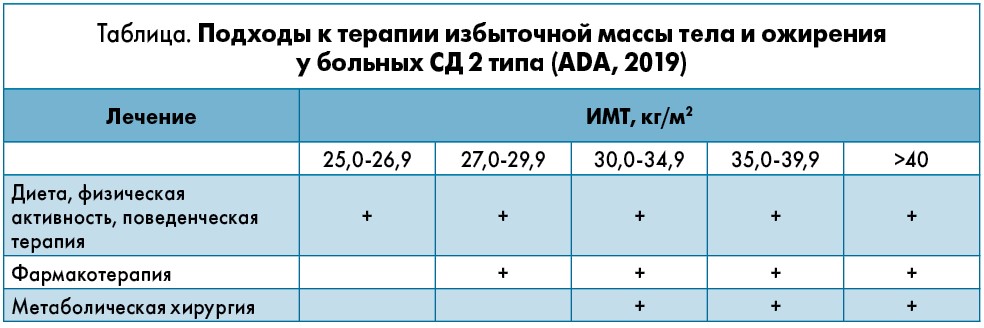
В руководстве ADA подчеркивается важность мониторинга значений индекса массы тела (ИМТ) у больных СД 2 типа: определять этот показатель следует при каждом обращении пациента за медицинской помощью с последующей обязательной фиксацией в медицинской документации (уровень доказательности В). Ведь именно показатели ИМТ помогут врачу определиться с необходимым объемом медицинской помощи для каждого пациента (табл.).
Определение ИМТ также позволит определить целевые значения массы тела, выбрать оптимальную интервенционную стратегию и точно информировать пациента о резком увеличении риска развития кардиоваскулярной патологии и смерти от всех причин при возрастании значений ИМТ.
Немедикаментозная коррекция
В руководстве ADA (2019) подчеркивается, что рационализация диеты, увеличение физической активности и коррекция образа жизни предназначены для снижения массы тела на >5%, а также для поддержания достигнутого результата; эти мероприятия следует рекомендовать больным СД 2 типа с избыточной массой тела / ожирением, готовым предпринять необходимые действия по изменению своего веса (уровень доказательности А). Эксперты отмечают целесообразность высокой интенсивности данных мероприятий (≥16 сессий на протяжении 6 мес) при условии, что изменение диеты, физической активности и бихевиоральная терапия обеспечивают энергетический дефицит в пределах 500-700 ккал/сут (уровень доказательности А).
Большое внимание в рассматриваемых руководствах уделяется закреплению достигнутого эффекта: «Пациентам, достигшим кратковременных целей в уменьшении массы тела, следует рекомендовать долгосрочные программы по поддержанию веса. Такие программы следует предоставлять как минимум ежемесячно, проводить мониторинг массы тела (еженедельно или чаще) и/или использовать стратегии, предполагающие самоконтроль достигнутого результата (подсчет пройденных шагов / расстояния). Следует рекомендовать продолжить употребление низкокалорийной пищи с поддержанием высокого уровня физической активности (200-300 мин/нед) (уровень доказательности А)». Эксперты ADA (2019) допускают возможность кратковременного поддержания очень низкокалорийной диеты (≤800 ккал/сут) и приема заменителей пищи у больных СД 2 типа, подчеркивая при этом необходимость чрезвычайно тщательного отбора пациентов и проведения такой коррекции рациона исключительно в медицинских учреждениях под пристальным врачебным контролем.
В более ранних рекомендациях, сформулированных экспертами ADA в содружестве с представителями EASD (2018), отмечается, что больным СД 2 типа следует придерживаться средиземноморской диеты, соблюдение которой способствует снижению массы тела и улучшению гликемического контроля: пациенты, следующие принципам этой диеты, на 37% реже нуждаются в назначении ГГП по сравнению с лицами, исключающими из рациона только жиры (отношение рисков (ОР) 0,63; 95% ДИ 0,51-0,86). Кроме того, средиземноморская диета способствует уменьшению уровня гликозилированного гемоглобина (HbA1c) по сравнению с контрольной диетой (средние различия (СР) -3,3 ммоль/моль; 95% ДИ от -5,1 до -1,5 ммоль/моль).
Такие жесткие рекомендации по изменению образа жизни и рационализации диеты строго обоснованы: убедительно доказано, что снижение массы тела у больных СД 2 типа с сопутствующей артериальной гипертензией, гиперлипидемией оказывает благотворное влияние на коморбидные состояния, способствуя уменьшению уровня HbA1c, триглицеридов и артериального давления (АД). Эксперты подчеркивают, чем больших успехов добьется пациент в нормализации своего веса, тем значительнее будет динамика в нормализации АД, снижении уровня общего холестерина (ХС) и ХС липопротеинов низкой плотности, уменьшении потребности в гипотензивных, гиполипидемических средствах и ГГП. Более того, некоторые пациенты, четко выполняя данные рекомендации, могут достичь нормативных значений гликемии, не принимая гипогликемических средств.
Look AHEAD: впечатляющие результаты
В данном контексте уместно будет привести результаты Look AHEAD – одного из самых крупномасштабных и длительных исследований, в котором изучалось влияние интенсивного изменения образа жизни на коррекцию массы тела. В этом исследовании приняли участие 16 медицинских центров США и 5145 больных СД 2 типа с ИМТ ≥25 кг/м2 (или ≥27 кг/м2 для лиц, принимавших инсулин). Пациентов рандомизировали в группу интенсивного изменения образа жизни (ИИОЖ) или осуществления стандартной поддержки и обучения (СПО) на протяжении 8 лет. Первичными конечными точками являлись уровни первичной кардиоваскулярной заболеваемости и смертности. Первоначально представители исследовательской группы Look AHEAD не доказали способность ИИОЖ уменьшать риск возникновения различных кардиоваскулярных событий у взрослых пациентов с СД 2 типа и избыточной массой тела / ожирением, однако они подчеркнули возможность снижения и длительного поддержания достигнутой массы тела у таких больных. Пациенты, вошедшие в группу ИИОЖ, смогли снизить свой вес в среднем на 4,7±0,2% от исходных значений в течение 8 лет, тогда как больные из группы СПО потеряли за это время только 2,1±0,2% массы тела (р<0,001). Интересно, что 50,3% и 35,7% представителей групп ИИОЖ и СПО соответственно смогли уменьшить исходный вес более чем на ≥5% (р<0,001). Подобная тенденция сохранялась в отношении потери ≥10% массы тела: пациенты из группы ИИОЖ чаще достигали такого впечатляющего результата, чем участники группы СПО (26,9 vs 17,2% соответственно). Приведенные результаты Look AHEAD красноречиво свидетельствуют о том, что 50% больных СД способны нормализовать массу тела только за счет интенсивного изменения привычного образа жизни, диеты и физической активности.
Не менее значимы результаты вторичного анализа результатов данного исследования (2016). В качестве первичной комбинированной конечной точки использовали уровень кардиоваскулярной смертности, распространенность нефатального инфаркта миокарда / нефатального инсульта, частоту госпитализации, обусловленной ишемической болезнью сердца. В качестве вторичных конечных точек дополнительно анализировали частоту выполнения хирургических вмешательств (аортокоронарного шунтирования, каротидной эндартерэктомии, чрескожного коронарного вмешательства) и госпитализаций по поводу сердечной недостаточности, заболеваний периферических кровеносных сосудов, а также уровень общей смертности. Оказалось, что риск достижения первичной конечной точки у пациентов, которые на протяжении первого года наблюдения смогли уменьшить свой вес минимум на 10%, снизился на 21% (скорректированное ОР 0,79; 95% ДИ 0,64-0,98; р=0,034); вероятность достижения вторичной конечной точки уменьшалась на 24% (скорректированное ОР 0,76; 95% ДИ 0,63-0,91; р=0,003) по сравнению с лицами, чей вес оставался стабильным или увеличивался.
Фармакотерапия
При подборе ГПП больным СД 2 типа с избыточной массой / ожирением эксперты ADA (2019) настойчиво рекомендуют врачам учитывать влияние этих лекарственных средств на массу тела (уровень доказательности Е). Представители данной авторитетной организации советуют, по возможности, минимизировать количество медикаментов для лечения коморбидной патологии, ассоциированной с увеличением массы тела (уровень доказательности Е). Вместе с тем специалисты ADA предостерегают от изолированного приема лекарственных средств, предназначенных для снижения массы тела, без надлежащей коррекции диеты, физической активности и проведения биохевиорального консультирования. «... такие медикаменты эффективны только в комплексе с вышеперечисленными мероприятиями», – гласит одно из положений руководства ADA (2019).
Метформин
Регламентируя особенности назначения гипогликемических препаратов, представители ADA (2019) в следующем порядке перечисляют наиболее оптимальные медикаменты для больных СД с сопутствующим ожирением / избыточной массой тела:
- метформин;
- ингибиторы α-глюкозидазы,
- ингибиторы натрийзависимого котраспортера глюкозы (SGLT2),
- агонисты рецепторов глюкагоноподобного пептида‑1 (АР ГПП‑1),
- миметики амилина.
Ингибиторы дипептидилпептидазы‑4 (ДПП‑4) оказывают нейтральное действие на массу тела. Больным СД с сопутствующим ожирением не следует назначать препараты, способствующие увеличению массы: секретагоги инсулина, тиазолидиндионы и, по возможности, инсулин.
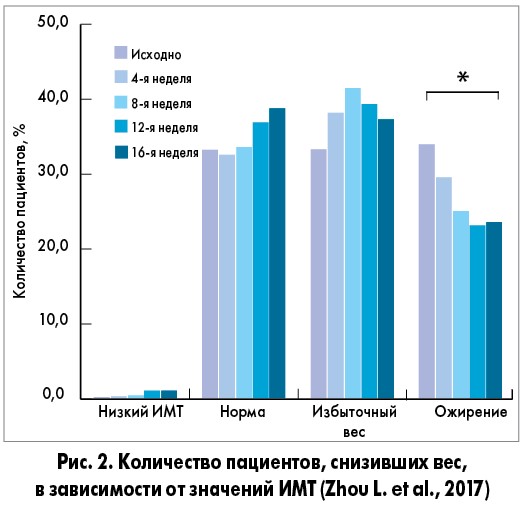
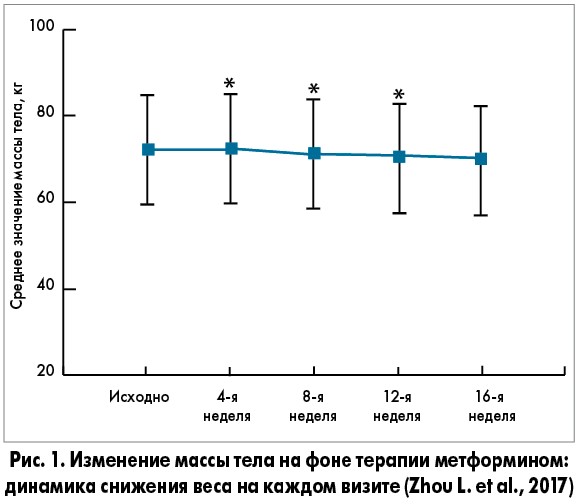 Предпочтительность назначения метформина, подчеркиваемая в руководствах ADA (2019) и ADA/EASD (2018), основывается на результатах многочисленных рандомизированных контролированных исследований (РКИ), систематических обзоров и метаанализов. Например, L. Zhou и соавт. (2017), представившие вторичный анализ одного РКИ, показали, что 16-недельная терапия метформином у больных СД 2 типа ассоциируется с плавным постепенным снижением массы тела, начиная с 4-й недели лечения. Ученые подчеркнули, что максимальный эффект в отношении коррекции массы тела развивается у лиц с сопутствующим ожирением, тогда как у пациентов с нормальным/низким ИМТ влияние метформина на данный показатель признано недостоверным (рис. 1, 2).
Предпочтительность назначения метформина, подчеркиваемая в руководствах ADA (2019) и ADA/EASD (2018), основывается на результатах многочисленных рандомизированных контролированных исследований (РКИ), систематических обзоров и метаанализов. Например, L. Zhou и соавт. (2017), представившие вторичный анализ одного РКИ, показали, что 16-недельная терапия метформином у больных СД 2 типа ассоциируется с плавным постепенным снижением массы тела, начиная с 4-й недели лечения. Ученые подчеркнули, что максимальный эффект в отношении коррекции массы тела развивается у лиц с сопутствующим ожирением, тогда как у пациентов с нормальным/низким ИМТ влияние метформина на данный показатель признано недостоверным (рис. 1, 2).
 Следует подчеркнуть, что метформин может использоваться для коррекции гипергликемии и массы тела не только у пациентов среднего возраста, но и у больных пожилого и старческого возраста, а также у детей и подростков. Относительно недавно М. Solymar и соавт. (2018) опубликовали результаты метаанализа 6 РКИ, в которых приняли участие больные (n=1541) СД 2 типа старше 60 лет. Ученые доказали, что 12-недельный прием метформина в этой когорте пациентов сопровождается снижением первоначальной массы тела на 2,23 кг (95% ДИ от -2,84 до -1,62 кг; р<0,001), падением концентрации общего ХС (-0,184 ммоль/л; р<0,001), ХС липопротеинов низкой плотности (ЛПНП; -0,182 ммоль/л; р<0,001). Авторы подчеркнули еще одно значимое преимущество терапии метформином: прием этого препарата достоверно уменьшал риск коронарных событий (на 4-5%) и уровень общей смертности (на 2%) у лиц преклонного возраста.
Следует подчеркнуть, что метформин может использоваться для коррекции гипергликемии и массы тела не только у пациентов среднего возраста, но и у больных пожилого и старческого возраста, а также у детей и подростков. Относительно недавно М. Solymar и соавт. (2018) опубликовали результаты метаанализа 6 РКИ, в которых приняли участие больные (n=1541) СД 2 типа старше 60 лет. Ученые доказали, что 12-недельный прием метформина в этой когорте пациентов сопровождается снижением первоначальной массы тела на 2,23 кг (95% ДИ от -2,84 до -1,62 кг; р<0,001), падением концентрации общего ХС (-0,184 ммоль/л; р<0,001), ХС липопротеинов низкой плотности (ЛПНП; -0,182 ммоль/л; р<0,001). Авторы подчеркнули еще одно значимое преимущество терапии метформином: прием этого препарата достоверно уменьшал риск коронарных событий (на 4-5%) и уровень общей смертности (на 2%) у лиц преклонного возраста.
В настоящее время метформин является препаратом выбора не только для лечения пожилых больных СД, но и для детей и подростков с избыточной массой тела / ожирением. По данным авторов систематического обзора и метаанализа 11 РКИ (Sun J. et al., 2019), у детей и подростков, принимавших метформин в дозе 1000-2000 мг на протяжении 8 нед – 18 мес, наблюдалось не только снижение массы тела, но и достоверное снижение концентрации ХС ЛПНП (СР -4,29; 95% ДИ от -7,45 до -1,12). Зафиксированный факт J. Sun и соавт. (2019) трактовали как улучшение метаболизма липидов на фоне лечения метформином, объясняя таким образом один из возможных механизмов нормализации массы при приеме этого ГГП.
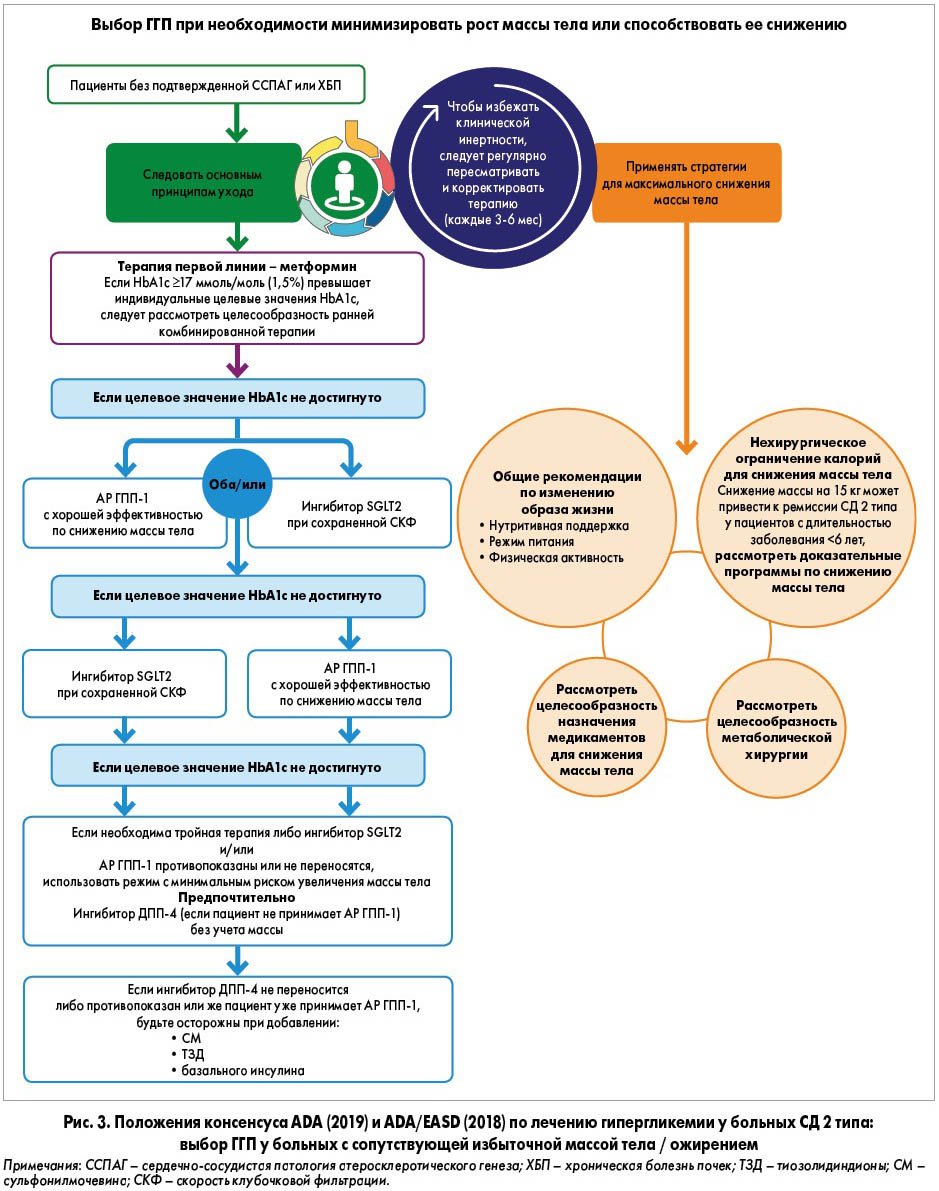
Американские и европейские эксперты предусматривают следующую тактику действий при назначении ГГП таким больным (рис. 3).
Таким образом, положения обоих руководств – ADA (2019) и ADA/EASD (2018) – единодушно подтверждают целесообразность назначения метформина в качестве ГГП выбора при наличии избыточной массы тела / ожирения. И только при недостаточном ответе на монотерапию метформином предусматривается возможность назначения ингибиторов SGLT2 и/или АР ГПП‑1. Такая рекомендация по предпочтительности первоначального применения метформина сформулирована с учетом большой доказательной базы, подтверждающей его эффективность, безопасность, переносимость, низкую стоимость и значительный опыт клинического применения. Эксперты ADA (2019) рекомендуют продолжать прием метформина максимально длительно (при условии хорошей переносимости и отсутствии противопоказаний). «Другие медикаменты, включая инсулин, следует добавлять к метформину», – подчеркивают представители ADA.
Дополнительные препараты
При недостаточном эффекте вышеперечисленных мероприятий руководство ADA (2019) предусматривает дополнительное назначение медикаментов, одобренных Управлением по контролю продуктов питания и лекарственных средств США (FDA) для коррекции массы тела: фентермин (допускается только кратковременное применение ≤12 нед), орлистат, лоркасерин, лираглутид, а также комбинации фентремина / топирамата ER, налтрексона / бупропиона ER, предназначенных для более длительного приема (>12 нед). Несмотря на то что эти препараты доказали свою способность усиливать результативность терапии, направленной на коррекцию массы тела и нормализацию гликемии, эксперты ADА/EASD (2018) не рекомендуют рутинное применение перечисленных медикаментов из-за их высокой стоимости, умеренной эффективности и наличия разнообразных побочных действий.
По мнению экспертов ADA, эффективность проводимой терапии по снижению массы тела следует оценивать ежемесячно на протяжении первых 3 мес лечения. При недостаточном ответе (снижение массы <5%) спустя 3 мес или при появлении значимых нежелательных явлений при дополнительном приеме медикаментов, корригирующих вес, следует отменить эти препараты и назначить альтернативные лекарственные средства либо рассмотреть целесообразность использования другого терапевтического подхода.
Метаболическая хирургия
При неэффективности вышеперечисленных консервативных мероприятий специалисты ADA (2019) рекомендуют прибегнуть к оперативному лечению: метаболическое хирургическое вмешательство показано больным СД 2 типа с ИМТ ≥40 кг/м2, а также взрослым пациентам с ИМТ 35,0-39,9 кг/м2, не достигшим значимых успехов в длительном снижении массы тела и улучшении течения коморбидной патологии (включая гипергликемию) посредством соответствующих нехирургических методик (уровень доказательности А). Подобное положение представители ADA сформулировали для больных с ИМТ 27,5-32,4 кг/м2, которые не смогли добиться желаемого эффекта в рамках консервативной терапии. Таким образом, согласно современному руководству ADA, хирургическое вмешательство может быть предложено не только больным с морбидным ожирением, ожирением 1-2 ст., но и лицам с избыточной массой тела.
Возвращаясь еще раз к исследованию Look AHEAD, следует привести результаты другого вторичного анализа его данных: Т. Wadden и соавт. (2019) оценивали эффективность бариатрического вмешательства у больных СД с сопутствующим ожирением. Оказалось, что пациенты, перенесшие бариатрическую операцию, смогли снизить свой вес на 19,3% на протяжении 10 лет по сравнению с больными из группы ИИОЖ и СПО, которым удалось уменьшить этот показатель только на 5,8 и 3,3% соответственно. Эти данные подтверждают высокую результативность метаболической хирургии, рекомендованной ADA (2019) и ADA/EASD (2018).
Спектр метаболических вмешательств, предлагаемых больным СД в настоящее время, достаточно широк: операции, уменьшающие объем желудка (вертикально-полосчатая гастропластика, бандажирование желудка, установка желудочного баллона), операции, приводящие к уменьшению всасывающей поверхности тонкого кишечника (еюноилеальное шунтирование, наложение анастомоза по Ру, билиопанкреатическое шунтирование). Хотя эксперты ADA не уточняют предпочтительный вид хирургического вмешательства, данные метаанализа L. Li и соавт. (2019) демонстрируют превосходство лапароскопической вертикальной продленной эксцизионной гастропластики (ЛВПЭГ) над лапароскопическим бандажированием желудка. Выполнение ЛВПЭГ позволило добиться значимого снижения массы тела через 6 мес (взвешенная разность средних (ВРС) -9,29; 95% ДИ от -15,19 до -3,40; р=0,002), 12 мес (ВРС -16,67; 95% ДИ от -24,3 до -9,05; р<0,001), 24 мес (ВРС -19,63; 95% ДИ от -29,0 до -10,26; р<0,001) и 36 мес (ВРС -19,28; 95% ДИ от -27,09 до -11,47; р<0,001) по сравнению с бандажированием желудка.
Эксперты ADA (2019) настаивают на выполнении метаболического оперативного вмешательства в высокоспециализированных хирургических стационарах с осуществлением последующей длительной поддержки пациентов и рутинного мониторинга микронутриентов, пищевого статуса. Несмотря на эти меры предосторожности, проведение таких вмешательств может осложниться развитием синдрома мальабсорбции, постоперационной пневмонией, тромбозом глубоких вен, легочной эмболией, раневой инфекцией, определяющих 0,25-2,0% уровень летальности. Кроме того, у 25% пациентов, перенесших метаболическое оперативное вмешательство, развивается выраженная депрессия, требующая длительного приема антидепрессантов.
Таким образом, наиболее безопасным, эффективным и экономически доступным методом коррекции избыточной массы тела / ожирения у больных СД 2 типа является комплексный подход, предполагающий модификацию образа жизни, рационализацию питания, увеличение физической активности в сочетании с длительной фармакотерапией метформином.
Литература
- https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight
- Look AHEAD Research Group. Eight-year weight losses with an intensive lifestyle intervention: the Look AHEAD study. Obesity (Silver Spring) 2014; 22:5-13
- Look AHEAD Research Group. Association of the magnitude of weight loss and changes in physical fitness with long-term cardiovascular disease outcomes in overweight or obese people with type 2 diabetes: a post-hoc analysis of the Look AHEAD randomised clinical trial. Lancet Diabetes Endocrinol. 2016 Nov; 4(11): 913-921. doi: 10.1016/S2213-8587(16)30162-0. Epub 2016 Aug 30.
- Wadden TA1. End-of-Trial Health Outcomes in Look AHEAD Participants who Elected to have Bariatric Surgery. Obesity (Silver Spring). 2019 Apr; 27(4): 581-590. doi: 10.1002/oby.22411.
- Melanie J. Davies. Management of hyperglycaemia in type 2 diabetes, 2018. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia. 2018. https://doi.org/10.1007/s00125-018-4729-5
- Margit Solymar. Metformin induces significant reduction of body weight, total cholesterol and LDL levels in the elderly – A meta-analysis. PLoS One. 2018; 13 (11): e0207947. doi: 10.1371/journal.pone.0207947
- Lingli Zhou. The magnitude of weight loss induced by metformin is independently associated with BMI at baseline in newly diagnosed type 2 diabetes: Post-hoc analysis from data of a phase IV open-labeled trial. Adv Clin Exp Med. 2017; 26 (4): 671-677.
- Sun J. The effects of metformin on insulin resistance in overweight or obese children and adolescents: A PRISMA-compliant systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore). 2019 Jan; 98 (4): e14249. doi: 10.1097/MD.0000000000014249.
- Li L. Meta-analysis of the effectiveness of laparoscopic adjustable gastric banding versus laparoscopic sleeve gastrectomy for obesity. Medicine (Baltimore). 2019 Mar; 98 (9): e14735. doi: 10.1097/MD.0000000000014735.
Медична газета «Здоров’я України 21 сторіччя» № 7 (452), квітень 2019 р