11 липня, 2019
Роль L-аргініну в лікуванні серцево-судинних захворювань: у фокусі – вибір ефективної дози
 L-аргінін – умовно незамінна амінокислота, що вперше була виділена 1886 р. E. Schulze та E. Steiger, а структура її встановлена E. Schulze та E. Winterstei 1897 р. [1]. L-аргінін використовується декількома шляхами для синтезу білка та низькомолекулярних біоактивних речовин (наприклад, оксиду азоту – NO, орнітину, проліну, креатину й поліамінів), які мають величезне фізіологічне значення. Крім того, аргінін регулює клітинні сигнальні шляхи й експресію генів для поліпшення серцево-судинної функції, підвищення чутливості до інсуліну [2], збільшення м’язової маси та зниження ожиріння в людей.
L-аргінін – умовно незамінна амінокислота, що вперше була виділена 1886 р. E. Schulze та E. Steiger, а структура її встановлена E. Schulze та E. Winterstei 1897 р. [1]. L-аргінін використовується декількома шляхами для синтезу білка та низькомолекулярних біоактивних речовин (наприклад, оксиду азоту – NO, орнітину, проліну, креатину й поліамінів), які мають величезне фізіологічне значення. Крім того, аргінін регулює клітинні сигнальні шляхи й експресію генів для поліпшення серцево-судинної функції, підвищення чутливості до інсуліну [2], збільшення м’язової маси та зниження ожиріння в людей.
Фізіологічна потреба тканин і органів в аргініні задовольняється його ендогенним синтезом або надходженням з їжею, проте для молодих людей і дорослих в умовах стресу чи хвороби ця амінокислота стає незамінною [3]. При надходженні з їжею L-аргінін всмоктується в тонкому кишечнику й транспортується в печінку, де основна його кількість утилізується в орнітиновому циклі [4]. Решта L-аргініну використовується як субстрат для синтезу NO [1], який є найважливішою субстанцією, що продукується судинним ендотелієм для регуляції судинного тонусу.
У фізіологічних умовах синтез NO з L-аргініну відбувається за допомогою ферменту NO-синтази (NOS), другим продуктом реакції є L-цитрулін [5]. Відомо декілька ізоформ NOS, названих за типом клітин, де вони були вперше виділені: нейрональна (nNOS), ендотеліальна (eNOS) і макрофагальна (iNOS) [1]. Саме еNOS локалізується в ендотеліальних клітинах і відповідає за синтез базального рівня та його зміну у відповідь на фізичні навантаження й хімічні стимули (брадикінін) [6], який відіграє важливу роль у реалізації механізмів локальної ендотеліальної цитопротекції, підтриманні судинного гомеостазу та фізіологічній регуляції артеріального тиску (АТ). Окрім того, еNOS виявлена в інших клітинах і тканинах, зокрема в кардіоміоцитах, еритроцитах, мегакаріоцитах і тромбоцитах [1].
З іншого боку, іNOS у судинній мережі присутня не тільки в макрофагах, а й у лімфоцитах, ендотеліальних клітинах, клітинах гладких м’язів або фібробластах. Вона активується під впливом бактеріальних ендотоксинів і запальних цитокінів, таких як фактор некрозу пухлини й інтерлейкіни, не залежить від кальцію та викликає синтез NO у високих концентраціях (у 1000 разів вищий порівняно з еNOS). У свою чергу, nNOS синтезує NO у фізіологічних кількостях, переважно як трансмітер у головному мозку й периферичній нервовій системі.
Роль NO в підтримці судинного гомеостазу зводиться до регуляції судинного тонусу, проліферації й апоптозу, а також регуляції оксидантних процесів. Окрім того, NO притаманні ангіопротекторні властивості [8]. NO також відповідальний за протизапальні ефекти, такі як інгібування експресії молекул клітинної адгезії ICAM‑1 (молекули міжклітинної адгезії 1 типу), VCAM‑1 (молекули адгезії судинного ендотелію 1 типу) та тканинного фактора; інгібування виділення хемокінів, таких як МСР‑1 (моноцитарний хемотаксичний фактор‑1). До того ж NO блокує агрегацію тромбоцитів і має фібринолітичний ефект [9].
За нормального функціонування ендотелію NO має антиатерогенний ефект: пригнічує утворення комплексів окисленого холестерину з ліпопротеїнами низької щільності (ЛПНЩ), запобігає вазоконстрикторним ефектам тромбоксану А2, серотоніну, що виділяються з тромбоцитів, знижує стабільність мРНК, моноцитарного хемотаксичного фактора, перешкоджає адгезії й агрегації тромбоцитів (цГМФ-залежний механізм), пригнічує експресію прозапальних генів (NF-κB). Недостатній синтез NO призводить до ушкодження мембран клітин продуктами вільнорадикального окислення. Пероксинітрит та інші реактивні сполуки, взаємодіючи з NO, посилюють захоплення ліпопротеїнів макрофагами судинної стінки. В умовах зниженого синтезу NO захисні механізми не функціонують, а отже, запускаються механізми атерогенезу. Цікаво, що L-аргінін не знижує рівень холестерину в крові, але в його присутності холестерин втрачає здатність відкладатися на стінках судин [10]. Клінічні дослідження з використанням перорального L-аргініну в пацієнтів із гіперхолестеринемією показали, що при пероральному прийомі L-аргінін покращує ендотелійзалежну вазодилатацію (ЕЗВД) [11] так само чи навіть більше, ніж після гіполіпідемічної терапії. Також було зафіксовано поліпшення ендотеліальної функції при гіперхолестеринемії в разі лікування L-аргініном у дозі 6,6 г/добу [12]. Плейотропні ефекти L-аргініну наведені в настанові з парентеральної нутриціології (ESPEN Guidelines on Parenteral Nutrition: On Cardiology and Pneumology, 2009), де препарат рекомендований для застосування в пацієнтів із хронічною серцевою недостатністю (СН) [13].
Посилення продукції й вивільнення NO, зумовлене L-аргініном, має антиоксидантний ефект і сприяє поліпшенню ендотеліальної функції [14], тому не викликає сумнівів у необхідності його призначення як доповнення до основної терапії, що сприяє поліпшенню біодоступності eNOS і покращує функціональний стан ендотелію при ішемічній хворобі серця (ІХС), гіпертонічній хворобі, СН, але питання підбору дози при різних патологічних станах досі вивчається. При низькій концентрації в плазмі крові L-аргінін сприяє покращенню ендотеліальної функції; при середньому рівні концентрації може чинити пряму вазодилатацію внаслідок стимуляції секреції інсуліну й гормона росту; високі рівні L-аргініну викликають неспецифічну вазодилатацію. Фармакокінетичні дослідження виявили, що пік концентрації аргініну в плазмі становив 50,0±13,4 мг/мл через 60 хв після прийому 10 г натще у хворих із базовою концентрацією аргініну 15,1±2,6 мг/мл. Автори встановили, що 20% аргініну поглинається після прийому пероральної дози 10 г, а з часом концентрація в плазмі знижувалася, але не поверталася до базового рівня навіть через 8 год [15]. В іншому дослідженні Боде-Богер і співавт. [16] повідомили, що після перорального прийому аргініну в дозі 6 г пікова концентрація спостерігалася через 90 хв і біодоступність становила 70%.
Безпека використання аргініну ретельно вивчена Shao та Hathcock [17]. Було виконано аналіз 38 клінічних випробувань із використанням аргініну в дорослих із 1990 по 2008 р., у тому числі в таких популяціях, як люди похилого віку й особи з патологією ниркової, легеневої та серцево-судинної систем. Пацієнти з певними шлунково-кишковими захворювання, злоякісними новоутвореннями, сильними опіками та травмами були виключені. Оцінювали небажані ефекти впливу на печінку й функції нирок. Автори виявили відсутність будь-якої моделі побічних ефектів,
що стосується використання аргініну, й тому література свідчить про високий рівень його безпечності [18]. Найбільше на сьогодні дослідження, що включало 792 пацієнти з гострим інфарктом міокарда, котрі приймали аргінін у дозі 9 г/добу порівняно з плацебо протягом 30 діб, не виявило побічних явищ [19].
Питання дози та тривалості застосування аргініну нині потребують подальшого вивчення. За результатами досліджень, добова доза аргініну коливається від 3 до 42 г [17], а допустима максимальна доза перорального аргініну для його максимального всмоктування також широко відрізняється, ймовірно, внаслідок використання різних лікарських форм (капсула, розчин), що впливає на переносимість і потребує проведення довгострокових випробувань [18]. У дослідженні авторів із залученням здорових добровольців показана добра переносимість внутрішньовенного та перорального аргініну в дозі менш як 30 г/добу [20].
Роль аргініну в патологічних процесах
Ожиріння, інсулінорезистентність, цукровий діабет 2 типу
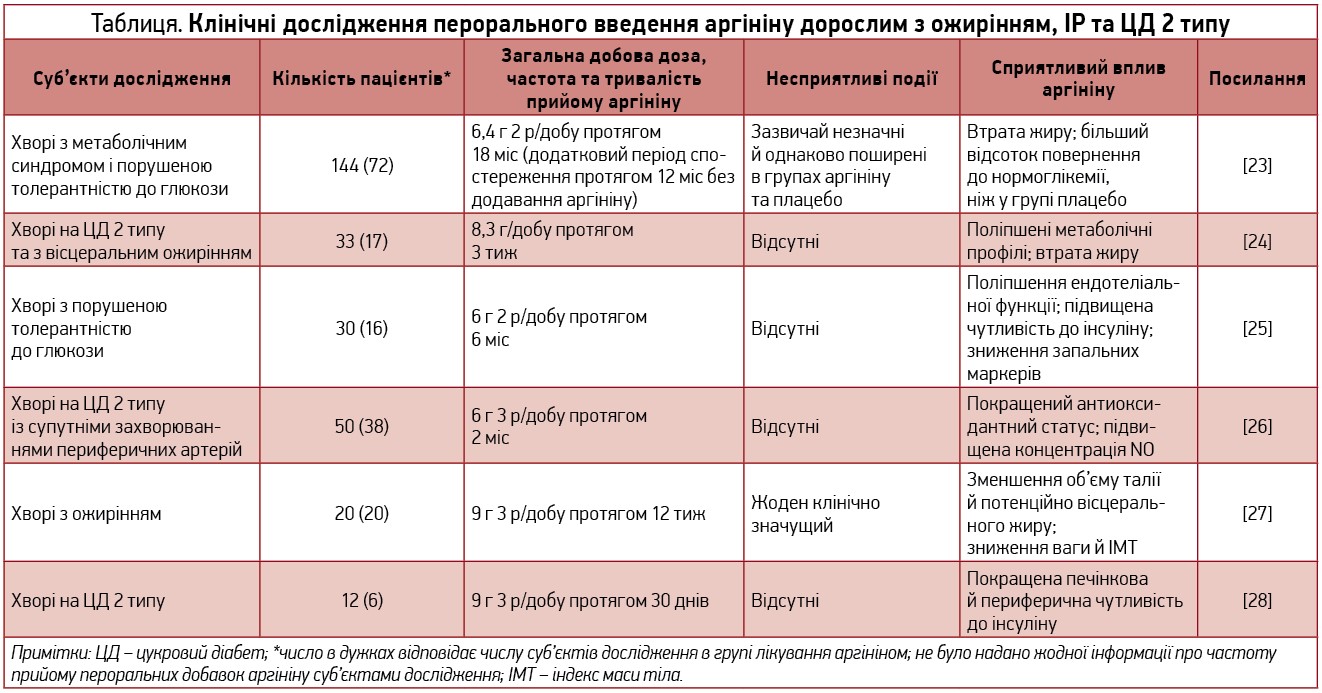
Встановлено, що ожиріння пов’язане зі зменшенням продукції NO, котре зумовлене порушенням біодоступності його субстрату – аргініну, а збільшення вмісту аргініну в ендотелії запобігає артеріальній гіпертензії (АГ) [4], яка часто поєднується з ожирінням [21]. Результати багатьох досліджень, у яких оцінювали використання аргініну в дорослих з ожирінням, дають змогу припустити, що аргінін може бути безпечним і ефективним терапевтичним засобом при ожирінні й позитивно впливає на корекцію метаболічних процесів [22], а саме на інсулінорезистентність – ІР (табл.) [18].
У дослідженні Monti та співавт. [29] оцінювали вплив довгострокових схем терапії L-аргініном на ризик розвитку ЦД 2 типу за участю 144 пацієнтів із порушеною толерантністю до глюкози (ІР; середній ІМТ – приблизно 30 кг/м2; середній вік – 57,7 року), котрі отримували низьку дозу аргініну (6,4 г/добу) чи плацебо протягом 18 міс. Після того як лікування було припинено, хворі спостерігалися ще протягом 12 міс. Під час 18-місячної фази лікування відбулися значні зміни, включаючи збільшення концентрації аргініну в плазмі натще в групі, що одержувала аргінін, порівняно з плацебо (50,0±11,3 проти 3,6±16,6 ммоль/л), більш значне зниження маси жиру й більший відсоток хворих, які повернулися до нормоглікемії в групі, що одержувала аргінін (42,4 проти 22,1% у групах аргініну та плацебо відповідно), хоча абсолютна втрата ваги чи показники метаболізму глюкози були однаковими в обох групах. Наприкінці розширеного періоду тільки 27,2% хворих з ІР, яких лікували аргініном, прогресували до ЦД 2 типу порівняно з 47,1% у групі плацебо.
Lucotti та співавт. [24] провели рандомізоване контрольоване дослідження в 33 здорових (середній ІМТ – 39,1 кг/м2) італійських пацієнтів із ЦД 2 типу, котрі отримували аргінін (8,3 г/добу) чи плацебо протягом 3 тиж. У групі з додаванням аргініну спостерігалося значне збільшення його концентрації в плазмі (з 81,8±12,3 мкмоль/л на початку дослідження до 131,8±16,6 мкмоль/л – наприкінці), тоді як концентрація в групі плацебо не змінилися, що демонструє явну ендотеліопротекторну перевагу аргініну [23].
В іншому дослідженні польського населення Jabіecka та співавт. [26] вивчали використання L-аргініну в 38 пацієнтів з атеросклеротичним захворюванням периферичних артерій нижніх кінцівок у поєднанні з ЦД 2 типу порівняно з 12 здоровими. Усіх лікували низькою дозою аргініну (6 г/добу) протягом 2 міс. Не було впливу на рівень глюкози натще чи концентрацію глікозильованого гемоглобіну, проте автори виявили значне збільшення концентрації NO та загального антиоксидантного статусу [30].
У дослідженні Hurt і співавт. описана ефективність аргініну в дозі 9 г/добу (по 3 г 3 р/добу) протягом 12 тиж у 20 жінок з ожирінням (ІМТ ≥30 та ≤40 кг/м2) віком ≥18 і ≤40 років. 13 жінок, які завершили дослідження, показали значне зменшення об’єму талії на 5,5% і зниження ваги на 2,9% [27].
Авторами проведено метааналіз 3761 повідомлення з ретельним вивченням статей за участю 723 хворих, які приймали L-аргінін (219 пацієнтів з ІХС, 136 – із хворобою периферичних артерій, 30 – із СН, 38 – зі стенокардією та 20 – з атеросклерозом). Зафіксоване покращення ЕЗВД, значне зниження АТ, позитивний вплив L-аргініну на продукцію NO в пацієнтів з ожирінням та/або ЦД 2 типу в поєднанні із серцево-судинними захворюваннями, що свідчить про можливість його використання як додаткової терапії в цих пацієнтів і необхідність подальшого вивчення його ефектів [31].
Артеріальна гіпертензія
Відомо, що NO, котрий продукується в ендотелії судин, відповідає за релаксацію гладких м’язів [11] і необхідний для зниження АТ. Будь-яке поліпшення функції ендотелію сприяє профілактиці серцево-судинних захворювань [32], а лікування L-аргініном сприяє помірному зниженню систолічного (САТ) і діастолічного АТ (ДАТ) [1].
За даними авторів, у пацієнтів з АГ L-аргінін ефективно знижував як САТ, так і ДАТ (від 2,2 до 5,4 мм рт. ст. і від 2,7 до 3,1 мм рт. ст. відповідно) [7]. Метааналіз 11 рандомізованих подвійних сліпих плацебо-контрольованих досліджень за участю 387 учасників із дозами аргініну в діапазоні від 4 до 24 г/добу протягом 2-24 тиж показав, що включення аргініну в схеми лікування сприяло зниженню САТ приблизно на 5 мм рт. ст. і ДАТ на 3 мм рт. ст. (P<0,001 для обох груп) [33]. У невеликому контрольованому дослідженні [34] у пацієнтів з АГ, рефрактерною до еналаприлу та гідрохлоротіазиду, було виявлено сприятливу відповідь у разі введення до схеми лікування L-аргініну перорально в дозі 6 г/добу.
У проспективному подвійному сліпому рандомізованому клінічному дослідженні було виявлено значне поліпшення ЕЗВД (з 1,7±3,4 до 5,9±5,4%; Р=0,008) у 18 пацієнтів з есенціальною гіпертензією на тлі прийому 6 г/добу L-аргініну. Перше дослідження гемодинамічних механізмів антигіпертензивного ефекту L-аргініну було проведено при його застосуванні в дозі 12 г/добу. У пацієнтів зменшився серцевий викид (на 0,4 л/хв), ДАТ (на 1,9 мм рт. ст.), рівень гомоцистеїну в плазмі (на 2,0 мкмоль/л), збільшився період напруження шлуночків (на 3,4 мс). В іншому дослідженні обстежено 13 пацієнтів з АГ і мікроваскулярною стенокардією до та після лікування L-аргініном (6 г/добу протягом 4 тиж). Також під впливом L-аргініну значно поліпшилися якість життя, функціональний клас (ФК) стенокардії, знизилися АТ, ЕЗВД передпліччя, значно збільшилася концентрація L-аргініну в плазмі.
За результатами нашого дослідження за участю 20 хворих на ревматоїдний артрит у поєднанні з АГ 1-2 ступеня, котрим у комплексну терапію включали L-аргінін у формі розчину для перорального застосування з режимом дозування 15 мл 2 р/добу (сумарна доза – 6 г/добу) протягом 4 тиж, у всіх хворих була досягнута нормалізація ендотеліальної функції за наявності її порушення в 95% хворих до початку лікування, досягнуто суттєве зменшення САТ і ДАТ (на 28,7 та 26,4% відповідно), зниження рівня адипонектину та покращення показників ІР [35].
L-аргінін та ІХС
Окислений холестерин ЛПНЩ підвищує експресію аргінази та знижує рівень eNOS в ендотеліоцитах, сприяючи зменшенню продукції NO, а при зменшенні вмісту NO в тканинах серця підвищується тонус коронарних судин і знижується коронарний кровоток. Такий ефект може бути пояснений здатністю NO знижувати чутливість скоротливих білків міокарда до іонів кальцію.
У дослідженні А. Palloshi та співавт. у 13 хворих зі стабільною стенокардією I-II ФК за умови лікування L-аргініном у дозі 2 г 3 р/добу протягом 4 тиж відзначалося зниження ФК стенокардії, САТ у спокої, поліпшення якості життя, підвищення концентрації L-аргініну та циклічного гуанозинмонофосфату (цГМФ) [28].
В іншому рандомізованому подвійному сліпому плацебо-контрольованому дослідженні з двома періодами лікування (аргінін/плацебо) тривалістю 2 тиж кожний узяли участь 36 хворих на стабільну стенокардію напруження II чи III ФК [36]. Час виконання навантаження збільшився на 16% у період лікування порівняно зі зменшенням на 4% під час періоду плацебо (Р=0,05). Також слід відзначити поліпшення якості життя, котру оцінювали за допомогою Сіетлського опитувальника (68±13 балів у групі лікування проти 63±21 балів у групі плацебо; Р=0,04).
Використання L-аргініну вивчено в декількох невеликих клінічних випробуваннях при лікуванні стабільної стенокардії напруження. У неконтрольованому пілотному дослідженні за участю чоловіків із тяжким перебігом (IV ФК) стенокардії введення пероральних добавок L-аргініну в дозі 9 г/добу протягом 3 міс як доповнення до стандартної терапії сприяло клінічному поліпшенню (до II ФК) у 7 з 10 пацієнтів. Цікаво, що в пацієнтів із клінічною відповіддю на L-аргінін зафіксовано зниження рівня маркерів клітинної адгезії та запальних цитокінів у сироватці крові, в тому числі інтерлейкіну 1 та 6. Рівні цих запальних маркерів не змінювалися в пацієнтів, які не мали клінічної відповіді. За даними літератури, L-аргінін у хворих із підтвердженою ІХС у дозі 21 г/добу протягом 3 днів сприяв значному покращенню ЕЗВД на відміну від групи плацебо [37].
У дослідженні W. H. Yin і співавт. у 31 пацієнта зі стабільною ІХС на тлі перорального прийому L-аргініну в дозі 10 г/добу протягом 4 тиж встановлено поліпшення ендотеліальной функції та зниження окислення [38]. Т. Lauer і співавт. (2008) показали збільшення мінімального діаметра просвіту судини в стенозованому сегменті з 0,98±0,06 до 1,14±0,07 мм (р<0,05) без впливу на інші сегменти в пацієнтів з ІХС у разі застосування інфузії 150 мкмоль/хв L-аргініну [39], а кровоток у післястенотичному сегменті збільшився на 24±3% [40].
Суперечливі дані отримані в дослідженні VINTAGE MI за участю 153 хворих, які перенесли гострий інфаркт міокарда з елевацією сегмента ST і приймали L-аргінін у дозі 3 г/добу 6 міс. Результати випробування показали відсутність зменшення жорсткості судинної стінки та поліпшення насосної функції серця. 8,6% хворих, які отримували L-аргінін, померли, й дослідження було призупинене. У ході аналізу причин смерті виявили, що 2 пацієнти померли від сепсису, 2 – знайдені вдома мертвими, 1 помер від повторного інфаркту міокарда, тобто негативний вплив аргініну доведено не було [41].
L-аргінін і СН
Вплив NO на серцево-судинну систему реалізується через його дію як на насосну функцію серця, так і на судинний тонус [42]. NO регулює реакцію кардіоміоцитів на адрено- та холінергічні стимули. Виявлено кореляцію рівня синтезу ендогенного NO та показників скоротливої функції міокарда лівого шлуночка. Показано, що NO поліпшує роботу лівого шлуночка на тлі зменшення споживання кисню як нормального, так й ішемізованого міокарда. При збільшенні концентрації NO проявляються негативні інотропний цГМФ-незалежний і хронотропний ефекти. Крім того, саме збільшення концентрації NO вважають однією з причин порушення скоротливої діяльності міокарда при інфаркті, кардіоміопатії та міокардитах.
За результатами досліджень [43], лікування L-аргініном у дозі 8 г/добу 4 тиж сприяло поліпшенню ЕЗВД, функції нирок (швидкості клубочкової фільтрації), натрійурезу та рівня ендотеліну плазми у хворих із хронічною застійною СН [12], покращувало фракцію викиду.
Показано, що у хворих на хронічну СН пероральний прийом L-аргініну в дозах між 5 та 13 г/добу протягом періоду до 6 тиж сприяв зниженню рівня ендотеліну‑1 у плазмі, поліпшенню показників АТ, загального функціонального стану [5], а також функції нирок порівняно з групою плацебо [44].
G. Watanabe та співавт. (2000) оцінили вплив перорального прийому L-аргініну в дозі 15 г/добу протягом 5 днів на ниркову гемодинаміку в рандомізованому подвійному сліпому перехресному дослідженні за участю 17 пацієнтів віком 56±12 років із хронічною застійною СН II-III ФК. Встановлено підвищення добової екскреції цГМФ із сечею з 0,8±0,5 до 1,4±1,1 мкмоль/добу (Р<0,01), кліренсу креатиніну зі 125±42 до 150±43 мл/хв (Р<0,05) і зниження рівня ендотеліну в плазмі крові з 3,1±0,8 до 2,5 пг/мл (Р<0,05). Відносне збільшення рівня екскреції натрію (47±12 проти 34±9% у групі плацебо; Р<0,05) і рівня гломерулярної фільтрації (44±31 проти 22±29; Р<0,05) також було більш значним після терапії L-аргініном [44].
В. Bednarz і співавт. (2004) встановили підвищення толерантності до фізичного навантаження у 21 пацієнта з хронічною застійною СН II-III ФК за NYHA після перорального прийому L-аргініну в дозі 9 г/добу [41].
За результатами нашого дослідження за участю 33 пацієнтів з ІХС і хронічною СН, які отримували як доповнення до основної терапії внутрішньовенно L-аргінін (Тівортін) у дозі 4,2 г / 100 мл протягом 7 діб із подальшим пероральним застосуванням у дозі 6 г (Тівортін аспартат) протягом 3 міс, виявлено значну позитивну регуляцію фактора росту ендотелію судин (VEGF), зниження активності матриксної металопротеїнази‑9, рівня циркулюючих рівнів ангіостатину та продуктів розпаду фібронектину. Тобто L-аргінін, впливаючи на поліпшення ангіогенної відповіді, сприяв перевагам з боку серцево-судинної системи в цієї групи хворих [45].
У малих клінічних випробуваннях також отримані переконливі докази на користь того, що L-аргінін може бути корисним для лікування СН [46].
Отже, за результатами досліджень, використання L-аргініну як додаткової терапії при серцево-судинній патології, а саме АГ, ІХС і СН, та у хворих з ожирінням, ЦД 2 типу й ІР мало позитивний вплив на перебіг захворювання та механізми розвитку за відсутності значущих небажаних побічних ефектів.
Нині обговорюється можливість подальшого дослідження з визначення диференціації використання L-аргініну з L-карнітином як додаткової терапії при серцево-судинній патології з метою позитивного впливу на патогенетичні ланки прогресування захворювань.
Висновок
Доцільність додаткового призначення L-аргініну до основної схеми лікування знайшло підтвердження при АГ, ІХС, СН, ЦД, ІР та відображено в рекомендаціях із парентеральної нутриціології (ESPEN Guidelines on Parenteral Nutrition: On Cardiology and Pneumology, 2009). Аналіз літератури свідчить, що L-аргінін продемонстрував свою безпечність у діапазоні верхньої межі 30 г/добу, хоча в більшості випробувань застосовувалася доза від 6 до 12 мг/добу.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 11 (456), червень 2019 р.