29 серпня, 2019
Пробіотики в практиці лікаря-інтерніста: фокус на практичні рекомендації WGO та ESPGHAN
За матеріалами науково-практичної конференції, 29 травня, м. Львів
Наприкінці травня у самобутньому яскравому Львові відбулася науково-практична конференція «Коморбідні стани в практиці лікаря-інтерніста. Сучасні проблеми панкреатології». Участь у заході взяли провідні профільні спеціалісти і практичні лікарі з багатьох областей нашої країни. Різноманіття тем наукових доповідей не залишило байдужим жодного учасника цієї конференції.
 Особливу увагу привернула доповідь професора кафедри терапії № 1 та медичної діагностики факультету післядипломної освіти Львівського національного медичного університету ім. Данила Галицького, доктора медичних наук Ольги Олександрівни Бондаренко на тему: «Мультифокус пробіотичної терапїї в практиці лікаря-інтерніста. Глобальні практичні рекомендації Всесвітньої гастроентерологічної організації «Пробіотики та пребіотики» (2017)».
Особливу увагу привернула доповідь професора кафедри терапії № 1 та медичної діагностики факультету післядипломної освіти Львівського національного медичного університету ім. Данила Галицького, доктора медичних наук Ольги Олександрівни Бондаренко на тему: «Мультифокус пробіотичної терапїї в практиці лікаря-інтерніста. Глобальні практичні рекомендації Всесвітньої гастроентерологічної організації «Пробіотики та пребіотики» (2017)».
Починаючи свій виступ, професор О. О. Бондаренко підкреслила, що мікроби з’явилися на земній кулі понад 4,5 млрд років тому. Відносно недавно, приблизно 1,5 млрд років тому, відбувся перехід від маленьких клітин прокаріот до більших за розмірами еукаріотичних клітин, подібних до клітин вищих тварин. Не дивно, що на поверхні та всередині людини також міститься значна кількість бактерій. Відомо, що в організмі людини присутні понад 500 видів мікроорганізмів, їх загальна маса становить 3-5 кг, приблизна кількість – 1014-1015 мікробних клітин, причому переважна більшість (майже 60%) знаходиться в шлунково-кишковому тракті, а саме в кишках (рис.).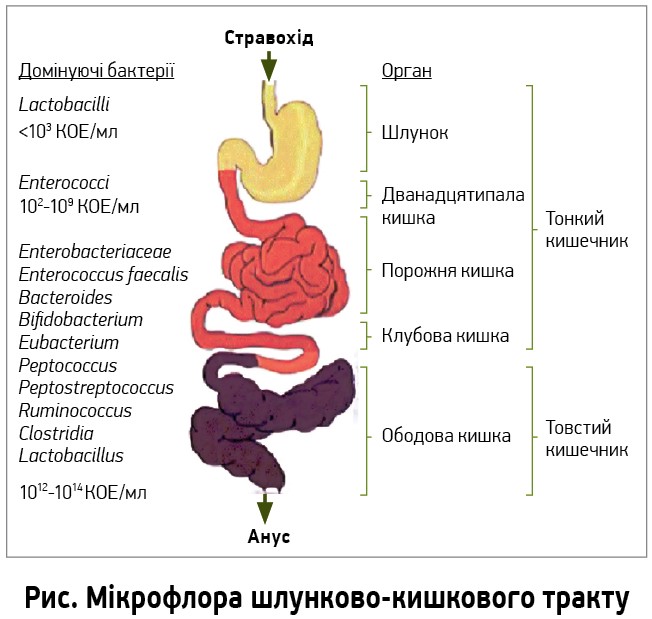
Встановлено, що кишкова мікробіота виконує багато різноманітних функцій. Найвідоміша з них – захисна – реалізується завдяки пристінковій мікрофлорі, що підвищує колонізаційну резистентність кишкової стінки, попереджає колонізацію кишки патогенною й умовно патогенною мікрофлорою. Завдяки ферментопродукуючій функції полегшуються гідроліз клітковини, білків, жирів, крохмалю, декон’югація жовчних кислот, а внаслідок синтетичної активності відбувається синтез вітаміну С, вітамінів групи В, амінокислот, холестерину, сечової кислоти, органічних кислот тощо. Кишкова мікрофлора бере участь у відновленні імунітету шляхом посилення синтезу імуноглобулінів, вона також сприяє дозріванню та функціонуванню імунокомпетентних органів. Завдяки функціонуванню мікробіоти інтенсифікуються всі види обміну речовин: білковий, жировий, вуглеводний; покращується травлення, засвоення їжі, інтелект; поліпшуються психоемоційні функції. Кишкова мікробіота посилює виведення токсинів, канцерогенів та алергенів, сприяє підвищенню активності імунної системи і в кінцевому підсумку – зростанню тривалості життя та покращенню його якості.
У деяких випадках склад і кількість кишкової мікрофлори змінюються або значно порушуються під впливом різноманітних факторів, що призводить до розвитку дисбіозу. Дисбіоз – це клініко-лабораторний синдром, пов’язаний зі змінами якісного та/або кількісного складу мікрофлори кишок із подальшим розвитком метаболічних та імунологічних порушень і можливим виникненням шлунково-кишкових розладів. Попри вагомі наслідки, початкові зміни мікробіому не мають значної специфічної симптоматики, тому виражені клінічні прояви з’являються протягом деякого часу.
Нині в клінічній практиці з метою відновлення складу та кількості мікробіоти застосовують пробіотики. Це живі мікроорганізми, які можуть позитивно впливати на стан здоров’я людини, нормалізувати склад і функції мікрофлори шлунково-кишкового тракту та здатні виявляти антагонізм проти патогенних й умовно патогенних мікробів. З‑поміж великої кількості пробіотиків у клінічній практиці найчастіше використовуються пробіотичні мікроорганізми, що належать до видів Lactobacillus та Bifidobacterium, а також дріжджі Saccharomyces boulardi та деякі види Escherichia coli.
Розрізняють декілька механізмів дії пробіотиків, їх можна класифікувати як імунологічні та неімунологічні. До імунологічних ефектів відносять активацію локальних макрофагів, зростання презентації антигена В‑лімфоцитами, локальну/системну продукцію секреторного імуноглобуліну А, модуляцію цитокінового профілю, появу толерантності до харчових антигенів. Великого значення надають неімунологічним ефектам. Доведено, що пробіотики сприяють травленню та конкурують за поживні речовини з патогенами, змінюють рівень місцевого рН для створення несприятливого навколишнього середовища для патогенів. Пробіотики виробляють бактеріоцини для пригнічення патогенів і здатні знищувати супероксидні радикали, стимулювати епітеліальну продукцію муцину та підсилювати бар’єрну функцію кишечнику. Встановлено, що пробіотики конкурують з патогенами за адгезію та модифікують бактеріальні токсини.
На сьогодні доведено, що застосування пробіотиків дозволяє запобігти розвитку колоректального раку, ці препарати використовуються в лікуванні та профілактиці діареї, в ерадикації Helicobacter pylori. Пробіотикам відводиться значна роль у профілактиці та лікуванні печінкової енцефалопатії, їх призначають за необхідності зміцнити імунну відповідь. Прийом пробіотиків дозволяє покращити стан пацієнтів із запальними захворюваннями кишечнику, синдромом подразненого кишечнику, некротичним ентероколітом, неалкогольною жировою хворобою печінки. Пробіотичні препарати значно покращують стан немовлят, які страждають від кольок, дорослих і маленьких пацієнтів із порушенням всмоктування лактози; пробіотики також застосовують із метою профілактики системних інфекцій.
Доповідач наголосила, що нині пробіотики являють собою велику групу, до складу якої входять лікарські засоби, біологічно активні добавки, харчові продукти: загалом в Україні зареєстровано понад 100 препаратів і продуктів, різноманітних за складом, якістю та кількістю пробіотичних мікроорганізмів. Обрати безпечний та ефективний препарат серед такої великої кількості засобів дуже складно. Тому вибір лікаря має базуватися на даних доказової медицини, які є вірним орієнтиром для вибору пробіотика. Варто послуговуватися спеціальними практичними рекомендаціями, які сформульовані відповідно до наявних даних доказової медицини – метааналізів, рандомізованих контрольованих досліджень. Найвідомішими є настанови ESPGHAN (Європейське товариство дитячої гастроентерології, гепатології та нутриціології) та WGO (Всесвітня гастроентерологічна організація), опубліковані у 2014 р. та 2017 р. відповідно. Європейські експерти, представляючи практичні рекомендації «Пробіотики для профілактики антибіотик-асоційованої діареї», назвали декілька пробіотичних штамів, які можна застосовувати в педіатричній практиці, й умовно розподілили пробіотики на групи залежно від сили та якості доказової бази. До пробіотиків, котрим була надана позитивна сильна рекомендація, належать Saccharomyces boulardii та Lactobacillus GG. Зазначені пробіотики представники ESPGHAN рекомендують приймати в дозі 250-750 мг/добу та >1010 КУЕ/добу відповідно, зазвичай протягом 5-7 діб. Слабку, але також позитивну рекомендацію отримали L. reuteri DSM та L. acidophilius LB. З метою профілактики антибіотик-асоційованої діареї експерти ESPGHAN рекомендують приймати такі пробіотичні штами, як LGG та S. boulardii (рівень доказів I, клас рекомендації A). Крім цього, S. boulardii показані також для профілактики та лікування Clostridium difficile-асоційованої діареї. Фахівці ESPGHAN констатували: S. boulardii має найвищу позитивну рекомендацію для лікування гострого гастроентериту. Професор О. О. Бондаренко підкреслила, що в Україні штам S. boulardii І‑745 міститься в препараті Ентерол.
У практичних рекомендаціях WGO «Пробіотики та пребіотики», які широко застосовуються в міжнародній медичній практиці, вказується, що застосування пробіотичних штамів S. boulardii показане як в амбулаторних, так і в стаціонарних умовах з метою профілактики антибіотик-асоційованої діареї, а також для лікування гострої діареї та профілактики C. difficile-асоційованої діареї. Експерти WGO рекомендують проводити коад’ювантну терапію при ерадикації H. pylori саме за допомогою штаму S. boulardii І‑745, зареєстрованого в нашій країні під торговою назвою Ентерол.
Рекомендації щодо використання S. boulardii можна знайти в інших міжнародних настановах, наприклад у підготовленому Гарвардською робочою групою документі (Recommendations for Probiotic Use: update 2015) та Маастрихтському консенсусі (Management of Helicobacter pylori infection – the Maastricht V / Florence Consensus Report, 2016).
Отже, пробіотична терапія характеризується широкими можливостями в різних розділах медицини, що сприяє неухильно зростаючій частоті її застосування в клініці внутрішніх хвороб. Світовими експертами застосування S. boulardii І‑745 (препарату Ентерол) визнано безпечним і корисним як у педіатричній, так і в дорослій популяції. Ентерол застосовується з метою профілактики та лікування колітів і діареї, пов’язаних із прийомом антибіотиків (у таких випадках прийом пробіотика слід розпочинати з першого дня антибіотикотерапії), корекції дисбіозу та синдрому подразненого кишечнику (тривалість лікування має становити 10-14 діб), лікування гострої діареї (препарат приймають протягом 3-5 діб). Ентерол має декілька форм випуску (капсули, порошок для перорального застосування), що дозволяє поводити терапію в пацієнтів різного віку. Препарат слід приймати щодня натщесерце, запиваючи капсули водою або розчиняючи порошок у воді чи молоці; максимальна тривалість застосування – 30 діб.
Ентерол робить пробіотичну терапію ефективною та безпечною, доступною та приємною як для дітей, так і для дорослих, у тому числі для осіб похилого віку.
Підготувала Лада Матвєєва
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (458-459), липень 2019 р.


