30 серпня, 2019
Важные вопросы офтальмологии: возрастная макулярная дегенерация после чернобыльской катастрофы, оптическая ишемическая нейропатия, розацеа-кератит
23-24 мая Одесса гостеприимно встретила врачей-офтальмологов на традиционных Филатовских чтениях. Обширная научная программа включала важнейшие вопросы офтальмологии, в частности лечение диабетических поражений органа зрения, наиболее распространенные ошибки клиницистов, актуальные аспекты терапевтического и хирургического лечения глаукомы, тактику ведения больных с травмами и ожогами глаза, проблемы офтальмологии детского возраста. В данном обзоре представлено три выбранных доклада, посвященных разноплановым поражениям органа зрения.
 Ученые продолжают анализировать последствия воздействия радиационного загрязнения территорий и низкодозового облучения вследствие чернобыльской катастрофы на здоровье и будущее нашего населения. Вопросам взаимосвязи возрастной макулярной дегенерации (ВМД) с чернобыльской катастрофой и низкодозовым облучением, ее лечению и профилактике был посвящен доклад директора Института радиационной гигиены и эпидемиологии ГУ «ННЦ радиационной медицины НАМН Украины» (г. Киев), доктора медицинских наук, профессора Павла Андреевича Федирко.
Ученые продолжают анализировать последствия воздействия радиационного загрязнения территорий и низкодозового облучения вследствие чернобыльской катастрофы на здоровье и будущее нашего населения. Вопросам взаимосвязи возрастной макулярной дегенерации (ВМД) с чернобыльской катастрофой и низкодозовым облучением, ее лечению и профилактике был посвящен доклад директора Института радиационной гигиены и эпидемиологии ГУ «ННЦ радиационной медицины НАМН Украины» (г. Киев), доктора медицинских наук, профессора Павла Андреевича Федирко.
ВМД является основной причиной ухудшения центрального зрения у лиц старше 50 лет, однако частота данного нарушения возрастает и среди молодых лиц трудоспособного возраста. В соответствии с ранее проведенными профессором П.А. Федирко и его сотрудниками исследованиями, воздействие низких доз ионизирующей радиации может служить еще одним важным фактором риска прогрессирования ВМД. Так, изучение макулярной области у лиц, подвергавшихся длительному воздействию низких доз ионизирующей радиации, показало значительную распространенность ВМД и тенденцию к ее возрастанию.
Радиационное облучение ускоряет развитие ВМД, поскольку ионизация среды вызывает появление свободных радикалов и пероксидных соединений, ведет к нарушениям микроциркуляции, повреждению мембран клеток сетчатой оболочки и митохондриальной дисфункции. При этом нарушения могут возникать рано и являются достаточно стойкими.
Согласно последним научным данным, специальные комплексы – нутрицевтики для здоровья глаз могут блокировать вышеуказанные звенья патогенеза ВМД. Поэтому для своего исследования профессор избрал диетическую добавку-нутрицевтик Нутроф® Форте (Théa, Франция), которая содержит в своем составе лютеин (10 мг), зеаксантин (2 мг), аскорбиновую кислоту (60 мг), токоферол (10 мг), цинк (10 мг), селен (25 мкг), медь (500 мкг), ресвератрол (1 мг), витамин D (5 мг), рыбий жир с омега-3 жирными кислотами (330 мг). В 2018 году она заменила прежде существующую формулу Нутроф® Тотал: в состав был добавлен витамин D с учетом его важной роли в предупреждении патологии глаз и распространенности гиповитаминоза D в популяции.
В этом авторском исследовании профессора П. А. Федирко приняли участие 616 лиц, подвергшихся длительному воздействию ионизирующей радиации в малых дозах, с начальными проявлениями ВМД (работники в зоне Чернобыльской АЭС). Всем им по показаниям был назначен Нутроф® (1 р/сут на протяжении 3 мес 2 р/год). При повторном обследовании было установлено, что 241 пациент принимал лечение по рекомендованной схеме (группа 1), 193 участника по разным причинам не придерживались данных рекомендаций (группа 2), 182 были исключены из исследования. В первой группе после более чем 2 лет приема препарата Нутроф® у 54,3% пациентов отсутствовало прогрессирование патологических изменений в макулярной зоне, а у 38,5% пациентов отмечено даже уменьшение площади патологического поражения в сравнении с исходным уровнем. Субъективно улучшение зрения отметили 70,13% пациентов группы лечения, 29,87% сообщали о стабилизации остроты зрения. Объективно улучшение центрального зрения отмечалось у 56,49% участников группы 1, стабилизация или уменьшение площади поражения сетчатки – у 92,8%, улучшение состояния микроциркуляции – у 59,3%.
Таким образом, результаты длительного наблюдения за группой больных ВМД, подвергавшихся длительному воздействию низкодозового облучения и принимавших комплексную диетическую добавку на основе лютеина, зеаксантина, ресвератрола, витаминов и микроэлементов (Нутроф® Форте), в сравнении с группой контроля свидетельствуют о ее положительном влиянии на состояние пациентов с начальной стадией ВМД.
 Старший научный сотрудник отдела воспалительной патологии глаза и микрохирургического лечения их последствий ГУ «Институт глазных болезней и тканевой терапии им. В. П. Филатова НАМН Украины» (г. Одесса), доктор медицинских наук Наталья Валерьевна Коновалова представила аудитории важнейшие вопросы касательно ишемической оптической нейропатии (ИОН).
Старший научный сотрудник отдела воспалительной патологии глаза и микрохирургического лечения их последствий ГУ «Институт глазных болезней и тканевой терапии им. В. П. Филатова НАМН Украины» (г. Одесса), доктор медицинских наук Наталья Валерьевна Коновалова представила аудитории важнейшие вопросы касательно ишемической оптической нейропатии (ИОН).
Согласно определению, ИОН – это состояние гипоксического повреждения (инфаркт ишемического генеза) любой части зрительного нерва протяженностью от хиазмы до диска зрительного нерва (ДЗН). ИОН является одной из основных причин слепоты и серьезных нарушений зрения. В последнее время отмечается рост распространенности сосудистой патологии за счет лиц молодого (30-44 года) и среднего (45-59 лет) возраста. Относительно патогенеза, клинических особенностей и тактики ведения пациентов с ИОН существуют разногласия. Это объясняется тем, что ИОН – не одно заболевание, а спектр многих нарушений, каждое из которых характеризуется собственными этиологией, патогенезом, клинической картиной. ИОН подразделяется на переднюю и заднюю формы в соответствии с наличием или отсутствием набухания ДЗН. Передняя ИОН связана с нарушением кровообращения в задних коротких цилиарных артериях, а задняя – в сосудах юкстабульбарной и орбитальной части зрительного нерва.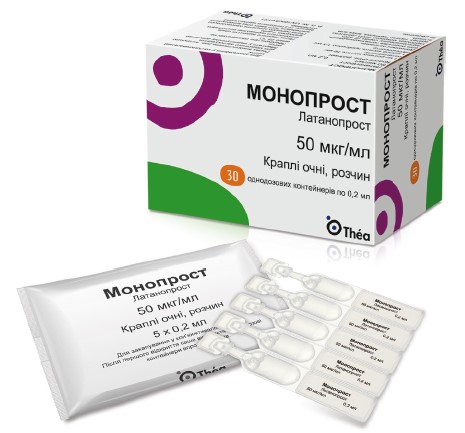
В соответствии с работами А. Н. Еременко, сосудистые оптические нейропатии можно также подразделить на острые (сосудистый секторальный папиллит, сосудистый папиллит, сосудистый ретробульбарный неврит, ишемический отек зрительного нерва) и хронические (хроническая сосудистая недостаточность зрительного нерва, простая склеротическая атрофия зрительного нерва, склеротическая атрофия зрительного нерва с псевдоглаукоматозной экскавацией).
Составляющими патогенеза ИОН выступают некоторые структурные особенности ДЗН, узкий склеральный канал; нарушение ауторегуляции кровотока в ДЗН вследствие атеросклероза или вазоспазма; ишемический инсульт или механические нарушения в аксонах нерва. Фоновыми заболеваниями, предрасполагающими к ИОН, являются гиперлипидемия, метаболический ацидоз, гиперкоагуляция, сахарный диабет, гипертоническая болезнь. Наиболее частыми местами для развития повреждений при ИОН выступают ламинарные и ретроламинарные области зрительного нерва.
 Хроническая ИОН составляет 62,8% от общего числа оптических нейропатий и в соответствии с выраженностью патологии делится на две группы: начальную и развитую. Начальная ИОН характеризуется минимальными, иногда обратимыми изменениями глазного дна и небольшими функциональными изменениями. Развитая ИОН включает простую склеротическую атрофию зрительного нерва и склеротическую атрофию зрительного нерва с псевдоглаукоматозной экскавацией.
Хроническая ИОН составляет 62,8% от общего числа оптических нейропатий и в соответствии с выраженностью патологии делится на две группы: начальную и развитую. Начальная ИОН характеризуется минимальными, иногда обратимыми изменениями глазного дна и небольшими функциональными изменениями. Развитая ИОН включает простую склеротическую атрофию зрительного нерва и склеротическую атрофию зрительного нерва с псевдоглаукоматозной экскавацией.
Одной из патогенетических основ ИОН выступают анатомические особенности области решетчатой пластинки: за последней диаметр центральных вены и артерии сетчатки меньше, чем в глазничной части. В норме решетчатая пластинка поддерживает сосуды, препятствуя их смещению и сдавливанию. Повышение внутриглазного давления вызывает деформацию решетчатой пластинки. В свою очередь, подобное вдавление с последующей деформацией сосудистого пучка вызывает дисбаланс внутриглазного и перфузионного давления со снижением последнего. Нарушения гемодинамики и перфузии сетчатки, выраженная ишемия выступают факторами риска возникновения ретинальной венозной окклюзии.
Итак, главный механизм передней ишемической нейропатии – понижение перфузионного давления в бассейне задних коротких артериальных сосудов. Поскольку ишемическое поражение сопровождается потерей нейронов и других клеток, в данных случаях необходима нейропротекция. Препарат Монопрост (Théa, Франция) представляет собой стабилизированную молекулу латанопроста и обладает нейропротекторными свойствами: как прямыми (поддерживает жизнеспособность и предотвращает апоптоз ганглионарных клеток, обладает прямым антиапоптозным действием посредством угнетения каспазы‑3), так и непрямыми (снижает внутриглазное давление, усиливает кровоток в области ДЗН).
Преимуществами Монопроста являются значительное снижение внутриглазного давления (до 36% от исходного уровня), эффект нейропротекции, отличная переносимость и приверженность к лечению, высокая безопасность применения, защита и увлажнение глазной поверхности, легкость контроля с помощью подсчета унидоз, стабильность при комнатной температуре. Немаловажно и то, что препарат не содержит консервантов. При переходе с консервантных средств на Монопрост повышается переносимость и комфортность лечения, улучшается качество жизни, у каждого второго пациента исчезает или уменьшается потребность в искусственных слезозаменителях, возрастает приверженность к лечению. Таким образом, Монопрост является гипотензивным и нейропротекторным средством с рядом важных преимуществ, которые обосновывают целесообразность его назначения при ИОН.
 Поражению поверхности глаза и особенностям лечения розацеа-кератитов посвятила свое выступление руководитель отдела патологии роговицы глаза ГУ «Институт глазных болезней и тканевой терапии им. В.П. Филатова НАМН Украины», член научного комитета Европейского общества заболеваний роговицы и поверхности глаза, член Немецкого офтальмологического общества, доктор медицинских наук, профессор Галина Ивановна Дрожжина.
Поражению поверхности глаза и особенностям лечения розацеа-кератитов посвятила свое выступление руководитель отдела патологии роговицы глаза ГУ «Институт глазных болезней и тканевой терапии им. В.П. Филатова НАМН Украины», член научного комитета Европейского общества заболеваний роговицы и поверхности глаза, член Немецкого офтальмологического общества, доктор медицинских наук, профессор Галина Ивановна Дрожжина.
Розацеа представляет собой хронический идиопатический дерматоз, при котором в патологический процесс вовлекается кожа лица, шеи, верхней части груди и спины. Распространенность данного дерматоза составляет 1-10%, преимущественно страдают люди со светлой кожей. Таким образом, розацеа не является редким заболеванием, однако часто остается недиагностированной. Генетическая предрасположенность отмечается у 30-40% больных розацеа. Наиболее часто розацеа развивается после 30 лет, а наиболее активный период развития изменений отмечается в 40-60 лет. Чаще болеют женщины, у которых наблюдаются обострения в период беременности, ранней менопаузы, климакса, однако у мужчин течение болезни является более тяжелым. Типичные проявления розацеа на коже лица включают эритему средней части лица (носа и щек), телеангиоэктазии (расширение мелких поверхностных сосудов лица), высыпания в виде папул и пустул, очаги гиперплазии сальных желез и соединительной ткани.
У 6-72% больных с розацеа отмечается поражение органа зрения. Вовлечение глаз в патологический процесс преимущественно является билатеральным, но асимметричным. Активность воспалительного процесса в глазу не всегда коррелирует с активностью воспалительного процесса на коже.
В патогенезе розацеа выделяют четыре ведущих механизма: сосудистые нарушения, дегенеративные изменения дермы, фотодинамическое поражение кожи и влияние микроорганизмов, таких как Demodex folliculorum, Demodex brevis, Helicobacter pylori.
Важнейшее звено патогенеза розацеа – нарушение тонуса поверхностных артериол кожи лица. У 15% пациентов с розацеа в коже формируются микроаневризмы, которые при увеличении количества провоцирующих факторов ведут к развитию телеангиоэктазий. Недостаточность кровообращения в лицевой вене приводит к замедлению перераспределения кровотока и венозному стазу в зоне оттока. В зоне оттока лицевой вены находится и конъюнктива, чем частично объясняется частое возникновение при розацеа конъюнктивитов.
Диагноз розацеа ставится дерматологом. Лабораторная диагностика включает соскоб с кожи лица для выявления клещей и исследование содержимого пустул (для исключения присоединения вторичной инфекции). Офтальмологическое обследование при розацеа должно включать оценку жалоб и субъективных ощущений с определением индекса заболевания поверхности глаза (OSDI), исследование состояния и выделительной функции мейбомиевых желез, определение величины слезопродукции (тест Ширмера І и ІІ), определение времени разрыва слезной пленки, окрашивание поверхности роговицы и конъюнктивы флуоресцеином, микробиологическое исследование содержимого конъюнктивальной полости, биомикроскопию переднего отдела глаза.
Розацеа-конъюнктивит подразделяется на диффузный (гиперемия и расширение сосудов тарзальной и бульбарной конъюнктивы) и узелковый. Для последнего характерно появление маленьких узелков сероватого цвета на бульбарной конъюнктиве вблизи лимба в межпальпебральном пространстве. Данные узелки часто напоминают фликтену, быстро появляются, подвергаются поверхностному изъязвлению и быстро исчезают. Более чем у 1/3 пациентов наблюдается снижение секреции водного компонента слезной жидкости. Качественные и количественные изменения последней ведут к развитию болезни сухого глаза (БСГ) смешанного типа.
Хроническое воспаление мейбомиевых желез, выступающее компонентом ассоциированных с розацеа поражений органа зрения, сопровождается гиперкератинизацией эпителия выводных протоков желез и снижением их секреции, что в дальнейшем ведет к нарушению стабильности и повышению осмолярности слезной пленки. Возникшие вследствие этого стимуляция продукции провоспалительных цитокинов и активация матриксных металлопротеиназ ведут к повреждению поверхности глаза.
Выделяют три степени тяжести глазных поражений при розацеа. Симптомами поражения 1 степени тяжести выступают умеренный зуд, сухость, ощущение песка в глазах, а объективными признаками – незначительное утолщение и покраснение краев век, телеангиоэктазии, умеренная гиперемия конъюнктивы. Для 2 степени характерны жжение в глазу и появление корочек по краю век, выраженная гиперемия конъюнктивы, иррегулярный край века с эритемой и отеком, появление халязионов или ячменей. При процессе 3 степени тяжести возникают боль, светобоязнь, снижение зрения, тяжелые изменения век, потеря ресниц, выраженный конъюнктивит, изменения роговицы с потенциальным снижением зрения, эписклерит, склерит, ирит (Wilkin J. et al., 2002).
Что касается роговицы (в 45-74% всех опосредованных розацеа поражений глаза), то в воспалительный процесс обычно вовлекаются ее нижние 2/3. Характерными признаками являются точечная кератопатия, иррегулярный эпителий, персистирующие дефекты эпителия, краевые инфильтраты роговицы, стерильные язвы с истончением стромы роговицы и формированием десцеметоцеле, неоваскуляризация роговицы, возможны перфорации роговицы.
У детей поражение глаза при розацеа часто предшествует кожным проявлениям и в 55% случаев остается недиагностированным. Классические характеристики опосредованного розацеа поражения глаза у детей включают хронический блефароконъюнктивит, рецидивирующие ячмени и халязионы, фликтенулезный кератоконъюнктивит, точечную кератопатию в нижней трети роговицы. Дифференциальную диагностику следует проводить с герпес-вирусным кератоконъюнктивитом, хламидийным конъюнктивитом, весенним катаром, недостаточностью стволовых клеток лимба.
В авторском исследовании профессора Г. И. Дрожжиной приняли участие 27 больных (52 глаза) с розацеа-кератитами (сосудистая форма – 14 пациентов, воспалительная – 8, фимозная – 5). Наиболее часто отмечались такие субъективные жалобы, как светобоязнь, ощущение инородного тела в глазу, жжение, снижение зрения. Что касается объективных признаков розацеа, то у всех больных были обнаружены дисфункция мейбомиевых желез (задний блефарит), эритема и телеангиоэктазии краев век, БСГ средней и тяжелой степени. У 48,2% участников были диагностированы халязионы. Следует отметить, что офтальмологические нарушения стали причиной направления к дерматологу и выявления розацеа в 74,1% случаев. Демодекоз кожи лица был выявлен у 25,9% пациентов, демодекоз век – в 81,5%.
Целями лечения розацеа являются уменьшение гиперемии и воспалительной инфильтрации кожи, регресс элементов кожных высыпаний, предотвращение деструкции роговицы и сохранение зрения. Обязательными компонентами лечения являются диета, устранение предрасполагающих и провоцирующих факторов, антибактериальная терапия, уход за кожей лица и терапевтическая гигиена век, фотопротекция, физиотерапия (криотерапия, электрофорез).
При лечении воспалительной (папуло-пустулезной) формы розацеа применяются деструктивные методики: электрокоагуляция, дермабразия, лазерная терапия.
Гигиена век является базовым этапом в лечении заболеваний век и поверхности глазного яблока, а также БСГ, обусловленной повышенным испарением слезной пленки. В данном исследовании гигиена век у пациентов проводилась с помощью теплых компрессов, салфеток Блефаклин® (Théa, Франция) и/или геля Теагель® (Théa, Франция) 2 р/сут. Блефаклин® обеспечиваeт очищение век, устранение корочек и чешуек, клеточного детрита; облегчение проникновения лекарственных веществ в ткани век; открытие протоков и нормализацию секреции мейбомиевых желез; улучшение структуры слезной пленки; санацию краев век, антисептическое и противовоспалительное действие; ликвидацию очага хронической инфекции. Важно, что в составе салфеток Блефаклин® не содержится ароматизаторов, парабенов и консервантов.
В свою очередь, гипоаллергенный гель Теагель® применяется для ежедневной гигиены век и ресниц при комплексной терапии чешуйчатого и себорейного блефаритов, гиперкератозов, аллергических реакций. Оригинальная формула Теагеля обладает следующими преимуществами:
- способствует удержанию геля на веках;
- содержит ингредиент полоксамер, который, образуя эмульсию, обеспечивает растворение и мягкое удаление слизи, чешуек, корочек и загрязнений с век и корней ресниц;
- сохраняет естественную гидратацию век; освежает, смягчает и успокаивает кожу век;
- не оставляет следов.
Кроме того, у участников исследования в зависимости от клинической картины розацеа-кератита применялись гели для век с метронидазолом и нитратом серебра, антисептики, антибиотики, мидриатики, ингибиторы коллагеназы, противовоспалительные препараты, антиоксиданты, эпителизирующие средства, кортикостероиды, слезозаменители, мягкие контактные линзы.
Также пациентам был назначен Теалоз® Дуо (Théa, Франция) – глазные капли, в состав которых входят трегалоза, являющаяся био- и осмопротектором, и гиалуронат натрия. Среди протекторных эффектов компонентов Теалоз® Дуо – защита клеточных белков, стабилизация липидов мембран, обновление клеточного материала путем индуцирования аутофагии, самовосстановление и снижение гибели клеток, а также снижение маркеров воспаления.
Профессор Г. И. Дрожжина подытожила, что лечение больных с поражением переднего отдела глаз при розацеа должно проводиться комплексно, с учетом лабораторных данных, рекомендаций дерматолога, состояния роговицы и поверхности глаза. В связи с поражением различных структур поверхности глаза кератопластика при розацеа-кератитах сопровождается высоким риском и неблагоприятным прогнозом. Лечение следует начинать как можно раньше, чтобы избежать осложнений и сохранить зрение.
Подготовила Лариса Стрильчук
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (458-459), липень 2019 р.


