6 вересня, 2019
Вивчення впливу антисептичного розчину Декасан® на процеси загоєння післяопераційної рани та приживлення алотрансплантату в експерименті
При наданні планової хірургічної допомоги застосування алотрансплантатів стало поширеною та науково-обґрунтованою практикою. У США щороку виконується понад 1 млн операцій із використанням різних видів сіток для пластики дефектів передньої черевної стінки [1]. На жаль, нам не вдалося знайти статистичних даних про щорічне використання сіток при виконанні хірургічних втручань із приводу гриж в Україні. Однак герніопластика алотрансплантатом є золотим стандартом при закритті грижових дефектів передньої черевної стінки у плановій хірургії.
Застосування сіток при герніопластиці багаторазово довело свою ефективність у порівнянні з методиками ушивання тканин та пластики власними тканинами в різних модифікаціях. Ушивання грижового дефекту без застосування алопластичного матеріалу демонструє високий рівень розвитку рецидиву грижі – рівень доказовості 1В. [2] При цьому International Endohernia Society (IEHS) у своїх рекомендаціях зазначає, що застосування сіток при герніопластиці суттєво знижує рівень розвитку рецидиву захворювання порівняно з ушиванням дефекту. Водночас спостерігається помірно вищий рівень місцевих ускладнень у післяопераційній рані при застосуванні сіток – рівень доказовості 1В. При цьому зазначається, що частота місцевих ускладнень у рані після герніопластики алотрансплантатом є дещо вищою у рандомізованих контрольованих дослідженнях, однак зіставною – у когортних [2].
Розвиток ускладнень у місці встановлення сітки є залежним від рівня потрапляння мікроорганізмів у рану та їх адгезії на поверхні імплантату [3]. З метою зменшення ризиків розвитку місцевих бактеріальних ускладнень у плановій хірургічній практиці застосовуються різні методи, у тому числі й уведення антибактеріальних препаратів широкого спектра дії у перед- або інтраопераційному періоді. Існує практика інтраопераційного змочування сітчастого імплантату у розчині антибіотика безпосередньо перед його встановленням та фіксацією у тканинах [3]. Проте дані щодо ефективності цих маніпуляцій із метою зниження ризику розвитку інфекційних ускладнень є обмеженими й демонструються в окремих ретроспективних рандомізованих контрольованих дослідженнях [4, 5].
Упродовж останніх років з’явилися публікації щодо застосування різних видів антисептиків для зрошування операційної рани перед встановленням сітчастого імплантату [5]. Ряд досліджень підтверджують можливість застосування 0,05% водного розчину хлоргексидину глюконату [4]. Однак цей антисептик демонструє певні ступені цитотоксичності навіть за низьких концентрацій [6]. Існують також дослідження щодо вивчення можливостей застосування карбоксиметилцелюлозного гелю, збагаченого хлоргексидином, але позитивні результати отримані лише в експерименті й потребують подальшого вивчення у клінічній практиці [7].
Пересторога щодо методики зрошення операційної рани розчинами антисептиків перед встановленням сітки, яка існує серед практичних хірургів, зумовлена також обмеженою інформацією про вплив антисептиків на процеси імплантації сітки у тканини. Особливо заслуговує на увагу можливість застосування антисептиків при використанні композитних сітчастих імплантатів.
Мета дослідження – вивчення впливу 0,02% розчину декаметоксину на загоєння післяопераційної рани та імплантацію композитної сітки в передню черевну стінку в експерименті.
Матеріали та методи
В експериментальному дослідженні проаналізовано результати моделювання інтраперитонеальної герніопластики за методикою ІРОМ (Intraperitoneal Onlay Mesh) у 12 кролів. Вибір експериментальної тварини (кроля) зумовлений можливістю моделювання інтраперитонеального розміщення композитної сітки розміром 4×4 см, що є технічно складним у малих гризунів. Всі тварини були карантинізовані й утримувались у стандартних умовах на базі віварію заводу ТОВ «Юрія-Фарм». У дослідженні були використані кролі обох статей породи «російська шиншила» вагою 2,1-2,9 кг.
Експериментальні тварини були рандомізовані на дві групи по 6 кролів. У дослідній групі всім кролям було виконано інтраабдомінальне встановлення композитної сітки PROCEED (Ethicon) розміром 4×4 см, із промиванням черевної порожнини та операційної рани розчином Декасан® (0,02% розчин декаметоксину у фізіологічному розчині NaCl) протягом 1-3 хв перед ушиванням операційної рани. У контрольній групі всім 6 кролям було виконано моделювання інтраабдомінальної герніопластики із встановленням композитної сітки PROCEED (Ethicon) розміром 4×4 см без застосування антисептиків для санації черевної порожнини та операційної рани.
Усі проведені оперативні втручання здійснювалися з дотриманням вимог Європейської конвенції про захист хребетних тварин, що використовуються для дослідних та інших наукових цілей (1986) та Науково-практичних рекомендацій щодо утримання лабораторних тварин та роботи з ними ДФЦ МОЗ України (2002).
В обох групах операції виконувалися під загальним знеболенням, із дотриманням вимог асептики та антисептики. У якості премедикації всім тваринам вводили 0,4 мл 2% розчину ксилазину гідрохлориду. З метою седації та аналгезії вводили 0,8 мл 0,1% розчину медетомідину гідрохлориду. Тварин на операційному столі розташовували спиною донизу, фіксуючи кожну лапу окремо. Шерсть на передній черевній стінці видаляли методом сухого гоління.
По завершенні операції в обох групах усім кролям вводили 0,8 мл 0,5% розчину атипамезолу гідрохлориду з метою усунення седації. Додатково всім тваринам вводили кетопрофен 3 мг/кг підшкірно з метою аналгезії. Антибіотикопрофілактику проводили шляхом внутрішньом’язового введення цефазоліну 1,0 г за 30 хв до оперативного втручання й повторно – через 12 годин. У подальшому всі тварини знаходилися в умовах віварію зі стандартним режимом перебування та харчування.
В обох групах тварин виводили з експерименту на 90-ту добу шляхом передозування препаратів для наркозу – внутрішньовенного введення 1,0 г тіопенталу натрію, розведеного у 5 мл 0,9% розчину натрію хлориду.
Після розтину черевної порожнини здійснювали макроскопічну оцінку вираженості злукового процесу. Для цього застосовували класифікацію, запропоновану Zühlke et al. (1990) для оцінки вираженості злукового процесу у черевній порожнині в експериментальних тварин [8]. Згідно з цією класифікацією, при макроскопічній оцінці вираженості злук розрізняють 4 ступеня:
І ступінь – фібринові напластування, дрібні ниткоподібні злуки або поодинокі злуки між органами, які можуть бути зруйновані тупими інструментами;
ІІ ступінь – ниткоподібні злуки, які можна зруйнувати тупими інструментами, але частково також наявність злук із початковою васкуляризацією, які можна зруйнувати тільки гострими інструментами;
ІІІ ступінь – добре васкуляризовані, щільні ниткоподібні злуки, які руйнуються лише гострими інструментами;
ІV ступінь – щільні, великі злуки між органами, які піддаються руйнуванню лише гострими інструментами і при хірургічному розділенні яких ушкодження органів майже неминуче.
Оцінювали також наявність зміщень, часткового або повного відриву імплантату від парієтальної очеревини.
Після розділення злук (частково тупим, частково гострим способом) виконували забір матеріалу для гістологічного дослідження та визначення міцності імплантації сітки у товщу передньої черевної стінки. Імплантат видаляли повністю, із додатковим захопленням прилеглих тканин м’язово-апоневротичного шару передньої черевної стінки. Фіксацію матеріалу здійснювали за допомогою 10% розчину формаліну у воді.
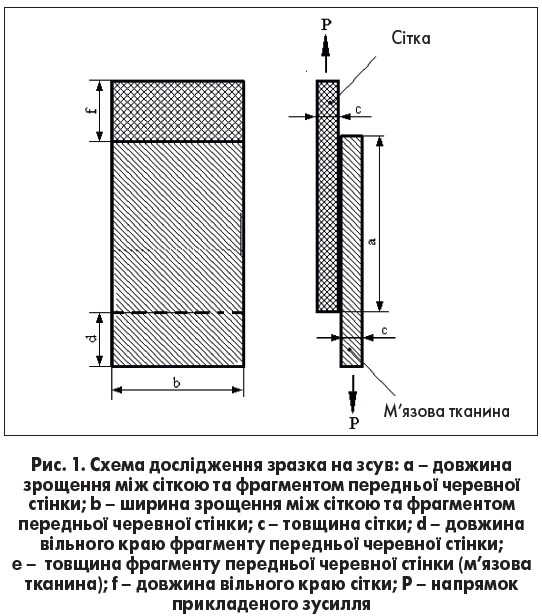
Мікроскопічну оцінку імплантації сітки в тканини передньої черевної стінки здійснювали шляхом гістологічного дослідження вилученого комплексу «передня черевна стінка – імплантат». Оцінку міцності фіксації сітки до передньої черевної стінки кроля проводили в Інституті проблем міцності ім. Г.С. Писаренка НАН України. Визначали максимальні напруження зсуву в момент руйнування зразка для комбінації «передня черевна стінка – імплантат». Напруження зсуву позначали τ* = Р/А, де А – прикладене зусилля, А – площа контакту сітки і фрагменту м’язової тканини передньої черевної стінки, А = a × b (рис. 1).
Механічні випробування міцності проводили на машині РМ‑05 з електромеханічним приводом.
Результати та їх обговорення
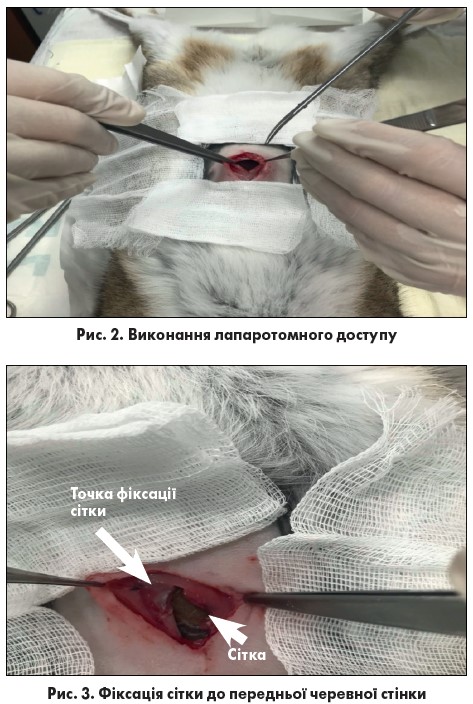
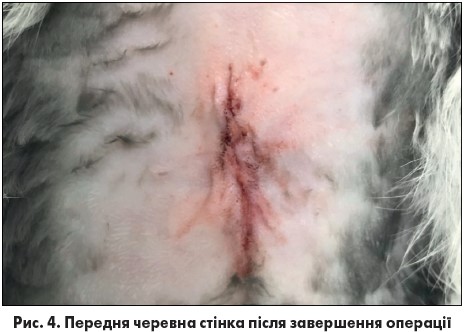
В обох групах операцію розпочинали шляхом виконання лапаротомії через повздовжній розріз шкіри по серединній лінії довжиною до 4 см (рис. 2). Наступним етапом у дослідній групі виконували введення 10 мл 0,02% розчину декаметоксину у черевну порожнину. Далі інтраабдомінально вводили композитну сітку розміром 4×4 см. Це легка поліпропіленова сітка, інкапсульована у розчин полі-п-діоксанону (PDS II). З одного боку вона вкрита окисленою регенерованою целюлозою, яким її розміщували всередину для контакту з вісцеральною очеревиною. Сітку фіксували окремими вузловими швами трансапоневротично до парієтальної очеревини (рис. 3). Після цього операційну рану промивали 10 мл 0,02% розчину декаметоксину. Виконували відновлення цілісності передньої черевної стінки пошарово, шляхом накладання безперервного шва на апоневроз прямого м’яза живота та на шкіру (рис. 4). У контрольній групі промивання черевної порожнини та операційної рани не здійснювали. Оперативне втручання виконували за аналогічною методикою, однак без застосування 0,02% розчину декаметоксину та будь-якого іншого антисептика. По закінченні оперативного втручання на рану накладали асептичну пов’язку, вдягали захисну попону. В обох групах за період спостереження ознак нагноєння післяопераційної рани не виявлено.
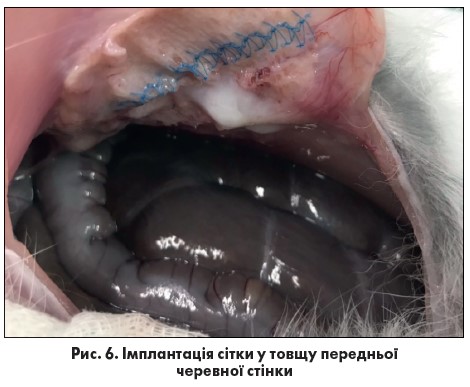
На 90-ту добу тварин обох груп виводили з експерименту. В обох групах зміщення або повного відриву імплантату від парієтальної очеревини не спостерігалося. У дослідній групі в одному випадку спостерігалася зона часткового відриву імплантату від парієтальної очеревини (рис. 5). Це може бути пов’язано з обмеженою кількістю накладених швів та відсутністю можливості проведення фіксації за типом «подвійної корони» в експерименті. В усіх тварин контрольної групи та у 5 тварин дослідної групи спостерігалося макроскопічно повне зрощення імплантату з парієтальною очеревиною передньої черевної стінки (рис. 6).
У таблиці представлена порівняльна характеристика ступенів вираженості злукового процесу у черевній порожнині при макроскопічній оцінці в дослідній та контрольній групах відповідно до класифікації Zühlke et al. (1990).
У дослідній групі у першому випадку спостерігалися щільні злуки між сіткою та пасмом великого чепця – ІІІ ступінь (див. рис. 5). Однак, на нашу думку, це пов’язано з частковим відривом сітки від парієтальної очеревини в даному випадку та тривалою травматизацією вісцеральної очеревини вільним краєм сітки. Ми не вважаємо це результатом можливого впливу зрошення 0,02% розчину декаметоксину, оскільки злуки утворилися саме в зоні вільного краю сітки й були відсутні у місці її щільного зрощення з парієтальною очеревиною. Аналізуючи результати макроскопічної оцінки злукового процесу у черевній порожнині, вважаємо зіставними ступені його вираженості в дослідній та контрольній групах.
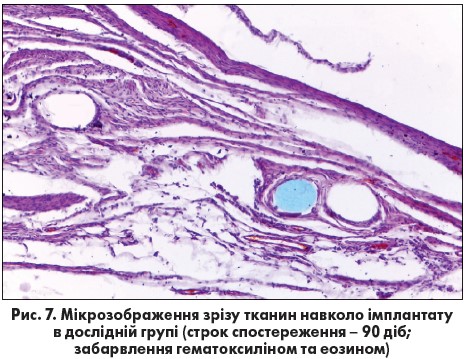
При гістологічному дослідженні препаратів комплексу «передня черевна стінка – імплантат» у дослідній групі спостерігались наступні зміни: мезотеліальна вистилка з боку черевної порожнини була відсутня на деяких ділянках у зоні наявних злук. Кожен філамент сітки оточений сполучнотканинною капсулою. Капсули переважно тонкі, проте навколо деяких філаментів відзначається формування товстих неоднорідних капсул. Імплантат проріс зрілою щільною сполучною тканиною. Сполучна тканина в ділянці розташування протеза переважно має прошарки, поблизу філаментів помірно інфільтрована лімфоцитами й нейтрофільними гранулоцитами. У складі деяких капсул відзначаються невеликі, переважно сплощені, гігантські клітини сторонніх тіл або ж поодинокі активовані макрофаги. У навколишніх тканинах виражених ознак патологічних змін не виявлено (рис. 7).
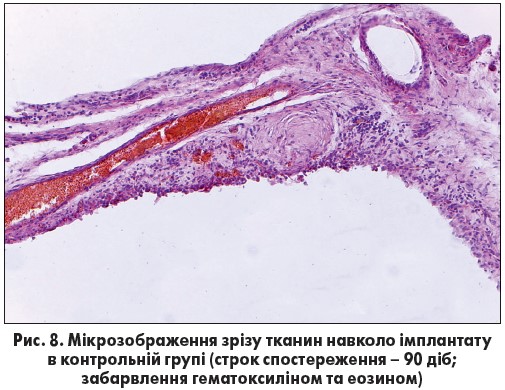
У дослідній групі в ділянці розташування сітчастого імплантату сформувався значний об’єм рубцевої тканини. Зона імплантації інфільтрована лімфоцитами, особливо навколо імплантату. Мезотеліальної вистилки не простежується. У ділянці імплантації відзначаються нечисленні розширені повнокровні кровоносні судини. На деяких ділянках відзначаються скупчення макрофагів зі збільшеним об’ємом цитоплазми. Наявні ознаки запалення в ділянці розташування імплантату (рис. 8).
Згідно з отриманими результатами гістологічних досліджень у дослідній групі при використанні 0,02% розчину декаметоксину спостерігається утворення неоперитонеуму (мезотеліальної вистилки) по переважній більшості поверхні імплантату та його щільна інвазія у товщу передньої черевної стінки. У контрольній групі також спостерігається оточення імплантату сполучною тканиною та його фіксація до передньої черевної стінки. Однак мезотеліальна вистилка не простежується, імплантат оточений рубцевою тканиною. Також у контрольній групі наявні ознаки запалення, яких не відмічається в дослідній групі при застосуванні 0,02% розчину декаметоксину.
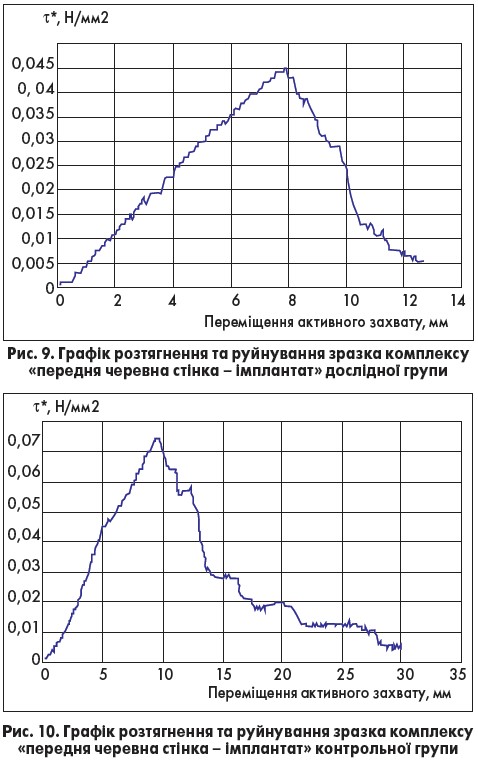
Середнє значення максимального напруження зсуву τ*max для комплексу «передня черевна стінка імплантат» у дослідній групі становило 0,062±0,06 МПа, у контрольній – 0,074±0,04 МПа. При аналізі результатів у контрольній групі визначаються достовірно вищі показники міцності зрощення сітки з передньою черевною стінкою, що може бути зумовлено більш вираженим утворенням рубцевої тканини на фоні запальних змін, описаних вище (рис. 9,10).
Висновки
При інтраабдомінальному розміщенні композитної поліпропіленової сітки промивання черевної порожнини та операційної рани розчином Декасан® перед її ушиванням дозволяє мінімізувати ризик інфікування ділянки хірургічного втручання. При цьому спостерігається повноцінна інтеграція сітки у товщу передньої черевної стінки з утворенням неоперитонеуму (в експерименті на кролях).
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 2 (36), травень 2019 р.