11 вересня, 2019
Токсическая кардиомиопатия, осложненная внутриполостным тромбозом и венозным тромбоэмболизмом
Токсическое воздействие различных лекарственных средств на миокард может проявляться в виде развития вторичной кардиомиопатии, следствием которой может быть дилатация камер сердца. В литературе представлено множество случаев поражения сердца после употребления алкоголя, психостимуляторов, наркотических веществ [2, 13]. В последние десятилетия отмечено частое (преимущественно среди молодежи) использование средств, содержащих амфетамин, не только как стимуляторов ЦНС, но и в составе препаратов, способствующих снижению веса (диэтилпропион, фенпропорекс) [4, 6, 10]. В связи с этим возрастает потребность в выявлении сердечно-сосудистых осложнений как побочных эффектов применения данных веществ. Употребление амфетаминосодержащих средств может вызывать развитие острого коронарного синдрома (ОКС), аритмии, дилатации камер сердца [5, 6, 11, 13]. Влияние амфетамина на миокард следует учитывать с точки зрения возможного риска возникновения токсической кардиомиопатии с дилатацией и дисфункцией левого желудочка (ЛЖ), а также тромбообразованием/тромбоэмболией у молодых пациентов с симптомами острой одышки, тахикардии и торакальной боли. Наиболее успешным методом выявления токсических осложнений является ранняя диагностика поражения сердца и сосудов с использованием различных методов визуализации: эхокардиографии (ЭхоКГ), магнитно-резонансной (МРТ), компьютерной томографии (КТ).
Пациент С., 33 года, поступил в отделение клинической фармакологии ННЦ «Институт кардиологии имени академика Н.Д. Стражеско» НАМН Украины г. Киева (далее – Институт кардиологии) с предварительным диагнозом «Дилатационная кардиомиопатия. Сердечная недостаточность (СН) со сниженной фракцией выброса (ФВ) ЛЖ. Тромб в верхушке ЛЖ. Правосторонний плевральный выпот. Асцит».
На момент поступления предъявлял жалобы на одышку при незначительной физической нагрузке, в покое, учащенное сердцебиение, периферические отеки.
Анамнез болезни. В течение 2 нед до госпитализации пациент проходил стационарное лечение по поводу двухсторонней нижнедолевой пневмонии. В связи с неэффективностью терапии (левофлоксацин, цефтриаксон, цефоперазон, мочегонные препараты, β-блокаторы) и прогрессированием СН направлен в консультативную поликлинику Института кардиологии.
Анамнез жизни. У пациента не было перенесенного ревматизма, заболеваний соединительной ткани, вирусных и бактериальных инфекций (в том числе вируса иммунодефицита человека, гепатитов, туберкулеза и т. д.), повышения артериального давления (АД), дислипидемии, сахарного диабета (СД) или других сердечно-сосудистых или цереброваскулярных заболеваний. Наследственность не отягощена. Курит более восьми лет, алкоголем не злоупотребляет. Со слов больного, в течение двух лет эпизодически принимал препараты, содержащие амфетамин.
 Объективно. Общее состояние средней тяжести. Нормостеник, бледность кожных покровов, акроцианоз. Деятельность сердца учащенная, аритмичная, экстрасистолия. АД – 100/60 мм рт. ст., частота сердечных сокращений (ЧСС) – 110 уд./мин, температура тела – 36,9 °С. В легких – ослабленное дыхание, притупление перкуторного звука в нижних отделах, преимущественно справа. Печень выступает на 4-5 см от края реберной дуги. Периферические отеки нижних конечностей (стоп, голеней).
Объективно. Общее состояние средней тяжести. Нормостеник, бледность кожных покровов, акроцианоз. Деятельность сердца учащенная, аритмичная, экстрасистолия. АД – 100/60 мм рт. ст., частота сердечных сокращений (ЧСС) – 110 уд./мин, температура тела – 36,9 °С. В легких – ослабленное дыхание, притупление перкуторного звука в нижних отделах, преимущественно справа. Печень выступает на 4-5 см от края реберной дуги. Периферические отеки нижних конечностей (стоп, голеней).
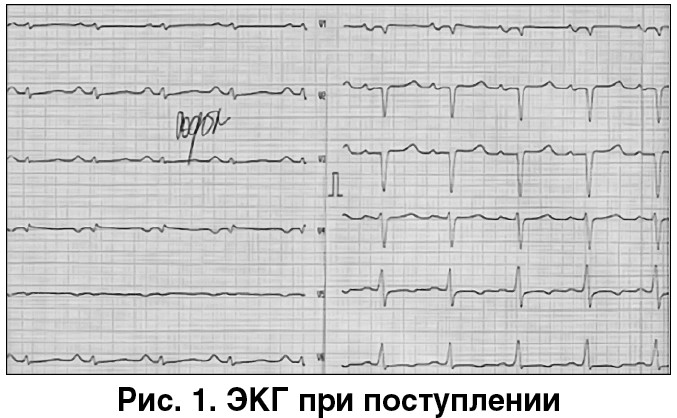
Электрокардиография (ЭКГ) (рис. 1). Синусовая тахикардия, низкий вольтаж в стандартных и усиленных от конечностей отведениях, малый прирост зубцов R в отведениях V1-V4, Р-pulmonale. В отведениях V5-V6 – депрессия сегмента ST до 1,0 мм, двухфазный зубец Т (–/+).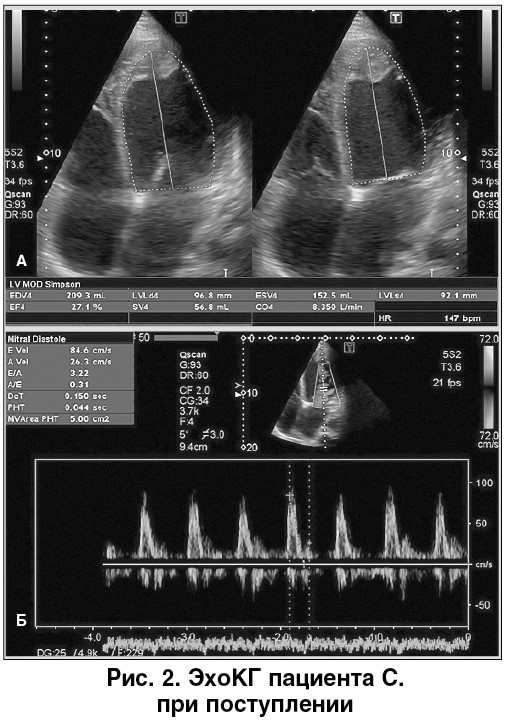
ЭхоКГ (рис. 2, 3). Дилатация камер сердца. Толщина задней стенки ЛЖ – 0,9 см, межжелудочковая перегородка (МЖП) – 1,0 см. Дилатация ЛЖ (конечно-диастолический объем – 209 мл, конечно-диастолический индекс – 120 мл/м2, конечно-систолический объем – 153 мл), диффузный гипокинез стенок ЛЖ, участки акинеза МЖП, верхушки ЛЖ. ФВ ЛЖ – 25-27%. В области верхушки ЛЖ выявлен тромб размером 25×17 мм. Наличие тромбов в полостях правого желудочка (ПЖ) и правого предсердия (ПП). Рестриктивный тип диастолической дисфункции ЛЖ (Е/А – 3,22). Дилатация обоих предсердий (площадь левого – 30 см2, правого – 27 см2), ПЖ. Нижняя полая вена расширена, коллабирует ≤25%, легочная артерия (ЛА) расширена, 27 мм. Гипертензия в ЛА, систолическое давление в ЛА – 55 мм рт. ст.
При рентгенологическом исследовании выявлены признаки кардиомегалии, правостороннего гидроторакса, нижнедолевой пневмонии (рис. 4).
Лабораторные исследования. Тропонин I <0,006 нг/мл. GeneXpert MTB/RIF: микобактерии туберкулеза – не выявлены. Вирус иммунодефицита человека 1/2 – не выявлен. Анти-HCV – не выявлены. С-реактивный протеин – 18,75 мг/мл. Ревматоидный фактор – негативный. Тест на наличие амфетамина – положительный.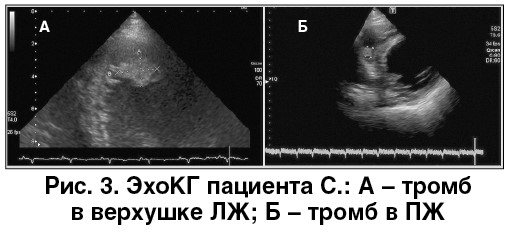
Пациенту назначена терапия: карведилол – 3,125 мг два раза в сутки, спиронолактон – 25 мг/сут, ивабрадин – 2,5 мг два раза в сутки, фуросемид – 40-80 мг в/в (инфузомат).
Антикоагулянтная терапия (АКТ). В данной ситуации, в соответствии с рекомендациями, препаратами выбора являются низкомолекулярные гепарины (НМГ) (пациенту был назначен эноксапарин 1 мг/кг массы тела два раза в сутки) с одновременным или 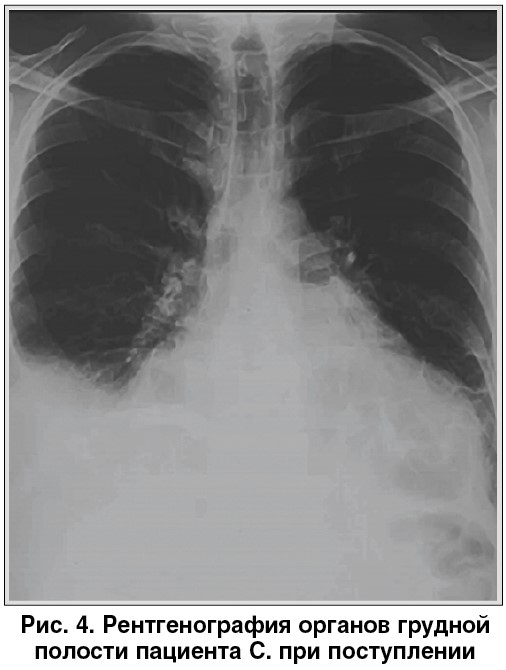 последующим переводом на прием пероральных антикоагулянтов (ПАК) (пациенту был назначен варфарин по 3 мг в комбинации с НМГ).
последующим переводом на прием пероральных антикоагулянтов (ПАК) (пациенту был назначен варфарин по 3 мг в комбинации с НМГ).
На 3-е сутки пребывания в стационаре состояние ухудшилось (рис. 5): внезапное усиление одышки, боль в грудной клетке, бледность, акроцианоз, частота дыхательных движений (ЧДД) – 24/мин, гипотония (АД – 80/60 мм рт. ст.), выраженная общая слабость, тахикардия, повышение температуры тела до 38,5 °С. Клиническая симптоматика была расценена как возможная тромбоэмболия легочной артерии (ТЭЛА). Вероятность ТЭЛА по шкалам Wells (1,5 балла), Женевского счета (3 балла), IMPROVE (0,4 балла) оценена как низкая [9, 14].
Однако наличие тромбов в правых отделах сердца у пациента могло послужить причиной развития ТЭЛА. Есть также данные, свидетельствующие о том, что тромбы в правых отделах сердца являются «транзитными», которые следует рассматривать как подтверждение венозной тромбоэмболии (ВТЭ), а прогноз преимущественно связан с гемодинамическим статусом, а не наличием тромбов [1]. Тромбы в правых камерах сердца могут быть визуализированы с помощью ЭхоКГ у ~4% пациентов с легочной эмболией [12]. По данным отдельных исследований, смертность у таких больных превышает 20% даже несмотря на проведение ургентного 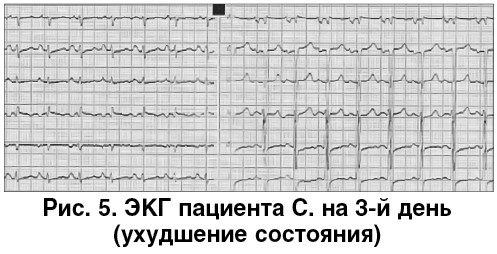 тромболизиса [8, 12]. В руководстве Европейского общества кардиологов (ESC) по ведению пациентов с ТЭЛА подчеркивается, что присутствие тромбов в правых отделах сердца следует рассматривать как потенциально опасное для жизни состояние у лиц с легочной эмболией [9].
тромболизиса [8, 12]. В руководстве Европейского общества кардиологов (ESC) по ведению пациентов с ТЭЛА подчеркивается, что присутствие тромбов в правых отделах сердца следует рассматривать как потенциально опасное для жизни состояние у лиц с легочной эмболией [9].
По ургентным показаниям пациенту была проведена мультиспиральная компьютерная томография (МСКТ) с контрастированием, которая является стандартом диагностики ТЭЛА [9, 14]. По данным КТ выявлены признаки двусторонней ТЭЛА, тромбоинфарктной пневмонии в базальных 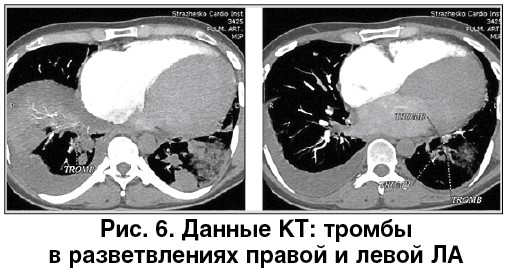 отделах, нижних долях обоих легких, тромботические массы в полостях сердца (рис. 6, 7).
отделах, нижних долях обоих легких, тромботические массы в полостях сердца (рис. 6, 7).
Согласно современной классификации, с учетом клинической картины заболевания (отсутствие гипотензии и шока: оценка по PESI – 83 балла, ІІ класс), данных инструментальных (ЭхоКГ, КТ) и лабораторных (отсутствие повышения уровня тропонина) методов исследования у пациента была диагностирована ТЭЛА промежуточно-низкого риска [9].
Больной был переведен в ОРИТ (руководитель – член-корреспондент НАМН Украины, д. мед. н., профессор А.Н. Пархоменко) c целью постоянного 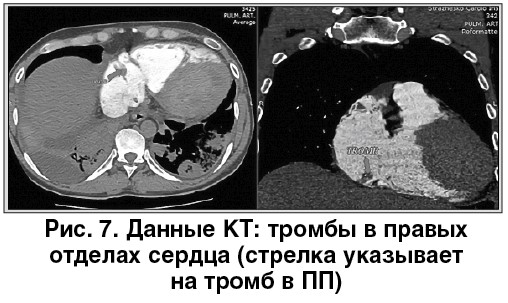 мониторного наблюдения за параметрами гемодинамики, антикоагулянтной и симптоматической терапии.
мониторного наблюдения за параметрами гемодинамики, антикоагулянтной и симптоматической терапии.
В соответствии с рекомендациями в данной ситуации проведение ТЛТ не показано. Основная патогенетическая терапия – антикоагулянты [7, 9].
Динамика лабораторных показателей на протяжении госпитального периода представлена на рисунках 8, 9. Особенностями изменений биохимических показателей были значительные повышения уровней АЛТ и АСТ в сравнении с исходными показателями, а также 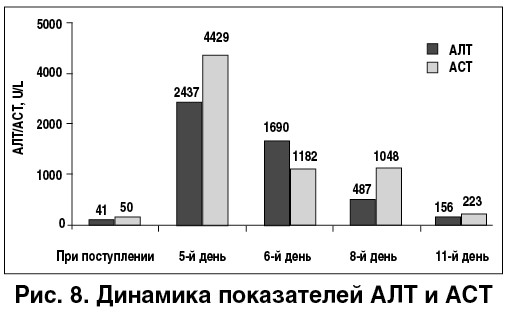 развитие коагулопатии, что можно расценивать как проявление печеночной недостаточности. После нормализации МНО пациенту был назначен варфарин в дозе 1,5 мг с последующим тщательным контролем лабораторных показателей.
развитие коагулопатии, что можно расценивать как проявление печеночной недостаточности. После нормализации МНО пациенту был назначен варфарин в дозе 1,5 мг с последующим тщательным контролем лабораторных показателей.
После стабилизации состояния проведена МРТ с целью верификации возможной причины поражения миокарда. По данным МРТ: отсутствовали признаки активного миокардита (фокусы измененного магнитно-резонансного сигнала с контурами высокой интенсивности относительно периферической зоны миокарда (Т2-взвешенные изображения), накапливающих контраст в позднюю фазу), перенесенного миокардита (фиброзные очаги в виде гиперинтенсивных участков различной формы, в том числе в фазу позднего усиления) [3].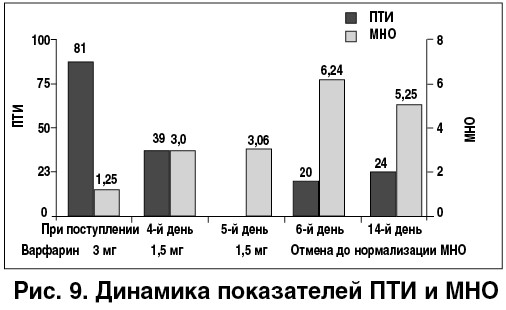
Единственным возможным фактором повреждения миокарда было токсическое влияние амфетаминосодержащих препаратов. В литературе описано несколько случаев дилатации сердца на фоне приема амфетамина, однако мультифокальный тромбоз и ТЭЛА встречаются преимущественно у пациентов при приеме кокаина [2, 4, 11].
На 15-е сутки пациент был выписан в удовлетворительном состоянии. ЭКГ при выписке: ритм синусовый, ЧСС – 75 уд./мин. Систолическая функция ЛЖ оставалась сниженной (ФВ ЛЖ – 27%) (рис. 10).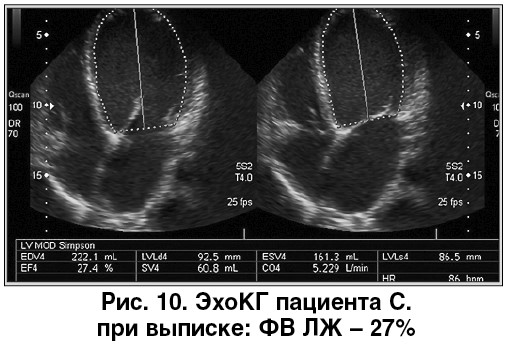
Комментарий
В статье описан клинический случай токсической кардиомиопатии с дилатацией камер сердца, множественным внутриполостным тромбообразованием, осложненной ТЭЛА.
Чем этот случай интересен с клинической точки зрения:
- трудность в оценке состояния и диагностике поражения сердца на ранних этапах, поскольку большинство из этих пациентов – молодого возраста, которые обращаются за медицинской помощью только при наличии выраженных симптомов;
- при сборе анамнеза не всегда удается выяснить прием амфетаминосодержащих препаратов;
- атипичное начало и течение заболевания (например, двухсторонние пневмонии, осложненные плевральным выпотом и кровохарканьем, резистентные к антибактериальной терапии, а также внезапное ухудшение состояния на фоне лечения);
- лабильность биохимических показателей (АСТ, АЛТ, ПТИ, МНО) на фоне лечения.
Представленный клинический случай демонстрирует успешность диагностики и консервативной тактики ведения пациента с токсической дилатационной кардиомиопатией, осложненной внутриполостным тромбообразованием и ВТЭ. Наличие тромбов в правых отделах сердца у пациента с токсической кардиомиопатией даже при низком риске развития ВТЭ ассоциируется с неблагоприятным прогнозом как ТЭЛА, так и внезапной смерти в раннем госпитальном периоде. Применение оптимальной АКТ в ранние сроки снижает риск рецидивов тромбообразования. Однако эта категория пациентов требует длительной терапии (мочегонные средства, титрование β-блокаторов, ингибиторов ангиотензинпревращающего фермента, до целевых доз, длительная АКТ) и мониторинга основных показателей (ФВ, ЧСС, АД, МНО, АСТ/АЛТ).
Заключение
Пациенты с токсической дилатационной кардиомиопатией, осложненной тромбообразованием, относятся к категории высокого риска:
- подвержены высокому риску внезапной сердечной смерти;
- исход заболевания зависит от тщательного контроля медикаментозного лечения и комплаенса (часто молодые пациенты самостоятельно прекращают лечение);
- высокая частота повторных эпизодов ВТЭ и эпизодов декомпенсации СН;
- систолическая функция миокарда ЛЖ восстанавливается очень медленно;
- необходимы регулярный мониторинг клинического состояния, функции сердца, лабораторных показателей, социальная адаптация.
Список литературы находится в редакции.
Спецвипуск «Клінічні випадки та сценарії у невідкладній кардіології», вересень 2019 р


