11 вересня, 2019
Острый коронарный синдром на фоне желудочных кровотечений при синдроме Маллори – Вейсса
Острый коронарный синдром (ОКС), как и острое желудочно-кишечное кровотечение (ЖКК), является жизнеугрожающим клиническим синдромом и требует ургентной медицинской помощи. Большую опасность представляет сочетание профузного ЖКК с ОКС с элевацией сегмента ST. По современным рекомендациям больным ОКС с элевацией сегмента ST [1] и лицам с профузными ЖКК показано проведение инвазивного вмешательства (коронароангиографии [КАГ] и эзофагогастродуоденоскопии [ЭФГДС]) в первые 2 ч от предполагаемого начала болезни. Наиболее распространенное внесердечное осложнение антитромботической терапии при ОКС с применением чрескожного коронарного вмешательства (ЧКВ) – клинически значимые геморрагические осложнения. В зарубежной литературе введен термин «внутрибольничная, или нозокомиальная, анемия, приобретенная в период госпитального лечения» (hospital-acquired anemia). По данным исследований, частота кровотечений у больных ОКС варьирует от 4 до 15%. В исследованиях PURSUIT и PARAGON (15 454 пациента с ОКС) частота тяжелых кровотечений по критериям GUSTO составляла 1,2%, а по шкале TIMI – 8,2% [3, 4]. Меньший риск осложнений отмечается при пункционном доступе через лучевую артерию по сравнению с таковым через бедренную [2].
Пациентка, 79 лет. Доставлена бригадой скорой медицинской помощи 12.02.2018 в 15:01, через 2 ч от начала болевого синдрома. Интенсивные боли – с 13:00. Вызов скорой медицинской помощи – в 14:22.
При поступлении в ОРИТ кардиологического профиля установлен синдромальный диагноз: ОКС с элевацией сегмента ST на электрокардиограмме (ЭКГ). Гипертоническая болезнь III стадии, 3-й степени, риск 4. Острая сердечная недостаточность (СН), Killip II. Хроническая СН стадии IIА.
Догоспитальная терапия: ацетилсалициловая кислота (АСК) – 650 мг, изосорбида динитрат – 2,5 мг, метоклопрамид – 10 мг, морфин – 10 мг, анальгин – 2000 мг.
При госпитализации – боли за грудиной средней интенсивности пекущего характера. Уровень артериального давления (АД) – 160/100 мм рт. ст., частота сердечных сокращений (ЧСС) – 78/мин, частота дыхательных дижений (ЧДД) – 16/мин. Масса тела – 95 кг. Рост – 163 см. Индекс массы тела – 36 кг/м2.
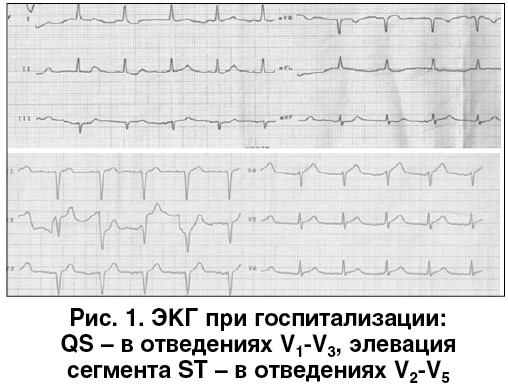 На ЭКГ: правильный синусовый ритм, горизонтальная электрическая ось сердца. QS – в отведениях V1-V3, элевация сегмента ST – в отведениях V2-V5 (рис. 1).
На ЭКГ: правильный синусовый ритм, горизонтальная электрическая ось сердца. QS – в отведениях V1-V3, элевация сегмента ST – в отведениях V2-V5 (рис. 1).
Анамнез. АГ с подъемами АД до 200/100 мм рт. ст. в течение пяти лет, стенокардия на протяжении двух лет. Лечилась нерегулярно и несистемно. Оперирована по поводу кист яичников в 2016 г. – экстирпация матки с придатками. Анамнестических данных о заболеваниях желудочно-кишечного тракта и кровотечениях нет.
Терапия: изосорбида динитрат в дозе 10 мг, клопидогрель по 300 мг, для купирования боли – фентанил по 0,1 мг.
√ В 15:15 – анализ крови: Hb – 137 г/л, Ht – 39%, эритроциты – 4,29×1012/л, цветовой показатель (ЦП) – 0,95, лейкоциты – 11,6×109/л, тромбоциты – 257×109/л, палочкоядерные – 6%, сегментоядерные – 76%, эозинофилы – 0%, лимфоциты – 13%, моноциты – 5%, скорость оседания эритроцитов (СОЭ) – 17 мм/ч. Группа крови: А (II) Rh (+), протромбиновый индекс (ПТИ) – 65,9%, фибриноген – 2,8 г/л, глюкоза – 8,8 ммоль/л, мочевина – 6,9 ммоль/л, креатинин – 0,079 ммоль/л, холестерин общий – 7,8 ммоль/л, триглицериды (ТГ) – 2,99 ммоль/л, креатинфосфокиназа-МВ (КФК-МВ) – 21 Ед/л.
При осмотре пациентки принято решение о проведении ЧКВ с учетом клинической картины заболевания, давности болевого синдрома, который сохранялся, наличия QS в отведениях V1-V3, элевации сегмента ST в отведениях V2-V5 на ЭКГ, несмотря на то что концентрация КФК-МВ не превышала нормальные значения.
√ В 15:35 – рвота с кровью. Реакция Грегерсена (++++). ЧКВ отложено в связи с открывшимся активным ЖКК. Начата гемостатическая терапия: установлен назогастральный зонд – эвакуировано до 650 мл крови. В желудок через зонд введено 5 г аминокапроновой кислоты. Пантопразол – 40 мг (в 15:35, 17:00, 20:00), этамзилат – 50 мг (в 15:40), в/в инфузия транексамовой кислоты – 1000 мг (в 16:00, 20:00), аминокапроновая кислота – 5 г (100 мл), ондансетрон – 4 мг.
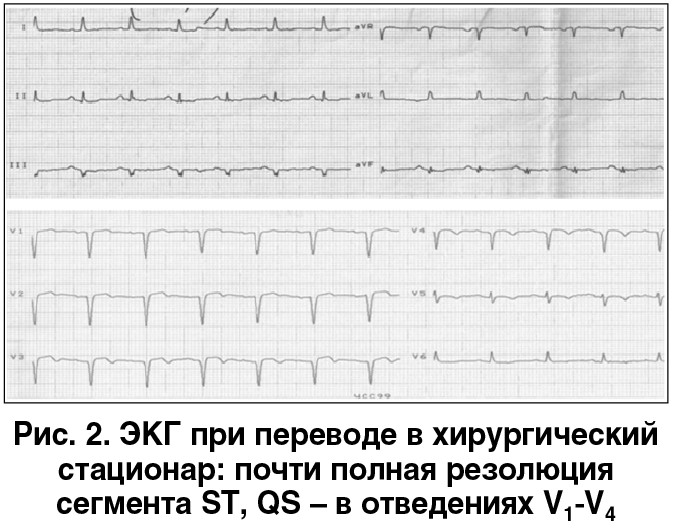 √ В 16:00 продолжается эвакуация геморрагического отделяемого через зонд.
√ В 16:00 продолжается эвакуация геморрагического отделяемого через зонд.
На ЭКГ уменьшилась элевация сегмента ST (рис. 2).
Консультация хирурга. Диагноз: ЖКК. Пупочная грыжа. Рекомендован перевод в хирургический стационар для дальнейшего лечения.
Консультация хирурга-гастроэнтеролога из стационара, куда планируется перевод больной. Диагноз: Острая язва желудка на фоне инфаркта миокарда (ИМ). Продолжение ЖКК. Рекомендовано:
- Фамотидин – 40 мг каждые 12 ч.
- Промывание зонда холодной аминокапроновой кислотой каждые 2 ч по 200 мл.
- Аминокапроновая кислота – 100 мл три раза.
- Транексамовая кислота – 100 мг три раза.
- Переливание плазмы (одногруппной).
- Раствор Рингера – 400 мл два раза.
- Коррекция электролитного баланса.
Учитывая сроки развития ИМ, эндоскопическое исследование на тот момент было противопоказано.
Рекомендовано лечение ИМ и дальнейшие мероприятия по остановке ЖКК в условиях кардиологического стационара. В 16:20 уровень Hb – 122 г/л, Ht – 35%, эритроциты – 3,88×1012/л. Выполняются рекомендации хирурга. В 21:30 – дальнейшее снижение Hb (109 г/л). Признаки активного кровотечения сохраняются.
√ В 22:44 с заместителем главного врача хирургического стационара выработана компромиссная тактика ведения больной и согласован перевод в гастрохирургическое отделение. При переводе АД – 120/70 мм рт. ст., ЧСС – 99/мин, ЧДД – 16/мин.
ЭФГДС в гастрохирургическом отделении 13.02.2018: пищевод – слизистая эрозирована; розетка кардии – линейный продольный разрыв слизистой 0,5 см, покрытый сгустком; в желудке – остатки кофейной гущи в большом количестве, эрозии по всей поверхности; в двенадцатиперстной кишке (ДПК) – язва 0,4 см в диаметре по медиальной стенке.
Заключение: эзофагит, синдром Маллори – Вейсса, эрозивный гастрит, язва луковицы ДПК.
Проведена электрокоагуляция язвенного дефекта.
В хирургическом отделении выполнены трансфузии эритроцитарной массы и замороженной плазмы. Гемостатическая терапия. Кровотечение остановлено.
Комментарий
В первую очередь следует прокомментировать назначение пациентке анальгина на этапе оказания неотложной медицинской помощи. Тактика обезболивания, которая была применена у пациентки с подозрением на ОКС, не соответствовала действующим рекомендациям (табл. 1). Назначение анальгина в столь высокой дозе – 2000 мг (при максимальной разовой 500 мг и максимальной суточной 1000 мг), безусловно, могло стать дополнительным фактором, увеличившим геморрагический риск, и потенцировать развитие кровотечения.
Основная задача как при ОКС, так и при ЖКК – экстренная госпитализация в стационар. Больные с клиникой ЖКК могут быть доставлены в хирургическое отделение, и при этом на ЭКГ выявляется ОКС, требующий ургентного вмешательства. Пациенты с ОКС могут быть госпитализированы в кардиологические отделения, и у них могут развиться признаки ЖКК уже на фоне введенных антикоагулянтов и принятых антитромбоцитарных препаратов, особенно в нагрузочных дозах.
Современные методики лечения ОКС и ЖКК требуют высокой квалификации специалистов для определения тяжести состояния пациента. При этом важно сразу определить, какой именно специалист должен первым приступить к оказанию неотложной помощи. Как правило, в особо тяжелых случаях это анестезиолог ОРИТ, и ему приходится в кратчайшие сроки самостоятельно или в лучшем случае совместно с кардиологами и хирургами принимать решение, в какую операционную отправлять больного – эндоскопическую или ангиографическую.
Оптимальным можно считать госпитализацию такого пациента в многопрофильный стационар, где есть возможность интервенционного вмешательства по поводу ОКС и эндоскопического вмешательства по поводу синдрома Маллори – Вейсса. Эта категория больных наиболее сложна для выбора врачебной тактики в отношении как лечения ОКС с применением инвазивных технологий, так и выполнения рекомендаций по антитромбоцитарной и антикоагулянтной терапии. При одновременном развитии ОКС и кровотечения факторы риска смерти взаимно усугубляются [5]. Поэтому желательно, взвесив все риски, выработать алгоритм действий в отношении конкретного больного с ОКС и активным ЖКК. Логичной представляется следующая последовательность действий:
- остановка кровотечения;
- интервенционное вмешательство на КА.
Согласно имеющимся рекомендациям, лечение ЖКК на фоне ОКС проводят в ОРИТ. Терапия заключается в назначении кислорода и гемотрансфузии до достижения показателей Ht 0,30. После стабилизации состояния на фоне мониторирования АД, ЭКГ и пульсоксиметрии больному выполняют эндоскопию с целью гемостаза. Во многих руководствах указано, что клинические рекомендации определяют современные позиции в диагностике и лечении больных с язвенными гастродуоденальными кровотечениями [6, 7]. Эндоскопический гемостаз – метод выбора, поскольку хирургическое вмешательство значительно повышает риск смерти [8]. ИМ и другая острая сердечная патология не являются абсолютными противопоказаниями для экстренного вмешательства: консилиум из трех специалистов может разрешить гастроскопическое вмешательство при инсульте, инфаркте и других тяжелых состояниях, если в этом есть необходимость для сохранения жизни пациента.
√ 19.02.2018 пациентка переведена из хирургического стационара в кардиологическую клинику с жалобами на выраженную слабость, периодические боли за грудиной жгучего характера и головокружение. На ЭКГ – графика переднеперегородочного, верхушечного и бокового ИМ (рис. 3).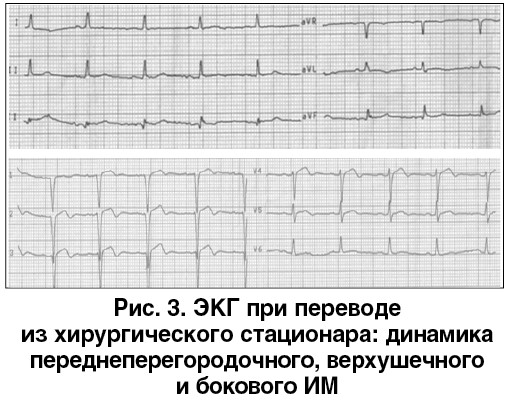
Анализ крови: Нb – 93 г/л, эритроциты – 3,2×1012/л, ЦП – 0,87, лейкоциты – 5,7×109/л, тромбоциты – 384×109/л, СОЭ – 54 мм/ч, палочкоядерные – 4%, сегментоядерные – 34%, эозинофилы – 2%, лимфоциты – 52%, моноциты – 8%, ПТИ – 88,2%, глюкоза – 4,9 ммоль/л, мочевина – 6,7 ммоль/л, креатинин – 0,081 ммоль/л, холестерин общий – 5,0 ммоль/л, ТГ – 1,48 ммоль/л.
Рентген органов грудной клетки: эмфизема легких.
УЗИ сердца: диаметр аорты – 33 мм, амплитуда открытия АК – 16 мм, кальциноз АК (++), скорость кровотока – 1,4 м/с, ЛП – 42 мм, левый желудочек (ЛЖ): конечно-диастолический размер – 59 мм, конечно-диастолический объем – 179 мл, конечно-систолический размер – 47 мм, конечно-систолический объем – 104 мл, аневризматическая деформация, ударный объем – 75 мл, минутный объем кровообращения – 7,0 л/м, фракция выброса (ФВ) – 42%, межжелудочковая перегородка – 9-13 мм, акинез, задняя стенка ЛЖ – 13 мм, нормокинез, амплитуда открытия митрального клапана – 27 мм, кальциноз (++), регургитация 2-й степени, правое предсердие – 15 мм.
Клинический диагноз от 21.02.2018: ИБС. Острый Q переднеперегородочный, верхушечный и боковой ИМ 12.02.2018. Гипертоническая болезнь III стадии, 3-й степени. Гипертензивное сердце. Аневризма ЛЖ в переднеперегородочном и верхушечном отделах. СН стадии IIА со снижением систолической функции (ФВ – 42%), III функциональный класс (ФК) по NYHA. Язвенная болезнь ДПК, эзофагит, эрозивный гастрит, ЖКК 12.02.2018, синдром Маллори – Вейсса. Вторичная постгеморрагическая гипохромная анемия. Варикозная болезнь нижних конечностей. Ожирение.
 Терапия: клопидогрель – 75 мг, карведилол – 6,25 мг дважды в сутки, пантопразол – 40 мг, препарат двухвалентного железа – 80/0,35 мг трижды в сутки, изосорбида динитрат (спрей) – 20 мг, торасемид – 40 мг.
Терапия: клопидогрель – 75 мг, карведилол – 6,25 мг дважды в сутки, пантопразол – 40 мг, препарат двухвалентного железа – 80/0,35 мг трижды в сутки, изосорбида динитрат (спрей) – 20 мг, торасемид – 40 мг.
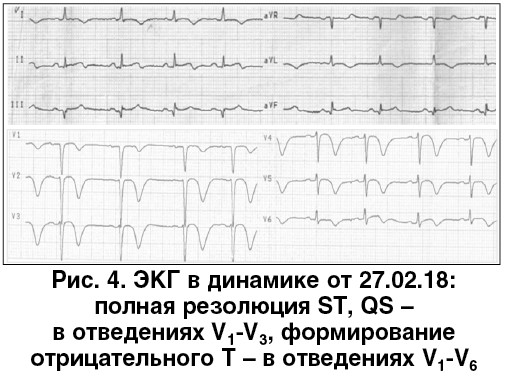
На фоне терапии на ЭКГ отмечалась полная резолюция сегмента ST (рис. 4).
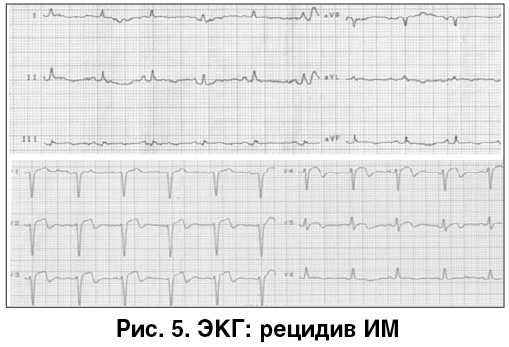
√ 28.02.2018 в 13:11 больная доставлена из кардиологического отделения в ОРИТ с жалобами на пекущие боли за грудиной, выраженную слабость, которые нарастают на протяжении 1 ч. На ЭКГ – графика ИМ (рис. 5). Принято решение о проведении ЧКВ с доступом через лучевую артерию.
Комментарий
 В украинской литературе и рекомендательных документах отсутствует описание четких алгоритмов действий при ОКС на фоне ЖКК. Алгоритм действий врача при кровотечениях, в том числе связанных с синдромом Маллори – Вейсса, можно найти в украинских клинических протоколах оказания медицинской помощи хирургическим больным с острыми ЖКК и тяжелым геморрагическим шоком [9, 10]. Тактику ведения больных при ОКС помогают также выработать обновленные действующие рекомендации ESC. Дозы антитромбоцитарных препаратов и антикоагулянтов указаны в таблице 2.
В украинской литературе и рекомендательных документах отсутствует описание четких алгоритмов действий при ОКС на фоне ЖКК. Алгоритм действий врача при кровотечениях, в том числе связанных с синдромом Маллори – Вейсса, можно найти в украинских клинических протоколах оказания медицинской помощи хирургическим больным с острыми ЖКК и тяжелым геморрагическим шоком [9, 10]. Тактику ведения больных при ОКС помогают также выработать обновленные действующие рекомендации ESC. Дозы антитромбоцитарных препаратов и антикоагулянтов указаны в таблице 2.
Следует отметить, что в реальной практике около половины пациентов получают неадекватную дозу антикоагулянтов, а во многих случаях терапия антикоагулянтами не проводится вообще. Вопросы вызывает и выбор тактики антитромбоцитарной терапии из-за высокого риска развития геморрагических осложнений. В этой ситуации выбор самого препарата и его индивидуальная дозировка имеют очень большое значение для прогноза и течения заболевания.
Пациентка была доставлена в катетеризационную лабораторию.
√ В 13:11 в/в введен фентанил в дозе 0,1 мг. Нагрузочная доза клопидогреля не применялась.
√ В 13:25 проведена КАГ лучевым доступом (рис. 6).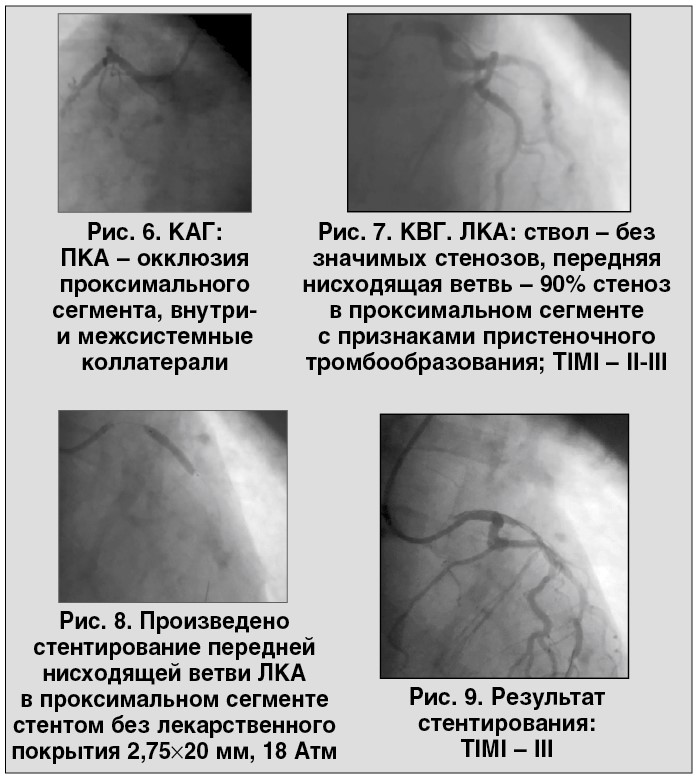
Больная возвращена из катетеризационной лаборатории в блок ОРИТ.
Терапия. В ОРИТ: изосорбида динитрат (спрей) в дозе 10 мг, нефракционированный гепарин (НФГ) по 5000 МЕ. В катетеризационной лаборатории: дополнительное введение НФГ в дозе 5000 МЕ, фамотидин по 20 мг.
Дальнейшая терапия в ОРИТ: инфузия НФГ по 1000 МЕ/ч под контролем активированного частичного тромбопластинового времени (АЧТВ). Через 4,5 ч – контроль АЧТВ (96 с): прекращена инфузия НФГ, затем начато подкожное введение эноксапарина в дозе 80 мг два раза в сутки до трех дней, клопидогрель в дозе 75 мг, инфузия пантопразола по 40 мг, затем 40 мг два раза в сутки, торасемид – 10 мг, эплеренон – 25 мг, карведилол – 12,5 мг/сут, ребамипид (простагландиновый стимулятор) – 100 мг три раза в сутки, препарат двухвалентного железа – 80/0,35 мг три раза в сутки, ондансетрон – 8 мг, аторвастатин – 40 мг, рамиприл – 5 мг, фентанил – 0,1 мг в 20:23 (в связи с болями в месте пункции на лучевой артерии).
√ 16.03.2018 больная выписана из стационара в стабильном состоянии, с общим режимом двигательной активности.
Лабораторные данные при выписке: Нb – 112 г/л, эритроциты – 3,65×1012/л, ЦП – 0,92, лейкоциты – 4,8×109/л, тромбоциты – 263×109/л, палочкоядерные – 2%, сегментоядерные – 63%, эозинофилы – 1%, лимфоциты – 30%, моноциты – 4%, СОЭ – 17 мм/ч.
Рекомендованное лечение при выписке: клопидогрель – 75 мг, эплеренон – 25 мг, карведилол – 12,5 мг/сут, рамиприл – 5 мг, пантопразол – 40 мг/сут, ребамипид – 100 мг три раза в сутки, препарат двухвалентного железа – 80/0,35 мг три раза в сутки, аторвастатин – 40 мг/сут.
Общее количество койко-дней, проведенных пациенткой в стационарах, – 32.
Комментарий
Следует подчеркнуть, что действующие руководства по ведению пациентов с ОКС и ЖКК носят исключительно рекомендательный характер и оставляют каждому лечащему врачу право на самостоятельное и окончательное решение в зависимости от конкретной клинической ситуации. Неоспоримыми положениями можно считать госпитализацию в многопрофильный стационар с возможностью проведения ЭФГДС и ЧКВ, рутинную регистрацию ЭКГ и определение группы крови и резус-принадлежности при поступлении всем больным. Необходимо, тщательно взвесив ишемический и геморрагический риски, индивидуально подобрать терапию пациенту с учетом эффективности и безопасности. Для хирургов бесспорным, а для кардиологов спорным остается вопрос применения транексамовой кислоты с гемостатической целью у больных с ОКС из-за ее свойства конкурентного ингибирования активатора плазминогена при исходно высоком ишемическом риске [16].
В представленном клиническом наблюдении мы выбрали индивидуальный вариант проведения антитромбоцитарной и антикоагулянтной терапии у пациентки с планируемым ЧКВ. По рекомендациям в случае ОКС с подъемом сегмента ST при проведении ЧКВ эноксапарин назначают в/в болюсно однократно. После первичного ЧКВ антикоагулянты обычно не применяются или используются в профилактических дозах (эноксапарин 4000 анти-Ха МЕ/сут подкожно) для предупреждения развития венозных тромбоэмболических осложнений у пациентов высокого риска (ESC, 2017).
В соответствии с инструкцией по применению эноксапарина при лечении ОКС с подъемом сегмента ST, у пациентов старше 75 лет дозировка препарата составляет 0,75 мг/кг каждые 12 ч. Рекомендуемая длительность лечения – 8 дней или до выписки из стационара, если период госпитализации составляет менее 8 дней.
Данный подход к проведению антикоагулянтной терапии (АКТ) является стандартным без учета наличия анемии и кровотечения.
В данном случае мы решили отступить от рекомендаций и выбрали тактику АКТ с учетом того, что у пациентки очень высокий геморрагический риск (недавнее кровотечение) и очень высокий ишемический риск (рецидив ИМ и отсутствие двойной антитромбоцитарной терапии [ДАТ] – монотерапия клопидогрелем). До, во время и после ЧКВ мы использовали НФГ с переводом на подкожное введение эноксапарина 80 мг два раза в сутки до трех дней для профилактики острого тромбоза стента и минимизации вероятности повторной геморрагии на фоне монотерапии клопидогрелем.
Следует отметить, что в обновленных рекомендациях ESC по лечению ОКС с подъемом сегмента ST (2017) уровень рекомендаций для эноксапарина повышен с IIb до IIa [1].
Клопидогрель был выбран с учетом развившегося ЖКК как препарат, применение которого сопряжено с более низким риском кровотечений. Клопидогрель – хорошо знакомый нам антиагрегант, который мы на протяжении многих лет применяем в самых разных клинических ситуациях. Эффекты клопидогреля тщательно изучены во многих клинических исследованиях, и их результаты, а также врачебная интуиция обусловили выбор этого препарата. Индивидуальным решением был также отказ от применения АСК в пользу монотерапии клопидогрелем.
Антитромбоцитарная монотерапия клопидогрелем в дозе 75 мг/сут на фоне пантопразола рекомендована больной при выписке, до получения результатов плановой контрольной ЭФГДС.
Данный клинический случай демонстрирует в очередной раз, что больные с сочетанной патологией требуют высокопрофессионального и вдумчивого подхода для выработки алгоритма действий.
Заключение
Развитие кровотечений связано с высоким уровнем смертности, а сами геморрагические осложнения являются независимым предиктором смерти больных ОКС. При возникновении кровотечений летальность значительно выше, чем при их отсутствии (18,6 против 5,1%). По данным исследования GUSTO, общий риск смерти в течение 30 дней после ОКС при развитии легкого кровотечения увеличивается на 1,6%, умеренного кровотечения – на 2,7%, а тяжелого – на 10,6%.
Через полгода после ОКС у пациентов, перенесших легкое кровотечение, общий риск смерти увеличивается на 1,4%, умеренное кровотечение – на 2,1%, тяжелое – на 7,5%. Мочегонные средства, вазопрессоры, фибринолитические средства, блокаторы гликопротеиновых IIb/IIIa-рецепторов тромбоцитов и НФГ являются препаратами, увеличивающими риск развития кровотечения даже при выборе тактики только фармакологического вмешательства, без проведения ЧКВ [11]. При проведении фибринолитической терапии частота значимых кровотечений увеличивается на 3,6%, при применении блокаторов гликопротеиновых IIb/IIIa-рецепторов тромбоцитов – на 6,5%, а при их совместном назначении – на 7,6% [12].
Таким образом, предотвращение возможного кровотечения необходимо для удержания баланса между эффективностью и безопасностью лечения ОКС. Для объективизации выбора тактики лечения с целью большей эффективности терапии и безопасности пациентов в практике используются шкалы ишемического и геморрагического рисков [4, 5].
Искусство проведения антикоагулянтной и антитромбоцитарной терапии у лиц с ОКС и ЖКК заключается не в том, чтобы отменить, а в том, чтобы продолжить под прикрытием ингибиторов протонной помпы сбалансированную оптимальную медикаментозную терапию, направленную на уменьшение ишемического риска пациента, не спровоцировав возобновление геморрагии.
Надеемся, что представленный клинический случай поможет врачам в их повседневной практике.
Список литературы находится в редакции.
Спецвипуск «Клінічні випадки та сценарії у невідкладній кардіології», вересень 2019 р




