30 травня, 2016
Современные взгляды на диагностику и лечение холестатических заболеваний печени
По материалам рекомендаций EASL, ACG
Продолжение. Начало в № 6, 7.
Прогрессирующий семейный внутрипеченочный холестаз
Термин «прогрессирующий семейный внутрипеченочный холестаз» (ПСВХ) объединяет 3 достаточно редких наследственных заболевания, которые могут манифестировать сразу после рождения или в молодом возрасте и быстро прогрессировать до терминальных стадий. Развитие каждого из ПСВХ обусловлено генетически детерминированным нарушением структуры канальцевой мембраны гепатоцита.
Наиболее изученным является ПСВХ 1 типа (болезнь Байлера). В основе этого заболевания лежит генетический дефект, вызванный мутацией гена АТР8В1, кодирующего белок FIC1 на хромосоме 18, ответственный за транспорт аминофосфолипидов через мембрану гепатоцитов. Дефицит АТР8В1 приводит к нарушению билиарной секреции первичных желчных кислот. Заболевание манифестирует очень рано – в неонатальном периоде появляется интенсивный кожный зуд, сопровождающийся патологическими изменениями печеночных проб. Наиболее распространенными внепеченочными проявлениями ПСВХ 1 типа являются диарея, панкреатит, отставание в физическом развитии, дефекты слуха. Эксперты EASL отмечают, что типичными лабораторными характеристиками болезни Байлера можно считать повышение сывороточных концентраций трансаминаз, билирубина и желчных кислот на фоне низкого уровня γ-ГТП. Прогноз неблагоприятный – большинство пациентов достигают терминальной стадии заболевания уже в первые десять лет жизни.
ПСВХ 2 типа (синдром Байлера) обусловлен мутацией гена АВСВ11, расположенного на хромосоме 2 и кодирующего белок BSEP, который осуществляет транспорт солей желчных кислот через каналикулярную мембрану. Первые симптомы ПСВХ 2 типа появляются в раннем детском возрасте: отмечаются клинические и биохимические признаки прогрессирующего заболевания печени, протекающего на фоне низких уровней γ-ГТП. Течение синдрома Байлера часто осложняется развитием гепатоцеллюлярной карциномы.
ПСВХ 3 типа развивается вследствие мутации гена АВСВ4, кодирующего белок MDR, ответственный за транспорт фосфолипидов через каналикулярную мембрану. Заболевание начинается с прогрессирующего холестаза в раннем детском возрасте. В отличие от ПСВХ 1 и 2 типа при этой патологии значительно возрастает уровень γ-ГТП, а при гистологическом исследовании биоптатов печени отмечают явления портального воспаления, фиброза/цирроза, а также выраженную пролиферацию желчных протоков.
В руководстве EASL подчеркивается, что в настоящее время не существует ни одной медикаментозной методики лечения ПСВХ, обладающей доказанной долгосрочной эффективностью (III/С2). УДХК является единственным препаратом, улучшающим биохимические показатели у части пациентов с ПВСХ (III/С2): прием УДХК способствует снижению активности печеночных ферментов у 50% больных ПСВХ 3 типа, но у пациентов с ПСВХ 1 и 2 типа подобная зависимость не прослеживается. Для уменьшения интенсивности зуда эксперты рекомендуют использовать рифампицин (III/С2), подчеркивая, что частичное отведение желчи оказывает благоприятный клинический и биохимический эффекты на течение ПСВХ 1 и 2 типа (III/С2). На поздних стадиях заболевания эксперты считают целесообразным проведение трансплантации печени (III/В1).
Доброкачественный рецидивирующий внутрипеченочный холестаз
Доброкачественный рецидивирующий внутрипеченочный холестаз (ДРВХ) 1 и 2 типа – острые холестатические заболевания, которые развиваются у подростков и лиц молодого возраста и являются доброкачественными формами ПСВХ 1 и 2 типа. К характерным проявлениям ДРВХ эксперты EASL относят периодическое обострение холестаза, желтухи и сильного зуда, которые полностью разрешаются через несколько недель или месяцев (III/С1). Течение ДРВХ 1 типа может осложняться панкреатитом, а ДРВХ 2 типа – патологией желчного пузыря.
В настоящее время эффективная терапия ДРВХ не разработана. Современные методы лечения ДРВХ предполагают назначение УДХК и рифампицина, а также проведение наружного дренирования желчных протоков (III/С2).
Лекарственно-индуцированное холестатическое поражение печени
Рассматривая различные формы лекарственно-индуцированного поражения печени (ЛИПП), эксперты EASL особое внимание уделили острому холестатическому ЛИПП, определив его как изолированное повышение уровня ЩФ в сыворотке крови (>2 верхних границ нормы) или снижение значений индекса АЛТ/ЩФ <2 (при этом значения обоих показателей, использованных для расчета указанного соотношения, превышают верхнюю границу нормы). В качестве сравнения в руководстве EASL приводятся также дефиниции гепатоцеллюлярного и смешанного типа ЛИПП. Гепатоцеллюлярная форма ЛИПП характеризуется изолированным повышением АЛТ (>2 верхних границ нормы) или значением соотношения АЛТ/ЩФ >5, в то время как смешанный тип ЛИПП определяется только индексом АЛТ/ЩФ, уровень которого при данной патологии колеблется от 2 до 5. Подчеркивая клинические различия между типами ЛИПП, эксперты EASL отмечают, что прогноз при холестатическом поражении печении более благоприятный, чем при гепатоцеллюлярном повреждении.
Среди разнообразных этиологических факторов холестатического ЛИПП ведущую роль эксперты отводят медикаментозным препаратам, подчеркивая при этом, что заболевание могут спровоцировать прием лекарственных трав и пищевых добавок. В подавляющем большинстве случаев поражение печени непредсказуемо и развивается по типу идиосинкратической реакции или по механизму гиперсенсибилизации, и только в небольшом проценте случаев возникновение ЛИПП прогнозируемо и зависит от дозы принятого медикамента. Согласно имеющимся статистическим данным, распространенность ЛИПП колеблется от 1 случая на 10 тыс. до 1 случая на 100 тыс. пациентов, при этом около 30% случаев ЛИПП являются холестатическими. Эксперты считают, что склонность к ЛИПП определяется не только генетической предрасположенностью, но и факторами окружающей среды.
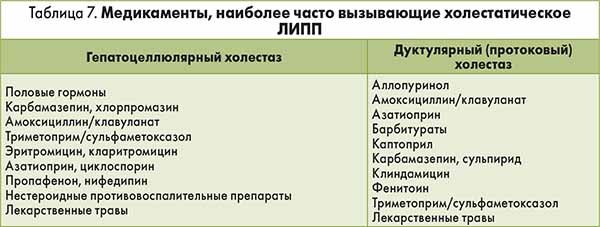
В качестве наиболее вероятных причин ЛИПП в руководстве EASL приводятся некоторые лекарственные препараты (табл. 7).
Возникновение лекарственно-индуцированного холестаза эксперты EASL объясняют двумя наиболее вероятными патогенетическими механизмами. В первом случае лекарственное средство ингибирует экспрессию гепатоцеллюлярных белков-переносчиков и/или их функцию, что приводит к нарушению секреции желчи на гепатоцеллюлярном уровне. В другом – медикаментозный препарат индуцирует идиосинкратическое воспаление или реакцию гиперчувствительности в мелких желчных протоках или на холангиоцеллюлярном уровне, что сопровождается развитием дуктулярного холестаза и ассоциируется с нарушением секреции желчи гепатоцитами. В очень редких случаях лекарственные препараты могут вызвать синдром исчезающих желчных протоков и спровоцировать развитие билиарного цирроза печени.
Диагностика
В руководстве EASL подчеркивается, что в настоящее время отсутствуют специфические диагностические тесты, позволяющие подтвердить или опровергнуть диагноз ЛИПП. В связи с этим диагностика ЛИПП требует клинического подтверждения и основывается на тщательно собранном медикаментозном анамнезе, анализе временной связи между приемом лекарственного средства и поражением печени, а также исключения других заболеваний.
Несмотря на то что провокационная проба может подтвердить диагноз ЛИПП, эксперты EASL считают ее потенциально опасной, неэтичной и не рекомендуют использовать в клинической практике. Однако отмечают, что в некоторых случаях непреднамеренная провокационная проба способствует установлению правильного диагноза. По мнению экспертов, при холестатическом ЛИПП не требуется выполнения биопсии печени (III/С2). В данной ситуации более целесообразно проведение тщательного 3-месячного мониторинга печеночных проб после отмены потенциально гепатотоксического препарата вплоть до нормализации уровня печеночных ферментов. Показанием к проведению биопсии печени может стать тяжелое, прогрессирующее или затяжное течение заболевания; тогда выполнение данного исследования позволит получить дополнительную информацию о типе поражения печени и исключить другие причины холестаза.
Лечение
В руководстве EASL подчеркивается, что в настоящее время единственным эффективным методом лечения холестатического ЛИПП является быстрая отмена препаратов, спровоцировавших развитие заболевания, и проведение тщательного клинического и биохимического мониторинга (III/С2). В некоторых случаях явления гепатотоксичности протекают настолько тяжело, что могут привести к нетрудоспособности и даже угрожать жизни пациента. В таких ситуациях только отмены препарата недостаточно, необходимо обеспечить быстрое связывание остатков лекарственного препарата, выведение его из организма и максимальную защиту печени от повреждения. Достижение указанных целей возможно при проведении интенсивной дезинтоксикации и назначении УДХК. В руководстве приводятся данные, подтверждающие, что терапия УДХК оказывает положительное влияние на течение заболевания в 2/3 случаев. Есть также сообщения, описывающие эффективность кортикостероидов в лечении лекарственно-индуцированного холестаза. При неэффективности указанных методик может потребоваться проведение трансплантации печени.
Исходы холестатического ЛИПП, особенно после успешного выведения лекарственных средств из организма, достаточно обнадеживающие. В большинстве случаев оно заканчивается длительным холестазом, после разрешения которого функциональная активность гепатоцитов, вероятно, полностью восстанавливается. У небольшого количества пациентов сохраняются персистирующие патологические изменения печеночных проб и нарушения гистологической структуры печени.
Холестатические заболевания беременных. Внутрипеченочный холестаз беременных
Давая определение внутрипеченочному холестазу беременных (ВХБ), эксперты EASL подчеркивают, что эта рецидивирующая форма холестаза характеризуется появлением интенсивного кожного зуда во время беременности (в большинстве случаев во II или III триместре), увеличением активности трансаминаз и повышением концентрации желчных кислот в сыворотке крови, а также спонтанным уменьшением или разрешением основных клинических симптомов через 4-6 нед после родов.
По мнению экспертов, клиническая значимость ВХБ заключается в потенциальной опасности для плода, т. к. приток большого количества желчных кислот обусловливает увеличение их концентрации в амниотической жидкости, пуповинной крови и меконии, что может привести к спонтанным преждевременным родам, увеличить риск асфиксии во время родов и вызвать внутриутробную смерть плода. В то же время интенсивный кожный зуд, усиливающийся в ночное время суток, значительно ухудшает качество жизни беременной.
Большую роль в развитии ВХБ отводят генетическим и гормональным факторам, а также влиянию окружающей среды. Высока вероятность возникновения ВХБ при многоплодной беременности, употреблении высоких доз оральных контрацептивов и прогестерона. Наследственная предрасположенность и семейный характер ВХБ указывают на наличие специфических генетических мутаций. В настоящее время выявлено несколько мутаций генов АВС и АТП8В1, кодирующих белки-транспортеры. Нарушение их активности может спровоцировать холестаз.
Диагностика
В руководстве EASL подчеркивается, что у беременных следует систематически проверять состояние кожных покровов, чтобы своевременно отличить следы расчесов от проявлений экземы. Хотя зуд кожных покровов может появиться до нарушений функций печени, активность печеночных проб (АЛТ, билирубин, γ-ГТП), концентрации желчных кислот, протромбиновое время должны оцениваться у каждой беременной, предъявляющей жалобы на зуд, и определяться повторно, если кожный зуд не исчезнет после родов.
Эксперты EASL отмечают, что диагностика холестаза беременных основывается на появлении зуда и увеличении концентрации желчных кислот в сыворотке крови (>11 мкмоль/л). В руководстве подчеркивается, что желчные кислоты являются наиболее чувствительным маркером холестаза беременных. При ранней клинической манифестации ВХБ (<33 нед гестации) уровень желчных кислот >40 мкмоль/л на любом сроке беременности ассоциируется с высоким риском возникновения осложнений у плода. Учитывая необходимость проведения дифференциального диагноза с острой жировой дистрофией печени беременных и HELLP-синдромом, эксперты специально перечисляют биохимические особенности ВХБ: в большинстве случаев холестаз беременных характеризуется сочетанным повышением содержания желчных кислот в сыворотке крови и ростом активности АЛТ, тогда как изолированное увеличение концентрации желчных кислот встречается крайне редко. Умеренное повышение уровня конъюгированного билирубина и легкая форма желтухи наблюдаются только в 10-15% случаев. Еще одной отличительной чертой ВХБ является содержание γ-ГТП: у беременных с мутацией гена АВСВ4 уровень γ-ГТП повышается, тогда как при наличии других мутаций концентрация этого маркера холестаза остается в рамках нормативных значений. Учитывая вероятность развития специфических заболеваний, таких как преэклампсия, HELLP-синдром и острая жировая дистрофии печени, течение которых также сопровождается изменением активности печеночных проб, эксперты настаивают на необходимости проведения тщательной дифференциальной диагностики между ними и ВХБ.
Эксперты EASL подчеркивают, если зуд и явления холестаза не исчезают после родов и периодически возникают снова, то необходимо исключить наличие других хронических холестатических заболеваний печени, например ПБЦ.
Лечение
Эксперты EASL утверждают, что препаратом выбора для лечения ВХБ является УДХК в дозе 10-20 мг/кг/сут. УДХК облегчает зуд и улучшает показатели печеночных проб у 67-80% женщин с ВХБ, однако практически не влияет на частоту возникновения внутриутробных осложнений. Если эффективность стандартной дозы УДХК недостаточна, то суточная доза может быть увеличена до 25 мг/кг.
Эксперты не рекомендуют включать дексаметазон (12 мг/сут на протяжении 7 дней) в схемы терапии ВХБ по причине его неэффективности. В руководстве также отмечается, что результативность S-аденозил-L-метионина в лечении ВХБ уступает таковой УДХК, однако предусматривается возможность применения этого кофермента при недостаточной эффективности стандартных доз УДХК (табл. 8).
Обструктивный холестаз во время беременности
Хотя у 10% беременных при инструментальном обследовании выявляют конкременты или билиарный сладж, выраженная клиническая симптоматика развивается только в 1,2% случаев. Обструктивный холестаз беременных диагностируется на основании появления жалоб и характерных симптомов, увеличения уровня печеночных ферментов (АЛТ, билирубин, γ-ГТП, ЩФ) и результатов абдоминального или эндоскопического УЗИ. При этом эксперты подчеркивают, что проведение рентгенологического исследования не является абсолютно противопоказанным даже в I триместре беременности (III/С2). Холестаз, обусловленный обструкцией общего желчного протока или обострением панкреатита на фоне желчнокаменной болезни, является показанием к проведению ЭРХПГ, а лечение симптоматических конкрементов желчных протоков у беременных заключается в проведении эндоскопической сфинктеротомии и экстракции конкрементов (II‑3/В1). Основываясь на результатах нескольких исследований, эксперты EASL считают ЭРХПГ относительно безопасной процедурой во время беременности, но указывают, что исследование должен проводить высококвалифицированный специалист. Положения руководства также предусматривают возможность седации при помощи низких доз меперидина, пропофола, фентанила и мидазолама.
Медикаменты для лечения холестатических заболеваний во время беременности
В руководстве подчеркивается, что у большинства женщин репродуктивного возраста с холестатическими заболеваниями печени беременность не сопровождается осложнениями, особенно при легком течении и неактивной фазе заболевания. Несмотря на это, вероятность развития АИГ или перекрестного синдрома во время беременности чрезвычайно высока, обострение заболевания возможно как во время самой беременности, так и в послеродовый период.
Рассматривая возможность назначения различных препаратов для лечения холестатических заболеваний печени во время беременности, эксперты EASL считают применение УДХК во II и III триместрах эффективным и безопасным (I/В1). В то же время безопасность применения УДХК в I триместре еще не доказана. Несмотря на то что УДХК не рекомендуется назначать во время грудного вскармливания, эксперты предполагают, что этот препарат безопасен для младенцев, т. к. в грудном молоке не были обнаружены даже следовые концентрации УДХК.
Прием преднизолона во время беременности и лактации считается относительно безопасным, но его использование сопряжено с высоким риском развития такого врожденного дефекта, как волчья пасть. При беременности азатиоприн классифицируется FDA как средство категории D. По мнению экспертов, терапию АИГ при помощи преднизолона и азатиоприна следует продолжать во время беременности для предупреждения обострений заболевания, которые могут быть более опасными в отношении исходов беременности, чем потенциальный риск от приема этих медикаментов (III/С2).
Лечение внепеченочных проявлений
Зуд
Рассматривая клинические особенности зуда кожных покровов, эксперты подчеркивают, что этот симптом может возникать при всех холестатических заболеваниях печени. В некоторых случаях он может быть совершенно невыносимым, приводя к временной нетрудоспособности пациента. Интенсивность кожного зуда колеблется на протяжении дня, его выраженность уменьшается на терминальных стадиях заболевания.
За исключением зуда при обструктивном холестазе коррекция данного патологического симптома проводится при помощи системных препаратов, т. к. местные средства оказываются неэффективными. Эксперты подчеркивают, что УДХК не уменьшает интенсивность холестатического зуда (кроме зуда при ВХБ). Положения руководства утверждают, что средством первой линии терапии является холестирамин. Основным фактором, ограничивающим широкое применение этого препарата, считается его неприятный вкус, поэтому эксперты рекомендуют принимать холестирамин вместе с каким-либо фруктовым соком. К средствам второй и третьей линии терапии относятся, соответственно, рифампицин (начальная доза – 150 мг/сут; целевая – 600 мг/сут; I/А1) и налтрексон (начальная доза – 25 мг/сут; целевая – 50 мг/сут; I/В1). При неэффективности этих препаратов назначают сертралин (II‑2/С2); также предусматривается возможность применения экспериментальных лекарственных средств и использования инвазивных методов лечения в условиях специализированных медицинских центров (III/С2).
Усталость
Больных ПБЦ может беспокоить усталость, выраженность которой не зависит от тяжести поражения печени. Однако прежде чем интерпретировать усталость как характерное проявление ПБЦ, эксперты рекомендуют исключить наличие сопутствующих заболеваний – гипотиреоза, анемии, сахарного диабета, депрессии (III/С2). Возможным способом уменьшения усталости может быть минимизация влияния факторов, способных усилить вегетативную дисфункцию (прием большого количества антигипертензивных препаратов) или привести к нарушению сна (употребление кофе на ночь) (III/С2). В руководстве подчеркивается, что трансплантация печени не является способом лечения усталости при отсутствии других показаний (III/С1).
В руководстве EASL указывается, что у пациентов с холестатическими заболеваниями печени очень высокий риск развития остеопороза, поэтому эксперты рекомендуют проводить клиническую оценку вероятности возникновения остеопороза у всех больных (III/С2). При выявлении признаков хронического холестатического заболевания печени следует определить минеральную плотность костной ткани при помощи двухэнергетической рентгеновской абсорбциометрии (III/С2). Эксперты предлагают проводить контрольные измерения минеральной плотности костной ткани 1 раз в год или чаще в зависимости от степени холестаза и наличия других факторов риска (III/С2).
В качестве медикаментозной профилактики остеопороза всем пациентам с холестатическими заболеваниями печени эксперты рекомендуют назначать препараты кальция (1000-1200 мг/сут) и витамин D (400-800 МЕ/сут), подчеркивая при этом, что данная мера не имеет доказательной базы (III/С2). Еще одним способом лечения остеопороза может быть назначение алендроната или других бисфосфонатов, прием которых показан при возникновении патологических переломов, а также в случае, если при проведении двухэнергетической рентгеновской абсорбциометрии значения показателя Т ниже -2,5 (I/В1). Целесообразность применения этих препаратов может быть рассмотрена при значениях Т -1,5 (III/С2).
Несмотря на то что за последние несколько лет наши знания о холестатических заболеваниях печени значительно расширились, своевременная диагностика и лечение этих нозологий по-прежнему требуют от врачей всеобъемлющих знаний, а успешное ведение пациентов невозможно без пристального внимания и терпения. Руководствуясь положениями практических рекомендаций, можно подобрать эффективную схему терапии практически любого холестатического заболевания печени, основная роль в медикаментозном лечении которых будет отведена УДХК или иммуносупрессантам.
В настоящее время на отечественном фармакологическом рынке широко представлены генерические препараты УДХК, каждый из этих гепатопротекторов имеет свою «изюминку», но у Урсохола, выпускаемого ЧАО «Фармацевтическая фирма «Дарница», их несколько.
Урсохол воплощает все лучшие свойства УДХК – обладает цито- и гепатопротекторным, антифибротическим и антихолестатическим, гипохолестеринемическим и иммуномодулирующим, антиапоптотическим и антиоксидантным эффектами. Благодаря этим особенностям применение Урсохола при холестатических заболеваниях печени сопровождается нормализацией физических свойств желчи, улучшением гепатобилиарной секреции с одновременным восстановлением текучести мембран и цитоскелета гепатоцитов. В зависимости от этиологии заболевания терапия Урсохолом может не только улучшить самочувствие больного, нормализовать клинико-лабораторные показатели, но и способствовать исчезновению морфологических признаков холестаза.
Еще одной особенностью Урсохола, выгодно отличающей его от других генериков УДХК, является оптимальное соотношение цены и качества. Урсохол, выпускаемый одним из лидеров украинской фармацевтической промышленности, производится на современном оборудовании с использованием инновационных технологий в контролированных условиях и полностью соответствует требованиям GMP. Пациенты с холестатическими заболеваниями печени, нуждающиеся в длительном приеме УДХК, особенно оценят Урсохол – ведь в упаковке содержится достаточное количество капсул, обеспечивающее непрерывный прием препарата на протяжении месяца и позволяющее больным тратить минимальное количество времени для посещения аптеки. Капсулы Урсохола имеют нейтральный вкус, небольшой размер и не вызывают особых затруднений при приеме. Оптимальная цена при высоком качестве и эффективности делает Урсохол доступным для многих пациентов с различными холестатическими заболеваниями печени. Сочетание всех вышеперечисленных положительных свойств в одном препарате позволяет повысить приверженность больных к лечению и, следовательно, увеличить эффективность медикаментозной терапии.
Список литературы находится в редакции.
| Медична газета «Здоров’я України 21 сторіччя» № 8 (381), квітень 2016 р. |