7 жовтня, 2019
Знеболення при гострих ураженнях кістково-м’язової системи: усвідомлений вибір препарату та шляху його введення
Швидке й ефективне знеболення є одним із клінічних пріоритетів у практиці невідкладної медицини, й насамперед це стосується надання медичної допомоги пацієнтам із гострими травматичними ураженнями кістково-м’язової системи. Протягом останніх років спостерігається очевидний зсув парадигми знеболення в бік ширшого застосування неопіоїдних аналгетиків, таких як нестероїдні протизапальні препарати (НПЗП) і парацетамол, які позбавлені ризику розвитку залежності та низки інших характерних для опіоїдів небажаних явищ (Todd K. H., 2017; Casamayor M. et al., 2018).
Серед НПЗП, що найчастіше використовуються з метою невідкладного знеболення при гострих ураженнях кістково-м’язової системи, безумовне лідерство належить диклофенаку, котрий характеризується вираженою знеболювальною, протизапальною та жарознижувальною дією. Саме до цього препарату, який за три десятиліття успішного застосування у світовій клінічній практиці здобув статус золотого стандарту симптоматичного лікування хронічних запальних і дегенеративних захворювань опорно-рухового апарату (передусім остеоартриту, остеохондрозу та ревматоїдного артриту), сьогодні прикута увага як до потужного аналгетику. Нині диклофенак призначається також із метою усунення гострого больового синдрому після травм та операцій, при міалгіях і невралгіях, подагрі, мігрені, дисменореї тощо.
Важливою перевагою диклофенаку є добре відомий і досконально вивчений механізм його дії. Протизапальна дія диклофенаку реалізується шляхом інгібування циклооксигенази (ЦОГ): він пригнічує обидві ізоформи цього ферменту (ЦОГ‑1 і ЦОГ‑2), зменшуючи синтез простагландинів (найперше PGЕ2) та тромбоксану. При цьому встановлено, що диклофенак у 4 рази більш селективний щодо ЦОГ‑2, ніж інші НПЗП. Однак, як зазначено в роботі T. D. Warner і співавт. (1999), його терапевтичні концентрації (тобто IC80) також інгібують 70% ЦОГ‑1, що може пояснювати збалансований ефект стосовно ризику кардіоваскулярних небажаних явищ (Atzeni F. et al., 2018). Остання обставина є особливо важливою, оскільки саме питання кардіоваскулярної безпеки тривалого застосування селективних інгібіторів ЦОГ‑2 останніми роками викликає істотне занепокоєння фахівців. Окрім блокади ЦОГ, диклофенак також блокує 5-ліпооксигеназу, зменшуючи продукцію прозапальних лейкотрієнів. Отже, диклофенак ефективно пригнічує активність як циклооксигеназного, так і ліпооксигеназного шляху метаболізму арахідонової кислоти, завдяки цьому швидко знижуючи інтенсивність запалення.
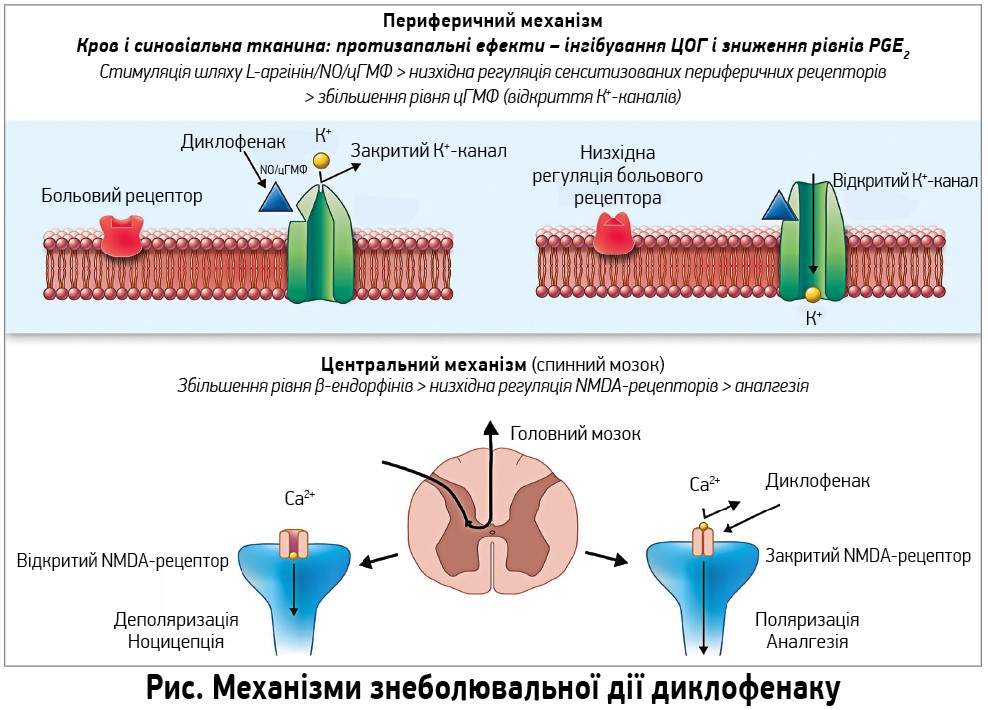
На додачу до вираженого впливу на запалення диклофенаку натрію притаманний потужний аналгетичний ефект, який і зумовлює дедалі ширше застосування цього НПЗП з метою купірування гострих больових синдромів. Антиноцицептивна дія диклофенаку реалізується як через центральні, так і через периферичні механізми, не пов’язані з його впливом на запалення (рис.).
Периферичні механізми знеболювальної дії диклофенаку, крім потужного інгібування активності ЦОГ у тканинах, включають зменшення кількості сенситизованих периферичних больових рецепторів завдяки стимуляції сигнального шляху L‑аргінін – оксид азоту (NO) – циклічний гуанозинмонофосфат (цГМФ) (Tonussi C. R., Ferreira S. H., 1994) та активації відкриття АТФ‑чутливих калієвих каналів (Alves D. P. et al., 2004). Центральні механізми реалізації аналгетичної активності диклофенаку включають збільшення концентрації β-ендорфіну (Martini A. et al., 1984) та послаблення гіпералгезії, опосередкованої NMDA‑рецепторами (Dong X. D., 2009). Крім того, наукові дослідження останнього десятиріччя виявили низку раніше невідомих механізмів реалізації терапевтичних ефектів диклофенаку. До них насамперед належать здатність зменшувати продукцію субстанції Р (запальний нейропептид), інгібувати γ-рецептори, що активуються проліфератором пероксисом (PPAR‑γ), блокувати кислотно-чутливі іонні канали (ASIC3 та ASIC1a), зменшувати синтез інтерлейкіну‑6 (Gan T. J., 2010). Ці нові дані свідчать про мультимодальний характер фармакологічної дії диклофенаку, котрий може сприятливо позначатися на профілі його безпеки при застосуванні в реальній клінічній практиці.
Вибір препарату диклофенаку
Диклофенак – надзвичайно популярний препарат як серед лікарів, так і серед пацієнтів. Обсяги його щорічної реалізації з урахуванням усіх лікарських форм істотно перевищують такі будь-яких інших НПЗП. На фармацевтичному ринку України наразі зареєстрована величезна кількість (близько 140) генеричних препаратів диклофенаку в різних лікарських формах. Цілком зрозуміло, що далеко не всі вони мають доведену еквівалентність оригінальному препарату й апріорно високу якість фармацевтичної сировини. Крім того, при порівнянні складу різних препаратів диклофенаку звертають на себе увагу відмінності в якісному складі допоміжних речовин, котрі, як відомо, можуть істотно впливати на показники фармакокінетики діючої речовини (наприклад, на швидкість вивільнення в шлунково-кишковому тракті, швидкість і повноту абсорбції тощо). Чи може лікар-практик самостійно об’єктивно оцінити якість кожного з цих 140 препаратів – питання риторичне. Саме тому, обираючи доступні за ціною генерики диклофенаку, варто зважати на репутацію виробника та наявність цього препарату на європейському фармацевтичному ринку, вимоги до реєстрації лікарських засобів на якому є суворішими. Серед високоякісних препаратів диклофенаку, що здобули довіру європейських та українських лікарів, на особливу увагу заслуговує диклофенак натрію компанії Berlin-Chemie (Німеччина) – він представлений у різних лікарських формах і дозуваннях під торговою маркою Диклоберл®. Беззаперечними перевагами препаратів лінійки Диклоберл® є:
1. Наявність різних лікарських форм випуску та дозувань:
- Диклоберл® N 75 – розчин для ін’єкцій 75 мг / 3 мл;
- Диклоберл® ретард – капсули тверді пролонгованої дії 100 мг;
- Диклоберл® 100 – супозиторії 100 мг.
- Диклоберл® 50 – супозиторії 50 мг.
2. Швидке настання протизапального та знеболювального ефектів.
3. Значна тривалість дії (при застосуванні пролонгованих форм).
4. Можливість комбінування пероральних форм із ректальними супозиторіями й ін’єкціями для максимальної індивідуалізації терапії.
Диклоберл® N 75 (диклофенак у формі ін’єкцій) переважно застосовують тоді, коли на перший план виходить потреба в швидкому настанні знеболювального ефекту, тобто при гострих больових синдромах. Ретардна форма диклофенаку натрію (капсули Диклоберл® ретард) забезпечує пролонговану дію та застосовується 1 раз на добу, покращуючи комплаєнс. Окрім власне фармакологічних властивостей диклофенаку, перевагою капсул Диклоберл® ретард є раціонально підібраний склад допоміжних речовин їхньої оболонки. Зокрема, амонійно-метакрилатний сополімер (тип А) «покриває» диклофенак і забезпечує його всмоктування саме в тонкій кишці, де цей процес є найактивнішим. Вказана речовина починає розчинятися при тих значеннях рН, які характерні для тонкої кишки. При цьому амонійно-метакрилатний сополімер є хімічно інертним і виводиться природним шляхом у первинному, неметаболізованому вигляді, не чинячи негативного впливу на організм людини.
Лікарська форма диклофенаку у вигляді супозиторіїв (Диклоберл® 100 та Диклоберл® 50) дає змогу уникнути ефекту першого проходження через печінку, забезпечує швидку й незалежну від прийому їжі абсорбцію препарату та може застосовуватися в пацієнтів, які внаслідок тих чи інших причин не можуть приймати препарат перорально. При застосуванні ректальних супозиторіїв Диклоберл® максимальна концентрація диклофенаку в плазмі крові досягається швидше (через 1 год), аніж при прийомі капсул пролонгованої дії (2-3 год). Отже, їх використання може мати переваги саме при гострому больовому синдромі (наприклад, у післяопераційний період, при дисменореї, нападі подагри, мігрені). Наявність двох дозувань препарату у формі ректальних супозиторіїв (100 та 50 мг) дозволяє легко підібрати оптимальну добову дозу та режим застосування в залежності від інтенсивності больового синдрому й запланованої тривалості лікування (загальна добова доза диклофенаку – 150 мг).
Застосування різних лікарських форм диклофенаку при гострих ураженнях кістково-м’язової системи: дані нового дослідження
Найчастішими шляхами введення диклофенаку в реальній клінічній практиці залишається пероральний і внутрішньом’язовий – саме вони є оптимальними в практиці невідкладної медицини при гострих ураженнях кістково-м’язової системи. Хоча висока аналгетична та протизапальна ефективність диклофенаку вже давно не викликає в лікарів жодних сумнівів, питання про необхідність її прямого порівняння при застосуванні препарату в різних лікарських формах у рамках відповідно спланованих великих рандомізованих контрольованих досліджень (РКД) донедавна залишалося відкритим. Відповідь на нього більшою мірою стосувалася «мистецтва лікування», ніж доказової медицини, оскільки таких досліджень із застосуванням одного й того самого НПЗП було вкрай недостатньо. Попередні дослідження, котрі порівнювали різні шляхи введення НПЗП, вказували на те, що пероральний прийом цих препаратів не поступається внутрішньом’язовому введенню стосовно досягнення ефективної аналгезії. Проте в цих дослідженнях використовувалися два різні типи НПЗП.
У цьому контексті значну зацікавленість фахівців закономірно викликали результати проспективного подвійного сліпого РКД із подвійним маскуванням, у ході якого порівнювали ефективність купірування гострого больового синдрому в дорослих із травматичними пошкодженнями кістково-м’язової системи за допомогою парентерального введення диклофенаку натрію чи його перорального прийому. Зовсім нещодавно вони були надруковані на сторінках авторитетного фахового видання Emergency Medicine Journal міжнародною групою вчених (Qureshi I. et al., 2019). Загалом у дослідження було включено 300 осіб віком від 18 до 65 років, які були госпіталізовані у відділення невідкладної терапії протягом перших 24 год від моменту настання гострого ушкодження кістково-м’язової тканини. Вони були рандомізовані в 2 рівні групи: одні (n=150) з метою знеболення отримували внутрішньом’язову ін’єкцію диклофенаку (75 мг) і плацебо перорально, а інші (n=150) – диклофенак перорально (100 мг) у поєднанні з внутрішньом’язовим уведенням розчину плацебо. Як первинна кінцева точка розглядалася частка учасників у кожній групі, в яких на тлі призначеного лікування вдавалося досягти зменшення інтенсивності больового синдрому щонайменше на 50% через 30 хв після отримання диклофенаку в призначеній їм лікарській формі. Ця первинна кінцева точка була досягнута в 99,3% пацієнтів (95% ДІ від 96,3 до 100) у групі внутрішньом’язового введення диклофенаку й у 86,7% пацієнтів (95% ДІ від 80,2 до 91,7) у групі перорального прийому. З точки зору оцінки безпеки важливо, що в жодній групі не було зареєстровано небажаних явищ.
Таким чином, у цьому РКД було виконане порівняння раннього постмедикаційного ефекту диклофенаку при його внутрішньом’язовому та пероральному введенні. Отримані результати засвідчили, що внутрішньом’язове введення асоційоване з більшою ймовірністю досягнення успіху за критерієм зменшення інтенсивності болю на 50% від початкової, а також із більшою загальною ефективністю в перші 30 хв після введення (різниця абсолютного ризику – 12,7%). Проте автори дослідження зазначають, що в певних клінічних обставинах (ураховуючи час на приготування до виконання ін’єкції та наявність відповідного персоналу) перевагу можна віддавати й пероральному прийому диклофенаку.
Отже, зважаючи на складний етіопатогенез гострого больового синдрому при ураженнях кістково-м’язової системи, що включає периферичні та центральні механізми формування відчуття болю, мультимодальний механізм антиноцицептивної та протизапальної дії диклофенаку є особливо затребуваним в умовах надання невідкладної медичної допомоги. Вибір препарату диклофенаку, який має максимально широкий діапазон лікарських форм (наприклад, препаратів лінійки Диклоберл®), дає лікарю змогу продемонструвати «мистецтво лікування» та на практиці реалізувати індивідуальний підхід до ведення кожного пацієнта.
Підготувала Анжела Томічева
Медична газета «Здоров’я України 21 сторіччя» № 17 (462), вересень 2019 р.