7 жовтня, 2019
Діагностична і лікувальна тактика при вентилятор-асоційованому трахеобронхіті: бути чи не бути антибіотикотерапії?
Проведення інтубації та механічної вентиляції легень (МВЛ) у 6-20 разів підвищує ризик інфікування нижніх дихальних шляхів (НДШ) та виникнення вентилятор-асоційованих інфекцій – трахеобронхіту (ВАТБ) або пневмонії (ВАП). Ризик інфекції прямо пропорційний тривалості перебування в інтенсивній терапії (ІТ), а смертність інфікованих пацієнтів удвічі вища, ніж неінфікованих (EPIC II Group of Investigators, 2009).
Найбільш несприятливий прогноз у пацієнтів із сепсисом, серед яких умирає кожен четвертий (Vincent J. et al., 2014). Респіраторні інфекції спричиняють половину всіх призначень антибіотиків в ІТ (Alves А., Pereira J., 2018). Необґрунтоване парентеральне застосування антибіотиків широкого спектра підвищує ризик реакцій гіперчутливості (анафілаксія, токсичний епідермальний некроліз, DRESS-синдром), специфічної токсичності, дисфункції мітохондрій з окисним пошкодженням та несприятливої взаємодії з іншими лікарськими засобами, а також дисбіозу з тривалим порушенням мікробіомів кишечнику і легень, що також підвищує схильність до інфекцій, зокрема й до пневмонії (Budden K. et al., 2017; McAleer J., Kolls J., 2018; Hakansson A. et al., 2018). Та найбільшою проблемою є виникнення резистентності мікробів, насамперед мульти- або тотальнорезистентних штамів. Резистентні до колістину грамнегативні бактерії нечутливі практично до всіх доступних на сьогодні антибіотиків (Kollef M., 2016). Цей огляд присвячено проблемі діагностики й лікування ВАТБ, тактику ведення якого досі чітко не визначено.
Щодо визначення ВАТБ немає єдиної думки. Більшість авторів пропонують діагностичні критерії, підсумовані в таблиці 1, які часто перекривають критерії ВАП (Nseir S. et al., 2002; ATS/IDSA guideline, 2005; Craven D. et al., 2009; Dallas J. et al., 2011). Дехто з авторів за обов’язковий критерій має гнійний характер ендотрахеального аспірату (ЕТА): ≥25 нейтрофілів і ≤10 плоских епітеліальних клітин у полі зору при малому збільшенні (Martin-Loeches I. et al., 2015). Не визначено потреби мікробіологічного дослідження (Torres A. et al., 2009). Часто ВАТБ ставлять як альтернативний діагноз через брак чітких діагностичних критеріїв ВАП (ATS/IDSA guideline, 2005).
Епідеміологія. Поширеність ВАТБ наближена до ВАП, більше того, трахеобронхіт може перейти у пневмонію, що трапляється у 12,2-34% пацієнтів. За даними літератури, частота ВАТБ коливається від 1,4 до 16,7% (Agrafiotis M. et al., 2010; Dallas J. et al., 2011; Shahin J. et al., 2013).
У зв’язку з тим, що цей стан перешкоджає самостійному диханню та екстубації, а також через імовірність пневмонії, пацієнти з ВАТБ зазвичай потребують тривалішої МВЛ і перебування в ІТ (Craven D. et al., 2013; Karvouniaris M. et al., 2013; Martin-Loeches I. et al., 2015). Щодо впливу ВАТБ на смертність, то в літературі є дані як про її підвищення, особливо при виникненні ВАП, так і про відсутність суттєвого збільшення летальності (Nseir S. et al., 2002; Agrafiotis M. et al., 2010; Martin-Loeches I. et al., 2015).
Етіологія. Найчастіше ВАТБ спричиняють грамнегативні бактерії – Pseudomonas aeruginosa, Acinetobacter baumannii, Klebsiella pneumoniae, Haemophilus influenza, Escherichia coli та Legionella pneumophila. Серед грампозитивних переважають метицилін-резистентний Staphylococcus aureus та Streptococcus pneumoniae (Bouza E. et al., 2003; Martin-Loeches I. et al., 2015). Досить часто ВАТБ спричиняють мультирезистентні штами бактерій (Craven D., Hjalmarson K., 2010; Dallas J. et al., 2011). Украй рідко причиною ВАТБ можуть бути гриби роду Candida або віруси, зокрема вірус простого герпесу, проте ці випадки здебільшого не призводять до ВАП (Luyt C. et al., 2007).
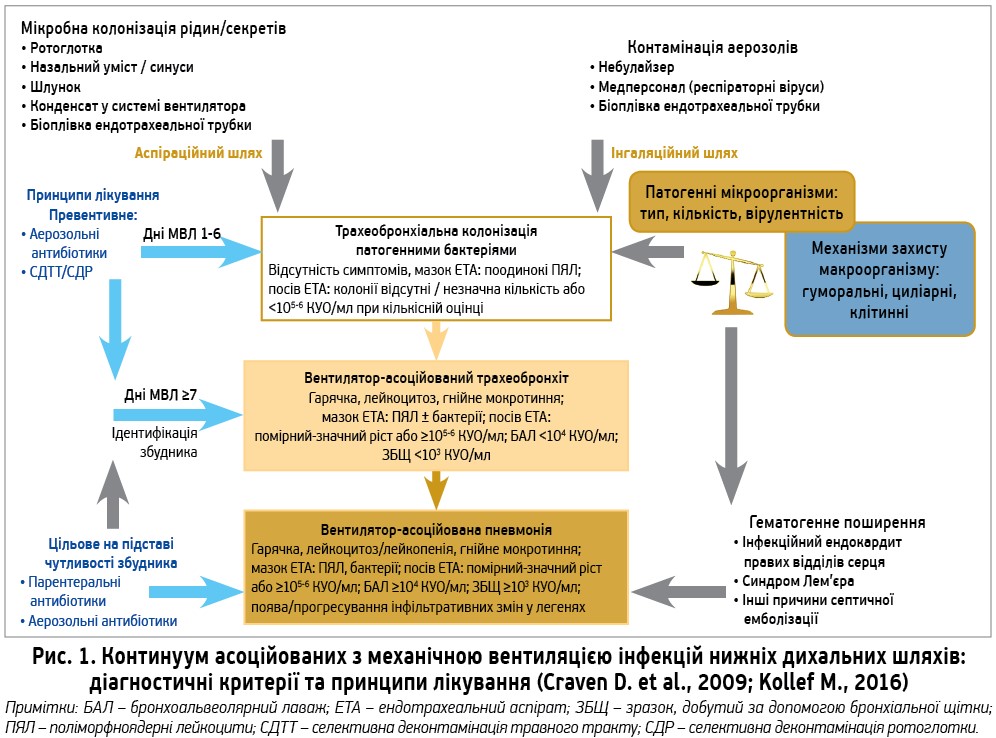
Патофізіологія. Тривалість МВЛ >48 год підвищує тиск у дихальних шляхах, зумовлює пошкодження легень, суттєво збільшує ризик респіраторного дистрес-синдрому (РДС) та інфікування НДШ (Jia X. et al., 2008). Ендотрахеальна трубка (ЕТ) створює бактеріям з носоглотки, приносових пазух, ротової порожнини і шлунково-кишкового тракту зручний, легкий, односторонній шлях до НДШ, що сприяє їх колонізації бактеріями (Chastre J., Fagon J., 2002; Craven D., 2006). Ризик ще вищий за умов застосування седативних засобів та недостатнього відсмоктування вмісту ЕТ (Craven D. et al., 2009). Бактерії можуть потрапити у НДШ з контамінованими матеріалами, наприклад з конденсатом вентилятора, аерозолем небулайзера, емболами з біоплівки ЕТ тощо (Craven D., 2006). З часом концентрація бактерій і запальні зміни критично збільшуються. Проте чи призведе це до ВАТБ/ВАП, значною мірою залежить від вірулентності мікроорганізмів та механізмів захисту макроорганізму (рис. 1).
Вірулентність бактерій дуже варіабельна, навіть у межах одного виду. Для прикладу, смертність при інфекції, спричиненій штамами P. aeruginosa, які містять ендотоксин ІІІ, у 7 разів вища порівняно зі штамами, які його не містять (El Solh A. et al., 2008). Захист легень забезпечують такі механізми: механічні (мукоциліарний кліренс), клітинні (поліморфноядерні лейкоцити (ПЯЛ), макрофаги й утворені ними цитокіни) та гуморальні (імуноглобуліни класів A, G, M, система комплементу). Їх ефективність щодо зупинки та елімінації бактерій, які колонізують НДШ, визначає клінічний результат (Tablan O. et al., 2004; Aujla S. et al, 2008). За умов високої вірулентності та/або зниження захисту виникає ВАТБ з гнійним бронхіолітом, що суттєво підвищує ризик ураження альвеол і виникнення ВАП (Craven D., Hjalmarson K., 2010). Результати аутопсій свідчать, що між трахеобронхіальними і пневмонічними процесами є прямий зв’язок (Nseir S., Marquette C., 2003).
При ВАП виникає значне пошкодження тканини легень, поглиблюються порушення оксигенації і значно підвищується ризик таких ускладнень, як емпієма, абсцес легень, вторинна бактеріємія, шок, смерть (Chastre J., Fagon J., 2002). Тому оптимальною стратегією є припинення переходу ВАТБ у ВАП, до пошкодження легень (Craven D. et al., 2009).
Діагностика. В інтубованого пацієнта беруть матеріал для мікробіологічного дослідження. Це ЕТА, з якого роблять забарвлений за Грамом мазок для мікроскопії, що дає змогу визначити наявність і характер запалення за кількістю ПЯЛ і містить інформацію про морфологію збудника; наявність бактерій у мазку переважно корелює з результатами посіву ≥105 мікроорганізмів/мл. Посів ЕТА допомагає визначити вид збудника та чутливість його до антибіотиків (рис. 1). Багато авторів уважають, що напівкількісний і кількісний методи оцінки росту бактерій у культурах ЕТА дають змогу диференціювати колонізацію та інфекцію (ВАТБ/ВАП), яка переважно виникає за умов помірного-значного росту бактерій при напівкількісній оцінці та ≥105-6 КУО/мл при кількісній оцінці культури (Nseir S. et al., 2002; Dallas J., Kollef M., 2009; Craven D. et al., 2013). У центрах, де не використовують цих критеріїв, є висока імовірність гіпердіагностики ВАТБ (Alves А., Pereira J., 2018).
Найбільшою проблемою у пацієнтів з підозрою на ВАТБ є диференціація з ВАП. Кількісна оцінка росту бактерій у зразках, добутих інвазивними методами з НДШ, як-от бронхоскопічний чи небронхоскопічний бронхоальвеолярний лаваж (БАЛ) чи зразки, добуті за допомогою бронхіальної щітки (ЗБЩ), допомагає покращити диференціацію. Через відсутність чітких діагностичних критеріїв ВАТБ та у зв’язку з подібністю результатів клініко-лабораторних досліджень, діагноз ВАТБ можна поставити тільки після виключення ВАП, критеріями якої є ріст бактерій ≥103 КУО/мл у ЗБЩ або ≥104 КУО/мл у БАЛ (Fagon J. et al., 2000). Пацієнтам із нижчими кількісними показниками росту при інвазивному заборі зразків безпечно не призначати антибіотиків (Croce M. et al., 1994; Bonten M. et al., 1997; Heyland D. et al., 1999; Fagon J. et al., 2000).
Іншим засобом диференціації ВАТБ і ВАП є виявлення легеневого інфільтрату. Проте в пацієнтів з попередніми інфільтратами, РДС, застійною серцевою недостатністю, пухлиною, ателектезом чи інфарктом легені це доволі складно. До того ж портативна рентгенографія грудної клітки у критично хворих пацієнтів часто дає низьку якість знімків, що ускладнює інтерпретацію (Klompas M. et al., 2008). Попередні дослідження продемонстрували, що тільки 68% ВАП можна діагностувати на підставі рентгенографії (Wunderink R. et al., 1992). Комп’ютерна томографія збільшує діагностичну чутливість приблизно на 44% (Syrjälä H. et al., 1998). Однак у нещодавно опублікованому багатоцентровому опитуванні майже половина опитаних центрів повідомили, що ніколи не розглядали можливості провести комп’ютерну томографію в критично хворих пацієнтів (Rodríguez A. et al., 2014).
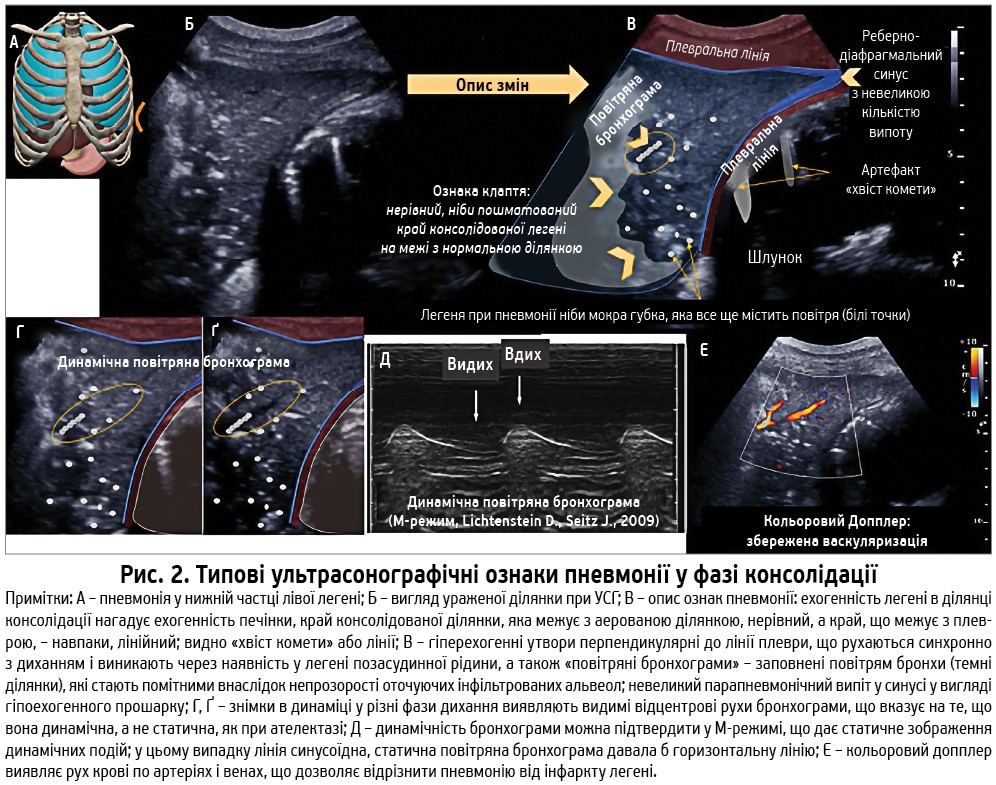
Виконана досвідченим фахівцем ультрасонографія (УСГ) легень є доступнішим методом візуалізації, що застосовується біля ліжка хворого. Доведено її високу чутливість і специфічність у діагностиці негоспітальної пневмонії серед пацієнтів, які не потребують МВЛ, особливо у випадках, коли рентгенографія легень недостатньо інформативна (Parlamento S. et al., 2009; Reissig A. et al., 2012). У проспективному дослідженні, яке охоплювало 99 пацієнтів з клінічними симптомами і рентгенологічними ознаками ВАП, виявлено, що наявність субплевральної консолідації і динамічні повітряні бронхограми є високочутливими і специфічними УСГ-ознаками ВАП, особливо у разі росту бактерій ≥104 КУО /мл у БАЛ або за наявності клінічних критеріїв, якщо результати культури негативні через застосування антибіотиків (Mongodi S. et al., 2016). Типові УСГ-ознаки пневмонії підсумовано на рисунку 2.
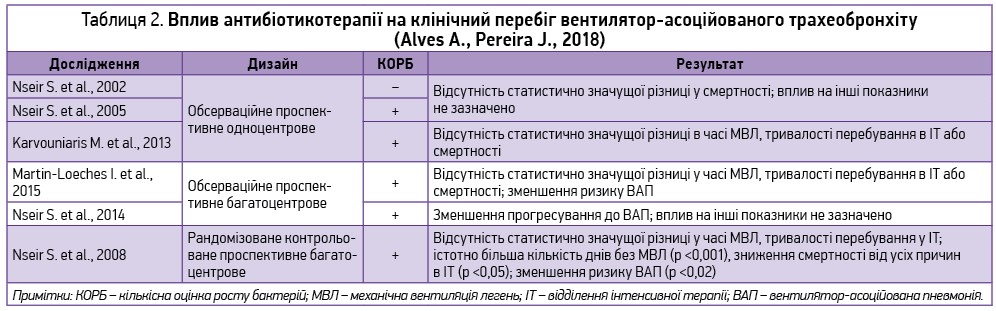
Призначати чи не призначати антибіотики? У таблиці 2 підсумовано дослідження, які вивчали вплив антибіотикотерапії на клінічний перебіг ВАТБ.
Питання доцільності призначення антибіотиків пацієнтам з ВАТБ не узгоджене, а його потенційні переваги чітко не визначені (ATS/IDSA guideline, 2005; Rodríguez A. et al., 2014). Припущення про користь від призначення їх здебільшого базуються на можливому скороченні часу МВЛ, терміну госпіталізації та зниженні ризику ВАП (Nseir S. et al., 2014; Martin-Loeches I. et al., 2015). Проте в літературі немає переконливих доказів таких переваг, незважаючи на істотне зниження інокуляції бактерій (Nseir S. et al., 2008). Дехто з авторів повідомляє про зменшення ймовірності ВАП (Nseir S. et al., 2008, 2014; Martin-Loeches I. et al., 2015), проте вірогідність інформації обмежена, бо в цих дослідженнях використовували лише рентгенографію легень. Крім того, зменшення прогресування до верифікованої ВАП не скорочує часу МВЛ, терміну госпіталізації та не знижує смертності (Alves А., Pereira J., 2018).
Окремі повідомлення про зниження летальності під впливом антибіотиків стосуються лише специфічних підгруп пацієнтів та показників смертності з усіх причин (Nseir S. et al., 2002, 2008). Ці докази суперечливі й не доведені іншими дослідженнями (Nseir S. et al., 2005; Karvouniaris M. et al., 2013; Martin-Loeches I. et al., 2015). У літературі немає виразних доказів, що ВАТБ підвищує смертність незалежно від застосування антибіотиків (Alves А., Pereira J., 2018).
Зважаючи на відсутність чітких переваг, вартість терапії, ризик виявів токсичності й потенційну небезпеку формування мультирезистентності бактерій, можна зробити висновок, що системні антибіотики не повинні рутинно призначатися пацієнтам з ВАТБ. Цей погляд поділяють нещодавно опубліковані рекомендації ведення пацієнтів з госпітальною та вентилятор-асоційованою пневмонією (ATS/IDSA guideline, 2016).
При вивченні перебігу трахеальної колонізації у 150 пацієнтів з МВЛ із застосуванням серійної кількісної оцінки росту культури БАЛ виявлено, що максимальна колонізація має місце пересічно за два дні до появи клінічних ознак ВАП (A’Court C. et al., 1993). У дослідженні, де після інтубації пацієнтам проводили серійну кількісну оцінку посівів ЕТА і призначали цільовий антибіотик при показниках >106 КУО/мл, спостерігалися кращі клінічні результати (табл. 2; Nseir S. et al., 2008). Тому кількісний моніторинг культури не лише сприяє ранній діагностиці інфекції, а й дає можливість вчасно призначити цільовий антибіотик (рис. 1).
Тривалість антибіотикотерапії при ВАТБ чітко не визначено, хоч віддають перевагу коротким курсам (до 7 днів), що зменшує імовірність настання резистентності (Craven D. et al., 2009).
Відсутність суттєвого покращання клінічного перебігу ВАТБ під впливом системних антибіотиків може зумовлюватися поганим проникненням і низькою концентрацією в дихальних шляхах (Mendelman P. et al., 1985). Застосування інгаляційних антибіотиків забезпечує високу концентрацію, ефективну місцеву дію з мінімальними системними виявами побічної дії (Russell C. et al., 2016). Такий спосіб терапії продемонстрував перспективні результати щодо зниження інокуляції бактерій (Palmer L. et al., 2008; Athanassa Z. et al., 2011; Palmer L., Smaldone G., 2014). Імовірно, це може зменшити ризик настання резистентності мікроорганізмів. Іншим методом профілактики є селективна деконтамінація, зокрема пероральна 2% розчином хлоргексидину, що також продемонструвало ефективне зменшення ризику ВАП (Liberati A. et al., 2004; Tantipong H. et al., 2008). Зазначені позитивні результати, здобуті під впливом місцевої терапії, потребують перевірки та підтвердження масштабними рандомізованими дослідженнями (Russell C. et al., 2016, Palmer L. 2015).
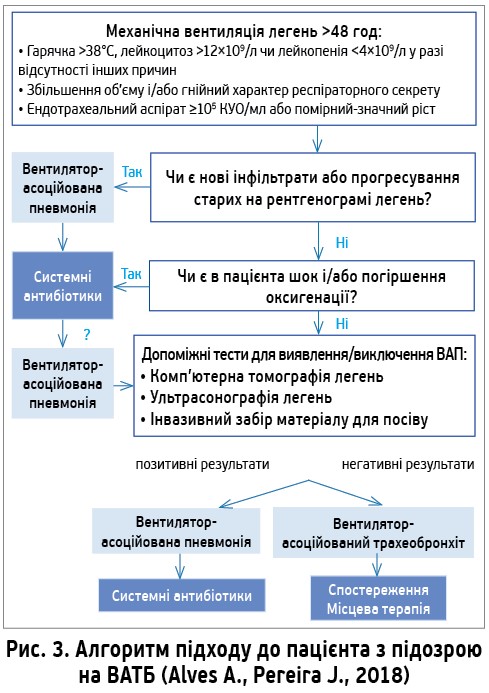 Утім, антибіотики показані пацієнтам з виявами септичного шоку чи погіршенням оксигенації (Athanassa Z. et al., 2011; Palmer L., Smaldone G., 2014). Саме ця категорія пацієнтів потребує ретельного обстеження для підтвердження чи спростування ВАП, імовірність якої за цих умов дуже висока (Kalil A. et al., 2016). Нещодавно запропоновано алгоритм підходу до пацієнта з підозрою на ВАТБ (рис. 3).
Утім, антибіотики показані пацієнтам з виявами септичного шоку чи погіршенням оксигенації (Athanassa Z. et al., 2011; Palmer L., Smaldone G., 2014). Саме ця категорія пацієнтів потребує ретельного обстеження для підтвердження чи спростування ВАП, імовірність якої за цих умов дуже висока (Kalil A. et al., 2016). Нещодавно запропоновано алгоритм підходу до пацієнта з підозрою на ВАТБ (рис. 3).
Висновки. З огляду на сучасне розуміння патогенезу вентилятор-асоційованих інфекцій, серійна кількісна оцінка результатів посіву дає змогу визначити цільовий антибіотик та оптимальний час його призначення. Така стратегія є більш обґрунтованою, ніж стратегія ранньої емпіричної системної антибіотикотерапії, яка здебільшого використовується у клінічній практиці.
Методологія обстеження, застосовувана в сучасних умовах, не виключає імовірності гіпер- чи гіподіагностики й не дає змоги чітко диференціювати ВАТБ і ВАП. Для покращання диференціації варто застосовувати сучасні методи візуалізації легень (КТ, УСГ) та проводити кількісну оцінку результатів посіву матеріалу, добутого інвазивними методами. Потрібно проводити подальші дослідження, на підставі яких будуть сформульовані єдині діагностичні критерії ВАТБ, що дасть змогу провести достовірну оцінку користі від системної чи місцевої антибіотикотерапії.
На підставі доступних сьогодні доказів можна зробити висновок, що системна антибіотикотерапія не призводить до статистично значущого зменшення часу МВЛ, тривалості перебування в ІТ та зниження смертності, але зменшує колонізацію та ризик ВАП і показана пацієнтам з проявами септичного шоку і/або порушеннями оксигенації. Через високу імовірність ВАП цій категорії пацієнтів особливо показані високочутливі додаткові методи діагностики.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 17 (462), вересень 2019 р.