18 жовтня, 2019
Зниження серцево-судинного ризику: як підвищити ефективність гіполіпідемічної терапії?
Якщо призначена пацієнтові доза статину не забезпечує досягнення цільового рівня холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ), рекомендована титрація дози препарату. Однак для пацієнтів високого серцево-судинного ризику ефективнішим може бути додавання до стартової дози статину езетимібу – гіполіпідемічного засобу, що селективно пригнічує абсорбцію ХС у кишечнику.
Лікування дисліпідемії, зокрема зниження підвищеного рівня ХС ЛПНЩ, є невід’ємною складовою ведення пацієнтів із серцево-судинним (СС) ризиком. У численних генетичних, епідеміологічних та клінічних дослідженнях було доведено ключову роль ХС ЛПНЩ у формуванні атеросклерозу, а також пряму залежність між вмістом ХС ЛПНЩ та ймовірністю розвитку ішемічної хвороби серця (ІХС) (Ference et al., 2017). На сьогодні не викликає сумніву, що зниження рівня ХС ЛПНЩ скорочує вірогідність атеросклеротичних серцево-судинних захворювань (ССЗ). На кожен 1 ммоль/л зменшення концентрації ХС ЛПНЩ у крові можна очікувати зниження відносного ризику розвитку ІХС приблизно на 20% (Ference et al., 2017).
Згідно з настановою Європейського товариства кардіологів і Європейського товариства атеросклерозу (ESC/EAC, 2019), для пацієнтів із дуже високим СС-ризиком рекомендований цільовий рівень ХС ЛПНЩ <1,8 ммоль/л (або зниження щонайменше на 50%), якщо вихідний показник ХС ЛПНЩ становить 1,8‑3,5 ммоль/л. Відповідно, для хворих із високим СС-ризиком потрібно досягти цільового рівня ХС ЛПНЩ <2,6 ммоль/л (або зниження щонайменше на 50%), якщо вихідний вміст ХС ЛПНЩ становить 2,6‑5,2 ммоль/л. В осіб із низьким або помірним СС-ризиком слід розглянути цільовий рівень ХС ЛПНЩ <3,0 ммоль/л.
Досягти зменшення концентрації ХС ЛПНЩ можна різними шляхами: блокуванням адсорбції ХС у кишечнику (езетиміб), інгібуванням біосинтезу ХС (статини), збільшенням кількості рецепторів та, відповідно, посиленням захоплення ХС ЛПНЩ клітинами печінки (інгібітори PCSK9).
Статини – препарати, що контролюють синтез ХС у печінці людини шляхом інгібування ферменту 3-гідроксил‑3-метилглутарил-коферменту А редуктази. Згідно з рекомендаціями ESC/EAC (2019) та Американської асоціації серця й Американської колегії кардіологів (AHA/ACC, 2018), це лікарські засоби першої лінії у терапії гіперхолестеринемії або комбінованих гіперліпідемій із метою профілактики ССЗ. У великому метааналізі CTT, що спирався на дані 26 рандомізованих клінічних досліджень за участю 170 тис. пацієнтів, було показано, що зниження рівня ХС ЛПНЩ на кожен 1 ммоль/л із використанням лише статинів супроводжується зменшенням смертності через будь-які причини на 10%, внаслідок ІХС – на 20%, ризику розвитку основних СС-ускладнень – на 23%, інсульту – на 17% (Baigent et al., 2010).
Окрім того, терапія статинами не завжди є ефективною щодо досягнення цільових рівнів ХС ЛПНЩ, особливо серед хворих високого та дуже високого ризику. Дослідники Akyea et al. (2019) спостерігали за 165 тис. пацієнтів без ССЗ в анамнезі, яким було призначено гіполіпідемічну терапію. Було показано, що понад 50% не досягли цільового рівня ХС ЛПНЩ. Це значно підвищило їхній ризик ССЗ, зокрема ІХС, інсультів та захворювань периферичних артерій. Ще гірша ситуація спостерігається серед осіб із дуже високим СС-ризиком. Епідеміологічні дослідження DYSIS І та ІІ мали на меті оцінити ефективність контролю гіперліпедемії у пацієнтів, які отримують статини. Результати показали, що в реальній клінічній практиці цільового рівня ХС ЛПНЩ досягає низький відсоток хворих із дуже високим СС-ризиком. Так, у дослідженні DYSIS ІІ, в якому взяли участь більш ніж 10 тис. осіб із дуже високим СС-ризиком, цільовий рівень ХС ЛПНЩ <1,8 ммоль/л спостерігався лише у 29,4% пацієнтів із ІХС та 18,9% із гострим коронарним синдромом (ГКС) (Gitt et al., 2017).
Якщо не вдається досягти цільового рівня ХС ЛПНЩ при монотерапії статином, рекомендована титрація дози препарату, а за її неефективності – призначення комбінованого лікування: статин + езетиміб або секвестранти жовчних кислот, або інгібітор PCSK9 (ESC/EAC, 2019). Але, як показують клінічні випробування, для пацієнтів високого СС-ризику замість титрації дози статину кориснішим може бути додавання езетимібу до вихідної дози статину.
Довідка «ЗУ»
Езетиміб – представник класу гіполіпідемічних засобів, які селективно пригнічують інтестинальну абсорбцію ХС і відповідних рослинних стеролів. Молекулярною мішенню езетимібу є переносник стеролів NPC1L1, що відповідає за всмоктування ХС та фітостеролів у кишечнику. Езетиміб не впливає на абсорбцію тригліцеридів, жирних, жовчних кислот, прогестерону, етинілестрадіолу або жиророзчинних вітамінів А і D.
Фармакокінетика. Езетиміб є перорально активним. Одночасний прийом їжі не впливає на його пероральну біодоступність. Після прийому внутрішньо езетиміб швидко всмоктується та активно кон’югує з утворенням фармакологічно активного глюкуроніду. Езетиміб та езетиміб-глюкуронід зв’язуються з білками плазми людини на 99,7 і 88‑92% відповідно. Вони повільно виводяться із плазми крові у процесі кишково-печінкової рециркуляції. Період напіввиведення обох речовин становить приблизно 22 год.
Езетиміб локалізується на щітковій смужці тонкої кишки й пригнічує абсорбцію ХС, зменшуючи доставку інтестинального ХС у печінку; статини знижують синтез ХС у печінці – разом ці механізми забезпечують його додаткове зменшення. Приймання езетимібу зі статином ефективно знижує ризик виникнення СС-ускладнень у пацієнтів з ІХС та ГКС в анамнезі.
Дослідження ACTE
Розглянемо детальніше випробування ACTE, в якому оцінювали ефективність та безпеку додавання езетимібу до розувастатину порівняно з підвищенням дози розувастатину в пацієнтів із гіперхолестеринемією та високим СС-ризиком (Bays et al., 2011).
Первинною метою дослідників було порівняння ефективності додавання езетимібу до розувастатину (5 або 10 мг) порівняно з подвоєнням дози розувастатину (із 5 до 10 мг/добу або з 10 до 20 мг/добу) щодо зниження ХС ЛПНЩ. До спостереження були залучені пацієнти з гіперхолестеринемією, високим та дуже високим ризиком розвитку ІХС, які не досягали рівня ХС ЛПНЩ, рекомендованого для лікування дорослих Національною освітньою програмою США з холестерину (NCEP ATP III), а саме <2,6 ммоль/л для осіб високого та дуже високого ризику без атеросклерозу судин та <1,8 ммоль/л для хворих дуже високого ризику з атеросклерозом судин.
Додатковими завданнями дослідження були порівняння ефективності терапії щодо зниження ХС ЛПНЩ залежно від стартової дози розувастатину, досягнення рекомендованого NCEP ATP III вмісту ХС ЛПНЩ <1,8 або <2,6 ммоль/л, зміна відносно вихідного значення рівня інших ліпідів, а також оцінка безпеки терапії.
Матеріали й методи
До мультицентрового (57 центрів у 10 країнах) рандомізованого подвійного сліпого у паралельних когортах дослідження ефективності та безпеки додавання езетимібу до розувастатину порівняно з титрацією дози розувастатину в пацієнтів із гіперхолестеринемією та високим ризиком ІХС були включені чоловіки та жінки віком від 18 до 79 років. Це були пацієнти з гіперхолестеринемією та високим ризиком ІХС (пацієнти із ≥2 факторами ризику, що відповідає 10-річному ризику розвитку ІХС за Фрамінгемською шкалою 10‑20%), дуже високим ризиком ІХС без атеросклерозу судин (хворі з вірогідністю ІХС, еквівалентною такій при цукровому діабеті або ≥2 факторами ризику, що відповідає 10-річному ризику ІХС за Фрамінгемською шкалою >20%) або дуже високим ризиком ІХС за наявності атеросклерозу судин (пацієнти зі встановленим діагнозом ІХС або з імовірністю, еквівалентною такій при ІХС та інших атеросклеротичних захворюваннях – хворобах периферичних артерій, атеросклерозі аорти або сонних артерій).
До участі залучалися пацієнти, які приймали розувастатин у дозі 5 або 10 мг або інші гіполіпідемічні препарати протягом ≥6 тижнів до скринінгу або не отримували ані статинів, ані езетимібу впродовж 6 тижнів до скринінгу. В осіб із високим або дуже високим ризиком без атеросклерозу судин рівень ХС ЛПНЩ до рандомізації мав складати ≥2,6, але ≤4,2 ммоль/л. У хворих із високим ризиком ІХС та атеросклерозом судин вміст ХС ЛПНЩ мав бути ≥1,8, але ≤ 4,2 ммоль/л; тригліцеридів (ТГ) натще – <3,9 ммоль/л. Після включення у дослідження пацієнти у відкритому режимі отримували розувастатин у дозі 5 або 10 мг/добу протягом вступного періоду 4‑5 тижнів залежно від СС-ризику, поточного застосування ліпідемічних засобів та рівня ХС ЛПНЩ.
Первинною кінцевою точкою ефективності була зміна концентрації ХС ЛПНЩ відносно вихідної, визначена для всіх учасників незалежно від доз препаратів. Вторинні кінцеві точки ефективності складалися з оцінки первинної для кожної групи окремо, а також частки осіб, які досягли цільового рівня ХС ЛПНЩ, рекомендованого NCEP ATP III, серед усіх учасників незалежно від доз препаратів. Інші вторинні кінцеві точки включали відсоток осіб, які досягли цільового рівня ХС ЛПНЩ, рекомендованого NCEP ATP III, для кожної групи окремо; пацієнтів, які досягли цільового рівня ХС ЛПНЩ <1,8 ммоль/л серед всіх учасників та для кожної групи окремо; зміну рівня інших ліпідів, ліпопротеїдів, С-реактивного білка (СРБ) для всіх учасників та для кожної групи окремо. Безпеку та переносимість оцінювали за всіма параметрами безпеки, які включали випадки побічної дії та дані лабораторних аналізів.
Довідка «ЗУ»
Розувастатин – синтетичний статин 4-го покоління з максимальною серед статинів гіполіпідемічною активністю щодо ХС ЛПНЩ (–65%), доброю переносимістю та безпекою, зокрема при застосуванні високих доз (40 мг/добу) (Schuster, Fox, 2004). Розувастатин – відносно гідрофільна сполука, яка селективно поглинається клітинами печінки, де зберігає активність. Препарат має найдовший серед статинів період напіввиведення та мінімально метаболізується системою цитохрому Р450, результатом чого є відсутність у розувастатину значущих лікарських взаємодій.
Розувастатин викликає не тільки істотне зниження рівня ХС ЛПНЩ, але й зменшення на 10‑35% рівня тригліцеридів і підвищення на 8‑14% ХС ліпопротеїнів високої щільності (McKenney, 2005).
Препарат продемонстрував ефективність як у вторинній, так і в первинній профілактиці ССЗ. У дослідженні JUPITER призначення розувастатину пацієнтам із нормальним рівнем ХС ЛПНЩ, але із високим С-реактивного білка привело до зменшення відносного ризику розвитку інфаркту міокарда на 54%, інсульту – на 48%, потреби в реваскуляризації – на 46%. На підставі цих даних FDА (США) та EMA (ЄС) затвердили нове на той час показання для застосування розувастатину – це первинна профілактика ССЗ (Schuster, Fox, 2004). Також розувастатин використовують для лікування пацієнтів високого та дуже високого СС-ризику.
Виразний гіполіпідемічний ефект розувастатину особливо важливий для амбулаторної клінічної практики, оскільки дозволяє скоротити терміни титрації дози препарату, забезпечує швидше настання сприятливого клінічного ефекту, підвищує прихильність пацієнта до терапії (Бубнова, Семенова, 2010).
Результати
Із 440 пацієнтів, які відповідали всім критеріям та взяли участь у дослідженні, 197 (44,8%) отримували розувастатин у відкритому режимі у дозі 5 мг/добу та 243 (55,2%) – 10 мг/добу протягом 4‑5 тижнів вступного періоду. Осіб, які приймали розувастатин у дозі 5 мг за вступний період (когорта І), рандомізували у групи, одна з яких застосовувала 5 мг розувастатину + 10 мг езетимібу, а в другій проводили титрацію стартової дози розувастатину до 10 мг. Хворих, які отримували розувастатин у дозі 10 мг впродовж вступного періоду (когорта ІІ), рандомізували у групи, одна з яких використовувала 10 мг розувастатину + 10 мг езетимібу, а у другій проводили титрацію стартової дози розувастатину до 20 мг. Із 440 пацієнтів 68% мали дуже високий ризик ІХС та атеросклероз, 18% – дуже високий ризик без атеросклерозу та 15% – високий ризик. Комплаєнс був високим в усіх групах і в середньому складав 98,5%.
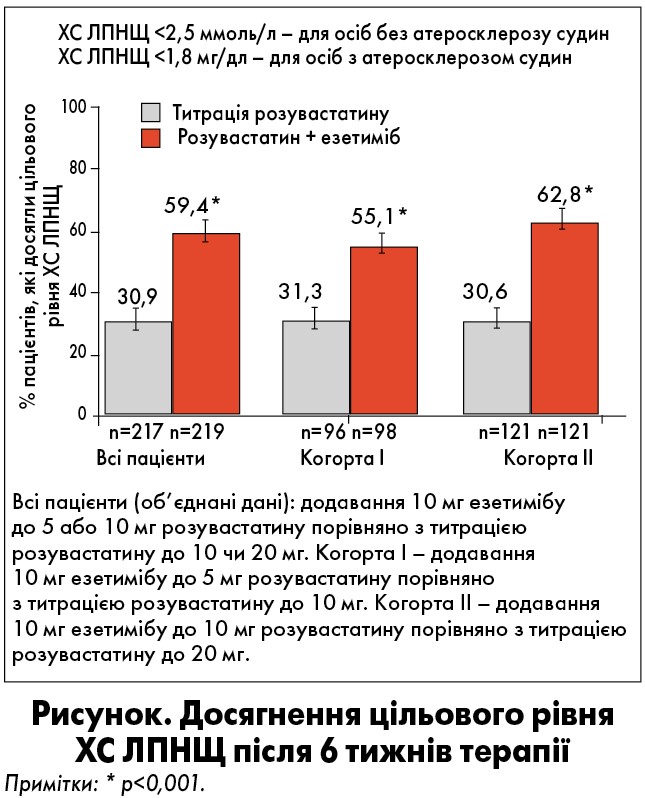 Додавання езетимібу по 10 мг до стартової дози розувастатину дозволило досягти суттєвішого зниження рівня ХС ЛПНЩ, ніж підвищення дози розувастатину як серед всіх пацієнтів (первинна кінцева точка), так і окремо у когортах (вторинна кінцева точка). Аналіз об’єднаних даних показав значно вищий відсоток досягнень цільових рівнів ХС ЛПНЩ (<2,6 ммоль/л для пацієнтів високого та дуже високого ризику без атеросклерозу судин та <1,8 ммоль/л – дуже високого ризику з атеросклерозом судин) у разі додавання до стартової дози розувастатину езетимібу по 10 мг, ніж при титрації у бік збільшення дози розувастатину (рисунок). У когорті ІІ (початкова доза розувастатину 10 мг) у групі 1 (у якій титрували дозу розувастатину до 20 мг) цільових рівнів ХС ЛПНЩ вдалося досягти у 30% хворих, тоді як в групі 2, де до розувастатину додавали езетиміб, аналогічний показник досяг рівня 62,8%.
Додавання езетимібу по 10 мг до стартової дози розувастатину дозволило досягти суттєвішого зниження рівня ХС ЛПНЩ, ніж підвищення дози розувастатину як серед всіх пацієнтів (первинна кінцева точка), так і окремо у когортах (вторинна кінцева точка). Аналіз об’єднаних даних показав значно вищий відсоток досягнень цільових рівнів ХС ЛПНЩ (<2,6 ммоль/л для пацієнтів високого та дуже високого ризику без атеросклерозу судин та <1,8 ммоль/л – дуже високого ризику з атеросклерозом судин) у разі додавання до стартової дози розувастатину езетимібу по 10 мг, ніж при титрації у бік збільшення дози розувастатину (рисунок). У когорті ІІ (початкова доза розувастатину 10 мг) у групі 1 (у якій титрували дозу розувастатину до 20 мг) цільових рівнів ХС ЛПНЩ вдалося досягти у 30% хворих, тоді як в групі 2, де до розувастатину додавали езетиміб, аналогічний показник досяг рівня 62,8%.
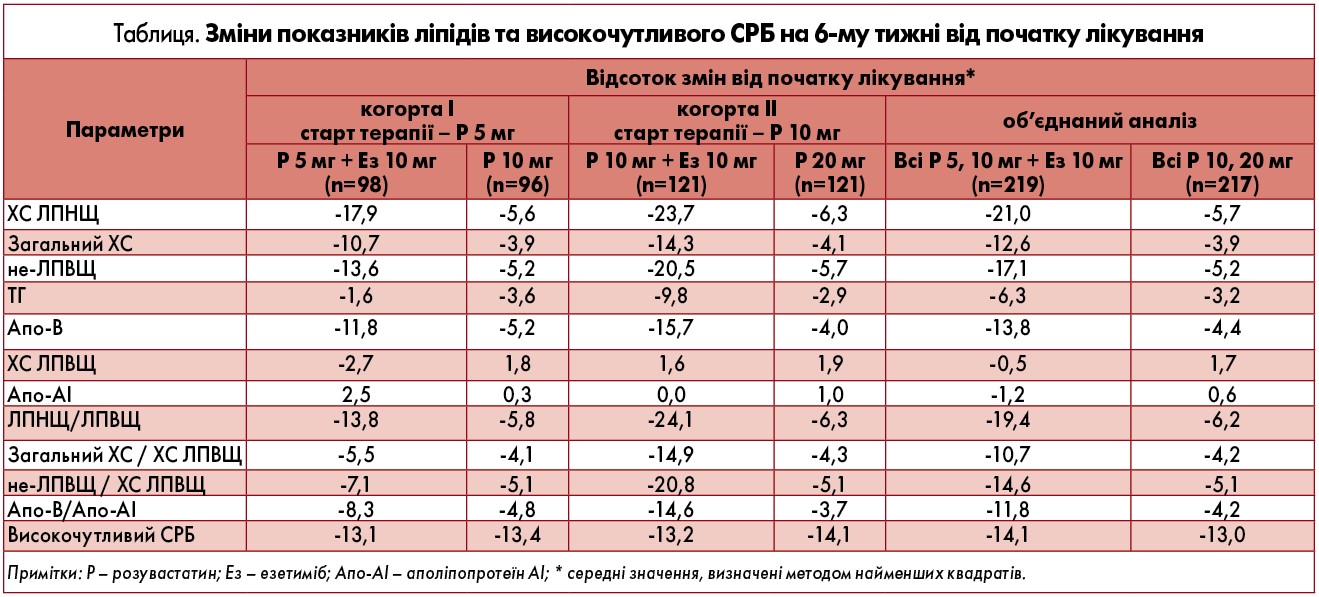
Аналіз об’єднаних даних показав, що додавання 10 мг езетимібу до стартової дози розувастатину привело до суттєвішого зниження рівня ХС ЛПНЩ порівняно з титруванням доз розувастатину в обох когортах (-21% проти -5,7% відповідно). Крім того, в обох когортах було показане значніше зменшення рівня ТГ у групах розувастатину з езетимібом, ніж у тих, де проводили титрування доз розувастатину (-6,3% проти -3,2% відповідно).
Аналіз інших ліпідів показав суттєвіше зниження рівня загального ХС, ХС не-ЛПВЩ та Апо-В у групах пацієнтів, які приймали розувастатин + езетиміб, порівняно із тими, що отримували подвоєні дози розувастатину (таблиця). Терапевтичний ефект езетимібу при додаванні до стабільної дози 5 або 10 мг розувастатину порівняно зі збільшенням його дози загалом зберігався незалежно від віку, статі, раси, ризиків, вихідного рівня ХС ЛПНЩ та ТГ, наявності метаболічного синдрому / діабетичного статусу.
Довідка «ЗУ»
На даний час на вітчизняному фармацевтичному ринку представлено препарат Розуліп® компанії «Егіс» (діюча речовина розувастатин в оптимальних дозах 10 і 20 мг). Крім того, нещодавно з’явився перший та єдиний на сьогодні комбінований препарат Розуліп® Плюс, до складу якого входять розувастатин та езетиміб у зручному дозуванні 10/10 і 20/10 мг.
Всі дози розувастатину (10, 20 мг) та комбінації розувастатин (5, 10 мг) + езетиміб (10 мг) загалом добре переносилися протягом шести тижнів дослідження. Аналіз об’єднаних даних для розувастатину (5 та 10 мг) + езетимібу (10 мг), а також щодо підвищення дози розувастатину (10 та 20 мг) показав співставну частоту небажаних явищ. Серйозних побічних ефектів, пов’язаних із прийманням препаратів, не спостерігалося.
Висновки
Згідно з результатами дослідження АСТЕ, зниження та досягнення цільового рівня ХС ЛПНЩ було суттєвішим при додаванні 10 мг езетимібу до стартової дози розувастатину, ніж при збільшенні дози розувастатину вдвічі. Додаткове використання езетимібу разом із 5 або 10 мг розувастатину дозволило знизити рівень ХС ЛПНЩ на 21%. Подвоєння стартової дози розувастатину викликало зменшення вмісту ХС ЛПНЩ на 6%. Зниження ХС ЛПНЩ спостерігалося незалежно від віку пацієнтів, статі, расової приналежності, ризиків, вихідних показників ХС ЛПНЩ, ТГ, наявності метаболічного синдрому / цукрового діабету.
Профілі безпеки та переносимості, що спостерігалися у дослідженні АСТЕ, були співставні для всіх варіантів лікування та відповідали описаним раніше для аналогічних за тривалістю курсів езетимібу та розувастатину. Серйозні побічні ефекти, пов’язані з прийманням препаратів, не спостерігалися, а частота реакцій з боку печінки, м’язів, ШКТ, шкіри була низькою та подібною до такої в інших випробуваннях комбінацій езетимібу зі статинами.
Підготувала Тетяна Ткаченко
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (65) вересень 2019 р.