23 січня, 2016
Использование количественного определения HBsAg для мониторинга естественного течения хронической HBV-инфекции
Поверхностный антиген вируса гепатита В (HBsAg) был открыт около 50 лет назад и по-прежнему является наиболее надежным маркером инфекции, вызванной вирусом гепатита В (HBV).
Значимость HBsAg состоит прежде всего в том, что он является составной частью оболочки вируса и играет ключевую роль в присоединении HBV к мембране гепатоцита, что инициирует инфекционный процесс. В нескольких исследованиях продемонстрированы значимость пептида в домене preS1 как ключевого в процессе специфического связывания с плазматической мембраной гепатоцита, а также возможность ингибирования этого процесса моноклональными антителами.
Кроме того, HBs-протеин является важным антигенным компонентом, индуцирующим защитные иммунные реакции в организме человека. Имеются данные о том, что обычный для HBV-инфекции избыток циркулирующего HBs-протеина может связывать специфические нейтрализующие антитела, предохраняя цельный вирион от иммунной атаки.Для клинициста HBsAg – один из наиболее надежных маркеров HBV-инфекции.
Хронологически вначале было налажено его качественное определение. Затем поиск маркеров, которые бы помогали мониторировать естественное течение заболевания и прогнозировать исходы противовирусной терапии (ПВТ), привел к открытию значимости количественного исследования HBsAg (qHBsAg).Первоначально qHBsAg рассматривался как альтернатива определению ДНК HBV для мониторинга вирусной нагрузки. Это было связано с тем, что стоимость исследования qHBsAg была невысокой и не требовала специального сложного оборудования, использующегося для ПЦР-анализа.
В 2004 г. Deguchi и соавт. впервые сообщили, что qHBsAg выше у пациентов с HBeAg-позитивным гепатитом и коррелирует с количественным содержанием ДНК вируса (r=0,862). Серия последующих работ подтвердила наличие упомянутой закономерности, хотя ряд авторов указали на явное несоответствие между содержанием ДНК вируса и qHBsAg у некоторых категорий больных.Современный интерес к qHBsAg вызван прежде всего данными о тесной связи между его содержанием и уровнем ковалентно-замкнутой циркулярной ДНК (cccDNA), которая представляет собой матрицу для репликации вируса, хранящуюся внутри ядра гепатоцита в виде микрохромосомы.
В современном арсенале средств для лечения хронического гепатита В (ХГВ) отсутствуют препараты, которые бы прямо воздействовали на cccDNA, что делает невозможным эрадикацию инфекции и обусловливает ее фактически пожизненную персистенцию в организме пациента.Непосредственное исследование содержания cccDNA в гепатоците пока недоступно в клинической практике, так как требует биопсии печени. Поэтому qHBsAg рассматривается, по сути, как суррогатный маркер cccDNA и важное дополнение к обследованию пациента с хронической HBV-инфекцией, но не как альтернатива измерению ДНК HBV. Связь между cccDNA, qHBsAg и количеством ДНК HBV при лечении адефовиром, впервые продемонстрированная Werle-Lapostolle и соавт., позволила рассматривать мониторинг qHBsAg как дополнительный маркер эффективности противовирусной терапии (ПВТ).Существующие методы детекции qHBsAg, такие как Architect QT (Abbott Laboratories) и Elecsys HBsAg II Quant (Roche Diagnostic), основаны на использовании антител к эпитопам S-протеина и не позволяют различать вирион-ассоциированный HBsAg, субвирусные частицы и HBsAg, продуцируемый из интегрированных последовательностей. С этим связаны дискордантные результаты исследований между qHBsAg и количественным содержанием ДНК HBV, но не сссDNA, в различные фазы болезни. Получаемые при помощи Architect значения обычно несколько выше, чем при использовании Elecsys. В то же время параллельные результаты использования обоих методов высоко коррелируют друг с другом (r=0,9881; p<0,001), за исключением тех случаев, когда в образцах содержатся YMDD-мутировавшие штаммы вируса. Установлено, что в редких случаях (около 5%), когда в сыворотке носителей присутствуют как HBsAg, так и anti-HBs, наличие антител не влияет на результаты количественного исследования HBsAg.В настоящем обзоре речь пойдет в основном о возможности использования количественного определения HBsAg для мониторинга естественного течения ХГВ.
Использование qHBsAg для мониторинга естественного течения ХГВ
При перинатальном инфицировании обычно развивается иммунотолерантная фаза HBV-инфекции, которая продолжается, как правило, первые 20-30 лет жизни и характеризуется наличием HBeAg, высокой виремией, нормальным уровнем аланинаминотрансферазы (АЛТ), а также отсутствием или минимальными гистологическими изменениями в печени. Далее следует фаза иммунного клиренса, что обычно ведет к исчезновению HBeAg и появлению антител к нему. Развивается фаза неактивного носительства вируса, или же, очень редко, происходит спонтанное излечение от HBV-инфекции. Однако у некоторых больных, несмотря на сероконверсию, наблюдается пролонгация неэффективного иммунного клиренса, сопровождающаяся наличием активного воспаления, повышенным риском развития цирроза печени, высоким уровнем АЛТ и ДНК HBV (хронический активный HBeAg-негативный гепатит В). Обычно разграничение фаз заболевания на основании упомянутых критериев не представляет особых сложностей. В то же время иногда очень сложно отличить больных активным HBeAg-негативным гепатитом от носителей вируса, если уровень трансаминаз в норме, а вирусная нагрузка превышает 2000 МЕ/мл. В этом случае существенным подспорьем может быть исследование qHBsAg.
HBeAg-позитивный ХГВ
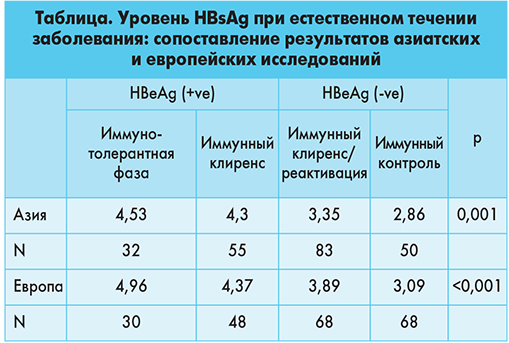
На основании результатов 2 перекрестных исследований показано, что уровень HBsAg был выше у пациентов с иммунотолерантной фазой болезни, чем в фазе иммунного клиренса (табл.): в европейском исследовании уровень HBsAg составил соответственно 4,96 и 4,37 log МЕ/мл, в азиатском – 4,53 и 4,03 log МЕ/мл. Одной из возможных причин более низкого уровня HBsAg в иммунотолерантную фазу в азиатском исследовании была возможность включения в исследование пациентов с АЛТ, превышающей норму менее чем в 2 раза, что не исключало наличия среди участников данной работы больных с начальной фазой иммунного клиренса. Другим объяснением может быть разница в уровне HBsAg, свойственная разным генотипам вируса. В эксперименте самая высокая экспрессия HBsAg наблюдалась при субгенотипе A2/Ae, затем – при A1/Aa и B2/Ba, а самая низкая – при субгенотипах B1/Bj, С и D. В исследовании, продолжавшемся 99±16 мес и включавшем пациентов с ХГВ, которые не получали ПВТ, qHBsAg у больных с иммунотолерантной фазой болезни составлял приблизительно 5 log МЕ/мл и был постоянным: медиана среднегодового отклонения составила -0,006 log МЕ/мл. В фазу иммунного клиренса уровень HBsAg в среднем составлял 4 log МЕ/мл без особой разницы между больными с активным заболеванием и пациентами с развившейся HBeAg-сероконверсией. Уровень HBsAg также оставался стабильным у HBeAg-позитивных пациентов с активным гепатитом с медианой ежегодного снижения 0,021 log МЕ/мл. Отношение HBsAg к HBV ДНК, отражающее соотношение субвирусных частиц к цельным вирионам, было схожим среди всех НВeAg-позитивных пациентов. В различных исследованиях медиана отношения HBsAg к HBV ДНК варьировала между 0,5 и 0,6 у всех НВeAg-позитивных больных с индивидуальными различиями от 0,1 до 2,0
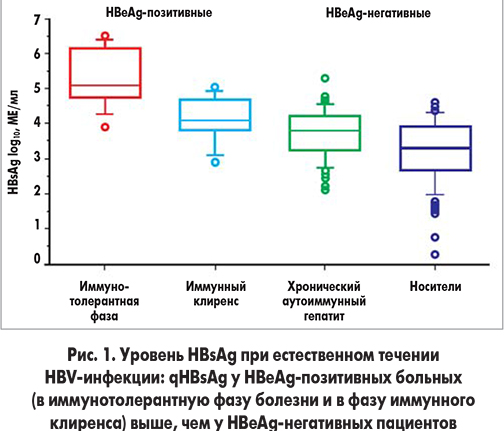
Таким образом, очень высокий уровень HBsAg (около 100 000 МЕ/мл) может быть свидетельством иммунотолерантной фазы инфекции. В фазу иммунного клиренса qHBsAg значительно снижается (рис. 1). И если между вирусной нагрузкой и qHBsAg в иммунотолерантную фазу и в фазу иммунного клиренса существует достаточно тесная связь (r=0,804 и r=0,773 соответственно), то в низкорепликативную фазу корреляция снижается (n=116, r=0,289; p=0,002) и отсутствует у пациентов с HBeAg-негативным ХГВ (n=67, r=0,146; p=0,237) или у больных, получающих лечение нуклеозидными/нуклеотидными аналогами (n=267).Это позволяет использовать qHBsAg для выделения группы активных носителей вируса и отличать их от больных с HBeAg-негативным ХГВ, протекающим с нормальным или пограничным уровнем трансаминаз.
К сожалению, работы, в которых было бы показано, что уровень HBsAg или соотношение HBsAg/HBV ДНК могут использоваться как предиктор HBeAg-сероконверсии, на сегодня отсутствуют. Продолжение в следующем номере.