8 листопада, 2019
Нейросимпозіум 2019: квінтесенція рекомендацій щодо терапії болю у спині та доцільність призначення вітамінів групи В за неврологічної патології
У межах щорічної міжнародної неврологічної конференції «Нейросимпозіум», що відбулася 10‑12 вересня 2019 р. в Одесі, професор Т.М. Слободін разом із професором О.Л. Товажнянською представили доповідь, присвячену актуальній темі болю у спині – поширеної скарги у клінічній практиці лікаря будь-якої спеціальності. Своєю чергою, доцент О.О. Клекот презентувала ґрунтовне пояснення доцільності призначення препаратів вітамінів групи В, вносячи цим зміни у парадигму терапії пацієнтів з ураженням як периферичної, так і центральної нервової системи.
Виступ професора кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Тетяни Миколаївни Слободін та професора кафедри неврології № 2 Харківського національного медичного університету, д. мед. н. Олени Леонідівни Товажнянської ґрунтувався на рекомендаціях щодо лікування пацієнтів із болем у спині, ухвалених останніми роками в Європейському Союзі загалом та у Великій Британії зокрема, а також у США.
На думку авторок доповіді, при роботі з пацієнтом, що страждає на біль у спині, передусім необхідно виключити «червоні прапорці»: інфекційну й онкологічну патологію, а також травматичне ураження.
Згідно з рекомендаціями Національного інституту охорони здоров’я та удосконалення медичної допомоги Великої Британії (NICE), якщо у пацієнта з люмбалгією немає ознак ураження корінців, слід призначати консервативну терапію і лише за браку поліпшення провести магнітно-резонансну томографію поперекового відділу хребта – рутинне обстеження таким методом піддається критиці.
 Із метою розв’язання питання доцільності терапії та поліпшення її успішності О.Л. Товажнянська підкреслила важливість використання шкали для скринінгу болю Кільського університету (Велика Британія), яка наведена в рекомендаціях NICE. Шкала містить вісім запитань, на які пацієнту пропонують відповісти, за кожну позитивну відповідь нараховується один бал. Чим більшу кількість балів набирає пацієнт у процесі тестування, тим вищими будуть ризик хронізації больового процесу та необхідність призначення медикаментозної терапії.
Із метою розв’язання питання доцільності терапії та поліпшення її успішності О.Л. Товажнянська підкреслила важливість використання шкали для скринінгу болю Кільського університету (Велика Британія), яка наведена в рекомендаціях NICE. Шкала містить вісім запитань, на які пацієнту пропонують відповісти, за кожну позитивну відповідь нараховується один бал. Чим більшу кількість балів набирає пацієнт у процесі тестування, тим вищими будуть ризик хронізації больового процесу та необхідність призначення медикаментозної терапії.
Для оптимізації консервативної терапії слід розуміти механізм больового синдрому при даній патології, який у більшості випадків полягає в іритації ноцицепторів внаслідок дії прозапальних факторів розвитку м’язового спазму. З точки зору патофізіології такий біль носить ноцицептивний чи ноцицептивно-запальний характер та потребує призначення:
- нестероїдних протизапальних препаратів (НПЗП), які є інгібіторами циклооксигенази – ключового ферменту біотрансформації арахідонової кислоти у простагландини, простациклін та тромбоксан;
- місцевих анестетиків;
- міорелаксантів: із доступних в Україні – тизанідин, циклобензаприн та тіоколхікозид.
 Щодо наступного використання рекомендацій Т.М. Слободін нагадала, що гострим вважається біль, який триває до чотирьох тижнів, підгострим – 4‑12 тижнів, хронічним – понад 12 тижнів. Нерідко у разі хронізації до патологічного процесу залучається корінець, розвивається радикулоневрит та наявний невропатичний компонент болю, який потребує призначення:
Щодо наступного використання рекомендацій Т.М. Слободін нагадала, що гострим вважається біль, який триває до чотирьох тижнів, підгострим – 4‑12 тижнів, хронічним – понад 12 тижнів. Нерідко у разі хронізації до патологічного процесу залучається корінець, розвивається радикулоневрит та наявний невропатичний компонент болю, який потребує призначення:
- антиконвульсантів: габапентину, прегабаліну (блокада каналів Na+ та Ca2+ периферичних нервів);
- антидепресантів, що інгібують зворотне захоплення серотоніну й норадреналіну, блокують Na+-канали та є антагоністами N-метил-D-аспартатних (NMDA) рецепторів;
- опіоїдних анальгетиків.
Оптимальна терапія необхідна, адже за тривалого перебігу больового синдрому залучаються надсегментарні відділи, у пацієнта активується мікроглія та розвиваються центральна сенситизація, гіперактивація заднього рогу та мигдалин.
За словами О.Л. Товажнянської, у низці досліджень було переконливо доведено, що додавання полівітамінних препаратів дозволяє оптимізувати алгоритм протибольової терапії та знизити ризик виникнення побічних реакцій завдяки зменшенню дозування або тривалості приймання основних препаратів, а також контролювати больовий синдром за рахунок:
- зниження гіпералгезії та гіперзбудливості нейронів;
- посилення синтезу серотоніну, дофаміну та ГАМК, зниження кінуреніну;
- поліпшення енергообміну й метаболізму, сприяння регенерації та ремієлінізації нервів.
 Доцент кафедри клінічної фармакології Вінницького національного медичного університету імені М.І. Пирогова, к. мед. н. Олександра Олексіївна Клекот присвятила лекцію раціональному використанню вітамінів групи В у неврології з погляду клінічної фармакології. Як показали дослідження, «точкою прикладання» вітамінів на клітинному рівні є протеом, тобто білки, що є кофакторними елементами важливих хімічних реакцій та забезпечують фізіологічний перебіг процесів життєдіяльності у клітині. Протеомний аналіз дозволив виявити існування 78 В6-залежних білків, 22 В1-залежних та 24 В12-залежних протеїнів. Саме тому вражаючою є кількість білків, функціонування котрих залежить від наявності вітамінів. Утім, відомо про потрійний синергізм біологічної ролі В1-, В6- та В12-залежних білків, їхній функціональний взаємозв’язок у забезпеченні роботи ядра, мітохондрій, клітинного матриксу, мембрани, цитозолю, пероксисом. Тому при одночасному поповненні їхньої кількості вдається підтримувати фізіологічний баланс.
Доцент кафедри клінічної фармакології Вінницького національного медичного університету імені М.І. Пирогова, к. мед. н. Олександра Олексіївна Клекот присвятила лекцію раціональному використанню вітамінів групи В у неврології з погляду клінічної фармакології. Як показали дослідження, «точкою прикладання» вітамінів на клітинному рівні є протеом, тобто білки, що є кофакторними елементами важливих хімічних реакцій та забезпечують фізіологічний перебіг процесів життєдіяльності у клітині. Протеомний аналіз дозволив виявити існування 78 В6-залежних білків, 22 В1-залежних та 24 В12-залежних протеїнів. Саме тому вражаючою є кількість білків, функціонування котрих залежить від наявності вітамінів. Утім, відомо про потрійний синергізм біологічної ролі В1-, В6- та В12-залежних білків, їхній функціональний взаємозв’язок у забезпеченні роботи ядра, мітохондрій, клітинного матриксу, мембрани, цитозолю, пероксисом. Тому при одночасному поповненні їхньої кількості вдається підтримувати фізіологічний баланс.
Нині у клінічній практиці препарати вітамінів частіше призначають за умови виявлення відповідного дефіциту. Їхнє використання, наприклад, при таких генетичних аномаліях, як хвороба «кленового сиропу» (порушення обміну амінокислот, за якого сеча набуває характерного запаху), або за патології центральної та периферичної нервової систем є актуальним та перспективним напрямом терапії. Це зумовлено асоціацією клінічних проявів неврологічної патології та дефіцитом таких вітамінів:
- тіамін (вітамін В1): норма споживання – 1,3‑2,6 мг/добу, дефіцит проявляється дистальною сенсорною поліневропатією, хворобою «кленового сиропу», раннім лактатацидозом;
- піридоксин (вітамін В6): норма споживання – 1,5‑3,0 мг/добу, дефіцит проявляється дистальною сенсорною поліневропатією з онімінням та парестезіями, нападами тоніко-клонічних судом;
- кобаламін (вітамін В12): норма споживання – 2,0‑3,0 мкг/д, проявами дефіциту є перніціозна анемія, підгостра дегенерація спинного мозку з дистальною сенсорною периферичною поліневропатією і випадінням сухожилкових рефлексів.
Нейротропна дія вітамінів групи В, за словами О.О. Клекот, ґрунтується на певних фізіологічних ефектах відповідних вітамінів. Так, В1 поліпшує функціонування нейронів за рахунок участі (як кофермент) у пентозофосфатному циклі, регуляції активності іонних каналів нейронів та нейроглії, передачі нервових імпульсів, захисті мембран від продуктів перекисного окиснення ліпідів, кінцевих продуктів гліколізу, ендотеліопротекції судин. В6 забезпечує провідність нейронів завдяки участі (як кофермент) у біосинтезі амінокислот та сфінголіпідів, регуляції імунної відповіді та процесів запалення в нейронах, когнітивних процесів у ЦНС, антиоксидантній дії, зв’язуванні вільних радикалів. В12 сприяє відновленню функціональності нейронів за рахунок поліпшення нервової провідності, регуляції процесів мієлінізації на генетичному рівні, посилення інтенсивності регенеративних процесів та ремієлінізації.
Тривалий час висловлювали сумнів щодо антиноцицептивного ефекту вітаміну В1, втім у численних дослідженнях доведено, що протибольовий ефект спостерігається за умови надмірного використання вітамінів групи В при їхньому дефіциті. Доклінічні результати свідчать, що вітамін В1 є структурним та функціональним елементом мембран нейронів, здійснює фізіологічну протекцію, стабілізацію мембран, блокує канали Na+ та пригнічує больову чутливість, зокрема при температурній гіпалгезії, зменшує запальний та невропатичний біль, тактильну алодинію. Так, вітамін В1 є ідеальним терапевтичним агентом при діабетичній, алкогольній поліневропатії та первинній дисменореї, що було підтверджено у дослідженнях.
Своєю чергою, препарати вітаміну В6 знижують температурну гіпералгезію, мають антиноцицептивну активність, компенсують зменшення вмісту даного вітаміну при запальних процесах у нервовій тканині, сприяють скороченню поведінкової та нейрофізіологічної больової чутливості, збільшують концентрацію серотоніну в різних ділянках мозку, чинять підтверджений знеболювальний ефект при діабетичній невропатії та тунельних синдромах.
Доведено переваги застосування вітаміну В12 при терапії больового синдрому в нижній частині спини.
Таким чином, антиноцицептивні ефекти вітамінів групи В полягають в усуненні ацидозу, стабілізації перекисного окиснення ліпідів, мембраностабілізації, пригніченні апоптозу, біосинтезі антиноцицептивних нейромедіаторів (норадреналін, серотонін, γ-аміномасляна кислота, дофамін), зменшенні вивільнення збуджувального нейромедіатора глутамату в синаптичних закінченнях, продукції медіаторів запалення.
Найбільший терапевтичний ефект можна отримати при вживанні комбінації вітамінів групи В. Також практикується додавання габапентинів, НПЗП, як-от диклофенаку, щодо чого зібрано найбільшу доказову базу та проведені метааналізи ефективності даної комбінації, наявні у Кокранівській базі даних. Виявлено, що комбінування 50 мг В1, 50 мг В6, 1 мг В12 із 50 мг диклофенаку дозволяє потенціювати анальгетичний ефект, зменшувати дозування та тривалість приймання знеболювального, звужувати спектр побічних явищ, підвищувати прихильність пацієнта до терапії та якість життя порівняно з монотерапією диклофенаком.
Однак О.О. Клекот наголосила, що через високу хімічну активність вітаміни групи В не можна вводити одночасно; наслідками порушення цього правила були: дестабілізація та деградація вітамінів у розчині; інактивація В12 внаслідок зміни рН реактивним В1; нівелювання ефективності В1 та В6 через дію іонів кобальту в складі В12; підвищення чутливості суміші до кисню, сонячного світла, температури.
Але розвиток фармацевтичної промисловості дозволив досягти максимальної стабілізації полівітамінних комплексів за рахунок додавання надлишку вітамінів у розчин, запобігання їхній дисоціації завдяки додатковим речовинам та регуляції кислотності розчину. Прикладом успішного комбінування вітамінів групи В є препарат, що містить:
- тіаміну гідрохлорид (В1, 100 мг), що має властивість добре розчинятись у воді, є високоактивним та зберігається при рН 2,7‑3,6;
- піридоксину гідрохлорид (В6, 100 мг), якому властива хороша розчинність у воді, висока стабільність у кислому розчині, чутливість до світла та можливість зберігання при рН 2,5‑3,5;
- ціанокобаламін (В12, 1 мг), що легко руйнується під впливом окисників і світла, група CN заміщується такими лігандами, як OH, NO2, SO3, CH3, однак вказані похідні під впливом цианід-іону знову перетворюються на ціанокобаламін.
Інноваційність та унікальність німецького препарату Нейробіон полягає у таких беззаперечних перевагах:
- кількісний вміст вітамінів забезпечує стійку комбінацію компонентів;
- ціанокобаламін стабілізується калію ціанідом (0,1 мг);
- необхідну кислотність забезпечує натрію гідроксид (73,0 мг);
- препарат не містить лідокаїн, що зумовлює низький ризик анафілаксії, аритмії та високу біодоступність у місці ін’єкції;
- не містить бензиловий спирт як консервант – це свідчить на користь препарату в плані безпеки щодо виникнення метаболічного ацидозу, гепатотоксичності та алергічних реакцій.
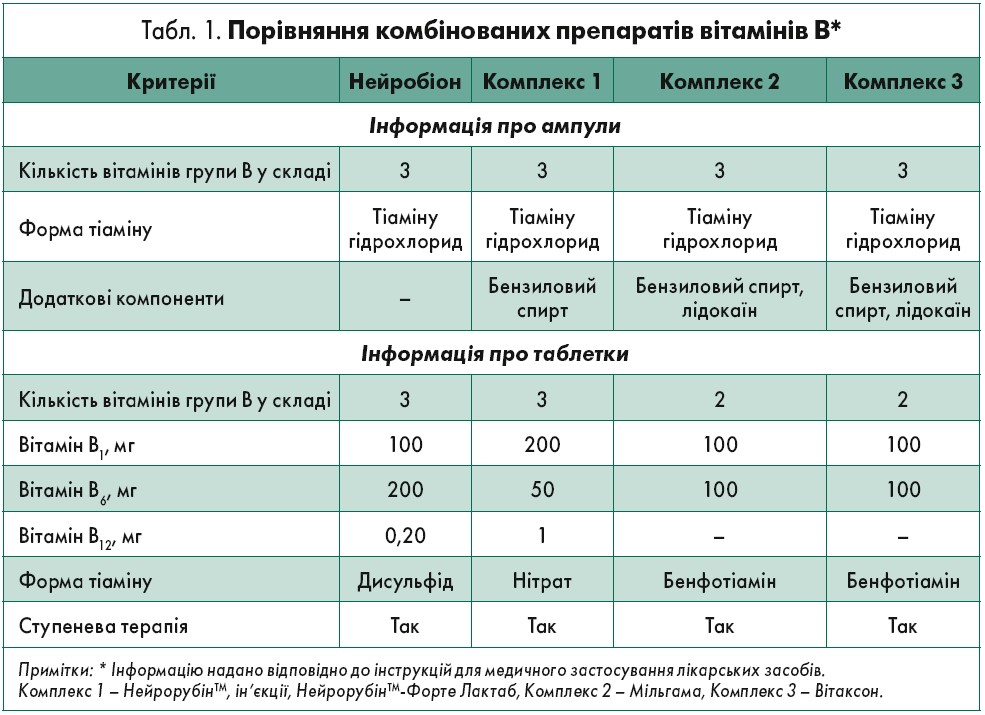
Якщо порівняти склад та характеристики відомих препаратів, що містять комбінації вітамінів В (табл. 1), Нейробіон є беззаперечним унікальним лідером стосовно безпеки. Бензиловий спирт, що входить до складу інших лікарських засобів із вітамінами групи В, належить до категорії «помірних токсинів». Він кумулюється в організмі за недостатньої метаболічної активності печінки, в якій у нормі перетворюється на гіпурову кислоту. В численних клінічних дослідженнях показано, що бензиловий спирт після парентерального введення викликає контактний дерматит, генералізовані алергічні реакції, нудоту, лихоманку, макулопапулярний висип, ангіоедему; в доклінічних випробуваннях на щурах встановлено його гемато- та гепатотоксичність, підвищення рівня глюкози натще. Тому безпечною дозою при парентеральному введенні вважається <200 мг.
Як відомо, прийманню полівітамінних препаратів пероральним шляхом притаманний ряд недоліків через появу фармакокінетичних проблем. Так, біодоступність вітамінів per os становить <10%, транспорт через мембрану ентероциту здійснюється повільно (8‑15 мг на добу), а у шлунково-кишковому тракті відбувається руйнування вітамінів тіаміназою.
У контексті зазначеного О.О. Клекот навела дані про обґрунтованість підвищення біодоступності пероральних препаратів вітамінів групи В, а саме створення жирозчинних форм тіаміну (В1). Так, бенфотіамін, октатіомін та тіаміну дисульфід добре всмоктуються у шлунково-кишковому тракті шляхом пасивної дифузії (до 50‑80% – у 4‑5 разів краще, ніж водорозчинний тіамін), не руйнуються тіаміназами кишківника, перетворюються на тіамін у таргетних клітинах.
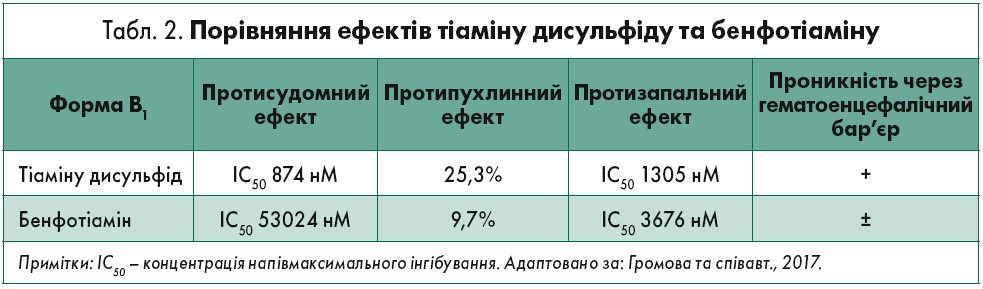
З огляду на позитивні властивості жиророзчинних форм вітамінів було створено таблетовану форму препарату Нейробіон, яка містить терапевтичні дози основних компонентів, що зумовлює досягнення антиноцицептивного ефекту: тіаміну дисульфіду (В1) – 100 мг; піридоксину гідрохлориду (В6) – 200 мг; ціанокобаламіну (В12) – 200 мкг. Важливим нюансом є можливість проникнення тіаміну дисульфіду через гематоенцефалічний бар’єр (табл. 2), тому препарат чинить повноцінну терапевтичну дію як на периферичну нервову систему, так і ЦНС.
Наявність двох лікарських форм, що були розроблені німецькою компанією Merck KGaA, дає можливість застосування ступінчастої терапії:
- ін’єкційна форма – протягом семи днів і додатково на 9-й та 12-й дні (досягнення стабільної біодоступності у нервовій тканині за рахунок створення терапевтичної концентрації);
- таблетована форма – на 8, 10, 11-й дні, а також щоденно впродовж 3-го та 4-го тижнів терапії (для профілактики рецидивів допускається приймання до трьох місяців).
Такий ступінчастий режим терапії, як було доведено у дослідженнях за участю пацієнтів із діабетичною поліневропатією, сприяє підвищенню швидкості нервової провідності, що є, безумовно, стратегічного важливим результатом терапії.
Додатково, з метою підтвердження профілю безпеки терапії, О.О. Клекот акцентувала увагу на тому, що вітамінотерапія не асоційована з канцерогенезом. Полівітамінні препарати не є джерелом енергії та пластичних матеріалів, натомість вони необхідні для створення протипухлинного імунітету на тканинному та клітинному рівні (особливо В1, В12), а також виконання ферментативних й ендокринних функцій в організмі. Так, у клінічних дослідженнях було виявлено, що застосування вітамінів В у фізіологічних дозах вагітними зменшує ризик розвитку пухлин мозку в дітей до п’яти років.
Наостанок О.О. Клекот зазначила, що завдяки застосуванню препарату Нейробіон компанії Merck KGaA пацієнтам гарантовано безпечну та високоефективну терапію комбінацією вітамінів В1, В6 та В12.
Підготувала Маргарита Марчук
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (50) жовтень 2019 р.