29 листопада, 2019
Роль монтелукасту в покращанні якості життя пацієнтів із персистуючою астмою

Бронхіальна астма (БА) визначається як хронічна непрохідність дихальних шляхів (ДШ) та їхня гіперреактивність, зумовлена імунологічно опосередкованим ремоделюванням. Етіологія БА є мультифакторною, включає складні генетичні механізми та зовнішні чинники, які грають взаємозамінні ролі (Maslan J., Mims J.W., 2014). Сьогодні астма – одне з найпоширеніших хронічних неінфекційних захворювань. БА посідає 16-те місце серед провідних причин інвалідності та 28-ме – серед основних причин тягаря хвороб, що вимірюються за скорегованими на інвалідність роками життя (disability-adjusted life years, DALYs). У Глобальному звіті щодо астми (The Global Asthma Report, 2019) наголошується, що у 2018 році на неї страждали 339 млн людей в усьому світі. Неконтрольована або неадекватно керована астма значуще знижує якість життя та підвищує ризик передчасної смерті.
Основними респіраторними симптомами астми є кашель, хрипи й задишка; усі ці симптоми спричинені хронічним запаленням ДШ. У комплекс патофізіологічних механізмів запального процесу при БА залучена ціла низка ефекторних клітин: еозинофіли, тучні клітини, нейтрофіли, макрофаги, Т-лімфоцити, дендритні та епітеліальні клітини ДШ. Усі вони генерують медіатори запалення – цитокіни та хемокіни, які відіграють ключову роль у розвитку патофізіологічних процесів при БА, відповідають за характер перебігу запалення ДШ та його хронізацію. Так, активовані Т-лімфоцити-хелпери 1 та 2 типів синтезують інтерлейкіни (IL) ІL‑1, IL‑5 та IL‑13, які стимулюють продукцію імуноглобуліну Е (IgE) та еозинофілів, сприяючи розвитку гіперреактивності ДШ. Тучні клітини слизової оболонки виділяють медіатори бронхоспазму, які включають гістамін, простагландини, а також цистеніл-лейкотрієни (CysLTs) – потужні бронхоконстриктори (Hon K.L. et al., 2014). Активація CysLTs веде до скорочення гладкої мускулатури, підвищення проникності судин, зниження мукоциліарного кліренсу, збільшення продукції слизу і стимулює міграцію лейкоцитів у вогнище запалення. Ремоделювання ДШ також опосередковано дією CysLTs, оскільки вони стимулюють не тільки гладку мускулатуру бронхів, але й проліферацію епітелію та відкладення колагену (Liu М., Yokomizo Т., 2015).
Довідка ЗУ
Лейкотрієни (ЛТ) – найважливіші прозапальні медіатори, синтезовані de novo клітинами дихальних шляхів (альвеолярними макрофагами, опасистими клітинами) та запальним інфільтратом (еозинофілами й нейтрофілами) при їх активації. Ці медіатори запалення опосередковують бронхоконстрикцію, гіперсекрецію слизу, підвищення судинної проникності, погіршення мукоциліарного кліренсу, хемотаксис еозинофілів у дихальні шляхи, проліферацію м’язових клітин бронхів. Крім того, ЛТ стимулюють диференціювання міофібробластів, що сприяє розвитку субепітеліального фіброзу. Механізм дії антагоністів лейкотрієнових рецепторів (АЛТР) базується на протидії ефектам ЛТ на рівні їх рецепторів. Зокрема, монтелукаст – специфічний конкурентний антагоніст рецепторів типу 1 цістеінілових ЛТ (сysLT1-рецепторів) у дихальних шляхах. Монтелукаст чинить протизапальну дію не тільки на дихальні шляхи, він характеризується доведеним системним протизапальним ефектом. Сучасні клінічні настанови рекомендують застосовувати АЛТР в якості монотерапії в пацієнтів із персистуючою БА як альтернативу або в поєднанні з топічними кортикостероїдами (ТКС), а також як альтернативу підвищенню дози ТКС або додаванню β2-агоніста тривалої діі (БАТД). У дослідженні Price і співавт. (2011), опублікованому в авторитетному виданні New England Journal of Medicine, в умовах реальної клінічної практики вивчали ефективність АЛТР у пацієнтів у віці від 12 до 80 років з погано контрольованою БА. Первинною кінцевою точкою була якість життя пацієнтів, оцінена за опитувальником MAQoLQ, після 2 міс лікування. У результаті було встановлено, що АЛТР еквівалентні ТКС на кроці 2 GINA (Глобальної ініціативи з менеджменту астми) і БАТД на кроці 3. У схожому дослідженні Chen і співавт. (2014) початок терапії з ТКС або АЛТР у дітей з астмою асоціювався з однаковою частотою загострень БА, що вимагають госпіталізації або призначення системних кортикостероїдів. Таким чином, в умовах реальної клінічної практики АЛТР демонструють дуже високу – порівнянну з ТКС – ефективність при БА, проте за певних фенотипах астми призначення АЛТР є безумовно виправданим (коморбідність БА та алергічного риніту, БА, індукована фізичним навантажанням, БА курців, літніх хворих тощо).
Наразі монтелукаст – найбільш широко використовуваний АЛТР, який ефективно впливає на численні біологічні та патофізіологічні механізми БА. В якості монотерапії або в комбінації з ТКС монтелукаст може зменшувати потребу в препаратах швидкого реагування (системних кортикостероїдах тощо), покращувати легеневу функцію, зменшувати симптоми і знижувати ризик загострень у дорослих пацієнтів та в дітей з БА.
Матеріали та методи дослідження
В 2019 році протягом 3 міс (із січня по березень) амбулаторно у відділенні пульмонології госпіталю м. Лахор проводилося відкрите проспективне інтервенційне дослідження. Проведення дослідження було схвалено інституціональним етичним комітетом, і всі пацієнти надали інформовану згоду. У дослідженні взяли участь 112 дорослих пацієнтів (середній вік становив 23,6±8,4 року), які хворіли на легку або помірної тяжкості астму не менше ніж 1 рік, лікувалися з цього приводу амбулаторно і раніше ніколи не приймали монтелукаст. Критеріями виключення стали пацієнти, які хворіли на астму менше 1 року, або нещодавно мали загострення, або раніше приймали монтелукаст для контролю симптомів. Учасники, які повідомили про будь-які несприятливі явища під час прийому монтелукасту, також були виключені з дослідження і припинили прийом препарату.
 Усі учасники в ході дослідження приймали монтелукаст у дозі 10 мг 1 раз на добу впродовж 4 тижнів в якості монотерапії, без додавання ІКС або БАТД. Якість життя пацієнтів оцінювалася за стандартною анкетою-опитуванням (Asthma Quality of Life Questionnaire – Standard, AQLQ-S). Пацієнти заповнювали анкету двічі: у день початку дослідження (0 день) та в кінці періоду спостережння, через місяць (30-й день). Загалом AQLQ-S являє собою 32-елементний інструмент оцінки якості життя, який включає 4 блоки питань щодо симптомів, щоденної активності, емоцій і контролю факторів довкілля. Кожен блок окремо та за загальною оцінкою вимірювався за 7-бальною шкалою Лірта; більш високий бал вказував на вищу якість життя та ефективність амбулаторного спостереження.
Усі учасники в ході дослідження приймали монтелукаст у дозі 10 мг 1 раз на добу впродовж 4 тижнів в якості монотерапії, без додавання ІКС або БАТД. Якість життя пацієнтів оцінювалася за стандартною анкетою-опитуванням (Asthma Quality of Life Questionnaire – Standard, AQLQ-S). Пацієнти заповнювали анкету двічі: у день початку дослідження (0 день) та в кінці періоду спостережння, через місяць (30-й день). Загалом AQLQ-S являє собою 32-елементний інструмент оцінки якості життя, який включає 4 блоки питань щодо симптомів, щоденної активності, емоцій і контролю факторів довкілля. Кожен блок окремо та за загальною оцінкою вимірювався за 7-бальною шкалою Лірта; більш високий бал вказував на вищу якість життя та ефективність амбулаторного спостереження.
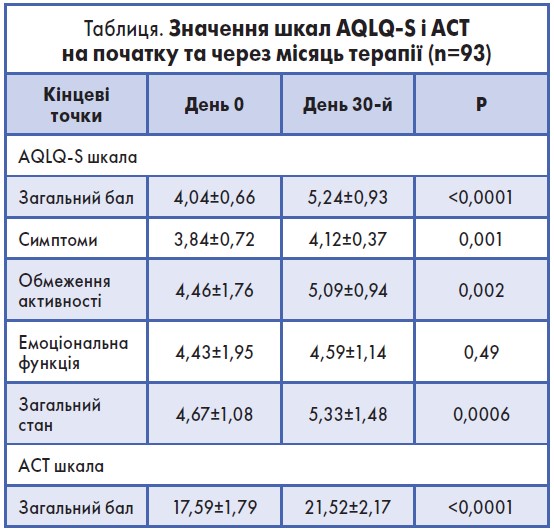
Ефективність лікування монтелукастом та рівень контролю симптомів оцінювалися за допомогою астма-тестів (Asthma Control Test, ACT). Ці тести пацієнти теж проходили двічі: у день початку дослідження та в кінці (через місяць). Середній показник АСТ <20 означав відсутність контролю астми, 20-24 свідчив про адекватний, а 25 – про відмінний контроль симптомів (табл.).
Результати та їх обговорення
Насамперед слід зауважити, що практична цінність дослідження полягає в тому, що воно підкреслило значення монотерапії монтелукастом в ефективному досягненні контролю астми та підвищенні якості життя пацієнтів. Так, за даними AQLQ-S, протягом періоду спостереження в пацієнтів було досягнуто статистично значуще покращання самопочуття в цілому (р≤0,0001) та підвищення щоденної активності внаслідок досягнення контролю симптомів і нормалізації емоційного стану зокрема. Якщо середній показник АСТ на початку періоду спостереження становив 17,59±1,79, то наприкінці цього періоду – 21,52±2,17.
Отримані під час наукової роботи результати корелюють з опублікованими раніше даними літератури, що також доводить роль монтелукасту в терапії персистуючої БА.
В якості ще одного прикладу можна навести дослідження MONICA (MONtelukast In Chronic Asthma); пацієнти з персистуючою астмою щоденно, протягом 6 міс, приймали монтелукаст у дозі 10 мг на тлі терапії ІКС та/або БАТД. Наприкінці періоду спостереження було зафіксовано статистично значуще покращання як за анкетами mini-AQLQ, так і за даними ACT (Virchow J.C. et al., 2010).
Метааналіз 50 РКД, проведений M. Miligkos та співавт. (2015), продемонстрував зниження ризику загострень БА до 0,60 у 6 дослідженнях із використання АЛТР в якості засобу монотерапії; у 4 дослідженнях коефіцієнт ризику загострення становив 0,80 за умови додавання АЛТР до ІКС.
У свою чергу, А. Bozek та співавт. (2012) виявили значуще зменшення середньої кількості випадків загострень астми (з 1,6 до 1,2 пацієнта щороку) після додавання мотелукасту до терапії ІКС та БАДТ протягом 2 років. Раніше W.A. Biernacki та співавт. (2005) також повідомляли про достовірне покращання результатів опитування за допомогою AQL у пацієнтів, яким монтелукаст був доданий до терапії ІКС.
У корейському дослідженні (Ye Y.M. et al., 2015) додавання монтелукасту до низькодозових ІКС при персистуючій астмі легкої та помірної тяжкості показало кращі результати в порівнянні зі збільшенням дози ІКС. При цьому було досягнуто підвищення показників об’єму форсованого видиху за 1-шу секунду та зменшення частоти загострень симптомів, що визначилося відповідними змінами на шкалі АСТ.
У дослідженні S.A. Khan та співавт. (2019) порівнювалась ефективність монотерапії монтелукастом та ІКС у пацієнтів із персистуючою астмою. Було показано, що в 1-й і 3-й тиждень монотерапії пікова швидкість видиху була достовірно вищою в групі монтелукасту (р<0,05) та зіставною в обох групах із 4-го по 8-й тиждень спостереження.
В іншому РКД вивчалася ефективність монотерапії монтелукастом у порівнянні з плацебо. Результати дослідження не виявили суттєвого впливу на АСТ, у той час як дані опитування його учасників за допомогою AQLQ-S продемонстрували значний прогрес (Baig S. et al., 2019).
У нещодавньому китайському дослідженні, проведеному X. Qu та співавт. (2018), було встановлено, що монтелукаст добре впливає на регуляцію клітинного балансу Т-хелперів 1 і 2 типів (співвідношення Th1/Th2), а також підсилює експресію CD4+CD25 і регуляторних Т-клітин. У пацієнтів з астмою це проявлялося зменшенням запалення ДШ та покращанням клінічних симптомів і легеневої функції.
M. Hoshino та співавт. (2018) довели, що, попри різні механізми дії, монтелукаст є еквівалентним тіотропію в якості додаткового засобу при терапії ІКС+БАДТ, який покращує легеневу функцію та знижує обструкцію бронхів.
Метааналіз 20 РКД, в яких вивчалося застосування монтелукасту як доповнення до терапії ІКС/БАТД у дорослих із персистуючою астмою, показав значне зменшення кількості загострень (ВШ=0,60), підвищення пікової швидкості видиху та зниження потреби в системних кортикостероїдах (Zhang Н.Р. et al., 2014)
Загалом дані наукових публікацій свідчать про позитивну роль монтелукасту в терапії БА легкого та середнього ступеня тяжкості. Препарат допомагає полегшити симптоми, зумовлені хронічним запаленням ДШ, зменшити частоту загострень і підвищити якість життя пацієнтів. Монтелукаст застосовується переважно як додатковий препарат до ІКС/БАДТ у пацієнтів, в яких не вдається досягти контролю симптомів на тлі терапії тільки ІКС та/або БАТД. Додаткова перевага монтелукасту також забезпечена можливістю його прийому 1 раз на добу та більш сприятливим фармакоекономічним аспектом проти ІКС або БАТД. Обидва ці фактори значуще підвищують прихильність пацієнтів до терапії.
Висновки
Монтелукаст є ефективним засобом контролю симптомів у пацієнтів із персистуючою астмою легкої та помірної тяжкості. Препарат можна застосовувати як доповнення до терапії ІКС та/або БАТД у пацієнтів із неконтрольованою астмою, а також як альтернативний засіб лікування.
Довідка ЗУ
На вітчизняному фармацевтичному ринку зареєстровано препарат Монтел (виробництва ПАТ НВЦ «Борщагівський ХФЗ») , одна таблетка якого містить 4, 5 або 10 мг монтелукасту. Після перорального прийому натще препарат швидко адсорбується з досягненням середньої плазмової концентрації протягом 3 год; бронходилатація наступає вже через 2 год після прийому. При цьому біодоступність препарату становить 64% і не залежить від прийомів іжі, препарат активно метаболізується в печінці й практично повністю виводиться з організму.
Монтел застосовується в якості додаткового засобу терапії у дітей та дорослих із персистуючою БА легкого й помірного ступеня тяжкості на тлі недостатнього контролю за допомогою ІКС та/або β2-агоністів короткої дії, які призначають на вимогу. Монтел також можна призначати разом з іншими препаратами, що застосовуються для запобігання загостренням або для тривалої терапї БА.
Важливими факторами, які забезпечують прихильність пацієнтів до лікування, є широкий профіль безпеки препарату, відсутність необхідності корекції дози у пацієнтів похилого віку з порушенням функції нирок або печінки, відсутність впливу на здатність керування транспортними засобами. Додатковими перевагами препарату Монтел є сприятливі фармакоекономічні характеристики, а також наявність трьох дозувань таблеток – для дітей різного віку та дорослих.
За матеріалами: Ayesha Ikram et al.,
Cureus. 2019 Jun; 11(6): e5046.
Підготувала Наталія Позднякова
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3 (48), жовтень 2019 р.


