3 грудня, 2019
Атезолізумаб у комбінації з хіміотерапією при плоскоклітинному НДРЛ IV стадії: заключний аналіз загальної виживаності в дослідженні IMpower131
РЕЛІЗ
Рандомізоване дослідження ІІІ фази IMpower131 було сплановано для оцінювання ефективності комбінації атезолізумабу та хіміотерапії (ХТ; карбоплатин + паклітаксел або наб-паклітаксел) у 1-й лінії лікування плоскоклітинного недрібноклітинного раку легені (НДРЛ) IV стадії [1].
Пацієнтів (n=1021) рандомізували 1:1:1 на групи А (атезолізумаб 1200 мг через кожні 3 тижні + карбоплатин ACU6 через кожні 3 тижні + паклітаксел 200 мг/м2 площі поверхні тіла через кожні 3 тижні), В (атезолізумаб + карбоплатин + наб-паклітаксел 100 мг/м2 1 раз на тиждень) та С (карбоплатин + наб‑паклітаксел). Пацієнти отримували 4 або 6 циклів ХТ та атезолізумаб до втрати клінічної користі, а потім – найкращу підтримувальну терапію. Частка пацієнтів із високою експресією ліганду білка програмованої клітинної смерті 1 (PD-L1) була однаковою у трьох групах.
Первинними кінцевими точками були виживаність без прогресування за оцінкою дослідника з використанням критеріїв RECIST 1.1 в ІТТ-популяції (тобто в усіх пацієнтів, які отримали принаймні 1 дозу досліджуваного препарату) та загальна виживаність (ЗВ), також в ІТТ-популяції [2].
На Всесвітній конференції з раку легені (WCLC), яка пройшла 7-10 вересня у Барселоні (Іспанія) за підтримки Міжнародної асоціації з вивчення раку легені (IASLC), професор Федеріко Капуццо з Італії представив заключні результати щодо ЗВ у дослідженні IMpower131.
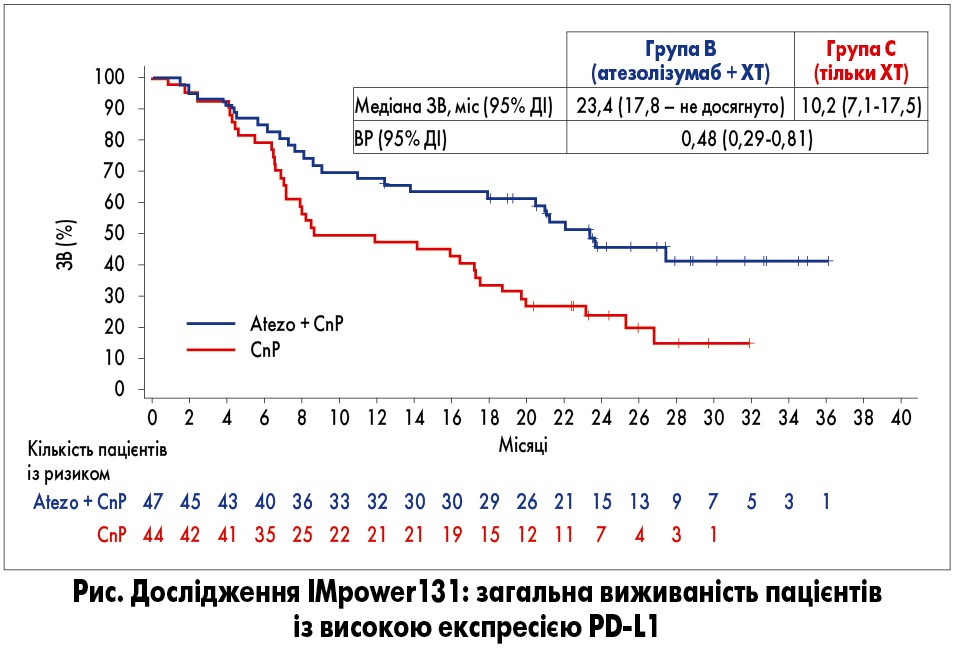
Медіана ЗВ в ІТТ-популяції становила 14,2 міс у групі В (атезолізумаб + ХТ) проти 13,5 міс у групі С (тільки ХТ), і ця різниця не досягла статистичної значимості. Проте у пацієнтів із високою експресією PD-L1 додавання атезолізумабу до ХТ значно подовжило ЗВ: медіана цього показника у групах В та С становила 23,4 vs 10,2 міс відповідно (рис.).
Пов’язані з лікуванням небажані події 3-4 ступеня спостерігалися у 68,0% пацієнтів групи В та в 57,5% хворих групи С; профіль безпеки застосованого лікування відповідав такому в попередніх аналізах.
«Дослідження IMpower131 надало нові докази ефективності імунотерапії у хворих на рак легені. Значне подовження виживаності при додаванні атезолізумабу до хіміотерапії у підгрупі з високою експресією PD-L1 підкреслює важливість біомаркерів для відбору пацієнтів», – зазначив професор Ф. Капуццо [3].
Література
- Jotte R.M., Cappuzzo F., Vynnychenko I. et al. IMpower131: Primary PFS and safety analysis of a randomized phase III study of atezolizumab + carboplatin + paclitaxel or nab-paclitaxel vs carboplatin + nab-paclitaxel as 1L therapy in advanced squamous NSCLC. J Clin Oncol. 2018; 36 (18 suppl; abstr LBA9000).
- Jotte R., Cappuzzo F., Vynnychenko I. et al. IMPOWER131: Final OS results of carboplatin + nab-paclitaxel ± atezolizumab in advanced squamous NSCLC. Presented at: IASLC 20th World Conference on Lung Cancer; September 7-10, 2019; Barcelona, Spain. Abstract OA14.02.
https://ascopost.com/news/september‑2019/final-overall-survival-results-of-impower131-trial-in-advanced-squamous-nsclc/
Підготував Олексій Терещенко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 3 (59), 2019 р.