21 грудня, 2019
Порушення ритму і провідності серця
 Під аритмією розуміють серцевий ритм, що відрізняється від нормального синусового ритму частотою, регулярністю і джерелом, а також порушенням зв’язку або послідовності між активацією передсердь і шлуночків. Порушення ритму серця, як правило, обумовлені різними захворюваннями, але також можуть виникнути самостійно. Це пов’язане, в основному, з наявністю кола re-entry (додаткові передсердно-шлуночкові шляхи проведення, тріпотіння передсердь), а також з чутливістю клітин-водіїв ритму, які можуть знаходитися у різних відділах серця, до адренергічних впливів.
Під аритмією розуміють серцевий ритм, що відрізняється від нормального синусового ритму частотою, регулярністю і джерелом, а також порушенням зв’язку або послідовності між активацією передсердь і шлуночків. Порушення ритму серця, як правило, обумовлені різними захворюваннями, але також можуть виникнути самостійно. Це пов’язане, в основному, з наявністю кола re-entry (додаткові передсердно-шлуночкові шляхи проведення, тріпотіння передсердь), а також з чутливістю клітин-водіїв ритму, які можуть знаходитися у різних відділах серця, до адренергічних впливів.
У структурі дитячої кардіологічної захворюваності та причин смертності порушення ритму серця займають провідне місце (60-70%). Їх поширеність серед дітей остаточно не відома, оскільки навіть у абсолютно здорових бувають епізоди тахі- і брадикардії, міграції водія ритму і поодинокі екстрасистоли. За даними М.А. Школьникової (1999), у клінічно здорових учнів найчастіше зустрічаються: міграція водія ритму (13,5%), брадикардія (3,5%), прискорений передсердний ритм (2,7%), екстрасистолія (1,9%), феномен (синдром) Вольфа – Паркінсона – Уайта (WPW, 0,5%), атріовентрикулярна блокада (АВБ) І ступеня (0,5%) і подовження інтервалу QT (0,3%).
Скарги пацієнтів з аритміями зазвичай зводяться до відчуття нерегулярної серцевої діяльності, нападів серцебиття або, навпаки, уповільнення роботи серця. Рідше порушення ритму серця супроводжуються задишкою, відчуттям важкості та болем у ділянці серця, синкопальними станами. Деяким порушенням ритму притаманна клініка важких розладів гемодинаміки, що виражаються нападами Морганьї – Адамса – Стокса або кардіогенного шоку.
Класифікація порушень ритму і провідності серця
На сьогоднішній день загальноприйнятою в Україні є класифікація порушень ритму і провідності серця, затверджена на VI Національному конгресі кардіологів України у 2000 р. (табл. 1).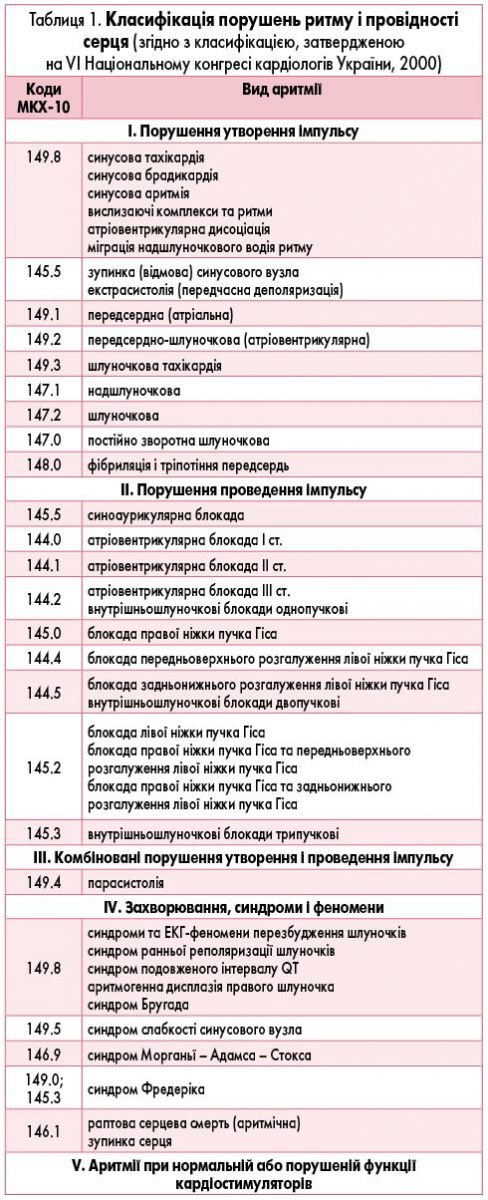
Згідно з цією класифікацією, всі порушення ритму і провідності серця у дітей поділяють на 5 груп:
- І – порушення утворення імпульсу;
- ІІ – порушення проведення імпульсу;
- ІІІ – комбіновані порушення утворення і проведення імпульсу;
- ІV – синдроми і феномени;
- V – аритмія при нормальній або порушеній функції кардіостимуляторів.
Порушення утворення імпульсу
Синусова тахікардія
Синусовою тахікардією називають стан, коли частота серцевих скорочень (ЧСС) перевищує вікові норми, при цьому зберігається правильний синусовий ритм.
В основі синусової тахікардії лежить підвищення автоматизму основного водія ритму – синоатріального вузла. Причинами її виникнення можуть бути різні ендогенні та екзогенні впливи: фізичне навантаження, розумове напруження, емоції, інфекція, лихоманка, анемія, гіповолемія, гіпотензія, дихальна гіпоксемія, ацидоз, гіпоглікемія, ішемія міокарда, гормональні порушення (тиреотоксикоз), міокардити, ревмокардити, інтоксикації, медикаментозні впливи. Синусова тахікардія може бути першою ознакою серцевої недостатності.
Синусова тахікардія у дітей зі здоровим серцем може бути обумовлена функціональними порушеннями в корі головного мозку і підкіркових ділянках, а також порушенням рівноваги тонусу вегетативної нервової системи з переважанням тонусу симпатичної іннервації.
Скаргами при синусовій тахікардії є серцебиття, відчуття тяжкості за грудиною.
Синусову тахікардію на електрокардіограмі (ЕКГ) доводиться диференціювати з надшлуночковими формами пароксизмальної тахікардії, тріпотінням передсердь з провідністю 2:1.
Проведення холтерівського моніторування ЕКГ при синусовій тахікардії у дітей не має необхідного рівня доказовості і не показане.
При лікуванні дитини із синусовою тахікардією слід визначити зовнішні фактори, що її викликають, і лікувати їх.
Для лікування симптоматичної синусової тахікардії використовують препарати, які пригнічують автоматизм синусового вузла і знижують тонус симпатичної нервової системи (b-адреноблокатори, дизопірамід, ізоптин, кордарон). Якщо походження синусової тахікардії явно неврогенне, доцільно вдатися до психотерапії, виключити з раціону міцний чай, каву, алкоголь. Також призначають невеликі дози транквілізаторів.
Синусова брадикардія
Синусовою брадикардією називається стан, коли ЧСС стає нижче за вікові норми, при цьому правильний синусовий ритм зберігається.
Синусова брадикардія зумовлена зниженням автоматизму синоатріального вузла. Основною причиною є підвищення тонусу блукаючого нерва. У нормі часто буває у спортсменів, однак може зустрічатися і при різних захворюваннях (мікседема, кардити, інфекції, підвищення внутрішньочерепного тиску), а також може мати медикаментозне походження (b-адреноблокатори, хінідинові препарати, кордарон, транквілізатори та ін.).
Клінічні ознаки синусової брадикардії можуть бути відсутні. Лише іноді пацієнти скаржаться на сповільнення ритму серця, слабкість, запаморочення. Надзвичайно виражена брадикардія може викликати ішемію мозку з явищами syncope.
Диференціюють синусову брадикардію на ЕКГ з синоаурикулярною блокадою 2:1, АВБ, вузловим ритмом.
На ЕКГ при синусовій брадикардії зберігаються всі основні ознаки нормального синусового ритму, окрім зниження його частоти.
Виразна синусова брадикардія може бути одним із симптомів синдрому слабкості синусового вузла. В такому разі провести диференціальну діагностику допомагає холтерівське моніторування ЕКГ.
Критеріями патологічної брадикардії, за даними холтерівського моніторування ЕКГ, є нижня межа ЧСС: у новонароджених – 80 і менше поштовхів за хвилину; у дітей 2-6 років – 60 і менше; у дітей 7-11 років – 45 і менше; у підлітків 12-16 років – 40 і менше.
Синусова аритмія
Синусовою аритмією називається неправильний синусовий ритм, обумовлений нерегулярним утворенням імпульсів у синоатріальному (СА) вузлі.
Найчастіше зустрічається дихальна синусова аритмія, при якій ЧСС збільшується на вдиху і зменшується на видиху. Часто зустрічається у дітей, з віком частота її в дитячій популяції знижується. Практично не має клінічної симптоматики, виявляється як нерегулярне серцебиття при аускультації або пальпації пульсу. На ЕКГ передсердно-шлуночковий комплекс такий же, як і при нормальному синусовому ритмі, за винятком розходжень в інтервалах Р-Р або R-R. Синусова аритмія не вимагає спеціального лікування і зникає тоді, коли пульс частішає.
Вислизаючі комплекси та ритми
Вислизаючі ритми (комплекси) є пасивними, ектопічними, з’являються на фоні пригнічення функції синусового вузла, запобігаючи виникненню епізодів асистолії. Оскільки автоматизм ектопічних центрів нижчий, ніж здорового СА-вузла, ЧСС при такому ектопічному ритмі, як правило, значно нижча за вікові норми, тому їх ще називають повільними.
Вислизаючий передсердний ритм виникає з передсердних вогнищ у періоди важкої синусової брадикардії або значної дисфункції синусового вузла. Частою причиною виникнення цієї аритмії є порушення вегетативної забезпеченості діяльності синусового вузла. Нерідко передсердні ритми спостерігаються у дітей з вегетативною дисфункцією. Проте причиною можуть бути запальні зміни в міокарді, вторинна кардіоміопатія.
Діагноз встановлюється згідно з результатами ЕКГ. За морфологією зубця Р розрізняють верхньо-, середньо- і ніжньопередсердні ритми.
Специфічного лікування немає. Терапія залежить від причини виникнення патології: протизапальні препарати при кардиті, кардіотрофічна терапія при вторинній кардіоміопатії і корекція вегетативних розладів при вегетативній дисфункції.
Атріовентрикулярні вузлові ритми з’являються при виникненні водія ритму в атріовентрикулярному вузлі. Епізоди атріовентрикулярного вузлового ритму реєструють у 19% новонароджених. Швидкість атріовентрикулярного вузлового ритму знаходиться, як правило, в діапазоні 40-60 ударів за хвилину.
На ЕКГ фіксується уповільнений ритм, зубець Р або відсутній, або негативний і розташований після комплексу QRS. Атріовентрикулярні вузлові ритми виникають у дітей з важкими кардитами, при отруєннях ліками (серцеві глікозиди, антиаритмічні препарати та ін.).
У лікуванні застосовують протизапальні та кардіотрофічні засоби, при отруєннях – антидоти чи відміняють препарат. Протипоказані препарати калію, β-адреноблокатори, серцеві глікозиди.
Ідіовентрикулярний вислизаючий ритм виникає, коли вищі водії ритму не здатні генерувати імпульси. Це буває, як правило, при важкому запальному і токсичному ураженні міокарда. Частота ідіовентрикулярного ритму складає 20-40 ударів на хвилину. На ЕКГ відсутній зубець Р, а шлуночковий комплекс розширений і деформований.
Атріовентрикулярна дисоціація
Атріовентрикулярна дисоціація – це стан, при якому передсердя і шлуночки не активуються синхронно, а скорочуються незалежно один від одного. Звичайно при атріовентрикулярній дисоціації ритм скорочення шлуночків або співпадає з ритмом скорочення передсердь, або перевищує його.
Ізоритмічна атріовентрикулярна дисоціація зустрічається при виразній синусовій брадикардії, коли частоти синусового і замісного ритмів приблизно однакові. Атріовентрикулярна дисоціація з інтерференцією виникає, коли частота ритму із нижніх відділів провідної системи перевищує частоту синусового ритму.
Атріовентрикулярну дисоціацію диференціюють з АВБ, при якій, на відміну від атріовентрикулярної дисоціації, ритм скорочення передсердь перевищує ритм скорочення шлуночків.
Лікування атріовентрикулярної дисоціації залежить від основного захворювання і його тяжкості.
Міграція надшлуночкового водія ритму
Міграція водія ритму виникає внаслідок ослаблення діяльності синусового вузла. Суб’єктивних і клінічних проявів зазвичай немає. Діагноз встановлюється на підставі ЕКГ, на якій видно, що джерелом ритму по черзі виступають то синусовий вузол, то різні відділи передсердь. При цьому зубець Р то позитивний, то сплощений, то негативний в межах одного і того ж відведення.
Короткі епізоди міграції водія ритму при добовому записі ЕКГ фіксуються у 54% здорових дітей. Такі епізоди часто зустрічаються у дітей з вегетативною дисфункцію, при дисметаболічних кардіоміопатіях, кардиті, а також у дітей з патологічним спортивним серцем. У лікуванні міграції водія ритму використовуються кардіотрофічні засоби. Обов’язково проводиться терапія основного захворювання.
Пароксизмальні тахікардії
Пароксизмальна тахікардія – це напад почастішання серцевих скорочень до 140-250 за хвилину, що раптово починається і так само раптово закінчується при збереженні в більшості випадків правильного регулярного ритму. Ці напади можуть бути нестійкими тривалістю менше 30 секунд і стійкими тривалістю більше 30 секунд.
За механізмом виділяють автоматичну, re-entry та тригерну тахікардії.
Автоматична тахікардія – це поява водія ритму, який генерує імпульси з частотою більшою, ніж СА-вузол. Для неї характерні періоди прискорення («розігрів») та сповільнення («охолодження») ритму. Автоматичний водій ритму може знаходитися в СА-вузлі, передсердях, атріовентрикулярному вузлі або шлуночках.
Тахікардія re-entry (реципрокна, повторного входу) – це виникнення стійкої циркуляції хвилі електричного збудження двома шляхами, які мають різну швидкість проведення та різний час відновлення здатності проводити хвилю збудження. Характерні раптовий початок, стабільна ЧСС під час нападу та раптове припинення.
Тригерна тахікардія – поява водія ритму, який має властивості як re-entry (виникає під час електричної стимуляції серця), так і автоматичної тахікардії (характерне прискорення та сповільнення ЧСС).
Залежно від локалізації ектопічного центру підвищеного автоматизму або постійно циркулюючої поворотної хвилі збудження виділяють передсердну, атріовентрикулярну і шлуночкову форми пароксизмальної тахікардії. Оскільки при передсердній та атріовентрикулярній тахікардії хвиля збудження поширюється по шлуночках звичайним шляхом, шлуночкові комплекси в більшості випадків не змінені. На поверхневій ЕКГ передсердна та атріовентрикулярна тахікардії відрізняються за формою і полярністю зубців Р, а також за розташуванням відносно шлуночкового комплексу QRS. Однак дуже часто на ЕКГ, зареєстрованій у момент нападу, на тлі різко вираженої тахікардії виявити зубець Р не вдається. В практичній аритмології передсердну та атріовентрикулярну форми пароксизмальної тахікардії часто об’єднують поняттям «надшлуночкова (суправентрикулярна) пароксизмальна тахікардія» (СВТ).
Частіше всього СВТ виникає у віці 4-5 років. У дітей до року перебіг СВТ тяжкий, з високою частотою і тривалістю пароксизмів.
Висока ЧСС зумовлює появу гемодинамічних розладів. Основною причиною змін гемодинаміки є вкорочення діастоли, що супроводжується зниженням наповнення шлуночків, зменшенням ударного і хвилинного об’єму кровообігу. Відомо, що при тахікардії з частотою вище 150 ударів на хвилину ударний об’єм знижується на 70‑80%, а хвилинний – на 30-50% від нормального. У такій ситуації порушується кровопостачання мозку, серця, нирок та інших життєво важливих органів. При тривалій тахікардії настає компенсаторна централізація кровотоку за рахунок рефлекторного звуження периферичних судин, спрямована на підвищення артеріального тиску. При недостатній компенсації розвивається аритмічна форма кардіогенного шоку.
Порушення кровопостачання головного мозку може супроводжуватися запамороченням, слабкістю, непритомністю, минущими неврозами. Тривала пароксизмальна тахікардія може призвести до серцевої недостатності, як правило, рефрактерної до лікарської терапії. Особливо швидко серцева недостатність розвивається при вузлових і шлуночкових пароксизмальних тахікардіях, коли порушується фізіологічний асинхронізм роботи передсердь і шлуночків. Пацієнти описують напад пароксизмальної тахікардії як відчуття прискореного серцебиття, що починається з різкого поштовху за грудиною і так само різко обривається. Пацієнт під час нападу відчуває страх, спостерігається рухове занепокоєння. Яремні вени набряклі, зі значною пульсацією.
При аускультації серця виявляють вирівнювання інтенсивності першого і другого тонів серця, паузи між тонами стають однаковими («маятниковий ритм»). Нерідко, однак, перший тон може бути посилений унаслідок зниження тиску в шлуночках серця. Найчастіше виявляється ритм галопу, який зникає після припинення нападу. Під час тахікардії часто можна почути систолічний шум у ділянці аорти або легеневої артерії, зумовлений турбулентністю кровотоку, що пов’язано зі збільшенням його швидкості.
Необхідно відзначити, що істинний механізм надшлуночкових форм тахікардії можна встановити лише при електрофізіологічному дослідженні.
Протокол діагностики та лікування порушень серцевого ритму у дітей (№ 362 від 19.07.2005) містить алгоритм лікування надшлуночкової тахікардії, який передбачає послідовність певних заходів.
Спочатку дитину вкладають на горизонтальну поверхню і забезпечують доступ свіжого повітря. Виконують рефлекторні заходи, що підвищують тонус блукаючого нерва: натискання шпателем на корінь язика; масаж каротидного синусу в ділянці сонної артерії протягом 5-10 секунд спочатку праворуч, а за відсутності ефекту – ліворуч; натиснення на епігастральну ділянку; у дітей старше 3-4 років – проба Вальсави (натужування при закритому носі протягом 10 секунд); додаткові прийоми, що використовуються у дітей старше 7 років, – повільне глибоке ковтання, занурення обличчя в холодну воду.
Надалі застосовують седативні засоби: корвалол, валокордин, валеріану (по 1 краплі на рік життя), аспаркам (панангін) по 1/3 таблетки залежно від віку.
За відсутності ефекту від рефлекторних прийомів і седативних засобів використовують антиаритмічні препарати.
Основним таким препаратом, що застосовують при лікуванні нападу СВТ у дітей, є 0,25% розчин верапамілу. Його вводять внутрішньовенно повільно під контролем АТ та ЧСС у дозі: дітям 1-5 років – 0,8-1,2 мл, 6-10 років – 1,2-1,5 мл, 11-15 років – 1,5-2 мл. Верапаміл протипоказаний при суправентрикулярній формі пароксизмальної тахікардії з аберантними шлуночковими комплексами, дітям 1-го року життя (розвиток тяжкої гіпотонії), при синдромі WPW (тому що можлива трансформація СВТ у фібриляцію шлуночків внаслідок прискорення антероградного проведення додатковими шляхами). Препарат не призначають одночасно з бета-адреноблокаторами.
1% розчин аденозину (АТФ) вводиться внутрішньовенно струминно, швидко в дозі 0,5-1 мл дітям дошкільного віку та 1 мл – дітям шкільного віку.
У рекомендаціях Європейського товариства кардіологів аденозин запропонований у якості препарату вибору при пароксизмальних тахікардіях незалежно від їх механізму. АТФ пригнічує автоматизм синусового вузла і атріовентрикулярного вузла на короткий час за рахунок підвищення калієвої провідності, зниження кальцієвого повільного току і антиадренергічної дії. Клінічна ефективність АТФ обумовлена швидким початком дії (до 10 с), мінімальними побічними ефектами (кашель, відчуття жару, гіперемія, брадикардія), які швидко проходять.
Можна вводити внутрішньовенно 0,025% розчин дигоксину. Дигоксин дає швидке насичення при вживанні per os у наступних дозах: недоношеним немовлятам – 20 мкг/кг на добу, новонародженим – 30 мкг/кг на добу, дітям до 2 років – 40-50 мкг/кг на добу, дітям старше 2 років – 30-40 мкг/кг на добу, поділені на 3 прийоми. Підтримувальна доза – 25-35% від повної дози насичення, поділені на 2 прийоми, в/в – 75% від дози per os.
За відсутності ефекту від проведеної антиаритмічної терапії пацієнта переводять до відділення інтенсивної терапії та реанімації або до кардіоревматологічного центру. В умовах відділення інтенсивної терапії вводять аміодарон внутрішньовенно крапельно на 5% розчині глюкози в дозі 5 мг/кг протягом 30 хв. За відсутності ефекту показана консультація кардіохірурга відносно необхідності проведення черезстравохідної електрокардіостимуляції або електроімпульсної терапії.
Слід пам’ятати, що аміодарон викликає подовження інтервалу QT і абсолютно протипоказаний дітям з синдромом подовженого інтервалу QT, а також негативно впливає на функцію щитовидної залози, тому слід уникати призначення цього препарату при її патології.
З метою лікування СВТ використовують також соталол або пропафенон. За неефективності монотерапії застосовують комбінацію цих препаратів.
Шлуночкова пароксизмальна тахікардія
При шлуночковій пароксизмальній тахікардії джерелом ектопічних імпульсів є скоротливий міокард шлуночків, пучок Гіса або волокна Пуркіньє. На відміну від інших тахікардій, шлуночкова має гірший прогноз у зв’язку зі схильністю переходити у фібриляцію шлуночків або з виникненням важких порушень кровообігу. Як правило, шлуночкова пароксизмальна тахікардія розвивається на тлі значних органічних змін серцевого м’яза.
Важливою ЕКГ-ознакою шлуночкової пароксизмальної тахікардії є так звана передсердно-шлуночкова дисоціація, тобто повна роз’єднаність у діяльності передсердь і шлуночків. Ектопічні імпульси, що виникають у шлуночках, часто не проводяться ретроградно до передсердь і вони збуджуються звичайним шляхом за рахунок імпульсів, що виникають в СА-вузлі. У більшості випадків хвиля збудження не проводиться від передсердь до шлуночків, оскільки атріовентрикулярний вузол знаходиться в стані рефрактерності (вплив частих імпульсів зі шлуночків). Шлуночки скорочуються з більшою частотою, ніж передсердя.
Слід також зазначити форму двобічної веретеноподібної шлуночкової пароксизмальної тахікардії, яка виникає на тлі подовженого інтервалу QT. Під час нападу комплекси QRS значно розширені, а їх спрямованість змінюється через 5-20 циклів, що створює враження їх «обертання» навколо ізоелектричної лінії. Цей вид шлуночкової тахікардії часто переходить у фібриляцію або мерехтіння шлуночків.
Нестійкою вентрикулярною тахікардією називають три або більше послідовних шлуночкових скорочень, які закінчуються мимовільно, без гемодинамічних порушень і тривають менше 30 секунд.
Стійка вентрикулярна тахікардія зберігається довше, ніж 30 секунд, і вимагає медичного втручання.
Короткі епізоди шлуночкової тахікардії присутні у 3% здорових підлітків. У пацієнтів із вродженими вадами серця захворюваність на шлуночкові тахікардії вища. Приблизно 30% дітей з тетрадою Фалло в післяопераційному періоді переносять мономорфні вентрикулярні тахікардії, 4,4% – поліморфні вентрикулярні тахікардії.
Вентрикулярні тахікардії можуть бути пов’язані з вадами аортального клапану, транспозицією магістральних судин, аномалією Ебштейна, синдромом Ейзенменгера, синдромом подовженого QT, вадами Фалло, аритмогенною дисплазією правого шлуночка та інфарктом міокарда.
Шлуночкова тахікардія характеризується механізмом повторного входу збудження і може бути спровокована й припинена за допомогою програмної стимуляції.
Шлуночкова тахікардія присутня у 50-60% пацієнтів з дилатаційною кардіоміопатією і стає причиною раптової смерті при цій патології у 8-50% випадків.
Мономорфні вентрикулярні тахікардії – це тахікардії з однаковими широкими комплексами QRS. Поліморфні вентрикулярні тахікардії – це тахікардії з широкими комплексами і перемінною морфологією QRS.
При зборі анамнезу звертають увагу на випадки шлуночкової тахікардії у родичів або їх раптової серцевої смерті.
При діагностиці проводять ЕКГ-дослідження, перевіряють електроліти (гіпокаліємія, гіперкаліємія, гіпомагніємія тощо). У пацієнтів з повторюваними епізодами непритомності проводять холтерівське моніторування ЕКГ або застосовують тривалі методи реєстрації ЕКГ з фіксацією подій порушення ритму.
Показана ехокардіографія і тест з фізичним навантаженням.
Електрофізіологічне дослідження виправдане у пацієнтів з епізодами непритомності невідомої етіології на тлі дисфункції лівого шлуночка.
За відсутності структурних змін з боку серця пацієнти з епізодами нестійкої вентрикулярної тахікардії мають хороший прогноз. Їм рекомендовано уникати медикаментів, що подовжують QT-інтервал, і своєчасно коригувати електролітні порушення.
При стійкій мономорфній вентрикулярній тахікардії застосовують прокаїнамід або аміодарон. При поліморфній шлуночковій тахікардії показана кардіоверсія, аміодарон і бета-блокатори, внутрішньовенне введення магнезії.
Операція із встановлення внутрішньосерцевого дефібрилятора показана пацієнтам із зупинкою серця внаслідок шлуночкової тахікардії в анамнезі або підвищеним ризиком раптової серцевої смерті.
З метою припинення нападу шлуночкової тахікардії використовують лідокаїн в дозі 1 мг/кг внутрішньовенно (максимум 100 мг у дозі) з повторним введенням через 5 хвилин (у разі відсутності відновлення синусового ритму) і подальшою інфузією 20-50 мкг/кг за хвилину. Новокаїнамід можна з обережністю використовувати за відсутності ефекту від терапії тільки при шлуночковій тахікардії зі стабільною гемодинамікою. Розчин магнію сульфату у дозі 50 мг/кг вводять лише у випадках зниження рівня магнію в крові або при поліморфній шлуночковій тахікардії. Слідкують за рівнем електролітів і глюкози. За відсутності ефекту розглядається питання щодо проведення електроімпульсної терапії.
Для профілактики тромбоемболії у пацієнтів з мітральною вадою серця, гіпертрофічною кардіоміопатією, тромбоемболіями в анамнезі до і після планової електричної кардіоверсії протягом 3-4 тижнів призначають непрямі антикоагулянти (фенілін, неодикумарин, варфарин, НОАК).
Серцеві глікозиди при шлуночковій пароксизмальній тахікардії протипоказані.
При частих приступах пароксизмальної тахікардії антиаритмічні препарати застосовують на постійний основі з метою попередження виникнення нападів.
Згідно з класифікацією D. Harrison, антиаритмічні препарати поділяються на 4 класи:
I клас – блокатори натрієвих каналів.
IA клас – препарати, які помірно сповільнюють проведення та подовжують потенціал дії (прокаїнамід, новокаїнамід, хінідін та ін.);
IB клас – препарати, які мінімально сповільнюють проведення і трохи скорочують потенціал дії (лідокаїн, мексилетин та ін.);
IС клас – препарати, які значно сповільнюють проведення і мінімально подовжують потенціал дії (пропафенон, флекаїнід, етацизин та ін.);
II клас – β-адреноблокатори (атенолол, пропранолол, ацебуталол та ін.);
III клас – препарати, які подовжують період реполяризації (аміодарон, соталол та ін.);
IV клас – блокатори кальцієвих каналів (верапаміл, дилтіазем та ін.).
До цієї класифікації не ввійшли, хоча і використовуються в аритмології, дигоксин, АТФ, препарати магнію.
Дози антиаритмічних препаратів і шляхи їх введення представлені в таблиці 2.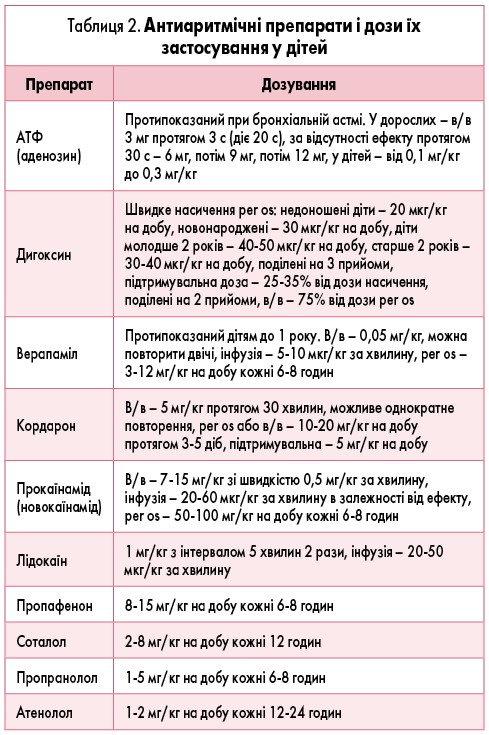
За відсутності ефекту від електричної кардіоверсії в/в струменево вводять кордарон у дозі 5 мг/кг. При лікуванні шлуночкової тахікардії з нормальним АТ кордарон вводять повільно протягом 10-20 хв. Можна використовувати лідокаїн в дозі 1 мг/кг в/в (максимум 100 мг) двічі з подальшою інфузією 20-50 мкг/кг за хв. За відсутності ефекту від вищевказаних препаратів новокаїнамід з обережністю можна використовувати тільки при шлуночковій тахікардії зі стабільною гемодинамікою. Розчин магнію сульфату у дозі 50 мг/кг вводять лише у випадках зниження рівня магнію в крові або при поліморфній шлуночковій тахікардії. Потрібно слідкувати за рівнем електролітів і глюкози.
Миготлива аритмія
Тріпотіння передсердь – re-entry тахікардія, при якій спостерігається прискорене ритмічне збудження і скорочення передсердь із частотою 250-400 імпульсів за хвилину. Частота скорочення шлуночків у результаті функціональної AВБ менша за частоту скорочення передсердь і реєструється у співвідношенні 1:2, 1:3, 1:4.
Фібриляція (миготіння) передсердь характеризується неритмічним, хаотичним серцевим ритмом, при якому відсутні координовані скорочення міокарда передсердь, частота яких може досягати 400 і більше за хвилину. При цьому тільки частина з цих скорочень передається через атріовентрикулярне з’єднання на шлуночки (до 200‑220 імпульсів за хвилину), внаслідок чого скорочення шлуночків теж неритмічні.
Найчастішими причинами миготливої аритмії у дітей є ревмокардит, кардіоміопатії, вроджені вади серця з перевантаженням передсердь, хронічне легеневе серце, синдром слабкості синусового вузла.
Тріпотіння передсердь є одним з найбільш частих видів аритмій у пацієнтів з набутими вадами мітрального клапана. Серед них з першим епізодом тріпотіння між 1 і 25 роками життя 81% мають вроджену ваду серця і тільки 8% – здорове серце.
Механізмом тріпотіння передсердь є повторний вхід збудження з циркуляцією хвилі re-entry в межах передсердь.
У новонароджених 80% випадків тріпотіння передсердь є безсимптомними і 20% можуть перебігати із застійною серцевою недостатністю. Старші пацієнти можуть відчувати сильне серцебиття, запаморочення, стиснення і біль у грудях, задишку і втому.
Розрізняють постійну (стійку) форму фібриляції передсердь тривалістю до 1-2 тижнів і більше та пароксизмальну форму. При виникненні фібриляції передсердь швидко розвивається синдром малого серцевого викиду, зростають прояви лівошлуночкової серцевої недостатності, виникає загроза тромбоемболії.
При тріпотінні і фібриляції передсердь діти скаржаться на прискорене серцебиття при фізичному або психоемоційному навантаженні, кардіалгії, головний біль, запаморочення.
Метою лікування тріпотіння і фібриляції передсердь є зменшення ЧСС і відновлення нормального синусового ритму. Як правило, після його відновлення діти не потребують тривалого антиаритмічного лікування.
Застосовують такі медикаментозні засоби: аміодарон, дигоксин, пропранолол. Тріпотіння і фібриляція передсердь із нестабільною гемодинамікою потребує застосування електричної кардіоверсії (1-2 Дж/кг при синхронізованій кардіоверсії, при несинхронізованій – 3-4 Дж/кг). Перед електричною кардіоверсією дигоксин необхідно відмінити.
Рецидиви тріпотіння передсердь можуть бути припинені шляхом введення антиаритмічних препаратів класів IA, IC і III. Препарати класів IA і IC покращують атріовентрикулярну провідність, тому спочатку необхідно знизити ЧСС (бета-адреноблокатори, верапаміл). Коли тріпотіння передсердь не піддається медичному контролю, проводять катетерну абляцію.
Після надання невідкладної допомоги пацієнти з тріпотінням чи фібриляцією передсердь повинні бути госпіталізовані у кардіоревматологічне відділення для лікування основного захворювання. За показаннями дитина може бути госпіталізована до відділення реанімації та інтенсивної терапії.
Протокол діагностики та лікування порушень серцевого ритму у дітей (№ 362 від 19.07.2005) передбачає наступний алгоритм лікування нападу тріпотіння і фібриляції передсердь:
- верапаміл 0,25% в/в повільно на 10-20 мл 5% розчину глюкози в дозі 0,15 мг/кг
або
- пропранолол 0,1% в/в дуже повільно в дозі 0,1‑0,2 мг/кг;
в умовах відділення реанімації та інтенсивної терапії за відсутності ефекту від уведення верапамілу та пропранололу, при наявності синдрому малого серцевого викиду і прогресуванні серцевої недостатності призначаються серцеві глікозиди. Дигоксин 0,025% в/м або в/в. Доза насичення – 0,03-0,05 мг/кг. Темп насичення – 3 дні. Підтримувальна доза – 1/5-1/6 від дози насичення. Одночасно призначають препарати калію (панангін, аспаркам).
Препаратом вибору для подальшої медикаментозної кардіоверсії при фібриляції передсердь є аміодарон 5% розчину в/в дуже повільно, в дозі 5 мг/кг на 10-20 мл 5% розчину глюкози. Після отримання ефекту переходять на пероральний прийом препарату.
Антиаритмічні засоби (дигоксин, аміодарон) у підтримувальних дозах призначаються на 3-4 тижні з подальшою відміною при досягненні стійкого ефекту.
При рецидивуючих формах тріпотіння передсердь методом вибору для відновлення ритму серця є черезстравохідна електростимуляція у сполученні з малими дозами аміодарону.
При брадикардитичній формі миготіння передсердь і появі синкопальних нападів, пов’язаних з брадикардією, із метою постійної електрокардіостимуляції в умовах кардіохірургічної клініки в серце імплантується кардіостимулятор.
Продовження у наступному номері.
Тематичний номер «Педіатрія» №4 (51), 2019 р.


