23 грудня, 2019
Рандомизированное исследование применения прогестерона у женщин с кровотечениями на ранних сроках беременности
Резюме
Общая информация
Кровотечение на ранних сроках беременности тесно связано с потерей беременности. Для сохранения беременности необходим прогестерон. Результаты нескольких небольших исследований свидетельствуют о том, что применение прогестерона может улучшить исходы беременности у женщин с кровотечениями на ранних сроках.
Методы
Мы провели многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование по сравнительной оценке применения прогестерона и плацебо у женщин с вагинальным кровотечением на ранних сроках беременности. Женщинам случайным образом назначали вагинальные суппозитории, содержащие 400 мг прогестерона или соответствующего плацебо, 2 раза в сутки с момента развития кровотечения до 16 нед беременности. Основной конечной точкой было рождение жизнеспособного ребенка на сроке не менее 34 нед беременности. В выборку для первичного анализа были включены все участницы, для которых были известны данные об основной конечной точке. Анализ чувствительности основной конечной точки, в который были включены все участницы, выполнялся с применением методики множественной подстановки, чтобы охватить отсутствующие данные.
Результаты
В общей сложности 4153 женщины, включенные в исследование в 48 больницах Великобритании, были рандомизированы в группы прогестерона (2079 женщин) или плацебо (2074 женщины). Данные о достижении основной конечной точки имелись у 97% женщин (4038 из 4153 женщин). Частота живорождения после 34 нед беременности составила 75% (1513 из 2025 женщин) в группе прогестерона и 72% (1459 из 2013 женщин) в группе плацебо (относительная частота 1,03; 95% доверительный интервал [ДИ] 1,00-1,07; р=0,08). Анализ чувствительности, в котором отсутствующие данные об основной конечной точке были подставлены, показал аналогичный результат (относительная частота 1,03; 95% ДИ 1,00-1,07; р=0,08). Частота нежелательных явлений в обеих группах достоверно не различалась.
Выводы
У женщин с кровотечением на ранних сроках беременности применение прогестерона в первом триместре не приводило к достоверному повышению частоты живорождения по сравнению с плацебо. (При финансовой поддержке Программы оценки медицинских технологий Национального института исследований в области здравоохранения Великобритании; текущий номер контролируемого исследования РК18М: 18КСТМ4163439.)
Каждая 5-я беременность завершается выкидышем [1]. Выкидыш может привести к обильному кровотечению, инфицированию и осложнениям, связанным с хирургическим вмешательством [2], а также вызвать психологические проблемы, включая тревожность, депрессию и посттравматическое стрессовое расстройство [3, 4].
Прогестерон, который вырабатывается желтым телом яичника, необходим для подготовки эндометрия к имплантации эмбриона и, таким образом, является незаменимым гормоном для успешного развития беременности. Дополнительно прогестерон вырабатывается после имплантации эмбриона и на ранних стадиях развития плаценты. В дальнейшем, начиная приблизительно с 12-й недели беременности, плацента становится основным источником прогестерона [5].
Физиологическая роль прогестерона побудила исследователей, врачей и пациенток рассмотреть необходимость восполнения прогестерона на ранних сроках беременности для предотвращения выкидышей. Восполнение прогестерона на ранних сроках беременности рассматривалось в двух ситуациях: в первом случае – для предотвращения выкидышей у женщин без клинической симптоматики, но с привычным выкидышем в анамнезе; во втором – для сохранения беременности у женщин с начавшимся кровотечением на ранних сроках беременности [6]. Ранее нами было проведено исследование касательно применения прогестерона для предотвращения выкидышей у женщин без клинической симптоматики [7]. В нем мы установили отсутствие благоприятного действия прогестерона у женщин с привычным выкидышем неизвестной этиологии в анамнезе. В настоящем исследовании участвовали женщины с вагинальным кровотечением на ранних сроках беременности.
Кокрановский обзор (впервые опубликованный в 2007 г. и последний раз обновленный в 2018 г.) [6] 7 рандомизированных исследований препаратов прогестерона с участием женщин с кровотечением на ранних сроках беременности выявил существенно меньший риск выкидыша у пациенток, получавших прогестерон, чем у получавших плацебо или не получавших лечение (отношение рисков [ОР] 0,64; 95% ДИ 0,47-0,87), хотя отмечалось, что исследования были небольшими (выборка в самом крупном исследовании составила 191 пациентку) и имели методологические недоработки.
Еще один Кокрановский обзор 13 исследований препаратов прогестерона с участием женщин с привычным выкидышем был впервые опубликован в 2003 г. и последний раз обновлен в 2018 г. [8]. Американская коллегия акушеров-гинекологов рассмотрела доказательства и пришла к выводу, что «Применение прогестинов при угрожающем выкидыше на ранних сроках беременности является спорным вопросом, и убедительных доказательств в поддержку их применения нет. Тем не менее у женщин, у которых уже было не менее трех выкидышей, применение прогестерона в первом триместре может оказаться полезным» [9].
Мы провели многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование в параллельных группах РRISМ (Рrogesterone in Spontaneous Мiscarriagе – Прогестерон при самопроизвольном выкидыше), чтобы выяснить, приведет ли применение прогестерона у женщин с кровотечением на ранних сроках беременности к более высокой частоте живорождения по сравнению с плацебо.
Методы
Обзор исследования
Исследование РRISМ было утверждено Управлением по контролю лекарственных средств и изделий медицинского назначения Великобритании, Национальным комитетом по этике научных исследований Великобритании (Южно-Центральный Оксфорд) и Отделом исследований и разработок Национальной службы здравоохранения в каждой участвующей больнице. Исследование проводилось в клиниках, включенных в научно-исследовательскую сеть Национального центра исследований выкидышей Томми, финансируемого Благотворительным фондом Томми.
Участницы исследования
Участниц исследования РRISМ набирали в 48 больницах Великобритании. Женщины могли быть включены в исследование, если им было от 16 до 39 лет, срок их беременности составлял менее 12 нед, у них было вагинальное кровотечение и имелось плодное яйцо в матке, визуализируемое при ультразвуковом исследовании. Верхний порог возраста матери 39 лет был выбран потому, что вероятность выкидыша в связи с хромосомными нарушениями увеличивается с возрастом [10], а применение прогестерона не может предотвратить такие выкидыши.
Участницы исключались из исследования, если на момент поступления копчико-теменной размер эмбриона составлял ≥7 мм без сердцебиения; плодное яйцо имело средний диаметр ≥25 мм, а зародышевый бугорок при ультразвуковом исследовании не визуализировался; при наличии признаков внематочной беременности; при наличии жизнеугрожающего кровотечения; если женщины принимали ранее или на момент поступления препараты прогестерона; при наличии противопоказаний к применению прогестерона (например, опухоли печени в анамнезе; рак половых органов или молочной железы в настоящее время, болезнь периферических артерий тяжелой степени или острая порфирия; идиопатическая желтуха беременных, выраженный зуд или пемфигоид беременных в анамнезе); если они участвовали в любом другом слепом плацебо-контролируемом исследовании лекарственных препаратов при беременности. Все участницы предоставили письменное информированное согласие.
Оценки в рамках исследования
Участниц случайным образом распределили в соотношении 1:1 в группы самостоятельного применения вагинальных суппозиториев, содержащих 400 мг микронизированного прогестерона, или соответствующего плацебо 2 раза в сутки с момента рандомизации до завершения 16-й недели беременности (или раньше, если беременность прервалась до 16 нед). Если вагинальное введение было нежелательным, участницы могли вводить суппозитории ректально. Рандомизацию провели с помощью защищенного централизованного интернет-ресурса с применением минимизации для уравновешивания исследуемых групп по возрасту женщин (<35 лет или ≥35 лет), индексу массы тела (ИМТ [масса тела в килограммах, разделенная на квадрат роста в метрах], <30 или ≥30), сердечной деятельности плода (есть или нет), расчетному сроку беременности на момент поступления (<42 дней или ≥42 дней) и объему вагинального кровотечения (графическая оценка величины кровопотери [РВАС] ≤2 или ≥3; оценка колеблется от 1 до 4, чем выше оценка, тем больше объем кровопотери) [11]. Внешний вид, способ и кратность введения прогестерона и плацебо были одинаковыми. Участницы, врачи и медицинские сестры, участвовавшие в исследовании, не были осведомлены о распределении в исследуемые группы до завершения исследования.
Оценка исходов
Основной конечной точкой было рождение жизнеспособного ребенка на сроке не менее 34 полных недель беременности. Дополнительные конечные точки включали срок от зачатия до даты завершения беременности, продолжающуюся беременность на сроке 12 нед, выкидыш (потерю беременности на сроке до 24 нед), рождение жизнеспособного ребенка на сроке <34 нед беременности, внематочную беременность, мертворождение (внутриутробную гибель плода на сроке не менее 24 нед беременности), прерывание беременности, неделю беременности, на которой произошли роды, массу тела новорожденного, размер плода (маленький или большой) для данного срока беременности, преэклампсию, оценку по шкале Апгар, выживаемость новорожденных через 28 дней после рождения и врожденные аномалии, а также другие дородовые, интранатальные, послеродовые и неонатальные исходы. Мы пытались собрать данные по конечным точкам у всех рандомизированных участниц, независимо от соблюдения ими назначенного лечения в терапевтической группе.
Статистический анализ
По нашим расчетам, в каждую исследуемую группу необходимо было включить 1972 женщины, чтобы обеспечить 90% статистическую мощность для выявления минимальной значимой абсолютной разности в 5 процентных пунктах между группами прогестерона и плацебо по частоте живорождения на сроке беременности не менее 34 нед (65% и 60%) при двустороннем уровне статистической значимости 0,05. Минимальная значимая разность была выбрана на основании общенационального опроса практикующих врачей в Великобритании. Мы планировали включить в исследование 4150 женщин с учетом ожидаемого выбывания из последующего наблюдения на уровне 5%.
Анализ основной конечной точки проводился в соответствии с принципом анализа в зависимости от назначенного лечения; основной анализ всех имеющихся данных был дополнен анализом чувствительности основной конечной точки, в который были включены все участницы с учетом отсутствующих данных путем множественной подстановки [12]. Для оценки отношения рисков и соответствующих 95% двусторонних доверительных интервалов применялась модель пуассоновской регрессии с робастными стандартными ошибками с поправкой на минимизацию переменных. Установлено, что данный метод отвечает требованиям и менее подвержен проблемам сходимости, чем другие аналогичные методы [13].
Для основной конечной точки величину p определяли с помощью двустороннего критерия χ2. План статистического анализа не включал положения о поправках на множественность при выполнении анализов дополнительных конечных точек. Следовательно, результаты представлены в виде точечных оценок и 95% доверительных интервалов без величины p. В отношении непрерывных конечных точек для оценки средних различий применялась модель линейной регрессии с той же поправкой, которая использовалась в анализе основной конечной точки. Ширина доверительных интервалов не корректировалась на множественность, поэтому интервалы не должны применяться для суждения о характерных терапевтических эффектах.
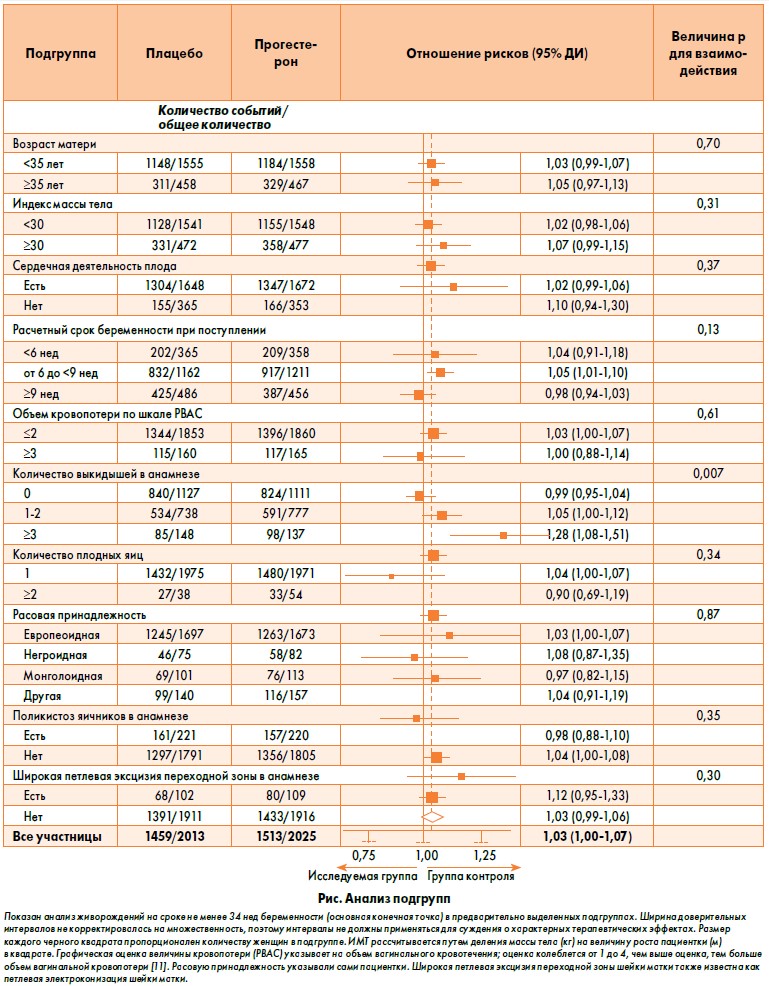
Мы проанализировали влияние терапии на основную конечную точку в предварительно выделенных подгруппах в соответствии с возрастом женщин (<35 лет или ≥35 лет), ИМТ (<30 или ≥30), сердечной деятельностью плода (есть или нет), расчетным сроком беременности на момент поступления (<6 нед, или от 6 до <9 нед, или ≥9 нед), величиной вагинальной кровопотери (оценка РВАС ≤2 или ≥3) [11], количеством предыдущих выкидышей (0, или 1-2, или ≥3), количеством плодных яиц (1 или ≥2), расовой принадлежностью (европеоидная, негроидная, монголоидная или другие), поликистозом яичников в анамнезе (есть или нет) и резекцией шейки матки в анамнезе (есть или нет). Эффекты в этих подгруппах изучались путем добавления переменных для взаимодействия подгруппы с исследуемой группой в регрессионную модель; чтобы определить, различались ли эффекты прогестерона и плацебо в различных подгруппах, использовался критерий χ2.
Промежуточные анализы основных конечных точек безопасности и эффективности выполнялись от имени комитета по мониторингу данных и безопасности статистиком клинического исследования (который не имел сведений о назначенном лечении) дважды. Так как анализы выполнялись с применением принципа Пето [14], поправки в итоговые значения критерия p для определения значимости не вносились.
Результаты
Участницы исследования
С 19 мая 2015 г. по 27 июля 2017 г. было выявлено в общей сложности 12 862 женщины, подходящие для участия в исследовании РRISМ; из них 4153 были случайным образом распределены в группы терапии прогестероном (2079 женщин) или плацебо (2074 женщины). Данные о достижении основной конечной точки имелись у 97% женщин (4038 из 4153). Демографические и исходные характеристики в обеих исследуемых группах были сопоставимы. Сведения о способе введения имелись для 88% (3662 из 4153) женщин: 99% (3611 из 3662) участниц суппозитории вводили вагинально, 1% (51 из 3662) – ректально.
Результаты
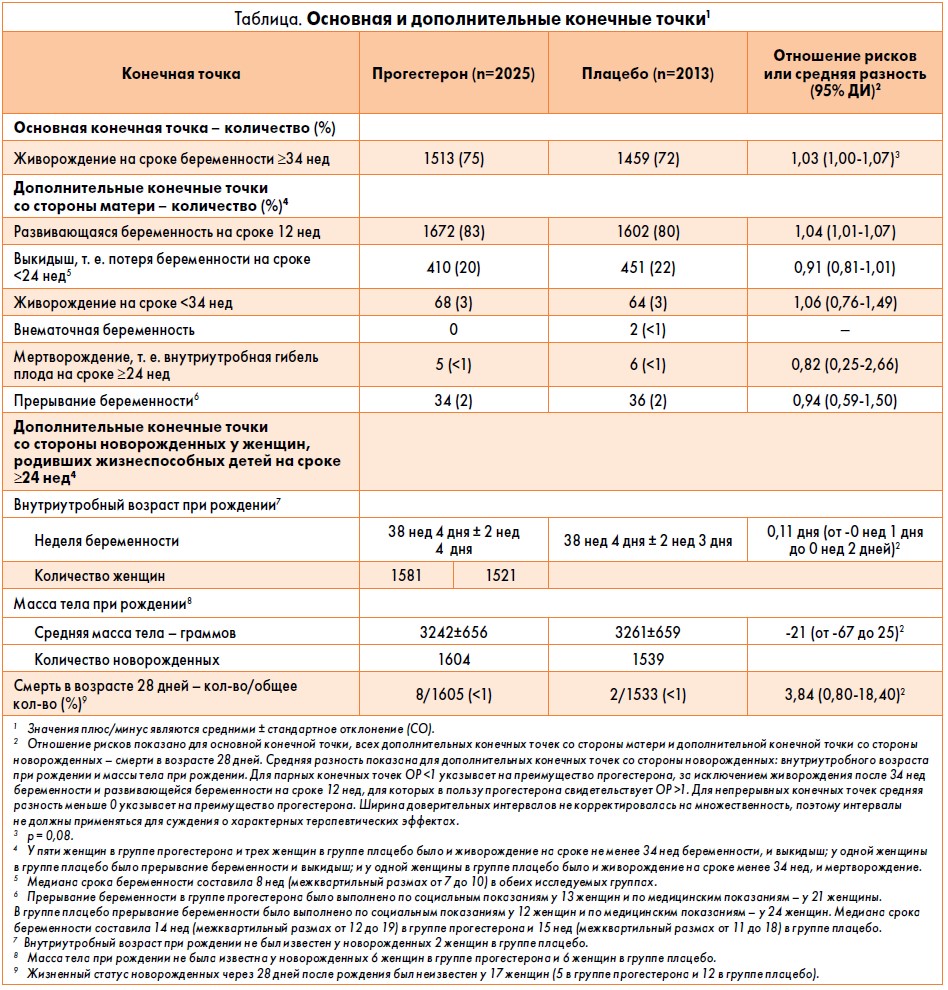
Частота живорождения после 34 нед беременности составила 75% (1513 из 2025 женщин) в группе прогестерона и 72% (1459 из 2013 женщин) в группе плацебо (ОР 1,03; 95% ДИ 1,00-1,07; р=0,08). Анализ чувствительности, в котором использовалась методика множественной подстановки отсутствующих данных, не изменил результатов (ОР 1,03; 95% ДИ 1,00-1,07; р=0,08).
Частота развивающейся беременности на сроке 12 нед составила 83% (1672 из 2025 женщин) в группе прогестерона и 80% (1602 из 2013 женщин) в группе плацебо (ОР 1,04; 95% ДИ 1,01-1,07). Частота выкидыша составила 20% (410 из 2025 женщин) в группе прогестерона и 22% (451 из 2013 женщин) в группе плацебо (ОР 0,91; 95% ДИ 0,81-1,01). Результаты остальных дополнительных конечных точек представлены в таблице.
Значимый эффект в подгруппе был выявлен только для одной из 10 предварительно выделенных подгрупп – для подгруппы участниц, выделенной в соответствии с количеством предшествующих выкидышей. Частота живорождения в подгруппе женщин, у которых ранее не было выкидышей, составила 74% в группе прогестерона и 75% в группе плацебо (ОР 0,99; 95% ДИ 0,95-1,04); частота у женщин с одним или двумя выкидышами в анамнезе составила 76% и 72% соответственно (ОР 1,05; 95% ДИ 1,00-1,12); а частота у женщин с тремя и более выкидышами в анамнезе – 72% и 57% соответственно (ОР 1,28; 95% ДИ 1,08-1,51; р=0,007 для взаимодействия между исследуемой группой и количеством выкидышей) (рисунок).
Не было достоверных различий между группами по проценту пациенток с серьезными нежелательными явлениями у матери или новорожденного (5% [105 из 2025 участниц] в группе прогестерона и 5% [98 из 2013 участниц] в группе плацебо), включая в том числе процент детей с врожденными аномалиями развития (3,4% в каждой группе); а также не было достоверных различий между группами по количеству серьезных нежелательных явлений у матерей или новорожденных.
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 3 (35), жовтень 2019 р.