25 грудня, 2019
Захист печінки від токсичного впливу лікарських засобів, фітопрепаратів, дієтичних добавок
 Недооціненою проблемою сучасної гепатології є медикаментозно-індуковане ураження печінки (МІУП). Ця патологія перебуває на межі компетенції лікарів різних спеціальностей, тому тема є актуальною не лише для гепатологів, а й для інших фахівців. Призначення лікарських препаратів є невід’ємною складовою будь-якої терапевтичної схеми. Якщо негативні наслідки застосування нестероїдних протизапальних препаратів (НПЗП), антибіотиків, протипухлинних чи інших засобів є передбачуваними, то гепатотоксичність рослинних засобів, дієтичних добавок часто залишається поза увагою клініцистів. Уникнути токсичної дії лікарських препаратів або мінімізувати її можна за рахунок своєчасного припинення прийому або застосування гепатотропних засобів. Останній метод має переваги у випадку, коли зниження дози або відміна прийому лікарських засобів є шкідливішими для пацієнта, ніж продовження терапії.
Недооціненою проблемою сучасної гепатології є медикаментозно-індуковане ураження печінки (МІУП). Ця патологія перебуває на межі компетенції лікарів різних спеціальностей, тому тема є актуальною не лише для гепатологів, а й для інших фахівців. Призначення лікарських препаратів є невід’ємною складовою будь-якої терапевтичної схеми. Якщо негативні наслідки застосування нестероїдних протизапальних препаратів (НПЗП), антибіотиків, протипухлинних чи інших засобів є передбачуваними, то гепатотоксичність рослинних засобів, дієтичних добавок часто залишається поза увагою клініцистів. Уникнути токсичної дії лікарських препаратів або мінімізувати її можна за рахунок своєчасного припинення прийому або застосування гепатотропних засобів. Останній метод має переваги у випадку, коли зниження дози або відміна прийому лікарських засобів є шкідливішими для пацієнта, ніж продовження терапії.
У рамках науково-практичної конференції «ХІ Український гастроентерологічний тиждень» (3-4 жовтня, м. Одеса) доповідь від групи авторів «Профілактика та лікування медикаментозно-індукованих уражень печінки: аспекти доказовості та власний досвід» представив президент Української гастроентерологічної асоціації, проректор з науково-педагогічної та післядипломної освіти, професор кафедри внутрішньої медицини № 1 Української медичної стоматологічної академії (м. Полтава), доктор медичних наук Ігор Миколайович Скрипник.
– З кожним роком поширеність МІУП зростає, хоча наявні статистичні дані не відображають реальну епідемічну ситуацію. За результатами нещодавніх популяційних досліджень, поширеність МІУП у країнах Європи не перевищує 0,15% (найвищий показник зареєстровано у Франції – 0,139%; A. Licata et al., 2017).
Серед органів і систем найбільш чутливими до токсичної дії лікарських засобів (що й стає причиною припинення прийому останніх) є гепатобіліарна та серцево-судинна системи, за ними слідують кров, м’язи, органи шлунково-кишкового тракту, репродуктивна, імунна системи й інші органи.
Виділяють 3 типи МІУП: гепатоцелюлярний (можуть спричиняти ацетамінофен, алопуринол, аміодарон, баклофен, фітопрепарати, ізоніазид, кетоконазол, лізиноприл, лозартан, метотрексат, омепразол, рифампіцин, статини, тетрацикліни тощо), холестатичний (амоксициліну клавуланат, анаболічні стероїди, клопідогрель, пероральні контрацептиви, еритроміцин, естрогени, ірбесартан, фенотіазини, трициклічні засоби тощо) та змішаний (амітриптилін, азатіоприн, каптоприл, карбамазепін, кліндаміцин, еналаприл, фенобарбітал, верапаміл тощо). Для встановлення варіанта ураження печінки немає потреби у проведенні дороговартісних аналізів, достатньо визначити рівень аланінамінотрансферази (АЛТ), лужної фосфатази (ЛФ), загального білірубіну (ЗБ). Гепатоцелюлярне МІУП характеризується підвищенням рівня АЛТ, холестатичне МІУП – АЛТ та ЗБ, змішане МІУП – АЛТ та ЛФ. У структурі причин МІУП «лідирує» застосування НПЗП – 35,5%, антибіотиків – 23,4%, імуносупресантів – 10,9%. Слід зазначити, що біологічна терапія рідко викликає МІУП (J. Drenth, 2018). Результати дослідження, проведеного в Португалії, дали змогу виявити схожу тенденцію: в етіологічній структурі МІУП домінувало застосування НПЗП (20,9%), антибіотиків (17,4%), антипсихотичних засобів (8,1%), а також фітопрепаратів (5,8%; J.M. Nules et al., 2009).
Детальніше варто зупинитися на питанні щодо ролі фітопрепаратів у МІУП, що часто залишається поза увагою клініцистів. 29-50% дієтичних добавок пацієнти використовують без узгодження з лікарем (Tarn et al., 2015), 63‑68% випадків МІУП на тлі прийому рослинних засобів і дієтичних добавок пов’язані з мультиінгредієнтністю продуктів (Navarro et al., 2014). Протягом останніх років спостерігається зростання частоти розвитку печінкової недостатності на тлі прийому анаболічних стероїдів (з 5% у 2004-2005 рр. до 14% у 2013-2014 рр.) та рослинних/дієтичних добавок (з 2% у 2004-2005 рр. до 6% у 2013-2014 рр.; Navarro et al., 2014; M. Manns, 2018).
Підвищують чутливість печінки до впливу лікарських засобів також генетичні предиктори, інфікованість гепатотропними вірусами. При вивченні геному хворих з МІУП на тлі прийому комбінації амоксициліну та клавуланової кислоти виявлено, що HLA І класу 1В*1801 алель пов’язаний з гепатоцелюлярним типом МІУП та виникненням несприятливих наслідків, HLA ІІ класу DRB1*1501-DQB1*0602 – із холестатичним та змішаним типом МІУП (C. Stephens et al., 2010). Інфікування вірусом гепатиту С індукує цитоліз, призводить до зниження інтрацелюлярного запасу глутатіону, що збільшує чутливість печінки до лікарських засобів.
Діагностична тактика у пацієнтів з МІУП включає такі завдання:
- Оцінка типу МІУП (гепатоцелюлярний, холестатичний, змішаний).
- Виключення інших причин ураження печінки (аутоімунний гепатит, вірусні гепатити, у тому числі виключення інфікування цитомегаловірусом і вірусом Епштейна – Барр у молодих осіб).
- Визначення тяжкості ушкодження печінки за такими показниками: ступінь лейкоцитозу, тромбоцитопенії, гіпербілірубінемії, гіпоальбумінемії, рівень холестерину, співвідношення прямий/загальний білірубін, протромбіновий час.
При підозрі на наявність МІУП пацієнту проводять загальний та біохімічний аналіз крові (рівень АЛТ, АСТ, лактатдегідрогенази, ЛФ, білірубіну, альбуміну, холестерину, холінестерази), коагуляційні та серологічні тести (визначення IgA, IgM, IgG, аутоантитіл ANA, AMA, AMA M2; вірусних маркерів – IgM анти-HAV, HBsAg, IgM-HBc, анти-HCV, HBV-DNA, HCV-RNA), ультразвукове дослідження органів черевної порожнини. Тяжкість ушкодження печінки визначають за шкалою Drug Induced Liver Injury Network (DILIN; табл.).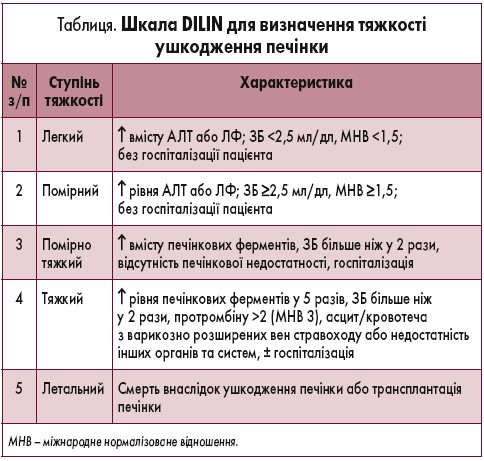
Крім додаткових методів дослідження, які, безперечно, є обов’язковими для встановлення правильного діагнозу, важливим етапом визначення зв’язку ушкодження печінки з дією лікарського препарату є детальний збір анамнезу, у ході якого необхідно також уточнити відомості про прийом рослинних засобів і дієтичних добавок. Корисним для лікаря може стати інтернет-ресурс LiverTox®, де представлена актуальна інформація щодо епідеміології, причин, діагностики, лікування та профілактики МІУП.
Відповідно до сучасних рекомендацій Китайської асоціації гепатологів (Chinese Society of Hepatology, CSH) щодо ведення пацієнтів з МІУП, при холестатичному типі МІУП призначають препарати урсодезоксихолевої кислоти та S-аденозил-L-метіонін (A. Reuben et al., 2010; Yue-Cheng Yu, 2017). В Україні адеметіонін представлений у вигляді препарату Гептрал®.
Для обґрунтування використання препарату Гептрал® у пацієнтів з МІУП необхідно розглянути механізм ураження печінки при ньому. При МІУП збільшується концентрація реактивних метаболітів і вільних радикалів, які активують пероксидне окиснення ліпідів. Цей процес супроводжується підвищенням рівня АЛТ та АСТ та цитолізом гепатоцитів. Адеметіонін є ендогенним донором СН-групи (бере участь у реакції трансметилювання, синтезі фосфоліпідної клітинної мембрани гепатоцитів) та джерелом цистеїну – субстрату для продукції глутатіону (C. Liber, 2002; J. Mato, 2011).
Позитивний вплив адеметіоніну (Гептрал®) для профілактики МІУП продемонстровано у низці досліджень:
- у ході подвійного сліпого рандомізованого дослідження за участю 72 чоловіків, хворих на псоріаз, виявлено, що доповнення основної терапії циклоспорином препаратом S-адеметіоніну у дозі 400 мг протягом 3 міс супроводжувалося мінімізацією оксидативного стресу та підтриманням нормальних показників АЛТ та АСТ (S. Nei et al., 2002);
- превентивне призначення адеметіоніну (Гептрал®)по 400 мг 2 р/добу онкологічним пацієнтам з підвищеним рівнем АСТ, АЛТ, ЛДГ у 2,5-4,0 рази перед поліхіміотерапією та в інтервалах між введенням хіміопрепаратів дозволило знизити рівень трансаміназ крові уже на 2-й тиждень прийому (D. Santini et al., 2003).
Важливою умовою проведення ефективної терапії при онкологічних захворюваннях є тривале підтримання високої дози лікарського препарату без її редукції. Шляхом ретроспективного аналізу даних щодо ролі адеметіоніну (Гептрал®) у профілактиці МІУП у пацієнтів з колоректальним раком було виявлено, що застосування гепатотропного засобу знижує потребу у редукції дози хіміопрепаратів до 3% порівняно з такою у пацієнтів, які не приймали препарат (18%; B. Vincenzi et al., 2011).
Профілактичне призначення S-адеметіоніну запобігає розвитку гепатотоксичних реакцій в динаміці поліхіміотерапії у пацієнтів з гострим лейкозом. Захисний ефект адеметіоніну ґрунтується на покращенні пластичності мембран гепатоцитів і підвищенні активності антиоксидантної системи. Слід зазначити, що ожиріння у пацієнтів з гострим лейкозом збільшує частоту та вираженість гепатотоксичних реакцій у динаміці хіміотерапії, проте призначення адеметіоніну сприяє покращенню показників функціонального стану печінки та запобіганню розвитку МІУП. У рамках цьогорічного Міжнародного конгресу EASL було зроблено висновок, що надлишкова маса тіла та неалкогольний стеатогепатит у хворих на хронічний лімфоцитарний лейкоз є провідними чинниками ризику гепатотоксичних реакцій у динаміці хіміотерапії, які характеризуються зростанням їх ступеня тяжкості паралельно зі збільшенням кумулятивної дози хіміотерапії (І. Skrypnyk, G. Maslova, 2019).
У адеметіоніну виявлений також антидепресивний ефект. В основі патогенезу депресії лежить порушення процесів біологічного метилювання. S-адеметіонін є джерелом СН3-груп у центральній і периферичній нервовій системі та сприяє активації постсинаптичних рецепторів, їх взаємодії з моноаміновими нейромедіаторами, а також безпосередньо бере участь у синтезі серотоніну (G.S. Papakostas et al., 2009). У пацієнтів із хронічними дифузними захворюваннями печінки має місце дефіцит ендогенного адеметіоніну, внаслідок чого виникає недостатність трансметилювання, розвиваються когнітивні розлади та втома.
Отже, для профілактики виникнення МІУП необхідно ідентифікувати гепатотоксичність під час передреєстраційних досліджень нових лікарських засобів, проводити моніторинг небажаних побічних явищ з боку печінки у конкретних хворих (регулярний контроль рівня АЛТ, АСТ – щомісячно протягом перших 6 міс) та своєчасно припиняти прийом препарату у разі виявлення порушень печінкових проб. При застосуванні ізоніазиду, антиретровірусних і протипухлинних препаратів доцільно одночасно призначати гепатотропні препарати. Навіть ретельне клінічне вивчення нових лікарських засобів не може повністю виключити можливість появи на фармацевтичному ринку ліків з гепатотоксичними ефектами, що зумовлює потребу застосування препаратів, які захистять печінку від небажаних явищ, зокрема адеметіоніну.
Підготувала Ілона Цюпа
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (54), 2019 р.


