2 січня, 2020
Інфекції сечовивідних шляхів: у якому напрямі рухатися? Нові альтернативи лікування ІСШ
За матеріалами симпозіуму в рамках 34-го щорічного конгресу EAU, 16 березня 2019 року, м. Барселона, Іспанія
Метою цього симпозіуму було розглянути нинішній сценарій, а також висвітлити зміни парадигми лікування гострих неускладнених інфекцій нижніх сечовивідних шляхів (нІСШ). Під час заходу було представлено декілька пов’язаних тем, які охоплювали антибіотикорезистентність (АБР), включно із сучасними даними дослідження GPIU (дослідження всесвітньої поширеності інфекційних захворювань в урології) і клінічними випадками, які ілюстрували вплив АБР на ведення пацієнтів з ІСШ/нІСШ та варіанти лікування ІСШ/нІСШ відповідно до сучасних рекомендацій.
Ключовим моментом симпозіуму була презентація найновіших даних еталонного клінічного дослідження III фази (подвійне сліпе, з подвійною імітацією, рандомізоване дослідження), що демонструють відсутність відмінностей лікування фітопрепаратом (BNO 1045) порівняно з антибіотикотерапією (фосфоміцину трометамолом ФТ) у разі гострого неускладненого циститу. На заході виступили доктор Зафер Тандогду (м. Единбург, Велика Британія, м. Осло, Норвегія) і доктор Бела Кьовес (м. Будапешт, Угорщина), професори Гернот Бонкат (м. Базель, Швейцарія) і Флоріан Вагенленер (м. Гіссен, Німеччина). Головою симпозіуму був професор Курт Г. Набер (м. Штраубінг, Німеччина).
Резистентність до протимікробних препаратів: роль дослідження GPIU у покращенні терапевтичного ефекту
З. Тандогду представив резистентність до протимікробних препаратів як глобальну клінічну проблему, особливо у випадку урологічних інфекцій. Інфекції, пов’язані з наданням медичної допомоги (ІПМД), асоціюються, зокрема, з високим рівнем резистентності до протимікробних препаратів. Урогенітальні інфекції, пов’язані з наданням медичної допомоги (УІПМД), належать до найпоширеніших ІПМД з приблизною частотою 7-11,0%. Рівень загрози, зумовлений УІПМД, може бути надзвичайно серйозним для пацієнтів, особливо якщо брати до уваги захворюваність і смертність. Кількість моніторингових досліджень, проведених у ХХ ст. з метою накопичення достовірних даних щодо УІПМД, дуже невелика. З іншого боку, декілька провідних досліджень, таких як дослідження EARS-Net Європейського центру з профілактики та контролю захворюваності (European Centre for Disease Prevention and Control – ECDPC), окремо не відстежували ІСШ або урологічних пацієнтів (https://ecdc.europa.eu/en/ about-us/partnerships-and-networks/disease-and-labora- tory-networks/ears-net).
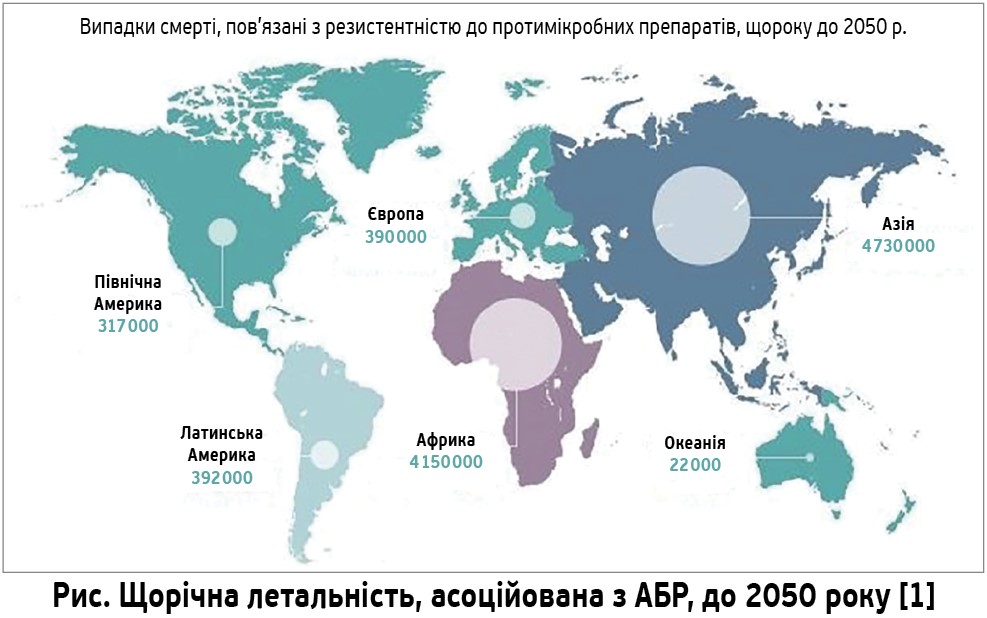
Факт перетворення АБР на загрозу здоров’ю вже не є сенсацією. У 2014 р. Джим О’Ніл і його команда на прохання уряду Сполученого Королівства опублікували огляд, що мав назву «Резистентність до протимікробних препаратів: подолання кризи здоров’я та благополуччя нації» (рис.) [2]. В цьому огляді йшлося, що до 2050 р. AБР може стати причиною 10 млн смертей на рік. Велися дискусії щодо цифри в 10 млн летальних наслідків, наведеної у звіті, оскільки це припущення спирається на статистичні екстраполяції без урахування реальних світових даних. Утім, цзрозуміло, що AБР стане однією з найпоширеніших причин смерті людини, якщо в найближчому майбутньому не вжити рішучих заходів [1].
З метою накопичення більш достовірних даних щодо УІПМД 2003 року Європейським підрозділом урологічних інфекційних захворювань (ESIU) за підтримки Європейської асоціації урологів (EAU) було розпочато дослідження GPIU.
GPIU – це єдине багатоцентрове міжнародне дослідження, розпочате понад 15 років тому, що відстежує УІПМД серед урологічних хворих в усьому світі в рамках протоколу регулярних спостережень. Дослідження GPIU може допомогти надати дані щодо адекватної емпіричної антибіотикотерапії в госпіталізованих урологічних хворих відповідно до керівних рекомендацій.
Основними цілями дослідження є оцінка урологічної практики на предмет контролю госпітальної інфекції та практики застосування антибіотиків, а також оцінка частоти й обставин виникнення ІСШ і хірургічних ранових інфекцій у госпіталізованих урологічних пацієнтів, включно із задіяними патогенами та їх протимікробною резистентністю [3].
Глобальний план дій ВООЗ
Боротьба з АБР є найвищим пріоритетом Всесвітньої організації охорони здоров’я (ВООЗ). Глобальний план дій щодо боротьби з протимікробною резистентністю був затверджений на Всесвітній асамблеї ВООЗ у травні 2015 р. Глобальний план дій націлений на забезпечення профілактики та лікування інфекційних захворювань безпечними й ефективними лікарськими засобами (who.int/news-room/ fact-sheets/detail/antibiotic-resistance).
Глобальний план дій щодо боротьби з резистентністю до протимікробних препаратів має 5 стратегічних цілей:
- підвищувати обізнаність та розуміння резистентності до протимікробних препаратів;
- покращувати контроль та дослідження;
- знижувати частоту виникнення інфекційних захворювань;
- оптимізувати застосування протимікробних препаратів;
- забезпечити постійні інвестиції в протидію резистентності до протимікробних препаратів.
Оптимізація антибіотикотерапії може рятувати життя?
Частота резистентних до лікарських засобів інфекцій становить приблизно 35%, проте може залежати від географічного регіону та проведення місцевої політики щодо контролю за інфекціями. Екстраполяція різних параметрів продемонструвала майже 50% розходження за типом захворювання та застосовуваним антибіотиком. Було підраховано, що у відділеннях з прихильністю до політики контролю за інфекціями було в 1,5 рази більше доступних для застосування антибактеріальних препаратів для лікування складних інфекцій через нижчі рівні резистентності. Зрештою, контрольований і керований вибір антибіотиків покращує стан у 12% пацієнтів. Отже, резистентні до протимікробних засобів інфекції є щоразу більшою проблемою в середовищі надання медичної допомоги, що вимагає негайних коригувальних заходів. З наявною практикою, якщо не дотримуватися програм контролю за інфекціями та не застосовувати дані моніторингу, нам менш імовірно вдасться забезпечити вибір адекватного антибіотика для лікування пацієнта. Дослідження GPIU є прекрасною платформою, що надає підтримку урологам.
Вплив АБР на ведення пацієнтів з ІСШ
Той факт, що ВООЗ оголосила резистентність до протимікробних засобів однією з найбільших загроз глобальному здоров’ю, ілюструє масштаб AБР і її вплив на людство (who.int/news-room/ fact-sheets/detail/antibiotic-resistance). Проблема AБР також впливає на лікування пацієнтів з ІСШ: частота ІСШ, спричинених грамнегативними бактеріями, резистентними до фторхінолонів, і мультирезистентними (МР) мікроорганізмами, постійно зростає. Зрештою, кількість терапевтичних невдач дедалі більшає навіть в емпіричному лікуванні позалікарняних ІСШ. Це зумовлює виникнення діагностичних завдань, які набувають все більшого значення у світлі МР-інфекцій. Як нам слід лікувати гострий епізод нІСШ, якщо її спричинили МР-бактерії, а карбапенеми є єдиними ефективними антибіотиками? Чи маємо бодай якісь альтернативи? Який підхід є найкращим для пацієнта з рецидивуючою безсимптомною бактеріурією, спричиненою патогеном, що продукує β-лактамази розширеного спектра (БЛРС)?
Клінічний випадок: звичайний епізод рецидивуючого циститу
Дуже цікавий клінічний випадок, представлений професором Б. Кьовес під час симпозіуму, стосувався типового епізоду у 26-річної жінки з ІСШ, рецидивуючою від початку статевого життя пацієнтки. Щороку в неї мали місце
Варіантами лікування, які можливо розглянути в таких випадках, є передусім застосування антибіотиків старших поколінь, як рекомендовано в рамках рекомендацій EAU, або ж неантибактеріальна терапія. Звичайно, остання має спиратися на достатні докази, що показують не меншу її ефективність у забезпеченні полегшення симптомів, ніж лікування антибіотиками, зазначеними в настановах EAU щодо лікування неускладненого циститу. Рекомендованим підходом для такого терапевтичного режиму може бути застосування фітотерапевтичного препарату, що підтримується доказами адекватного рівня, тобто комбінації кореня любистку, трави золотисячнику та листя розмарину (BNO 1045) [4].
До стратегій профілактики, які також можуть забезпечити зниження кількості епізодів, як продемонстровано в цьому клінічному спостереженні, належали: збільшення вживання рідини; імуноактивна профілактика; відновлення вагінальної мікрофлори; уникнення факторів ризику; самолікування без застосування антибіотиків.
Результати, наведені в цьому клінічному випадку, показали, що зазначені заходи дозволили досягнути зниження кількості епізодів лише до 2-3 на рік. Незважаючи на певні обмеження, цей клінічний випадок чітко продемонстрував, що належне лікування епізодів рецидивуючої ІСШ обов’язкове, щоб уникнути МР. Лікування гострого циститу, зумовленого БЛРС-продукуючими бактеріями, із застосуванням терапевтичних підходів відповідно до рекомендацій або шляхом застосування доказового симптоматичного лікування без антибіотиків є підходом, що заслуговує на довіру.
Чи можемо ми змінити усталену практику лікування гострого неускладненого циститу?
В усьому світі ІСШ є одним із найчастіших показань для призначення антибіотиків [5]. З огляду на рідкісність ускладнень нІСШ вважаються доброякісними та самовиліковними, основна мета лікування при цьому – досягнення швидкого полегшення симптомів. Симптоми надокучливі, а отже, потенційно докорінно порушують щоденну активність і знижують якість життя [6]. Типові симптоми, що вказують на гострий цистит, можуть проявлятися частим сечовипусканням, імперативними позивами до сечовипускання, пекучими болями при сечовипусканні, відчуттям неповного спорожнення сечового міхура після сечовипускання, болем у нижніх відділах живота та кров’ю в сечі [7].
За останні 10 років деякі загальноприйняті концепції в області урології почали піддаватися сумніву. Наприклад, достатньо шкідливий вплив лікування безсимптомної бактеріурії в здорових невагітних жінок, які не проходять селективних урологічних процедур [8], нині прийнятий і відображений у рекомендаціях [9], тим більше що середовище сечового міхура більше не вважається стерильним [10, 11].
Останні дані тепер також показують, що лікування без застосування протимікробних препаратів може бути привабливим варіантом і забезпечує альтернативу використанню антибіотика як терапію першої лінії [4]. Проте чому ж нам необхідно замінювати антибіотикотерапію? Чи матиме пацієнт будь-які ризики від такої альтернативи? І які варіанти терапії без застосування протимікробних препаратів можна розглядати для гострого циститу?
Поза сумнівом, належна антибіотикотерапія має місце в лікуванні ІСШ. На жаль, це лікування також призводить до АБР уропатогенів і бактерій-коменсалів. Крім того, надмірне та неправильне застосування антибіотиків зменшує їхню ефективність при загрозливих для життя станах, таких як уросепсис. Небажані впливи застосування антибактеріальних засобів на мікробіом кишечнику та вагінальну флору наразі є широко визнаними [12].
Результатом розвитку практики є намагання досягти належного контролю симптомів гострого неускладненого циститу з одночасним скороченням застосування антибіотиків. Хворі жінки стають все більш обізнаними щодо проблем, пов’язаних із надмірним і неправильним застосуванням антибіотиків, а отже, мають більше бажання відтермінувати або навіть уникати застосування антибактеріальних засобів при гострому циститі. Knottnerus і співавт. [13] повідомляли, що понад третина жінок із симптомами ІСШ мали бажання відкласти антибіотикотерапію, якщо їх просив це зробити сімейний лікар. Крім того, більшість із цих жінок повідомляли про спонтанне покращення симптомів через 1 тиж.
Професор Ф. Вагенленер представив 4 порівняльні дослідження, які показують, що стартова терапія нестероїдним протизапальним препаратом (НПЗП) може зменшувати застосування антибіотиків у жінок із неускладненою ІСШ [14-17]. Ігноруючи пілотне дослідження з невеликим розміром вибірки, що порівнювало ібупрофен 400 мг 3 р/добу протягом 3 днів із ципрофлоксацином 250 мг 2 р/добу протягом 3 днів [15], у 3 більших дослідженнях НПЗП – ібупрофен у дозі 400 мг або 600 мг 3 р/добу протягом 3 днів – у порівнянні з ФТ (3 г фосфоміцину) одноразово або з півмецилінамом 200 мг 3 р/добу протягом 3 днів відповідно показав гірші результати, ніж антибіотики [14, 16]. Це справедливо й для порівняння диклофенаку 75 мг 2 р/добу з норфлоксацином 400 мг 2 р/добу протягом 3 днів [17]. Разом із тим в усіх трьох дослідженнях спостерігалося помітне зниження застосування антибіотиків. Проте найбільше зниження застосування антибіотиків спостерігалося для мультимодальної фітотерапевтичної комбінації трьох рослин (BNO 1045) з полегшенням симптомів, зіставним у групах фітотерапії та лікування антибіотиками [4].
У 4 більших дослідженнях [4, 14, 16, 17] у групі лікування без антибіотиків у 5-7 випадках на дослідження виникав пієлонефрит, на відміну від 0-1 випадку при антибіотикотерапії.
Попередження з минулого: варто практикувати обачне застосування антибіотиків при нІСШ
Професор Г. Бонкат, приватний лектор в Університеті Базеля та голова Європейської комісії протоколів для урологічних інфекцій, представив варіанти лікування ІСШ/нІСШ відповідно до чинних європейських міжнародних (і національних) протоколів. Неускладнений цистит спостерігається лише в невагітних жінок без відомих значимих анатомічних або функціональних відхилень сечовидільної системи або супутньої патології [9].
У рамках цієї конкретної дискусії висвітлювалися попередження з минулого. Так, слова Александра Флемінга: «У цьому разі людина, яка бездумно грає з лікуванням пеніциліном, морально відповідальна за смерть людини, яка помирає від пеніцилінорезистентної інфекції. Сподіваюся, біду можна попередити», показують, що винахідник пеніциліну скоро зрозумів не лише те, наскільки корисними є препарати, що мають антибактеріальний ефект, а й те, наскільки небезпечним може бути майбутнє без них [18]. Сьогодні ми думаємо, що А. Флемінг передбачав проблеми, пов’язані з МР-мікроорганізмами, резистентними щонайменше до одного класу протимікробних препаратів. Інша проблема полягає в тому, що все більше великих фармацевтичних компаній оголошують завершення досліджень антибіотиків (https://www.busi- nessinsider.de/major-pharmaceutical-companies-drop- ping-antibiotic-projects-superbugs‑2018-7?r=US&IR=T). Насправді асортимент розроблюваних антибіотиків достатньо вузький, з малою кількістю або й взагалі без інноваційних нових засобів, а також препаратів для лікування захворювань, що найчастіше зумовлюються антибіотикорезистентними бактеріями, як-от ІСШ (reactgroup.org/ news-and-views/news-and-opinions/year‑2018/whats- cooking-in-the-antibiotic-pipeline/).
Клінічно доведені альтернативи антибіотикам для лікування нІСШ
Професор Ф. Вагенленер повідомив про нещодавно опубліковане дослідження ефективності, яке порівнювало комбінацію лікарських трав BNO 1045 та одноразовий прийом фосфоміцину (у вигляді ФТ) серед жінок із гострими неускладненими нІСШ. BNO 1045 являє собою таблетку з оболонкою, що містить порошок трави золототисячнику (Centaurii herba) 18 мг, корінь любистку (Levistici radix) 18 мг і листя розмарину (Rosmarini folium) 18 мг. Рандомізоване подвійне сліпе міжнародне дослідження III фази за участю 659 жінок із гострими неускладненими нІСШ (AUC) показало, що фітофармацевтичний препарат BNO 1045 має не меншу ефективність, ніж антибіотикотерапія шляхом одноразового прийому ФТ, щодо терапевтичного ефекту та зменшення вираженості симптомів. Фітоекстракт із його багатоспрямованою активністю представляє корисний варіант симптоматичного лікування.
Протизапальний [19], знеболювальний [20], спазмолітичний [21] та антиадгезивний ефекти [19] спеціального екстракту BNO 1045 були продемонстровані в різноманітних доклінічних дослідженнях in vivo та in vitro.
Віднесення цих фармакологічних ефектів до клінічних переваг висвітлене в рандомізованому контрольованому подвійному сліпому, з подвійною імітацією, багатоцентровому міжнародному дослідженні III фази, що включало 659 жінок віком 18-70 років із типовими симптомами вперше діагностованого гострого неускладненого циститу [4]. Пацієнтки в групі BNO 1045 отримували протягом 7 днів по 2 таблетки BNO 1045 3 р/добу плюс одноразово
Показано, що 83,5% пацієнток у групі BNO 1045 та 89,8% жінок у групі ФТ не потребували додаткової антибіотикотерапії. Таким чином, комбінація трьох лікарських рослин статистично була не менш ефективною, ніж антибіотик ФТ, у лікуванні гострого неускладненого циститу щодо первинної кінцевої точки (∆= -6,3%, нижча межа довірчого інтервалу: -11,99%; p=0,0014). Зникнення симптомів (вимірювалося із застосуванням шкали симптомів гострого циститу – ACSS [22] – як сумарна оцінка для типових симптомів) було зіставним в обох групах протягом дослідження. Фітотерапія добре переносилася.
Отже, BNO 1045 є доведеною ефективною заміною антибіотикам для лікування гострого неускладненого циститу в жінок і допомагає значною мірою скоротити амбулаторне застосування антибактеріальних засобів. Це надзвичайно важливо в контексті стратегії раціонального використання антибіотиків та в кінцевому підсумку уникнення небезпеки АБР (who.int/news-room/fact-sheets/de- tail/antibiotic-resistance).
Висновки
Як одні з найпоширеніших бактеріальних інфекцій, що особливо часто уражають жінок, ІСШ мають не лише велике індивідуальне, а й соціально-економічне значення. Насамперед рекомендується проведення антибіотикотерапії, яка, однак, пов’язана з розвитком протимікробної резистентності та ушкодженням природної мікробіоти. Критичний перегляд застосування антибіотиків та інтенсивний пошук альтернатив, який до того ж відповідає бажанням багатьох жінок, привели до роздумів щодо проведення виключно симптоматичної терапії гострих неускладнених інфекцій нижніх відділів сечовивідних шляхів. Останні дослідження з використанням НПЗП показали значне зниження застосування антибіотиків для симптоматичного стартового лікування, проте з вищою частотою виникнення симптомів.
Нове клінічне дослідження засвідчило, що спеціальний екстракт трьох лікарських рослин: розмарину, золототисячнику та любистку – має не меншу ефективність, ніж фосфоміцин, в аспекті терапевтичного впливу. Крім того, зменшення вираженості симптомів за шкалою ACSS було зіставного рівня. Це дослідження може стимулювати більш широке застосування доказових альтернатив антибіотикотерапії для лікування неускладнених інфекцій нижніх відділів сечовивідних шляхів у рутинній клінічній практиці, зменшуючи розповсюджене застосування антибіотиків.
Стаття друкується в скороченні.
Список літератури знаходиться в редакції.
Naber et al. UTI – quo vadis? New alternatives to treat uncomplicated urinary tract infections
Clinical Phytoscience 2019; 5: 40. Doi: 10.1186/s40816-019-0132-0
Медична газета «Здоров’я України 21 сторіччя» № 23 (468), грудень 2019 р.