21 січня, 2020
Конгрес EAACI‑2019
 1-5 червня в Лісабоні (Португалія) відбувся черговий конгрес Європейської академії алергії та клінічної імунології (EAACI-2019). Ця масштабна подія об’єднала тисячі лікарів із багатьох країн світу та подарувала можливість поглибити свої знання у сфері сучасної алергології та клінічної імунології. Представлені на конгресі доповіді та воркшопи, які охопили 17 розділів імунології та алергології, стосувалися картографічної структури алергенів, аеробіології, ендотипів захворювання, біологічних препаратів, а також геноміки, протеоміки та метаболоміки. Усі делегати отримали ефективні алгоритми для кращого розуміння алергічних та імунних розладів, засновані на принципах доказової медицини, та познайомилися з результатами найбільш перспективних досліджень у цій сфері.
1-5 червня в Лісабоні (Португалія) відбувся черговий конгрес Європейської академії алергії та клінічної імунології (EAACI-2019). Ця масштабна подія об’єднала тисячі лікарів із багатьох країн світу та подарувала можливість поглибити свої знання у сфері сучасної алергології та клінічної імунології. Представлені на конгресі доповіді та воркшопи, які охопили 17 розділів імунології та алергології, стосувалися картографічної структури алергенів, аеробіології, ендотипів захворювання, біологічних препаратів, а також геноміки, протеоміки та метаболоміки. Усі делегати отримали ефективні алгоритми для кращого розуміння алергічних та імунних розладів, засновані на принципах доказової медицини, та познайомилися з результатами найбільш перспективних досліджень у цій сфері.
 Регулярний прийом бактеріального лізату з 21 виду бактерій зменшує кількість загострень бронхіальної астми (БА) у школярів та епізодів свистячих хрипів (візингу) у дітей дошкільного віку.
Регулярний прийом бактеріального лізату з 21 виду бактерій зменшує кількість загострень бронхіальної астми (БА) у школярів та епізодів свистячих хрипів (візингу) у дітей дошкільного віку.
Пероральний бактеріальний лізат (БЛ) Broncho Vaxom, який приймають курсами по 10 днів поспіль протягом 3 міс, не зареєстрований у США та частині країн Європи у зв’язку з недостатньою кількістю даних щодо ефективності та безпеки. Цей препарат досі розглядався як засіб альтернативної медицини, але результати двох метааналізів, проведених у Польщі та Нідерландах, показали перспективи його використання для профілактики хронічних захворювань органів дихання в дітей.
БЛ – це коктейль із неактивних екстрактів патогенних респіраторних бактерій. Мікроорганізми піддаються впливу високих температур для руйнування клітинної структури, але білки при цьому залишаються неушкодженими. Потрапивши в кишечник, білки активують дендритні клітини, які підвищують імунну модуляцію, стимулюють вироблення антитіл і нормалізують Th1/Th2 баланс цитокінів, що забезпечує захист дихальних шляхів від патогенів.
У Нідерландах авторами метааналізу стали de Boer та співавтори. Після огляду англомовної літератури критеріям включення відповідали 24 дослідження, де повідомлялося про ефективність препарату в якості додаткової терапії для профілактики інфекцій дихальних шляхів.
Дослідники виявили, що частота загострень астми після лікування за допомогою БЛ у пацієнтів віком 6-18 років була значно нижчою в порівнянні з плацебо (середня різниця –0,86; р<0,00001). Крім того, у досліджуваній групі спостерігалося зменшення загострень хронічного обструктивного захворювання легень на 23% (відносний ризик (ВР) 0,77; р=0,0002). Прийом БЛ також знижував рівень людського інтерлейкіну (IL)-4 та збільшував сироваткові рівні IL‑10, інтерферону-γ та CD4+ клітин, що є імунологічно сприятливим при респіраторних захворюваннях.
Більшість досліджень мали недостатню силу доказів, але всі вони показали, що Broncho Vaxom достовірно зменшує частоту захворювань дихальних шляхів. Наразі de Boer із командою набирає учасників для нової наукової роботи, в якій буде оцінюватися вплив БЛ на частоту загострень БА в дорослих із паралельним моніторингом даних мікробіому, що стане першим подібним дослідженням.
Результати метааналізу, проведеного в Польщі, представив увазі присутніх Якуб Золкевич (Jakub Zolkiewicz). Включені в метааналіз дослідження хоч і були слабкими, але показали достовірне зниження частоти виникнення епізодів візингу в дітей дошкільного віку.
 Подвійне сліпе паралельне плацебо-контрольоване дослідження ефективності оральних бактеріальних лізатів у запобіганні захворюванням нижніх дихальних шляхів, що супроводжуються візингом (ORBEX), проводиться наразі у США. Сьогодні приблизно 30% дітей переносять епізоди візингу протягом першого року життя. Зростання показника захворюваності пов’язують зі зменшенням контакту дітей із мікробами, що призводить до незрілості імунної системи.
Подвійне сліпе паралельне плацебо-контрольоване дослідження ефективності оральних бактеріальних лізатів у запобіганні захворюванням нижніх дихальних шляхів, що супроводжуються візингом (ORBEX), проводиться наразі у США. Сьогодні приблизно 30% дітей переносять епізоди візингу протягом першого року життя. Зростання показника захворюваності пов’язують зі зменшенням контакту дітей із мікробами, що призводить до незрілості імунної системи.
Епідеміологічні дослідження серед сімей амішів, які займаються фермерством та часто контактують із тваринами, виявили практично повну відсутність епізодів візингу та випадків БА в дітей, що й лягло в основу пошуку засобу для безпечного підвищення рівня антигенного навантаження, яким може стати Broncho Vaxom.
Регулярне нанесення емолієнтів дітям 1-го року життя не запобігає виникненню атопічного дерматиту (АД)
 Емолієнти є основою лікування пацієнтів з АД, саме тому низка дослідників вирішили оцінити ефективність цих засобів в якості профілактики захворювання. Результати двох великих незалежних клінічних досліджень показали, що емолієнти не запобігають АД.
Емолієнти є основою лікування пацієнтів з АД, саме тому низка дослідників вирішили оцінити ефективність цих засобів в якості профілактики захворювання. Результати двох великих незалежних клінічних досліджень показали, що емолієнти не запобігають АД.
Першу дослідницьку роботу з профілактики АД та алергій у дітей – PreventADALL було проведено Skjerven і співавторами. Відбір учасників розпочався ще в допологовому періоді під час планового ультразвукового дослідження. Критеріями виключення стали: наявність понад 2 плодів; народжені до 35-го тиж вагітності; народжені з тяжкими захворюваннями.
Наступного дня після пологів 2397 немовлят були рандомізовані до однієї з 4 груп: 575 дітей – у групу шкірного втручання, 642 дитини – у групу харчового втручання, 583 немовляти – у групу шкірного й харчового втручань, 597 немовлят – у групу без втручань.
У групі шкірного втручання немовлят купали у воді з рідким парафіном та трилаурет‑4-фосфатною олією, а обличчя змазували кремом Ceridal. Комплаєнс визначався при використанні масляної ванни та крему не менше ніж 3, 5 днів на тиждень протягом 16 із 25 тижнів.
Усі діти перебували на грудному вигодовуванні, але немовлятам із групи харчового втручання у віці від 3 до 6 міс у прикорм вводили арахіс, молоко, пшеницю та яйця.
Через 12 міс стан 2172 немовлят оцінили з метою виявлення АД (первинна кінцева точка); 224 учасники вибули зі спостереження, 1 учасник відкликав згоду на участь у дослідженні. Результати виявилися не такими, як очікувалося. У немовлят у віці 12 міс АД частіше фіксували в малюків із груп шкірного або харчового втручань на відміну від немовлят, які отримували обидва види втручань або не отримували зовсім (11,1 проти 9,0 проти 5,3 проти 8,1% відповідно; р=0,000). Таким чином, раннє посилення шкірного бар’єру або введення прикорму не слугувало профілактикою розвитку АД.
Аналогічні результати було отримано в дослідженні Boyle та співавт. «Посилення бар’єру для запобігання екземі» (BEEP). Дослідники вивчали частоту виникнення АД у когорті 2-річних дітей, які після народження були рандомізовані на 2 групи: досліджувану й контрольну. Усі учасники дослідження мали близького родича з діагнозом «екзема», «алергічний риніт» або БА.
Батьки 693 немовлят із досліджуваної групи мали застосовувати емолієнт у вигляді крему або гелю протягом 12 місяців. Батькам 701 дитини з контрольної групи заборонялося наносити креми та гелі.
Комплаєнс у досліджуваній групі (використання емолієнтів не менше ніж 3 дні на тиждень) становив 74%, у контрольній – 85%.
 Після двох років під спостереженням залишилося 598 дітей у досліджуваній групі та 612 – у контрольній. Частота виникнення АД у групі втручання та контролю була порівнянна (23 проти 25%; скоригований ВР 0,95; р=0,61). Вік першого епізоду АД також практично не відрізнявся в досліджуваній та контрольній групах як наприкінці 1-го (20 проти 20%), так і 2-го року спостереження (31 проти 32%).
Після двох років під спостереженням залишилося 598 дітей у досліджуваній групі та 612 – у контрольній. Частота виникнення АД у групі втручання та контролю була порівнянна (23 проти 25%; скоригований ВР 0,95; р=0,61). Вік першого епізоду АД також практично не відрізнявся в досліджуваній та контрольній групах як наприкінці 1-го (20 проти 20%), так і 2-го року спостереження (31 проти 32%).
Отримані результати неабияк розчарували дослідників та спростували попередні дані, отримані в невеликих пілотних дослідженнях.
Прояви алергічних реакцій на котів можна значуще зменшити завдяки додаванню в раціон тварин anti-Fel d1 IgY
 Результати нового дослідження виявилися справді революційними: відтепер людям з алергією на котів не доведеться відмовлятися від улюбленців, достатньо скорегувати їхнє харчування.
Результати нового дослідження виявилися справді революційними: відтепер людям з алергією на котів не доведеться відмовлятися від улюбленців, достатньо скорегувати їхнє харчування.
Група дослідників під керівництвом Ebenezer Satyaraj годували курей великою кількістю білка Fel d1, який спричиняє 95% випадків алергії на котів. Кури виробляли антитіла й відкладали яйця, які містили анти-Fel d1. Виготовлений із цих яєць корм давали кішкам. Анти-Fel d1 нейтралізував Fel d1 в їхній слині, а коли коти вмивалися, антиген прилипав до їхньої шерсті. У результаті кількість активного Fel d1 зменшилася на 47% (р=0,001).
Анти-Fel d1 діє саме в ротовій порожнині, а не в кишечнику. Оскільки коти зазвичай їдять кілька разів на день, кількість анти-Fel d1 у роті постійно зростає.
 Wedner і співавт. у своєму подвійному сліпому перехресному дослідженні оцінювали 11 людей без БА, які по-різному реагували на високий і низький рівень Fel d1 під час первинного тестування.
Wedner і співавт. у своєму подвійному сліпому перехресному дослідженні оцінювали 11 людей без БА, які по-різному реагували на високий і низький рівень Fel d1 під час первинного тестування.
У трьох різних випадках учасники експерименту перебували 3 год у закритих камерах, заповнених ковдрами із шерстю котів, які отримували анти-Fel d1, або ковдрами із шерстю котів із контрольної групи.
На 1-му тиж камеру наповнили ковдрами котів із групи контролю, які дотримувалися звичної дієти. На 2-му тиж учасників помістили в камеру, наповнену ковдрами котів досліджуваної або контрольної групи. На 4-му тиж учасники потрапляли в кімнату, протилежну тій, в якій вони знаходилися на 2-му тижні.
 Під час перебування в кожній із камер учасники заповнювали дві анкети з оцінки якості життя – загальний показник назальних симптомів (TNSS) та загальний показник очних симптомів (TOSS) – кожні 15 хвилин. Оцінка за TNSS на 1-му тиж виявилася достовірно кращою в досліджуваній групі в порівнянні з групою контролю (р=0,035); закладеність носа також була меншою (р=0,055). Поліпшення було зафіксовано і за шкалою TOSS, але воно не було достовірним, хоча при змішаній моделі аналізу свербіж очей був набагато нижчим у досліджуваній групі (р=0,015).
Під час перебування в кожній із камер учасники заповнювали дві анкети з оцінки якості життя – загальний показник назальних симптомів (TNSS) та загальний показник очних симптомів (TOSS) – кожні 15 хвилин. Оцінка за TNSS на 1-му тиж виявилася достовірно кращою в досліджуваній групі в порівнянні з групою контролю (р=0,035); закладеність носа також була меншою (р=0,055). Поліпшення було зафіксовано і за шкалою TOSS, але воно не було достовірним, хоча при змішаній моделі аналізу свербіж очей був набагато нижчим у досліджуваній групі (р=0,015).
 Незважаючи на те що в дослідженні використовувався метод засліплення, більшість учасників із точністю могли сказати, чи знаходилися вони в камері зі зменшеною кількістю алергенів, чи в контрольній камері.
Незважаючи на те що в дослідженні використовувався метод засліплення, більшість учасників із точністю могли сказати, чи знаходилися вони в камері зі зменшеною кількістю алергенів, чи в контрольній камері.
У деяких пацієнтів з АД новий препарат – комбінація Янус-кінази (JAK) та інгібітора тирозинкінази селезінки (SYK), відома як ASN002 (Asana BioSciences), може знизити рівень Staphylococcus aureus у шкірному мікробіомі
Staphylococcus aureus часто висівають зі шкіри пацієнтів з АД, але бактерії не виявляються на шкірі здорових людей. Роль S. аureus при АД незрозуміла, але навряд чи він є причиною захворювання. Швидше за все, ослаблений шкірний бар’єр є сприятливим фактором для росту цього патогена.
Neumann та співавт. оцінювали вплив ASN002 на рівень колонізації S. aureus у шкірному мікробіомі пацієнтів з АД (від легкого до тяжкого). У дослідженні фази 1b 36 пацієнтів із середньотяжким і тяжким АД були рандомізовані для перорального прийому ASN002 в одній із трьох доз – 20 мг, 40 мг або 80 мг або плацебо протягом 28 днів.
На 29-й день оцінювали зміну індексу тяжкості АД (EASI) від вихідного рівня. Первинною кінцевою точкою було зниження показника EASI щонайменше на 50% (EASI 50). Результати відображені в таблиці.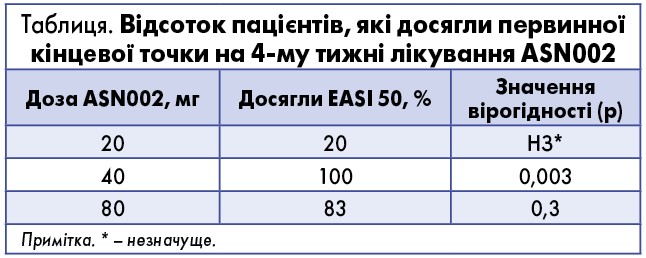
У подальшому Neumann та співавт. оцінювали склад мікробіому шкіри на початку лікування, 29-й та 43-й день терапії. Науковці сподіваються, що рівень колонізації S. аureus зможе використовуватися як прогностичний чинник для визначення ефективності терапії Янус-кіназою у хворих на АД.
Рівень довіри між пацієнтами та лікарями відіграє вагому роль в ефективності терапії хворих на харчову алергію.
 Більшість пацієнтів із харчовими алергіями страждають на невпевненість та тривожність через своє захворювання, що часто призводить до обмеження вживання навіть тих продуктів, на які пацієнти не мають алергії. Це загрожує виникненням розладів харчової поведінки. Важливо, щоб пацієнти отримували максимально збалансоване харчування. А цього можна досягнути лише за умови довіри в тандемі лікар-пацієнт.
Більшість пацієнтів із харчовими алергіями страждають на невпевненість та тривожність через своє захворювання, що часто призводить до обмеження вживання навіть тих продуктів, на які пацієнти не мають алергії. Це загрожує виникненням розладів харчової поведінки. Важливо, щоб пацієнти отримували максимально збалансоване харчування. А цього можна досягнути лише за умови довіри в тандемі лікар-пацієнт.
Завжди необхідно враховувати такі фактори:
- Культурні та соціально-економічні особливості сім’ї хворого.
- Рівень освіти та інтелекту. Завжди потрібно розмовляти з пацієнтами на зрозумілій для них мові, не використовувати складні терміни та спокійно реагувати на інформацію, знайдену хворими в інтернеті, з приводу якої вони хочуть порадитися.
- Стать. Зазвичай юнаки та дівчата по-різному ставляться до свого захворювання. У той час як хлопці дуже неохоче розповідають своїм друзям про харчову алергію, що відносить їх до групи ризику, дівчата не проти поговорити про свої харчові проблеми, вважаючи захворювання фактором, який робить їх «особливими».
Дотримання всіх цих рекомендацій посприяє встановленню більш довірливих стосунків із пацієнтами, що підвищить рівень їхньої прихильності до лікування.
EAACI‑2019 допоміг усім учасникам цього заходу набути наукового, культурного та соціально-інтерактивного досвіду у своїй дуже важливій у сучасній світовій медицині сфері. Отримані на конгресі знання дадуть можливість застосовувати як в науковій, так і в клінічній практиці більш індивідуалізовані схеми лікування алергічних та імунних захворювань.
Підготувала Ганна Кирпач
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3 (48), 2019 р.




