7 лютого, 2020
Гастропарез і демпінг-синдром: сучасні концепції та ведення пацієнтів
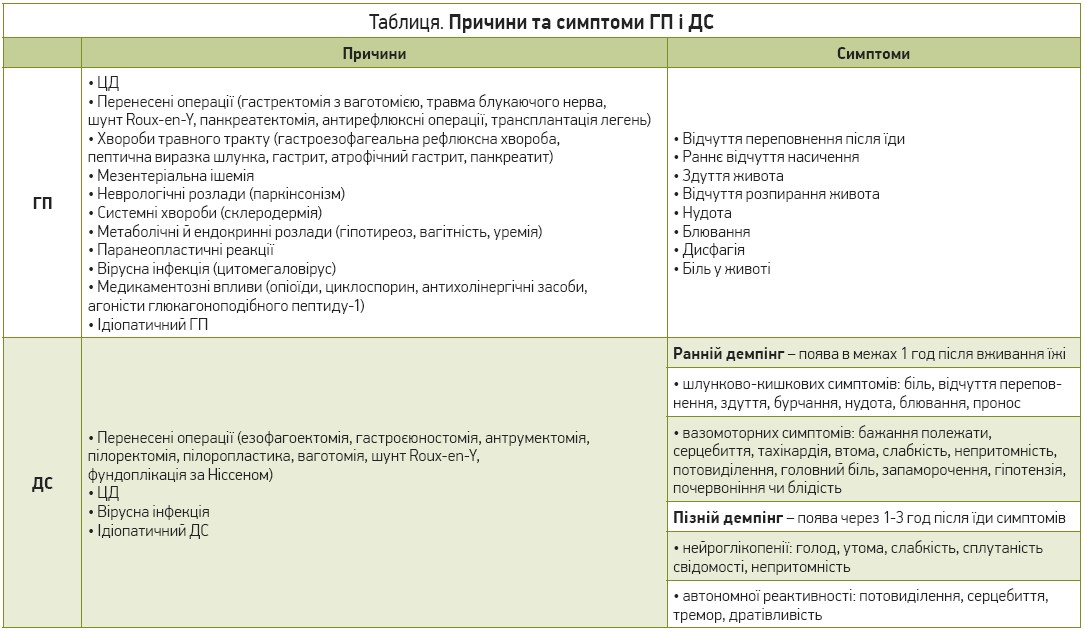
Гастропарез (ГП) – це синдром, який характеризується типовими симптомами (табл.), об’єктивною затримкою випорожнення шлунка за відсутності його механічної непрохідності (Bharucha A., 2015). Через те, що не всі пацієнти звертаються по медичну допомогу, а лікарі недостатньо ретельно оцінюють симптоми та проводять подальшу діагностику, цей стан часто не діагностують.
Поширеність ГП у загальній популяції чітко не визначена, в середньому – 1,8% (Rey E. et al., 2012). Серед пацієнтів переважають жінки (70%) та особи віком понад 65 років (Nusrat S., Bielefeldt K., 2013). Ризик вищий у хворих на цукровий діабет (ЦД) 1 типу, серед яких 10-річна частота ГП сягає 5,2% проти 1% у хворих на ЦД 2 типу та 0,2% в осіб без діабету (Choung R. et al., 2012). Дослідження, що включали пацієнтів зі спеціалізованих центрів, демонструють набагато вищі показники – 58 і 30% у хворих на ЦД 1 та 2 типів відповідно (Horowitz M. et al., 1991). Іншою групою ризику є пацієнти після хірургічних втручань, хоча частота післяопераційного ГП залежить від виду втручання: 0,4-5,0% – після гастректомії, 20-50% – після пілорозберігальної панкреатодуоденектомії (Dong K. et al., 2006) та 67% – після кріоабляції раку підшлункової залози (Dong K. et al., 2004).
Демпінг-синдром (ДС) є частим післяопераційним ускладненням, яке виникає внаслідок швидкого проходження їжі в тонкий кишечник через зміни анатомії шлунка після стравохідної, шлункової та баріатричної хірургії (Camilleri M. et al., 2011; van Beek A. et al., 2017). За часом появи симптомів після вживання їжі ДС поділяють на ранній (упродовж 1 год) і пізній (від 1 до 3 год) (Tack J. et al., 2009, 2014). Частіше трапляється ранній демпінг, у чверті пацієнтів можливий пізній демпінг (Tzovaras G. et al., 2012), іноді спостерігається поєднана форма.
Поширеність ДС також істотно залежить від виду хірургічного втручання: у кожного п’ятого пацієнта – після ваготомії та пілоропластики, у 40% – після шунтування шлунка (Roux-en-Y) і рукавної гастропластики, у кожного другого – після езофагоектомії (Papamargaritis D. et al., 2012; Banerjee A. et al., 2013). Розповсюдженість синдрому продовжує зростати через епідемію ожиріння та часте проведення баріатричних операцій (Berg P., McCallum R., 2016).
Причини, патофізіологія та клінічні прояви
Підозра на ці порушення має виникати за умови появи після прийому їжі симптомів, указаних у таблиці. Більшість проявів не є специфічними, вони можуть спостерігатися при багатьох інших хворобах, але наявність специфічних етіологічних факторів збільшує ймовірність діагнозу.
В етіології ГП домінують діабет і перенесені хірургічні втручання (Hyett B. et al., 2009). Іноді причину не вдається з’ясувати (ідіопатичний ГП), що частіше трапляється в молодих жінок і приблизно у 20% випадків пов’язано з вірусною інфекцією (Oh J. et al., 1990; Bityutskiy L. et al., 1997). Рідше ГП спричиняють хвороба Паркінсона, амілоїдоз, пухлини, склеродерма та мезентеріальна ішемія (Camilleri M. et al., 2013). Окрему групу становить медикаментозний ГП, який завжди треба виключати, особливо за умови застосування агоністів глюкагоноподібного пептиду‑1 (ГГП‑1), антихолінергічних засобів, опіоїдів і циклоспорину (Maes B. et al., 1999; Salehi M. et al., 2008). Вплив агоністів ГГП‑1 треба завжди підозрювати у хворих на ЦД, перш ніж вважати, що це діабетичний ГП. Затримка евакуації шлункового вмісту спостерігається у 28-65% хворих на ЦД (Jones K. et al., 2001; Samsom M. et al., 2003). ГП здебільшого виникає через 10 років після появи ЦД та корелює з мікросудинними ускладненнями, зокрема ретино- й невропатією, поганим глікемічним контролем, незадовільним харчовим статусом, а також із ризиком гіпоглікемії (Jung H. et al., 2009; Choung R. et al., 2012; Camilleri M. et al., 2013; Horváth V. et al., 2014).
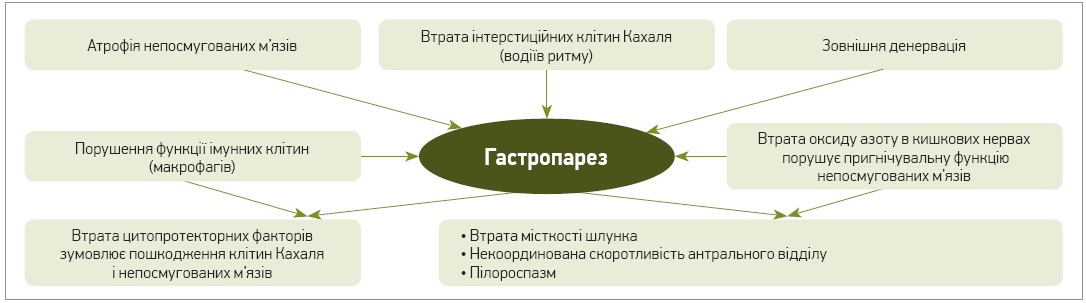
З‑поміж механізмів, які спричиняють затримку евакуації шлункового вмісту (рис. 1), розглядають зовнішню денервацію шлунка, порушення пригнічувальних впливів на непосмуговані м’язи внаслідок нижчого вмісту оксиду азоту в кишкових нервах, втрату інтерстиційних клітин Кахаля, атрофію гладеньких м’язів і порушення функції імунних клітин (Camilleri M. et al., 2011). Клітини Кахаля є водіями ритму, бо генерують повільні електричні імпульси в шлунку, забезпечуючи спонтанну моторику та перистальтику травного тракту. Порушення в мережі клітин пейсмейкерів і шлункові дизритмії призводять до ГП (O’Grady G. et al., 2012).
ГП пов’язаний зі значною захворюваністю та смертністю, а його симптоми часто виснажливі (Bielefeldt K., 2012; Woodhouse S. et al., 2017). Найчастіше пацієнтів турбують раннє відчуття ситості, повноти чи розпирання після їди, нудота, блювання, здуття та біль у верхній частині живота (Liu N., Abell T., 2017). Останнім симптомом часто нехтують лікарі, хоча він виникає в 72-90% пацієнтів. У 72% біль з’являється після їди, в 74% – у нічний час (Cherian D. et al., 2010; Camilleri M. et al., 2013). Отже, не пов’язаний зі вживанням їжі біль не виключає ГП. Усі пацієнти страждають від нудоти, котра в поєднанні з блюванням знижує якість життя (Cherian D., Parkman H., 2012). Натомість втрата маси тіла не характерна для ГП. Важливо, що обов’язковою умовою для діагностики ГП є наявність симптомів.
При синдромі раннього демпінгу швидкий перехід їжі в тонку кишку зумовлює рідинний зсув унаслідок гіперосмолярності та вивільнення шлунково-кишкових гормонів. Серед них найбільше значення мають інсулін, глюкагон і вазоактивні речовини – інкретини (ГПП‑1 і шлунковий інгібіторний поліпептид), нейростатин і вазоактивний кишковий пептид (Tack J., 2007). Вивільнення гормонів спричиняє шлунково-кишкові та вазомоторні симптоми (табл.). Основним вазомоторним симптомом є гіпотензія, що виникає внаслідок зсуву рідини й активації симпатичної нервової системи (Tack J. et al., 2009, 2014).
За умови пізнього демпінгу швидке всмоктування глюкози, зумовлене наявністю неперетравлених вуглеводів у тонкій кишці, посилює вивільнення ГПП‑1, що перевищує вплив інсуліну та призводить до гіпоглікемії через
Хоча вказані механізми зазвичай виникають після хірургічних втручань, демпінг можливий і в неоперованих пацієнтів. У цьому разі прискорення евакуації шлункового вмісту зумовлене розладами внутрішньої іннервації, основною причиною яких є ЦД (Mehagnoul-Schipper D. et al., 2000; van Beek A. et al., 2017). Отже, діабет може спричиняти як затримку, так і прискорене випорожнення шлунка. Демпінг частіше виникає на ранніх стадіях захворювання та переважає в пацієнтів із ЦД 2 типу. Через схожість симптомів у хворих на ЦД іноді важко диференціювати ці стани, блювання збільшує ймовірність ГП, а діарея – демпінгу (Hejazi R. et al., 2010).
Описані також ідіопатичні форми демпінгу, найімовірніше, спричинені вірусною інфекцією, оскільки половина таких пацієнтів повідомляє про симптоми гастроентериту в анамнезі (Berg P. et al., 2014).
Симптоми за умови раннього демпінгу зазвичай з’являються через 30-60 хв після вживання їжі та включають шлунково-кишкові й вазомоторні (Tack J. et al., 2009). Симптоми пізнього демпінгу зумовлені вегетативною реактивністю та нейроглікопенією (Eagon J. et al., 1992). ДС не лише суттєво погіршує якість життя, а й може призвести до зменшення маси тіла на 30% (Arts J. et al., 2009). Причинами госпіталізації є гіпоглікемія, епізоди сплутаності чи непритомності, судоми, епілепсія (Marsk R. et al., 2010).
Діагностика
ГП та ДС треба диференціювати з кількома органічними й функціональними хворобами. Особливо важко диференціювати демпінг і синдром подразненого кишечнику, функціональну диспепсію та ГП (Tack J. et al., 2004; Camilleri M. et al., 2013). Тому точний діагноз можна встановити лише після проведення певних тестів (Bredenoord A. et al., 2003).
Діагноз ГП встановлюють на підставі ретельно зібраного анамнезу й об’єктивного обстеження, що допомагають виявити характерні симптоми та виключити інші хвороби. Наступним діагностичним кроком є фіброгастродуоденоскопія (ФГДС) для виключення механічної непрохідності шлунка. Для підтвердження затримки евакуації шлункового вмісту потрібні сцинтиграфія шлунка, дихальний тест і бездротова телеметрична капсула для оцінки моторики (Tougas G. et al., 2000; Abell T. et al., 2008). Отже, ГП діагностують за наявності типових симптомів, які корелюють із прийомом їжі, після встановлення затримки спорожнення шлунка (Camilleri M. et al., 2013). Важливо, що навіть підтверджена затримка евакуації шлункового вмісту в безсимптомного пацієнта не дає змоги діагностувати ГП.
Золотим стандартом і найуживанішою методикою встановлення затримки випорожнення шлунка є сцинтиграфія. Проте деякі європейські центри частіше застосовують дихальні тести через простоту виконання та добру кореляцію з результатами сцинтиграфії (Keller J. et al., 2018). Тестовий прийом їжі зазвичай включає білий хліб, масло, воду та яєчний омлет з октановою кислотою, що містить 13С. Після цього оцінюють уміст 13C у видихуваному повітрі (Camilleri M., 2007).
Альтернативним методом оцінки фізіології шлунка, його спорожнення та моторики без застосування іонізувального випромінювання є магнітно-резонансна томографія (МРТ). З’являється дедалі більше доказів того, що МРТ є надійним неінвазивним методом діагностики ГП (de Zwart I., de Roos A., 2010).
Зважаючи на важливість порушення генерації імпульсів клітинами Кахаля в патофізіології ГП, ще одним потенційним діагностичним тестом є вимірювання повільних хвиль. Комбінація електрогастрограми та магнітогастрограми дає змогу відрізнити пацієнтів із ГП від пацієнтів групи контролю (Bradshaw L. et al., 2016).
Для діагностики ДС важливими є попередні операції та наявність типових симптомів. Для ідентифікації клінічно значущих симптомів демпінгу запропоновано дві анкети – шкала Sigstad та опитувальник Arts (van Beek A. et al., 2017; Arts J. et al., 2009). Також можна використовувати просту візуальну аналогову шкалу (Mine S. et al., 2010).
Порівняно з ГП об’єктивні тести для оцінки демпінгу менш опрацьовані. Вимірювання глюкози крові можна розглядати лише в пацієнтів із симптомами пізнього демпінгу (van Beek A. et al., 2017). За умови гіпоглікемії надійніше визначати рівень глюкози в плазмі крові, а не в капілярній крові. Діагностичними вважаються рівні глікемії в межах 2,8-3,3 ммоль/л (Ritz P., Hanaire H., 2011).
Більшу діагностичну цінність мають провокаційні проби. Це оральний глюкозотолерантний тест (ОГТТ) і тест на толерантність змішаної їжі (van der Kleij F. et al., 1996). Під час ОГТТ пацієнт приймає всередину 50 або 75 г цукру, після чого кожні 30 хв упродовж 3 год вимірюють уміст глюкози в крові, гематокрит, артеріальний тиск і пульс. Збільшення гематокриту на 3% та/або прискорення пульсу за 10 хв свідчать про ранній демпінг, тоді як розвиток гіпоглікемії вказує на пізній (Tack J. et al., 2009). Другий тест передбачає оральне споживання їжі, котра включає вуглеводи, жири та білки, з наступним визначенням глюкози й інсуліну кожні 30 хв (Salehi M. et al., 2014; Khoo C. et al., 2014). Однак треба пам’ятати, що епізоди гіпоглікемії після прийому їжі можливі навіть у здорових людей, тому цей тест має високу ймовірність хибнопозитивних результатів (Emous M. et al., 2015).
Проводять також дослідження випорожнення шлунка, хоча їх специфічність і чутливість доволі низькі (van Beek A. et al., 2017).
Лікування
Стратегії лікування ГП та ДС схожі. На сьогодні рекомендовано мультидисциплінарний підхід, першим етапом якого є модифікація харчування й освіта пацієнта, другим – фармакотерапія, заключним – хірургічні втручання (рис. 2).
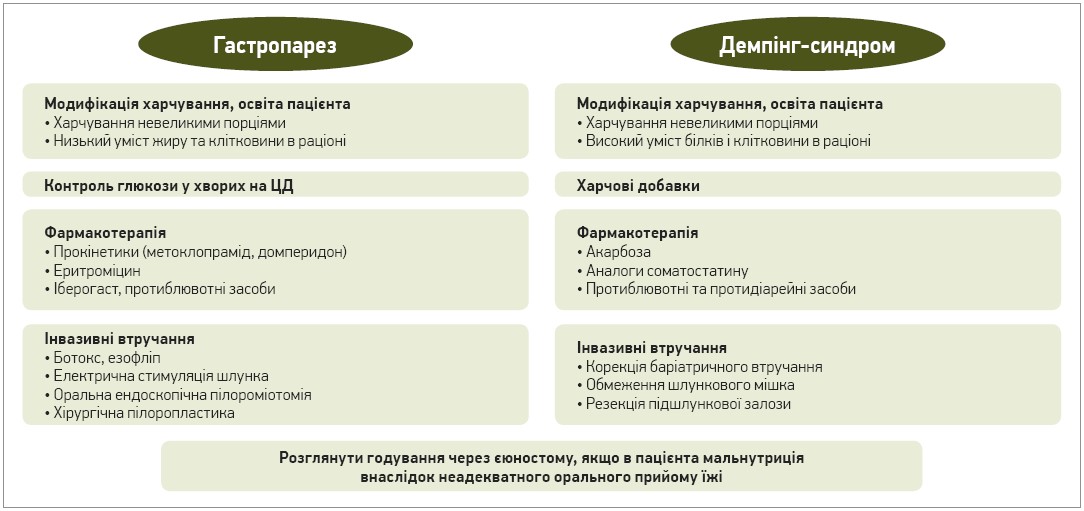 Рис. 2. Алгоритм лікування ГП і ДС
Рис. 2. Алгоритм лікування ГП і ДС
За умови гострого ГП проводять пероральну чи внутрішньовенну корекцію дегідратації та порушень електролітного балансу (Waseem S. et al., 2009). У тяжких випадках може знадобитися декомпресія шлунка за допомогою назогастрального зонда (Camilleri M. et al., 2013).
У разі хронічного перебігу ГП першим кроком є консультування пацієнтів щодо харчування та модифікація дієти. Рекомендовано невеликі порції їжі з низьким умістом жиру та клітковини (Camilleri M. et al., 2013). Важливе значення мають консультації дієтолога, оскільки ГП може спричинити недоїдання та порушення орального споживання їжі через блювання (Parkman H. et al., 2011).
Хоча поки що немає рандомізованих контрольованих досліджень (РКД), які підтвердили би, що зниження рівня HbA1c справді покращує симптоми, епідеміологічні дослідження пов’язують ГП із незадовільним глікемічним контролем (Bytzer P. et al., 2002). Тому хворим на діабет показаний адекватний контроль глікемії.
За відсутності клінічного покращення переходять до фармакотерапії, що включає декілька лікарських засобів (Quigley E., 2000). Насамперед це прокінетики з класу антагоністів дофамінових рецепторів 2 типу – метоклопрамід і домперидон, ефективність яких доведена в РКД (McCallum R. et al., 1983; Patterson D. et al., 1999). Проте позитивний вплив, найімовірніше, не пов’язаний із прискоренням спорожнення шлунка, оскільки цей процес погано корелює із симптоматичною реакцією (Janssen P. et al., 2013). Можливо, він зумовлений зменшенням гіперчутливості шлунка чи покращенням його адаптації (Stanghellini V., Tack J., 2014). Дані щодо тривалої ефективності прокінетиків обмежені. Крім того, їх застосування може спричинити декілька потенційно небезпечних проявів побічної дії, особливо при тривалій терапії. У 1% пацієнтів, які вживають метоклопрамід, виникає пізня (тардивна) дискінезія, тоді як домперидон може зумовлювати серйозні серцеві побічні ефекти. Тому ці препарати треба застосовувати в мінімально ефективних дозах не довше ніж 3 міс (Rao A., Camilleri M., 2010).
Макролідний антибіотик еритроміцин покращує спорожнення шлунка внаслідок стимуляції рецептора мотиліну й може застосовуватися коротким курсом за відсутності ефекту від прокінетиків (Richards R. et al., 1993).
Частим і набридливим симптомом ГП є нудота, контролювати котру можна такими протиблювотними засобами, як прохлорперазин, дифенгідрамін або антагоністи 5-гідрокситриптамінових рецепторів 3 підтипу (Waseem S. et al., 2009). Можна також розглядати призначення селективного антагоніста рецепторів нейрокініну‑1 апреританту, що зменшує нудоту, блювання й інші симптоми ГП (Pasricha P. et al., 2018).
Безрецептурний рослинний препарат іберогаст часто застосовується для лікування функціональної диспепсії. Незважаючи на відсутність впливу на випорожнення шлунка, у плацебо-контрольованому кросовер-дослідженні показано його позитивний вплив на симптоми ГП (Braden B. et al., 2009).
Є також декілька інтервенційних підходів, які продемонстрували різні результати. Короткочасний ефект спостерігається після введення в пілоричну мускулатуру ботулінічного токсину під час ФГДС (Ezzeddine D. et al., 2002; Lacy B. et al., 2002; Miller L. et al., 2002; Friedenberg F. et al., 2004), хоча його ефективність не була підтверджена в РКД (Arts J. et al., 2007; Friedenberg F. et al., 2008).
Іншим варіантом терапії є електрична стимуляція шлунка, під час якої електричний струм надходить до непосмугованих м’язів імплантованими електродами, покращуючи випорожнення шлунка та позитивно впливаючи на симптоми ГП (Angeli T. et al., 2016). Ця процедура рекомендована пацієнтам із тяжкими симптомами, проте подвійне сліпе РКД продемонструвало незначне поліпшення та значний ризик ускладнень (Abell T. et al., 2003). Результати метааналізу, котрий включав 10 досліджень, указують, що найбільше користі ця процедура приносить пацієнтам із діабетичним ГП, тоді як у пацієнтів з ідіопатичним і постхірургічним ГП ця процедура менш ефективна (Chu H. et al., 2012).
Ще однією методикою є оральна ендоскопічна пілороміотомія, що продемонструвала певну ефективність у пацієнтів із ГП, хоча для беззаперечних доказів необхідні подальші дослідження (Khashab M. et al., 2017; Dacha S. et al., 2017; Gonzalez J. et al., 2017; Gonzalez J. et al., 2017; Rodriguez J. et al., 2017).
Наразі найновішою методикою є езофліп – балонний катетер, розроблений для розширення шлунково-кишкового тракту. Неконтрольовані дослідження виявили високі показники технічної успішності, збільшення здатності до розтягування та симптоматичне поліпшенням після дилатації пілоричного відділу шлунка (Gourcerol G. et al., 2015). Після проведення РКД езофліп може мати значення в лікуванні тяжких випадків ГП.
Останнім кроком лікування є хірургічне втручання, що має розглядатися й обговорюватися індивідуально за участю мультидисциплінарної команди, оскільки клінічні дані щодо доцільності проведення таких втручань обмежені. Нещодавній огляд клінічних випадків, який включав 28 пацієнтів, указує на покращення симптомів, випорожнення шлунка та зменшення потреби в застосуванні прокінетиків через 3 міс після операції (Hibbard M. et al., 2011). Хірургічне лікування особливо показане пацієнтам із порушеним оральним харчуванням. У цих випадках доцільно розглядати накладання єюностоми. Черезшкірне чи хірургічне встановлення зонда гастростоми-єюностоми забезпечує декомпресію шлунка та дає змогу проводити ентеральне годування (Felsher J. et al., 2004).
Лікування ДС також передбачає насамперед модифікацію харчування й освіту пацієнтів за участю дієтолога (Khoshoo V. et al., 1991; Kellogg T. et al., 2008). Рекомендовано часті (6 разів на добу) прийоми їжі малими порціями з високим умістом клітковини та білка. Слід уникати швидко засвоюваних вуглеводів та алкогольних напоїв і вживати рідину не швидше ніж через 30 хв після вживання їжі, оскільки рідина прискорює спорожнення шлунка (van Beek A. et al., 2017). Лежання впродовж 30 хв після їди також затримує евакуацію шлункового вмісту (Ukleja A., 2005).
Як другий крок можна використовувати харчові добавки, котрі підвищують в’язкість їжі, як-от гуарова камідь, пектин або глюкоманан (Harju E., Larmi T., 1983; Kneepkens C. et al., 1988). Однак у більшості пацієнтів вони посилюють газоутворення та здуття (van Beek A. et al., 2017).
Третім кроком є застосування фармакотерапії, проте поки що для лікування ДС використовують лише акарбозу й аналоги соматостатину. Акарбоза – це інгібітор α-глюкозидази, що зменшує травлення вуглеводів у просвіті дванадцятипалої кишки та використовується для лікування постпрандіальної гіпоглікемії при синдромі пізнього демпінгу (Ng D. et al., 2001; Ritz P. et al., 2012). Застосування акарбози часто спричиняє метеоризм (Hasegawa T. et al., 1998).
Аналоги соматостатину (октреотид) мають декілька корисних впливів у разі демпінгу. Вони сповільнюють спорожнення шлунка та проходження їжі через тонку кишку, зменшують вивільнення шлунково-кишкових гормонів, включаючи секрецію інсуліну, та пригнічують постпрандіальну вазодилатацію (van Beek A. et al., 2017). Октреотид можна вводити підшкірно тричі на добу чи внутрішньом’язово кожні 2-4 тиж (Didden P. et al., 2006; Arts J. et al., 2009; Deloose E. et al., 2014). Найважливішими побічними ефектами є стеаторея, діарея, нудота, утворення жовчних каменів, біль у місці введення та збільшення маси тіла. Тому за умови щоденного застосування початкові дози не мають перевищувати 25 мкг із наступним титруванням до максимальної дози 100 мкг. Тривалість лікування в разі підшкірного введення не має перевищувати 2 тиж, за умови внутрішньом’язового введення – 2 міс (van Beek A. et al., 2017).
Для контролю неспецифічних симптомів (нудота, діарея) використовують симптоматичні засоби – протиблювотні (меклізин, прометазин) і протидіарейні (настоянка опію, лоперамід). Антихолінергічні препарати (дицикломін, гіосціамін, пропантелін) також сповільнюють спорожнення шлунка та мають спазмолітичну дію. Активатор калієвих каналів діазоксид усуває гіпоглікемію й може використовуватися за умови пізнього демпінгу (Vilarrasa N. et al., 2016). Утім, досвід їх використання в пацієнтів із ДС дуже обмежений.
Хірургічні втручання (ревізійна хірургія) мають обговорюватися в кожному конкретному випадку, оскільки дані щодо їх ефективності також обмежені (van Beek A. et al., 2017).
Отже, ГП та ДС найчастіше виникають після хірургічних втручань і в пацієнтів із діабетом. Через неспецифічність симптомів ці стани треба диференціювати з органічними хворобами та функціональними порушеннями травного тракту: ГП – із пептичною виразкою, раком шлунка, целіакією й абдомінальною ішемією; ранній демпінг – із виразкою анастомозу, внутрішньою грижею та хворобами жовчного міхура, пізній демпінг – з інсуліномою та медикаментозними впливами. Встановлення діагнозу в симптомних пацієнтів передбачає проведення тестів, які підтверджують затримку чи прискорення евакуації шлункового вмісту. Для успішного ведення таких пацієнтів рекомендовано мультидисциплінарний командний підхід із залученням дієтолога, ендокринолога, гастроентеролога й абдомінального хірурга, що забезпечує персоніфікацію лікування. Це особливо важливо за умови тяжких резистентних симптомів, оскільки варіанти терапії та дані щодо їх ефективності доволі обмежені.
Vavricka S. R., Greuter T. Gastroparesis and dumping syndrome: current concepts and management. J. Clin. Med. 2019; 8: 1127. doi: 10.3390/jcm8081127.
Переклала з англ. Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 1 (470), січень 2020 р.