7 лютого, 2020
Імуномодулююча та протизапальна дія пробіотиків: клінічне значення
.jpg) Висока поширеність хронічних неінфекційних захворювань, зокрема ожиріння, діабету, неалкогольної жирової хвороби печінки (НЖХП) [23], є глобальною проблемою, що призводить до суттєвого зростання смертності та інвалідності населення, а також до неабияких витрат на охорону здоров’я. Швидке прогресування згаданих захворювань пов’язане з впливом безлічі тригерів довкілля, які взаємодіють із генетичними та епігенетичними чинниками.
Висока поширеність хронічних неінфекційних захворювань, зокрема ожиріння, діабету, неалкогольної жирової хвороби печінки (НЖХП) [23], є глобальною проблемою, що призводить до суттєвого зростання смертності та інвалідності населення, а також до неабияких витрат на охорону здоров’я. Швидке прогресування згаданих захворювань пов’язане з впливом безлічі тригерів довкілля, які взаємодіють із генетичними та епігенетичними чинниками.
Мікробіота кишечнику та здоров’я людини
Мікробіота кишечнику вважається ключовим фактором, що забезпечує зв’язок між змінами в навколишньому середовищі та здоров’ям людини (рис. 1). Так, відомо, що стабільність кишечнику є результатом тривалого процесу спільної еволюції, спрямованого на постачання організму численних метаболітів, біоактивних молекул, кофакторів і сигнальних молекул, які зазвичай відсутні в раціоні та не виробляються самим хазяїном [9].
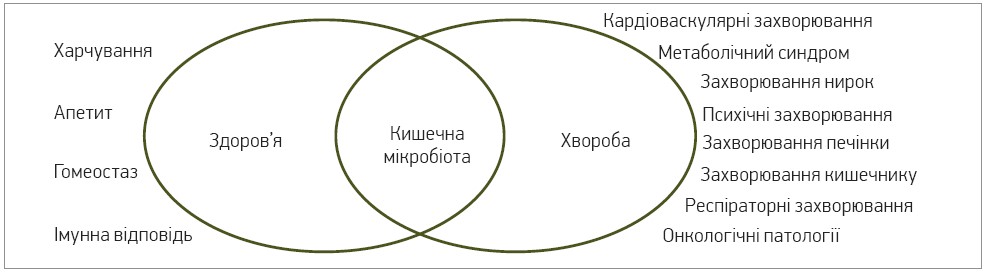 Рис. 1. Вплив кишечної мікрофлори на здоров’я людини та розвиток патології [8]
Рис. 1. Вплив кишечної мікрофлори на здоров’я людини та розвиток патології [8]
Важливу роль у підтримці здоров’я людини відіграє кишковий бар’єр. Бактерії різними шляхами впливають на його функції [34]. Кишечник також впливає на функціональні системи організму через нейробіохімічні, нейроендокринні та нейроімунні механізми осі «шлунково-кишковий тракт – центральна нервова система» [21].
Оскільки імунна система в процесі онтогенезу розвивається та адаптується в умовах симбіотичного зв’язку з мікробіотою, мікрофлора кишечнику виконує імунорегуляторну функцію [3, 37].
Мікробні коротколанцюгові жирні кислоти (КЖК) є джерелом енергії для ентероцитів, вони забезпечують цілісність кишечного бар’єру, підвищують імунну толерантність слизової оболонки [20]. Останній ефект пояснюють тим, що КЖК виконують роль сигнальних молекул, зменшуючи вироблення прозапальних цитокінів і збільшуючи вміст популяції регуляторних Т‑клітин. Також КЖК підтримують рН просвіту кишечнику, впливають на його моторику, пригнічують ріст патогенів та стимулюють апоптоз ракових клітин [6].
Описано особливості кишечнику залежно від маси тіла та індексу маси тіла [4]. Доведено, що при дисбіозі змінюється активність низки факторів, які визначають розвиток дисліпідемії та зумовлюють виникнення ожиріння [13, 22]. Порушення кишечного бар’єру внаслідок дисбіозу також може впливати на розвиток таких патологічних станів, як дисфункція і/або запалення кишечнику [22], метаболічний синдром [7], НЖХП [13, 14], цукровий діабет (ЦД) 2 типу [7, 14], синдром хронічної втоми [27], висока тривожність [36], колоректальний рак [30] тощо.
Останнім часом великий інтерес викликають епігенетичні впливи кишечнику. Як відомо, епігенетика вивчає особливості експресії генів при сталому генетичному коді за рахунок зміни третинної структури ДНК‑ланцюга і, таким чином, доступності ДНК для молекул. До епігенетичних впливів зокрема належить метилювання ДНК, посттрансляційна модифікація гістонів, РНК‑інтерференція тощо [10]. Організм найбільш чутливий до дії різних факторів протягом періоду пре- і раннього постнатального розвитку. Відповідно, виникає активуючий або репресуючий епігенетичний вплив на експресію генів. Так, доведено, що метаболічні порушення часто зумовлені змінами внутрішньоматкових умов [18, 28].
На людський епігеном можуть впливати різні фактори, особливо ті, що діють на кишечнику та її метаболіти [17]. Недавнє пілотне дослідження показало зв’язок між складом кишечнику та активністю метилювання ДНК генів, пов’язаних із розвитком ожиріння та серцево-судинних захворювань [15]. Унаслідок дефіциту деяких субстратів (метионіну, бетаїну та холіну) та/або кофакторів (фолатів, вітамінів В12, В2 та В6), які виробляє кишечник, підвищується концентрація гомоцистеїну в плазмі крові, виникає гіпометилювання у важливих епігеномічних ділянках, що спричиняє розвиток різних захворювань, зокрема судинних та онкологічних [8, 24]. Зменшення продукції мікробіотою масляної кислоти, яка інгібує гістондеацетилазу 3, порушує метаболічний контроль [13]. Це асоціюється з розвитком хронічного низькоінтенсивного запалення [30] через активацію Toll-подібних рецепторів [5] і експресію тумор-некротичного фактора альфа (TNF‑α), інтерлейкіну (ІЛ)-1 бета (IЛ‑1β), IЛ‑2, IЛ‑4, IЛ‑6 та IЛ‑17.
Механізми протизапальної та імуномодулюючої активності пробіотиків
Сьогодні в схеми лікування багатьох захворювань включено пробіотикотерапію. За визначенням пробіотичні бактерії мають бути безпечними, стійкими до кислотності та жовчних кислот і здатними прилипати та колонізуватися в кишечнику.
Доведено, що колонізація кишечнику пробіотиками необов’язкова. Необхідно, щоби певна кількість живих бактерій потрапила в товсту кишку, де вони можуть вплинути на місцеву екологію кишечнику, фізіологію та метаболізм.
Основними мішенями для пробіотиків є епітеліальні клітини кишечнику та імунні клітини.
Основні механізми впливу пробіотиків активно вивчаються Серед них: антагоністичний вплив на різні мікроорганізми та конкурентна адгезія до слизової та епітелію (протимікробна активність) [33], посилення вироблення слизу та підвищення цілісності бар’єру (посилення бар’єрної функції), модуляція імунної системи людини (рис. 2) [4].
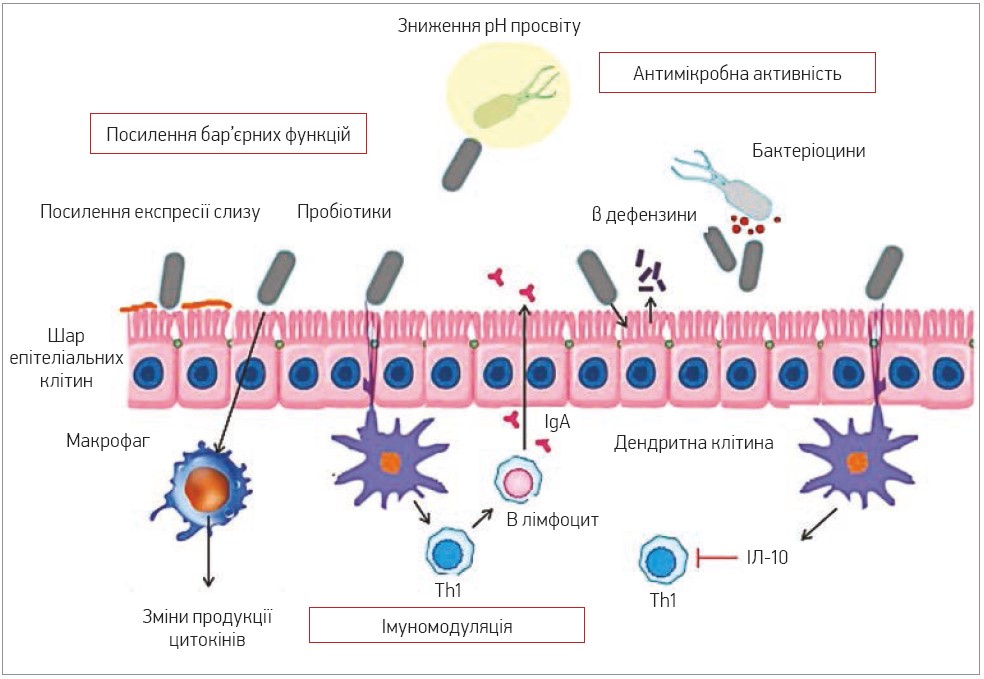 Рис. 2. Механізми імуномодуляції та забезпечення протизапальної дії під впливом пробіотиків
Рис. 2. Механізми імуномодуляції та забезпечення протизапальної дії під впливом пробіотиків
Протизапальна дія пробіотиків пояснюється посиленням вироблення бутирату [13], зниженням експресії прозапальних цитокінів унаслідок дії на Toll-like рецептори [25], підвищенням синтезу антимікробних пептидів [19]. Біоактивні продукти пробіотиків і коменсальних бактерій можуть активувати аутофагію в епітеліальних клітинах кишечнику [2] і тому гальмувати розвиток патогенів. [35]. Застосування пробіотиків знижує рівень С‑реактивного білка [19].
Імуно-опосередковані механізми дії пробіотиків включають модуляцію як вродженого, так і адаптивного імунітету [26]. Посилення вродженого імунітету пов’язано з активацією макрофагів та вивільненням із них прозапальних цитокінів, підвищенням бар’єрної функції слизової оболонки кишечнику. Крім того, пробіотики та деякі з продуктів їхнього метаболізму можуть діяти як ліганди рецепторів вродженої імунної системи, безпосередньо впливаючи на ключові протизапальні шляхи [19]. Пробіотики також можуть регулювати генну експресію ентероцитів і дендритних клітин [37].
Так, пробіотичний штам Bacillus subtilis впливає на адаптивний імунітет завдяки активації Т- та В‑лімфоцитів та вивільнення із останніх імуноглобулінів – IgG та IgA. Здатність модулювати експресію та продукцію регуляторних T- і В‑лімфоцитів, ІЛ‑10 виявлено в Lactobacillus, Bifidobacterium bifidum, Bifidobacterium animalis, Streptococcus thermophiles, Bifidobacterium infantis.
Lactobacillus rhamnosus посилює кишечні бар’єрні функції завдяки підвищенню експресії муцину в клітинах кишечнику [22, 37] та викликає модулювання діяльності келихоподібних клітин і шару слизу кишечнику, нормалізуючи всмоктування та моторику травного тракту [22].
У ході експерименту встановлено, що прийом пробіотичної суміші лактобацил та біфідобактерій суттєво зменшував метаболічні та запальні ефекти 14-тижневої збагаченої на жир дієти (зростання маси тіла, концентрації глюкози в сироватці крові, інсулінорезистентності) [11].
В останні роки доведено, що метаболіти мікробіоти травного тракту відіграють особливу роль у запобіганні розвитку ожиріння та інсулінорезистентості саме через дію на епігенетичні механізми [24, 29]. Будучи самі донорами метильних груп, пробіотичні бактерії впливають також на біодоступність багатьох їх харчових джерел.
Встановлено, що якщо вагітні жінки вживали Lactobacillus rhamnosus GG і Bifidobacterium lactis Bb12, то і в них самих, і в їхніх дітей після народження зменшувалося метилювання в промоторах генів FTO та MC4R, які пов’язані з розвитком ожиріння [32].
Ефективність пробіотиків з точки зору доказової медицини
Результати багатьох клінічних досліджень продемонстрували, що пробіотики можуть мати важливе значення в підтримці гомеостазу кишечнику за рахунок модуляції імунітету та підвищення бар’єрної функції епітелію [16]. Так, наприклад, Lactobacillus paracasei запобігає викликаній антибіотиками вісцеральній гіперчутливості. Клінічна ефективність пробіотиків доведена в процесі лікування або в профілактиці деяких захворювань, пов’язаних із шлунково-кишковим трактом, включаючи «діарею мандрівників», антибіотик-асоційовану діарею, некротизуючий ентероколіт тощо [16].
Доведено, що пробіотичні добавки добре переносяться, ефективні та безпечні для пацієнтів із запальними захворюваннями кишечнику, зменшують клінічні прояви в пацієнтів із легким та помірним перебігом виразкового коліту [25].
За даними системного огляду та метааналізу 105 досліджень (n=6826), встановлено, що споживання пробіотиків призвело до зменшення впливу метаболічних факторів ризику розвитку ЦД 2 типу та стеатогепатиту в пацієнтів із захворюваннями обміну речовин [14].
Як показали результати рандомізованого клінічного дослідження, дієта з пробіотиками знижує рівень холестерину та глюкози в крові пацієнтів похилого віку [29]. Зокрема, значуще знижує рівень холестерину крові використання лактобацил (L. acidophilus, L. plantarum) та Bifidobacterium bifidum [12].
У пацієнтів із синдромом хронічної втоми пробіотики покращували самопочуття, а також лабораторні показники оксидативного стресу та запалення [33].
За даними кількох рандомізованих клінічних досліджень, мікробна модифікація пробіотиками може зменшити шлунково-кишкові симптоми та мультиорганне запалення при ревматоїдному артриті, виразковому коліті та розсіяному склерозі [20].
Доведено, що застосування пробіотиків, як і трансплантація кишечної мікробіоти, ефективні при остеопорозі, незагоєнні ран, аутоімунних захворюваннях шкіри, порушенні настрою, поведінки, зниженні пам’яті [13].
На українському ринку нещодавно з’явилася дієтична добавка Лактіалє® Мульті (ПАТ «Фармак», Україна), одна капсула якої містить сумарно 2,0×109 колонієутворюючих одиниць пробіотичних мікроорганізмів: 7 різних штамів лактобацил (L. casei, L. plantarum, L. rhamnosus, L. acidophilus, L. delbrueckii ssp bulgaricus, L. helveticus, L. salivarius), 4 різні штами біфідобактерій (B. bifidum, B. breve, B. longum, B. infantis), а також Bacillus subtilis, Lactococcus lactis ssp. lactis, Streptococcus thermophilus.
Як відомо, Bifidobacterium breve широко застосовують у педіатрії, оскільки цей штам домінує в кишечнику дітей, які перебувають на грудному вигодовуванні, і виявляє протимікробну та імуностимулюючу активність [5]. Bifidobacterium longum модулює метаболізм просвіту кишечнику, стабілізує його мікробіоту [34], а Lactococcus lactis ssp. lactis сприяє активності травних ферментів та антимікробній стійкості [1].
Як вже було зазначено, указані пробіотичні штами:
- сприяють підтриманню й збереженню балансу кишкової флори;
- допомагають зміцнювати природний захист організму;
- сприяють врівноваженню імунної відповіді;
- підсилюють стійкість організму до шкідливого впливу довкілля, зокрема в разі прийому антибіотиків, перебування на дієті, в осіб похилого віку, при стресових ситуаціях, «діареї мандрівників»;
- запобігають розвитку таких хронічних неінфекційних станів та захворювань, як атеросклероз, остеопороз, ожиріння, ЦД, НЖХП тощо.
Дітям 8-12 років згадану дієтичну добавку рекомендують вживати під час їжі по 1 капсулі 1 раз на добу, дітям >12 років та дорослим – по 1 капсулі 2 рази на добу.
Сьогодні асоціація між кишечною мікробіотою, метаболізмом, пошкодженням тканин/клітин та регенерацією не викликає сумнівів. Основним напрямом профілактики та корекції хронічних неінфекційних захворювань залишається модифікація способу життя. Нові стратегії лікування/профілактики мають базуватися на пробіотичній модуляції мікробіоти кишечнику для забезпечення протизапальної та імуномодулюючої дії. З точки зору фармакоекономіки для цього можна рекомендувати дієтичну добавку Лактіалє® Мульті, яка містить штами основних пробіотичних бактерій із доведеною ефективністю.
Література
- Adel M., El-Sayed A.M., Yeganeh S., Dadar M4, Giri SS. Effect of Potential Probiotic Lactococcus lactis Subsp. lactis on Growth Performance, Intestinal Microbiota, Digestive Enzyme Activities, and Disease Resistance of Litopenaeus vannamei. Probiotics Antimicrob Proteins. 2017 Jun;9(2):150-156. doi: 10.1007/s12602-016-9235-9.
- Al-Bari A. A. Probiotic Action: Activating Autophagy in the Management of Diabetes Mellitus. EC Microbiology. 2016; 4 (3): 699-670.
- Bourlioux P., Koletzko B., Guarner F., Braesco V. The intestine and its microflora are partners for the protection of the host: report on the Danone symposium «the intelligent intestine,» held in Paris, June 14, 2002. Am J Clin Nutr. 2003;78(4):675-683. DOI:10.1093/ajcn/78.4.675.
- Cerdó T., García-Santos J. A., Bermúdez M. G. Campoy C. The Role of Probiotics and Prebiotics in the Prevention and Treatment of Obesity. Nutrients. 2019, 11, 635; doi:10.3390/nu11030635.
- Cionci N.B., Baffoni L., Gaggìa F., Di Gioia D. Therapeutic Microbiology: The Role of Bifidobacterium breve as Food Supplement for the Prevention/Treatment of Paediatric Diseases. Nutrients. 2018, 10, 1723; doi:10.3390/nu10111723.
- Correa-Oliveira R., Fachi J. L., Vieira A., Sato F. T., Vinolo M. A. R. Regulation of immune cell function by short-chain fatty acids. Clin Transl Immunology. 2016;5(4): e73. doi:10.1038/cti.2016.17.
- Dávila L.A., Pirela V. B., Díaz-Vasquez W., Villasmil N. R. et al. The Microbiome and the Epigenetics of Diabetes Mellitus. http://dx.doi.org/10.5772/ intechopen.76201.
- Day R. L.J., Harper A. J., Woods R.M Davies O. G. et al. Probiotics: current landscape and future horizons. Future Sci. 2019. FSO391.
- Devaux C.A., Raoult1 D. The Microbiological Memory, an Epigenetic Regulator Governing the Balance Between Good Health and Metabolic Disorders. Front. Microbiol. 2018. 9:1379. doi: 10.3389/fmicb.2018.01379.
- Friso S., Carvajal C.A., Fardella C.E., Olivieri O. Epigenetics and arterial hypertension: the challenge of emerging evidence. Transl Res. 2015; 165(1): 154-65.
- Holowacz S., Guigne C., Chene G., Mouysset S. et al. A multispecies Lactobacillus-and Bifidobacterium-containing probiotic mixture attenuates body weight gain and insulin resistance after a short-term challenge with a high-fat diet in C57/BL6J mice. (2015) PharmaNutrition, 3 (3). 101-107. ISSN2213-4344.
- Isacco C.G., Ballini A., De Vito D., Inchingolo A. M. et al. Probiotics in Health and Immunity: A First Step toward Understanding the Importance of Microbiota System in Translational Medicine http://dx.doi.org/10.5772/intechopen.76201.
- Kiousi D.E., Karapetsas A., Karolidou K., Panayiotidis M. I. Probiotics in Extraintestinal Diseases: Current Trends and New Directions. Nutrients 2019, 11, 788; doi:10.3390/nu11040788.
- Koutnikova N., Genser B., Monteiro-Sepulveda M., Faurie J. et al. Impact of bacterial probiotics on obesity, diabetes and non-alcoholic fatty liver disease related variables: a systematic review and meta-analysis of randomised controlled trials. BMJ Open 2019;9: e017995. doi:10.1136/bmjopen‑2017-017995.
- Kumar H., Lund R., Laiho A., Lundelin K. et al. Gut microbiota as an epigenetic regulator: pilot study based on whole-genome methylation analysis. mBio. 2014;5(6). pii: e02113-14. doi: 10.1128/mBio.02113-14.
- Lee B.J., Bak Y.-T. Irritable Bowel Syndrome, Gut Microbiota and Probiotics. J Neurogastroenterol Motil. 2011; 17(3): 252-266. DOI: 10.5056/jnm.2011.17.3.252.
- Lee H.-S.The interaction between gut microbiome and nutrients on development of human disease through epigenetic mechanisms. Genomics Inform 2019;17(3): e24.https://doi.org/10.5808/GI.2019.17.3.e24.
- Leow MK. Environmental origins of hypertension: phylogeny, ontogeny and epigenetics. Hypertens Res. 2015; 38(5): 299-307.
- Lescheid D. W. Probiotics as regulators of inflammation: A review. Functional Foods in Health and Disease 2014; 4(7):299-311.
- Liu Y., Alookaran J. J., Rhoads J. M. Probiotics in Autoimmune and Inflammatory Disorders. Nutrients 2018, 10, 1537; doi:10.3390/nu10101537.
- Lu L.L., Zhu G. Gut–Brain Axis and Mood Disorder. Front. Psychiatry 9:223. doi: 10.3389/fpsyt.2018.00223.
- Martín R., Chamignon C., Mhedbi-Hajri N., Chain F. The potential probiotic Lactobacillus rhamnosus CNCM I‑3690 strain protects the intestinal barrier by stimulating both mucus production and cytoprotective response. Scientific RepoRts | (2019) 9:5398 | https://doi.org/10.1038/s41598-019-41738-5.
- Meroni M., Longo M., Dongiovanni P. The Role of Probiotics in Nonalcoholic Fatty Liver Disease: A New Insight into Therapeutic Strategies. Nutrients 2019, 11, 2642; doi:10.3390/nu11112642.
- Miro-Blanch J., Yanes O. Epigenetic Regulation at the Interplay Between Gut Microbiota and Host Metabolism. Frontiers in Genetics. 2019; 10: 638.
- Plaza-Díaz J., Ruiz-Ojeda F.J., Vilchez-Padial L.M., Gil A. Evidence of the Anti-Inflammatory Effects of Probiotics and Synbiotics in Intestinal Chronic Diseases. Nutrients 2017, 9, 555; doi:10.3390/nu9060555.
- Plaza-Díaz J., ID Ruiz-Ojeda F.J., Gil-Campos М., Gil A. Immune-Mediated Mechanisms of Action of Probiotics and Synbiotics in Treating Pediatric Intestinal Diseases. Nutrients 2018, 10, 42; doi:10.3390/nu10010042.
- Preez S. D., Corbitt M., Cabanas H., Eaton N. A systematic review of enteric dysbiosis in chronic fatigue syndrome/myalgic encephalomyelitis. Systematic Reviews.2018; 7:241 https://doi.org/10.1186/s13643-018-0909-0.
- Smith C.J., Ryckman K. K. Epigenetic and developmental influences on the risk of obesity, diabetes, and metabolic syndrome. Diabetes, Metabolic Syndr and Obes: Targ and Ther. 2015; 8; 295-302.
- tols-Gonçalves D., Tristão L. S. Henneman P., Nieuwdorp M. Epigenetic Markers and Microbiota/Metabolite-Induced Epigenetic Modifications in the Pathogenesis of Obesity, Metabolic Syndrome, Type 2 Diabetes, and Non-alcoholic Fatty Liver Disease. Current Diabetes Reports (2019) 19: 31. https://doi.org/10.1007/s11892-019-1151-4.
- Tsai Y., Lin T., Chang C., Wu8 T. et al. Probiotics, prebiotics and amelioration of diseases. Journal of Biomedical Science. 2019;26:3. https://doi.org/10.1186/s12929-018-0493-6.
- Valentini L., Pinto A., Bourdel-Marchasson I., Ostan R. et al. Impact of personalized diet and probiotic supplementation on inflammation, nutritional parameters and intestinal microbiota e The “RISTOMED project”: Randomized controlled trial in healthy older people
- Vähämiko S., Laiho A., Lund R., Isolauri E., Salminen S., Laitinen K. The impact of probiotic supplementation during pregnancy on DNA methylation of obesity-related genes in mothers and their children. Eur J Nutr. Springer Berlin Heidelberg. 2018;0(0):1-11.
- Venturini L., Bacchi S., Capelli E., Lorusso L. et al. Modification of Immunological Parameters, Oxidative Stress Markers, Mood Symptoms, and Well-Being Status in CFS Patients after Probiotic Intake: Observations from a Pilot Study. Oxid Med Cell Longev. 2019;2019:1684198. doi: 10.1155/2019/1684198. eCollection 2019.
- Wong C. B., Odamaki T., Xiao J. Beneficial effects of Bifidobacterium longum subsp. longum BB536 on human health: Modulation of gut microbiome as the principal action. Journal of Functional Foods. 2019; 54: 506-519.
- Wu Y., Wang Y., Zou H., Wang B. et al. Probiotic Bacillus amyloliquefaciens SC06 Induces Autophagy to Protect against Pathogens in Macrophages. Front. Microbiol. 2017; 8:469. doi: 10.3389/fmicb.2017.00469.
- Yang B., Wei J., Ju P., Chen J. Effects of regulating intestinal microbiota on anxiety symptoms: A systematic review. Gen Psychiatr. 2019;32(2): e100056. doi: 10.1136/gpsych‑2019-100056. eCollection 2019.
- Zhang C.X., Wang H. Y., Chen T. X. Interactions between Intestinal Microflora/Probiotics and the Immune System. Biomed Res Int. 2019 Nov 20;2019:6764919. doi: 10.1155/2019/6764919. eCollection 2019.
 Лактіалє® Мульті – для підтримки нервової та імунної систем!*
Лактіалє® Мульті – для підтримки нервової та імунної систем!*
* Згідно з листком-вкладишем до Лактіалє® Мульті.
Реклама дієтичної добавки. Не є лікарським засобом. Декларація про відповідність продукції «Лактіалє® Мульті» вимогам українського законодавства у галузі харчових продуктів від «31» липня 2019 р. Виробник: АТ «Фармак», 04080, м. Київ, вул. Кирилівська, 63. тел.: +38 (044) 239-19-40 /факс: +38 (044) 485-26-86 e-mail: info@farmak.ua /веб-сайт: www.farmak.ua
Медична газета «Здоров’я України 21 сторіччя» № 1 (470), січень 2020 р.


