17 лютого, 2020
Современные алгоритмы назначения сахароснижающей терапии пациентам с СД 2 типа: важное обновление консенсуса ADA и EASD (2019)
В последнее время взгляды на цели лечения сахарного диабета (СД) 2 типа претерпели существенные изменения: если еще недавно главным фокусом внимания выступало достижение целевых уровней гликемии, то сейчас наряду с этим важнейшее значение придается раннему и активному предупреждению развития осложнений, в первую очередь со стороны сердечно-сосудистой системы и почек. Подобная трансформация парадигмы менеджмента пациентов с СД 2 типа стала возможной благодаря проведению в последние годы целого ряда масштабных клинических исследований, результаты которых вывели на приоритетные позиции такие современные противодиабетические препараты, как агонисты рецепторов глюкагоноподобного пептида-1 (арГПП‑1) и ингибиторы натрий-глюкозного котранспортера 2 типа (SGLT2). Именно представители этих двух классов продемонстрировали способность не только снижать уровень глюкозы крови, но и достоверно уменьшать риск развития сердечно-сосудистых событий и замедлять темпы снижения почечной функции у пациентов с СД 2 типа.
Безусловно, получение доказательных данных такого рода не могло не сказаться на содержании современных клинических рекомендаций. Так, уже в конце августа 2019 г. Европейское общество кардиологов (European Society of Cardiology, ESC) и Европейская ассоциация по изучению сахарного диабета (European Association for the Study of Diabetes, EASD) выпустили новые совместные рекомендации по лечению и профилактике сердечно-сосудистых заболеваний (ССЗ) у пациентов с СД либо предиабетом (Cosentino F. et al., 2109). В этом документе указывается на необходимость обязательно оценивать степень сердечно-сосудистого риска (средний, высокий, очень высокий) и в качестве сахароснижающей терапии первой линии рекомендовать пациентам с очень высоким / высоким сердечно-сосудистым риском (например, лицам с поражениями органов-мишеней или наличием сразу нескольких факторов риска) арГПП‑1 либо ингибиторы SGLT2, причем независимо от того, принимают уже они метформин или еще не получали лечения.
Совместно с европейскими экспертами свои подходы к стартовой сахароснижающей терапии оперативно скорригировали и американские диабетологи: 19 декабря прошлого года в онлайн-версии известного журнала Diabetologia был опубликован (Buse J. B. et al., 2019) обновленный краткий алгоритм коррекции гипергликемии при СД 2 типа, являющийся неотъемлемой частью консенсусных рекомендаций Американской диабетологической ассоциации (ADA) и EASD. Появление данного обновления, вносящего важные изменения в предыдущую редакцию документа, датированную 2018 г. (Davies M.J. et al.), основывается на результатах важнейших исследований по оценке кардиоваскулярных исходов у пациентов с СД 2 типа, которые были опубликованы в течение 2019 г. Авторы новой редакции начали работу над ней в июле прошлого года и уже в октябре подали соответствующую статью для публикации в журналах Diabetes Care и Diabetologia. Ключевые изменения этих доказательных рекомендаций, а также результаты положенных в их основу клинических исследований, безусловно, заслуживают подробного рассмотрения. Итак, какие же именно исследования привлекли столь пристальное внимание экспертов в области диабетологии и заставили их внести принципиальные изменения в консенсус, принятый менее года назад?
К числу таких основополагающих клинических испытаний, бесспорно, относится исследование REWIND (Researching Cardiovascular Events with a Weekly Incretin in Diabetes), в ходе которого оценивалось применение арГПП‑1 дулаглутида (Gerstein H. C. et al., 2019). В это исследование было включено значительное количество пациентов с СД 2 типа с высоким сердечно-сосудистым риском, но без ранее диагностированного ССЗ – 68,5% от общего числа участников. В большинстве же других исследований по оценке кардиоваскулярных исходов, в которых применялись арГПП‑1, пациенты с наличием лишь факторов сердечно-сосудистого риска составляли меньшинство участников. Кроме того, важной особенностью данного исследования явилась значительная длительность периода последующего наблюдения за пациентами: ее медиана (5,4 года) существенно превысила таковую в предшествующих клинических исследованиях по оценке кардиоваскулярных исходов у лиц с СД 2 типа. Частота развития первичных тяжелых сердечно-сосудистых нежелательных явлений (major adverse cardiovascular event, MACE) в исследовании REWIND составила 2,7 на 100 пациенто-лет с показателем относительного риска (ОР) 0,88 (95% ДИ 0,79-0,99) в пользу дулаглутида. При этом не отмечалось какого-либо различия во влиянии на частоту развития MACE в подгруппах пациентов с ССЗ в анамнезе и без такового. Следует уточнить, что в исследовании REWIND предшествующее ССЗ определялось как анамнестические сведения об инфаркте миокарда (ИМ), ишемическом инсульте, нестабильной стенокардии с соответствующими изменениями на электрокардиограмме (ЭКГ), ишемии миокарда, подтвержденной при проведении визуализационных исследований или стресс-тестов, а также о выполненной ранее реваскуляризации коронарных, сонных либо периферических артерий.
! Таким образом, если ранее рекомендация экспертов ADA и EASD заключалась в том, что у пациентов с СД 2 типа убедительным показанием для лечения арГПП‑1 или ингибиторами SGLT2 является диагностированное ССЗ, то в настоящее время они также считают, что назначение арГПП‑1 может рассматриваться и с целью снижения риска MACE у пациентов с СД 2 типа без диагностированного ССЗ, но с наличием индикаторов высокого риска, а именно у пациентов в возрасте ≥55 лет со стенозом (>50%) коронарных артерий, сонных артерий или артерий нижних конечностей, гипертрофией левого желудочка (ГЛЖ), расчетной скоростью клубочковой фильтрации (рСКФ) <60 мл/мин/1,73 м2 либо альбуминурией.
Что касается ингибиторов SGLT2, то интересные данные в отношении их эффектов были получены в исследовании DECLARE-TIMI 58 (Dapagliflozin Effect on Cardiovascular Events – Thrombolysis in Myocardial Infarction 58), в ходе которого ингибитор SGLT2 дапаглифлозин сравнивали с плацебо. В это исследование также было включено большее относительное количество участников с СД 2 типа без ранее диагностированного ССЗ атеросклеротического генеза (ССЗАГ), но с наличием многочисленных сердечно-сосудистых факторов риска (59,4%), и оно также характеризовалось более длительным периодом последующего наблюдения (медиана – 4,2 года), чем другие испытания по оценке ингибиторов SGLT2 (Wiviott S. D. et al., 2019). Дапаглифлозин продемонстрировал сердечно-сосудистую безопасность, но не привел к статистически значимому снижению частоты МАСЕ (8,8% в группе дапаглифлозина и 9,4% в группе плацебо; ОР 0,93; 95% ДИ 0,84-1,03; р=0,17). Однако применение дапаглифлозина обеспечило статистически значимое снижение частоты достижения другой комбинированной первичной конечной точки оценки эффективности, включавшей сердечно-сосудистую смерть либо госпитализацию по поводу сердечной недостаточности (СН) (4,9% в сравнении с 5,8%; ОР 0,83; 95% ДИ 0,73-0,95; р=0,005). Кроме того, в исследовании DECLARE-TIMI 58 было установлено благоприятное влияние терапии дапаглифлозином и на вторичные почечные конечные точки оценки эффективности.
Метаанализ результатов клинических исследований по оценке кардиоваскулярных исходов на фоне терапии ингибиторами SGLT2, проведенный Т. A. Zelniker и соавт. (2019), свидетельствует о наличии у этих препаратов классового эффекта, заключающегося в снижении частоты госпитализаций по поводу СН и замедлении прогрессирования хронической болезни почек (ХБП) в подгруппах высокого и низкого риска ССЗ без влияния на частоту МАСЕ в условиях отсутствия диагностированного ССЗАГ.
Анализ результатов 2 клинических исследований по оценке кардиоваскулярных исходов на фоне применения ингибиторов SGLT2 – DECLARE-TIMI 58 (Kato E. T. et al., 2019) и программы CANVAS (Canagliflozin Cardiovascular Assessment Study) (Figtree J. A. et al., 2019) – указывает на то, что преимущества терапии ингибиторами SGLT2 в плане влияния на частоту госпитализаций по поводу СН и сердечно-сосудистую смертность наиболее выражены у лиц с предсуществующей СН со сниженной ФВ (СНсФВ) в сравнении с лицами без СНсФВ. Важно отметить, что госпитализация по поводу СН являлась вторичным исходом, относительно низкое количество пациентов имели СН исходно, и данные в отношении ФВ были доступны только у части больных. В исследовании DECLARE-TIMI 58 лица с СН, но без снижения ФВ, а также пациенты без СН, по-видимому, не получали преимуществ от лечения дапаглифлозином в плане снижения частоты таких исходов, как МАСЕ и сердечно-сосудистая смерть. Преимущество в снижении частоты госпитализаций по поводу СН было наиболее выраженным у пациентов с исходной ФВ <30%, выраженным у пациентов с ФВ <45% и пограничным у пациентов с ФВ ≥45% или у участников без СН.
Исследование DAPA-HF (Dapagliflozin and Prevention of Adverse Outcomes in Heart Failure) по изучению эффектов дапаглифлозина стало первой работой по оценке такого исхода, как СН, на фоне применения данного противодиабетического препарата (McMurray J.J. et al., 2019). Следует особо подчеркнуть, что в него были включены пациенты с СН со значением ФВ ≤40%, причем как с СД 2 типа, так и без этого эндокринологического заболевания. Результаты исследования продемонстрировали преимущества дапаглифлозина в плане снижения частоты достижения первичной комбинированной конечной точки (сердечно-сосудистая смерть, госпитализация по поводу СН и срочные обращения к врачу по причине СН), а также частоты связанных с СН событий и смертности (как сердечно-сосудистой, так и общей) у пациентов со сниженной ФВ независимо от наличия/отсутствия СД 2 типа.
! Поэтому в настоящее время эксперты ADA и EASD рекомендуют назначение ингибиторов SGLT2 пациентам с СД 2 типа и СН (в особенности у больных с СНсФВ) с целью снижения частоты госпитализаций по поводу СН, MACE и сердечно-сосудистой смертности.
Значительное внимание экспертов было уделено также рассмотрению вопроса о том, при каком уровне гликозилированного гемоглобина (HbA1c) будут реализовываться показанные в исследованиях кардиоваскулярные преимущества арГПП‑1 и ингибиторов SGLT2. Следует отметить, что в исследовании REWIND по оценке арГПП‑1 дулаглутида не было установлено нижнего порогового значения HbA1c для определения пригодности пациентов к участию в нем. Результаты REWIND продемонстрировали эквивалентную эффективность препарата в плане снижения частоты MACE при уровне HbA1c выше и ниже медианного значения – 55 ммоль/моль (7,2%) (Gerstein H. C. et al., 2019). Ни одно из клинических исследований по изучению кардиоваскулярных исходов на фоне применения ингибиторов SGLT2, в которых оценивались MACE в качестве первичных конечных точек, не включало пациентов с уровнем HbA1c <48 ммоль/моль (<6,5%), и имеется лишь незначительное количество данных для обоснования принятия клинического решения о назначении указанных противодиабетических препаратов у пациентов с уровнем HbA1c <53 ммоль/моль (<7%) (Inzucchi S. E. et al., 2018). Однако кардиоваскулярные преимущества ингибиторов SGLT2, по-видимому, не ограничиваются группой пациентов с повышенным уровнем HbA1c. Как уже отмечалось, для участия в исследовании DAPA-HF были отобраны пациенты с СНсФВ как с СД 2 типа, так и без него (Inzucchi S. E. et al., 2018). При этом преимущество в плане снижения сердечно-сосудистой смертности и событий, связанных с СН, на фоне применения дапаглифлозина было достоверным в обеих этих подгруппах, свидетельствуя о том, что эффекты дапаглифлозина на данные конечные точки не зависят от уровня HbA1c (Inzucchi S. E. et al., 2018).
! В связи с этим в настоящее время эксперты ADA и EASD рекомендуют рассматривать решение о лечении пациентов группы высокого риска с установленным диагнозом СД 2 типа препаратом из класса арГПП‑1 или ингибитором SGLT2 с целью снижения частоты MACE, госпитализаций по поводу СН, сердечно-сосудистой смертности или замедления прогрессирования ХБП независимо от исходного уровня HbA1c либо индивидуального целевого уровня HbA1c.
При этом эксперты по-прежнему придерживаются рекомендации о том, что замена лекарственного средства с доказанными преимуществами в отношении риска ССЗ, ХБП и частоты госпитализаций по поводу СН на препарат без таковых у пациентов высокого риска является обоснованной тогда, когда для них установлены индивидуализированные целевые уровни гликемии.
Первым исследованием, в ходе которого в качестве первичной конечной точки оценивался именно почечный исход терапии противодиабетическим препаратом, стало CREDENCE (Canagliflozin and Renal Events in Diabetes with Established Nephropathy Clinical Evaluation), в ходе которого применялся ингибитор SGLT2 канаглифлозин (Perkovic V. et al., 2019). Первичная комбинированная конечная точка включала терминальную стадию болезни почек (диализ, трансплантация почки либо стойкое значение рСКФ <15 мл/мин/1,73 м2), удвоение уровня сывороточного креатинина или смерть в результате патологии почек либо от сердечно-сосудистых причин. В исследование CREDENCE были включены пациенты с СД 2 типа и ХБП, получавшие максимально переносимую дозу ингибиторов ангиотензинпревращающего фермента либо блокаторов рецепторов ангиотензина, с соотношением альбумин/креатинин (А/К) в моче 300-5000 мг/г и значением рСКФ в диапазоне от 30
! На основании доступных в настоящее время данных эксперты ADA и EASD рекомендуют использовать ингибиторы SGLT2 с целью профилактики госпитализаций вследствие СН, МАСЕ и сердечно-сосудистой смерти, а также с целью замедления прогрессирования ХБП у пациентов с СД 2 типа.
На основании анализов вторичных конечных точек, выполненных в клинических исследованиях с оценкой кардиоваскулярных исходов, можно уверенно утверждать, что преимущества терапии ингибиторами SGLT2 в плане почечных исходов являются очевидными у пациентов со значением соотношения А/К в моче >300 мг/г и значениями рСКФ в диапазоне 30-90 мл/мин/1,73 м2 и менее изученными – при более ранних стадиях ХБП.
В рамках реализации программы CANVAS возникла определенная озабоченность в отношении повышенного риска ампутаций на фоне применения канаглифлозина в сравнении с плацебо (Figtree G. A. et al., 2019). В исследовании CREDENCE было показано (Perkovic V. et al., 2019), что на фоне применения канаглифлозина в дозе 100 мг не наблюдалось значимого повышения риска ампутаций в сравнении с плацебо (ОР 1,11; 95% ДИ 0,79-1,56), хотя в целом их риск был выше, чем в исследованиях по оценке других ингибиторов SGLT2. Это могло быть связано с используемыми стратегиями снижения риска: исключение пациентов с анамнезом травматической ампутации в течение 12 мес скрининга или с активной язвой стопы, остеомиелитом, гангреной либо критической ишемией нижней конечности в течение 6 мес скрининга; кроме того, предусматривалось прерывание терапии в случае возникновения любого из вышеперечисленных явлений с тщательным рассмотрением индивидуальных рисков и преимуществ до возобновления применения канаглифлозина после разрешения явления.
! В настоящее время эксперты ADA и EASD придерживаются рекомендации о том, что пациенты с язвами на стопах или больные с высоким риском ампутации должны получать лечение ингибиторами SGLT2 только после тщательно взвешенного консенсусного решения специалистов с учетом рисков и преимуществ, а также при условии всестороннего обучения уходу за стопами и принятия соответствующих мер по профилактике ампутации.
Основываясь на данных опубликованных к настоящему времени исследований, эксперты ADA и EASD считают, что у пациентов с СД 2 типа и диагностированным ССЗАГ (таких как лица, перенесшие ИМ, ишемический инсульт, нестабильную стенокардию с изменениями на ЭКГ, ишемию миокарда, подтвержденную данными визуализационных исследований или стресс-тестов, либо реваскуляризацию коронарных, сонных или периферических артерий), для которых МАСЕ представляют собой наиболее серьезную угрозу, самым высоким уровнем доказательности в плане снижения их риска характеризуются арГПП‑1.
Исследование PIONEER 6 (Peptide Innovation for Early Diabetes Treatment 6), которое представляло собой клинической испытание по оценке кардиоваскулярной безопасности перорального арГПП‑1 семаглутида, включало 3183 пациента с СД 2 типа и продемонстрировало кардиоваскулярную безопасность этой лекарственной формы, а также значимое снижение сердечно-сосудистой смертности (ОР 0,49; 95% ДИ 0,27-0,92) (Husain М. et al., 2019). Пероральная лекарственная форма семаглутида, внедрение которой в клиническую практику, несомненно, улучшит приверженность пациентов к терапии, уже получила разрешение на маркетинг в США. Ожидается, что в скором времени аналогичное решение будет принято и регуляторными органами ЕС.
! У пациентов с диагностированным ССЗАГ или без такового, но с наличием СНсФВ либо ХБП (рСКФ от 30
При этом с участием пациентов с СД 2 типа и низким сердечно-сосудистым риском, не имеющих ХБП, к настоящему времени пока не было проведено исследований по оценке кардиоваскулярных либо почечных преимуществ арГПП‑1 или ингибиторов SGLT2.
Некоторые метаанализы (Zelniker T. A. et al., 2019; Giugliano D. et al., 2019; Kristensen S. L. et al., 2019) свидетельствуют о наличии гетерогенности в оценках частоты МАСЕ и сердечно-сосудистой смерти на фоне применения арГПП‑1, хотя это обосновано результатами единственного исследования, в котором изучался ликсисенатид. Аналогичным образом, существует некоторая гетерогенность в оценке сердечно-сосудистой смертности при применении ингибиторов SGLT2. Неясно, являются ли различия в точечных оценках преимуществ и опасностей результатом различий в эффектах препаратов, дизайне и особенностях проведения исследований или же они представляют собой случайные эффекты. При принятии индивидуализированного клинического решения о назначении тех или иных препаратов из этих классов специалисты здравоохранения должны учитывать специфические характеристики и предпочтения конкретных пациентов, внимательно изучать инструкции для медицинского применения препаратов, а также результаты метаанализов и первичных исследовательских отчетов. Нужно также понимать, что для многих пациентов лечение арГПП‑1 или ингибитором SGLT2 в некоторых учреждениях здравоохранения сопряжено с ощутимыми прямыми финансовыми издержками, и это обстоятельство также необходимо учитывать врачам при принятии терапевтических решений.
В данном контексте заслуживают внимания результаты исследования CAROLINA (Cardiovascular Outcome Study of Linagliptin vs Glimepiride in Type 2 Diabetes), для участия в котором были рандомизированы взрослые пациенты с СД 2 типа и высоким кардиоваскулярным риском. Они получали либо ингибитор дипептидилпептидазы-4 (ДПП‑4) линаглиптин, либо производное сульфонилмочевины глимепирид. В качестве первичной конечной точки в данном исследовании оценивалась частота МАСЕ, и по этому критерию не было продемонстрировано достоверного различия между группами (ОР 0,98; 95% ДИ 0,84-1,14). На момент завершения исследования у линаглиптина в сравнении с глимепиридом были отмечены преимущество в виде снижения массы тела (в среднем на 1,5 кг), а также существенные преимущества в плане снижения частоты гипогликемии, хотя серьезные гипогликемические события реже отмечались на фоне приема глимепирида (0,45 на 100 пациенто-лет) (Rosenstock J. et al., 2019). В сочетании с другими клиническими исследованиями по оценке кардиоваскулярных исходов на фоне применения ингибиторов ДПП‑4, включая продемонстрировавшее сердечно-сосудистую безопасность линаглиптина исследование CARMELINA (Cardiovascular and Renal Microvascular Outcome Study with Linagliptin; Rosenstock J. et al., 2019), результаты исследования CAROLINA подали обнадеживающий сигнал о безопасности глимепирида – недорогого и эффективного препарата сульфонилмочевины. Однако остается неясным, могут ли эти результаты быть экстраполированы на другие препараты сульфонилмочевины.
Интересную дополнительную информацию о преимуществах стартовой комбинированной сахароснижающей терапии предоставило также исследование VERIFY (Vildagliptin Efficacy in Combination with Metformin for Early Treatment of Type 2 Diabetes). Изначальное назначение комбинации ингибитора ДПП‑4 вилдаглиптина и метформина сопровождалось меньшей частотой вторичной неэффективности гликемического контроля (HbA1c ≥53 ммоль/моль, или ≥7%) в сравнении с монотерапией метформином либо последовательным включением метформина и вилдаглиптина в схему терапии (Matthews D. R. et al., 2019). В настоящее время эксперты рекомендуют принимать решение о возможности стартовой комбинированной терапии в случае впервые диагностированного СД 2 типа на основании консенсусного заключения специалистов.
Следует отметить, что, несмотря на ожидаемый прогресс в лечении пациентов с СД 2 типа и профилактике серьезных осложнений этого заболевания, который призвано обеспечить практическое внедрение обновленных клинических рекомендаций, перед клиницистами по-прежнему стоят несколько нерешенных вопросов в отношении оптимального применения инновационных противодиабетических препаратов из классов арГПП‑1 и ингибиторов SGLT2. Один из них заключается в том, может ли комбинированное применение арГПП‑1 и ингибиторов SGLT2 обеспечить дополнительное преимущество в плане профилактики МАСЕ, сердечно-сосудистой смерти, снижения частоты госпитализации по поводу СН и замедления прогрессирования ХБП. Три ранее проведенных исследования продемонстрировали эффективность такой комбинации для снижения уровня HbA1c и массы тела (Zinman B. et al., 2019; Ludvik B. et al., 2018; Frías J. P. et al., 2016), но ни в одном из них не рассматривалось влияние сочетанного назначения препаратов этих двух классов на кардиоренальные конечные точки. Второй вопрос, который возникает на основании данных последних вторичных анализов исследований ингибиторов SGLT2, заключается в том, существуют ли подгруппы пациентов, которые получают непропорциональные либо очень незначительные преимущества от лечения более современными противодиабетическими препаратами. Появляющиеся доказательства того, что ингибиторы SGLT2 могут быть особенно эффективны в предотвращении неблагоприятных исходов у пациентов с СД 2 типа и СНсФВ, повышают вероятность более целенаправленного использования этих средств. Наконец, остаются неясны механизмы действия, посредством которых арГПП‑1 и ингибиторы SGLT2 обеспечивают кардиоренальные преимущества при СД 2 типа. Исследования в этой области, бесспорно, будут очень полезны для оптимизации подходов к применению инновационных противодиабетических препаратов с целью снижения риска развития кардиоваскулярных и почечных осложнений СД 2 типа. На основании изменений, внесенных в 2019 г. в предыдущие консенсусные рекомендации (Davies M. J., D’Alessio D.A., Fradkin J. et al. Management of hyperglycaemia in type 2 diabetes, 2018. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia. 61 (12): 2461-2498), экспертами ADA и EASD (Buse J. B. et al., 2019) предлагаются обновленные модифицированные алгоритмы ведения пациентов с СД 2 типа (рис. 1, 2).
Рис. 1. Сахароснижающая терапия при СД 2 типа: общий подход (Davies M.J., D’Alessio D.A., Fradkin J. et al., 2018)
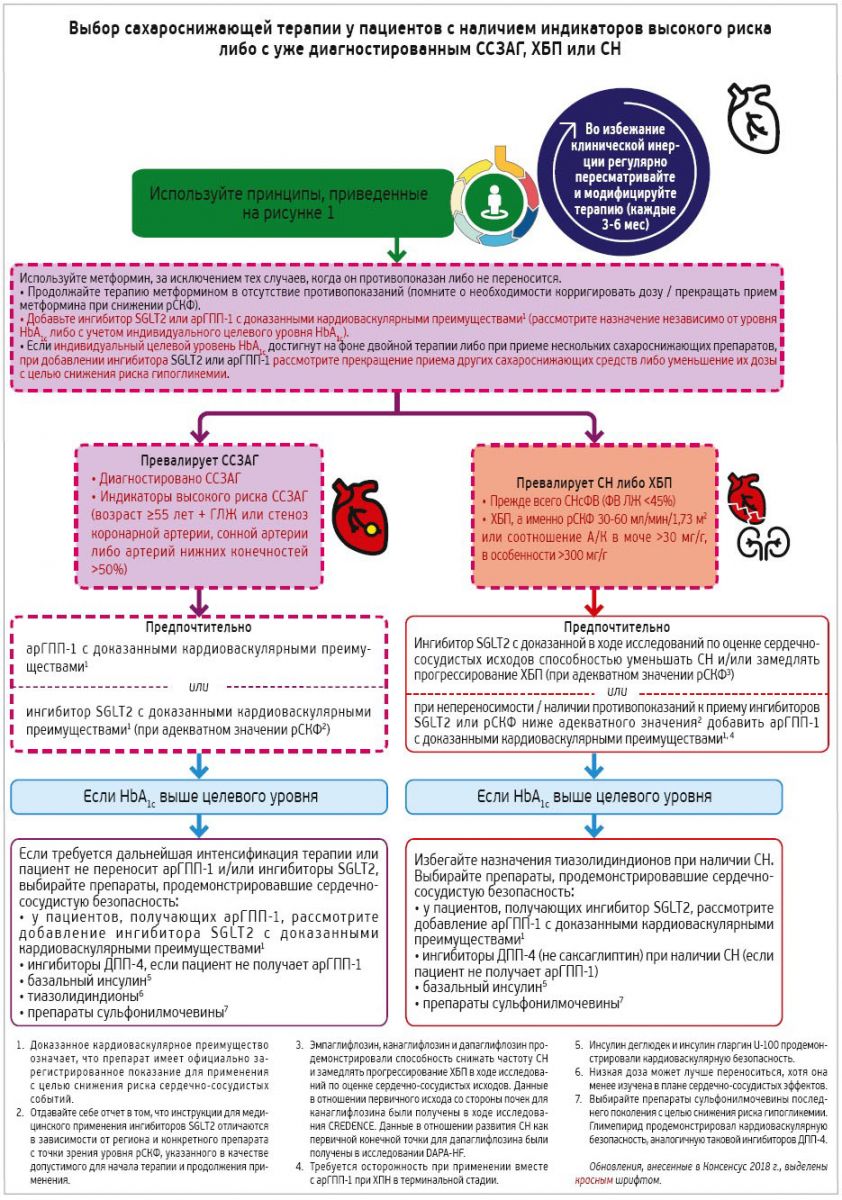 Рис. 2. Ведение пациентов с СД 2 типа: общие положения (Davies M.J., D’Alessio D.A., Fradkin J. et al., 2018)
Рис. 2. Ведение пациентов с СД 2 типа: общие положения (Davies M.J., D’Alessio D.A., Fradkin J. et al., 2018)
Ключевые изменения, внесенные в консенсусные рекомендации ADA и EASD (2019)
Предыдущие рекомендации состояли в том, что при наличии СД 2 типа установленный диагноз ССЗ считался убедительным показанием для лечения арГПП‑1 или ингибитором SGLT2. Теперь же экспертами предлагается следующий подход.
Общие рекомендации
- У пациентов группы высокого риска с диагностированным СД 2 типа решение о лечении арГПП‑1 или ингибитором SGLT2 с целью снижения риска развития MACE, госпитализаций по поводу СН, сердечно-сосудистой смерти или прогрессирования ХБП должно рассматриваться независимо от исходного либо индивидуального целевого уровня HbA1c.
- Специалисты здравоохранения должны участвовать в совместном принятии решений относительно стартовой комбинированной терапии в случаях впервые выявленного СД 2 типа.
Рекомендации в отношении применения арГПП‑1
- У пациентов с СД 2 типа и диагностированным ССЗАГ (больные, перенесшие ИМ, ишемический инсульт, нестабильную стенокардию с изменениями на ЭКГ, ишемию миокарда, подтвержденную результатами визуализационных исследований либо стресс-тестов, или реваскуляризацию коронарных, сонных либо периферических артерий), для которых MACE представляют собой самую серьезную угрозу, наиболее высоким уровнем доказательности в плане снижения их риска обладают арГПП‑1.
- Назначение арГПП‑1 с целью снижения риска MACE также может рассматриваться у пациентов с СД 2 типа без диагностированного ССЗ, но с наличием индикаторов высокого риска, а именно у пациентов в возрасте ≥55 лет с наличием стеноза (>50%) коронарных артерий, сонных артерий либо артерий нижних конечностей, ГЛЖ, рСКФ <60 мл/мин/1,73 м2 или альбуминурии.
Рекомендации в отношении применения ингибиторов SGLT2
- У пациентов с диагностированным ССЗАГ либо без такового, но с наличием СНсФВ (ФВ <45%), ХБП (рСКФ от 30 до ≤60 мл/мин/1,73 м2 или соотношения А/К в моче >30 мг/г, в особенности при значении А/К >300 мг/г) наиболее высоким уровнем доказательности в отношении замедления прогрессирования указанных патологических состояний характеризуются ингибиторы SGLT2.
- Ингибиторы SGLT2 рекомендованы пациентам с СД 2 типа и СН (в особенности с СНсФВ) с целью снижения частоты госпитализаций по поводу СН, частоты развития МАСЕ и сердечно-сосудистой смертности.
- Ингибиторы SGLT2 рекомендованы пациентам с СД 2 типа при наличии ХБП для профилактики ее прогрессирования, а также для уменьшения частоты госпитализаций по поводу СН, снижения риска развития MACE и сердечно-сосудистой смерти.
- Пациентам с язвами на стопах или больным с высоким риском ампутаций лечение ингибиторами SGLT2 следует назначать только после тщательного коллегиального обсуждения с учетом всех рисков и преимуществ, а также при условии комплексного обучения уходу за стопами и принятия соответствующих мер по профилактике ампутаций.
Подготовила Елена Зотова
Медична газета «Здоров’я України 21 сторіччя» № 2 (471), січень 2020 р.



