17 лютого, 2020
Лікування діабету в пацієнтів віком понад 65 років: настанови Ендокринного товариства* для клінічної практики
Цукровий діабет (ЦД) – це вікова хвороба, оскільки третина населення США віком ≥65 років відповідає її критеріям, серед них >90% – 2 типу, і майже половина – критеріям предіабету. Уперше діагностований ЦД переважає в осіб віком 65-79 років. Приблизно в 50% пацієнтів віком 60-69 років і в 60-65% осіб старших вікових груп тривалість хвороби перевищує 10 років. Утім, кожен п’ятий пацієнт віком ≥80 років повідомляє, що ЦД виник до 5 років: за відсутності регулярного скринінгу хворобу пізно діагностують, тому її тривалість часто недооцінюється. За прогнозами, впродовж наступних 30 років поширеність ЦД істотно зросте через старіння населення, збільшення мінорних груп високого ризику, а також подовження тривалості життя хворих унаслідок зниження ризику серцево-судинної смерті.
Пацієнти старших вікових груп більш схильні до всіх діабетичних ускладнень (рис. 1), серед яких особливе клінічне значення мають хронічна хвороба нирок (ХХН), втрата зору, інфаркт міокарда, серцева недостатність (СН), інсульт, ураження периферичних артерій і нервів.
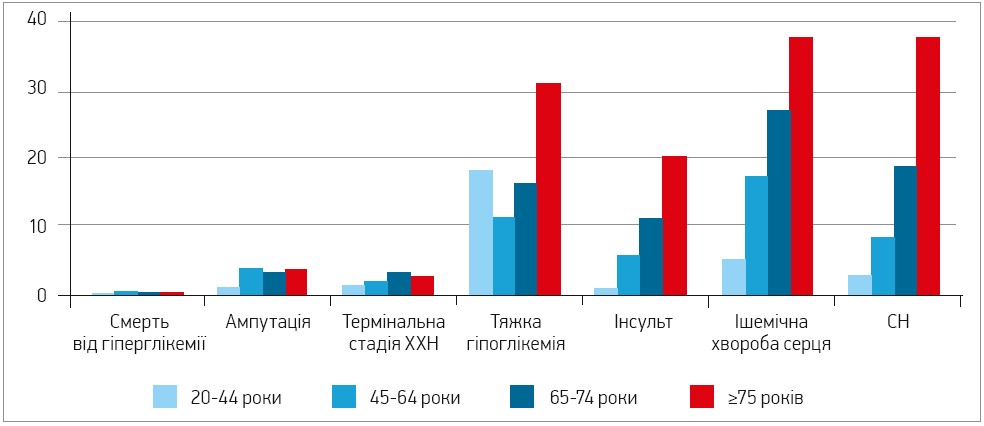 Рис. 1. Частота ускладнень ЦД у дорослих на 1000 осіб у 2009 р.
Рис. 1. Частота ускладнень ЦД у дорослих на 1000 осіб у 2009 р.
У половини хворих на ЦД старшого віку виявляють альбумінурію та/або зменшення швидкості клубочкової фільтрації (ШКФ), що вказує на діабетичну нефропатію, котра спричиняє до 50% усіх випадків термінальної ХХН у США, особливо в осіб віком ≥75 років. Ризик ампутації в цій когорті вдесятеро вищий, аніж в осіб відповідного віку без діабету.
Патофізіологія гіперглікемії
Унаслідок складної взаємодії між генетичними факторами, способом життя та старінням (рис. 2) особи старшого віку більш схильні до ЦД 2 типу. Складність зумовлена значною гетерогенністю в патофізіології, клінічних особливостях і швидкості прогресування хвороби. З віком істотно погіршується толерантність до глюкози та знижується секреція інсуліну через порушення функції β-клітин підшлункової залози. Такі розлади зменшують адаптацію до інсулінорезистентності (ІР), спричиненої способом життя, та призводять до трансформації предіабету в ЦД 2 типу. Токсичність глюкози внаслідок хронічної гіперглікемії ще більше посилює ІР і погіршує функцію β-клітин. Отже, діабетична гіперглікемія посилюється з віком через погіршення функції та проліферації β-клітин. Замикає хибне коло ліпотоксичність, зумовлена впливом продуктів ліполізу жирових клітин та акумуляцією жиру поза межами жирової тканини, притаманної вісцеральному ожирінню. Неоднорідність ЦД 2 типу, ймовірно, пояснюється індивідуальною особливістю впливів численних гіперглікемічних чинників, розуміння яких у кожному конкретному випадку може сприяти правильному вибору глюкозознижувальних засобів (ГЗЗ).
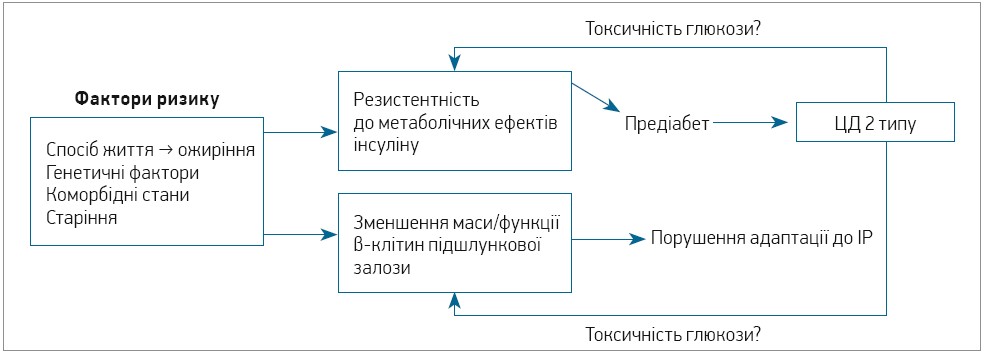 Рис. 2. Модель гіперглікемії, пов’язаної з віком
Рис. 2. Модель гіперглікемії, пов’язаної з віком
Скринінг порушень обміну глюкози та профілактика ЦД
Для скринінгу рекомендовано визначати рівень глікемії натще та/або глікований гемоглобін (HbA1c). У певної частки осіб цієї вікової групи визначення HbA1c може бути неточним через супутні хвороби, котрі впливають на тривалість життя еритроцитів. За умови нормальних результатів початкового скринінгу повторне обстеження рекомендовано проводити хоча би раз на 2 роки. Індивідуальне рішення щодо скринінгу залежить і від можливості застосування певних дій, які врешті будуть корисними для пацієнта. Наприклад, скринінг не виправданий у разі тяжкої невиліковної хвороби – термінальної стадії раку чи тяжкої недостатності певних органів або систем. У таких ситуаціях рекомендовано спільне прийняття рішень із пацієнтом.
Якщо результати скринінгу відповідають критеріям предіабету (табл. 1), рекомендовано провести оральний глюкозотолерантний тест (ОГТТ) для визначення глікемії через 2 год після навантаження, особливо за наявності ознак, які відносять пацієнта до категорії високого ризику, – надмір маси тіла / ожиріння, ЦД у родичів 1 ступеня спорідненості, етнічність із високим ризиком (афро-, латино- та корінні американці, азіати, мешканці островів Тихого океану), серцево-судинне захворювання (ССЗ) в анамнезі, артеріальна гіпертензія (рівень артеріального тиску (АТ) ≥140/90 мм рт. ст. або антигіпертензивна терапія), холестерин ліпопротеїнів високої щільності ≤0,9 ммоль/л (35 мг/дл) і/або тригліцериди крові ≥2,82 ммоль/л (250 мг/дл), апное уві сні, низька фізична активність. Спільне прийняття рішення щодо проведення ОГТТ рекомендовано слабким і виснаженим пацієнтам. Перед ОГТТ проводять стандартну дієтичну підготовку.
Особам із предіабетом рекомендовано модифікацію способу життя (МСЖ), описану в Програмі профілактики для сповільнення прогресування ЦД. Оскільки метформін не затверджений Управлінням із контролю якості продуктів харчування та лікарських засобів США (FDA) для профілактики ЦД, його не рекомендовано призначати особам із предіабетом.
Ведення пацієнтів із діагностованим ЦД
Роль ендокринолога та діабетолога. Рекомендовано, щоб ці спеціалісти співпрацювали з лікарем первинної ланки, мультидисциплінарною командою та пацієнтом у розробленні індивідуальних терапевтичних цілей для осіб із вперше діагностованим діабетом. Ці фахівці також несуть головну відповідальність за ведення хворих у таких випадках: ЦД 1 типу, потреба в комплексному лікуванні гіперглікемії для досягнення терапевтичних цілей, періодична тяжка гіпоглікемія, множинні ускладнення ЦД.
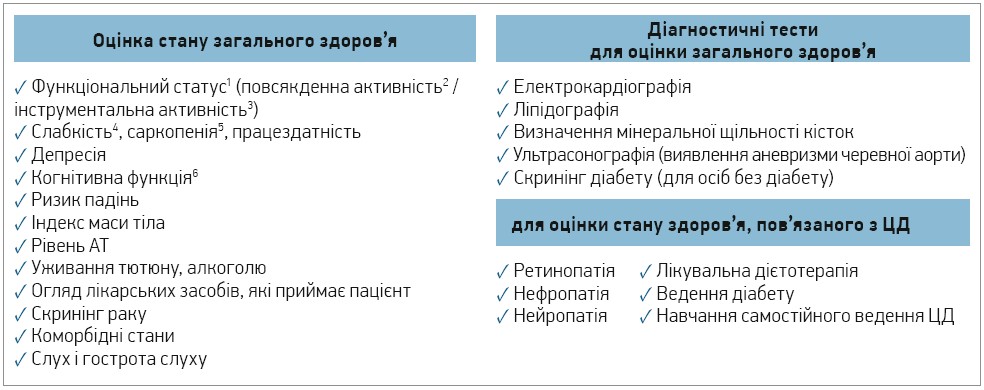
Обстеження хворих на діабет передбачає оцінку стану здоров’я (рис. 3), на підставі якої визначають цілі та стратегію лікування (рис. 4). У пацієнтів старших вікових груп важливо оцінювати фізичний стан (слабкість, функціональний статус) і когнітивну функцію, котра часто порушена через хворобу Альцгеймера, судинну деменцію та власне діабет. У пацієнтів із когнітивними розладами чи деменцією запропоновано спростити схему прийому ліків та обирати більш м’які глікемічні цілі (рис. 4) для поліпшення прихильності до терапії та запобігання пов’язаним із нею ускладненням.
Рис. 3. Оцінка стану здоров’я у хворих на ЦД віком ≥65 років
Примітки. 1 Здатність виконувати звичні буденні дії для задоволення основних потреб і підтримки здоров’я й добробуту.
2 Включає такі види активності: купання, одягання, вживання їжі, відвідування туалету та пересування.
3 Приготування їжі, здійснення покупок, управління грошима, користування телефоном, прийом ліків.
4 Стан підвищеної вразливості до фізичних/психологічних стресорів унаслідок зменшення фізіологічних резервів багатьох органів і систем, що обмежує здатність підтримувати гомеостаз, часто супроводжує ЦД і може бути ознакою поганої реакції на втручання. Тести для оцінки: шкала Fried включає проведення 2 процедур (оцінка швидкості ходьби й вимірювання сили стиснення динамометром) і 3 запитання стосовно втрати маси тіла, ступеня виснаження й обсягу фізичного навантаження, що може виконати пацієнт; шкала FRAIL не потребує проведення процедур, включає 5 запитань стосовно втоми, піднімання сходами, ходьби, кількості захворювань і втрати маси тіла.
5 Вікова втрата м’язової маси, а отже, сили м’язів і фізичної працездатності, що значно посилюється при ЦД. Методи оцінки: рентгенівська абсорціометрія, біоелектричний імпеданс або швидкий скринінговий тест Sarc-F (включає 5 запитань щодо анамнезу падінь, здатності піднімати предмети та проблем із рухливістю).
6 Скринінг треба проводити під час діагностики ЦД. За умови нормальних результатів оцінку повторюють кожні
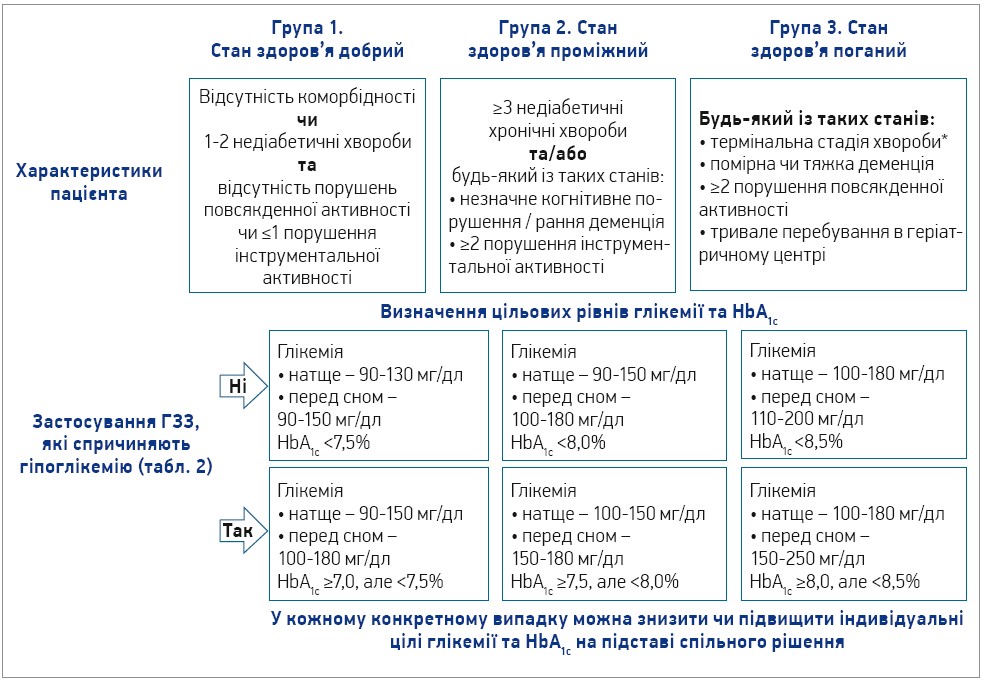
Рис. 4. Визначення групи здоров’я та цільових рівнів глікемії
Примітка: * хвороби з обмеженими можливостями лікування чи короткою очікуваною тривалістю життя.
Лікування гіперглікемії в амбулаторних умовах
Цільові рівні глікемії мають обиратися так, щоб відповідати стратегіям забезпечення загального здоров’я, знижувати ризик діабетичних ускладнень і мінімізувати ризик гіпоглікемії (рис. 4). У хворих на ЦД старшого віку гіпоглікемія підвищує ризик виникнення травм унаслідок падіння, посилює когнітивні розлади, збільшує захворюваність і смертність. Тяжка гіпоглікемія пов’язана з ускладненнями з боку дихальної системи, травного тракту та практично подвоює ризик мікро- й макроваскулярних діабетичних ускладнень, а також серцево-судинної та загальної смерті. Тому вибір терапії передбачає уникнення призначення ГЗЗ, здатних посилити ризик розвитку гіпоглікемії (табл. 2).
З іншого боку, надто високі рівні глікемії, котрі тривалий час перевищують глюкозуричний поріг >200 мг/дл, збільшують ризик дегідратації, електролітних розладів, інфекції сечових шляхів, запаморочення й падінь. Гіперглікемічні кризи, спричинені діабетичним кетоацидозом, гіперглікемічним гіперосмолярним синдромом або їх комбінацією (гіперосмолярним кетоацидозом), є тяжкими ускладненнями недіагностованої та нелікованої гіперглікемії, що в пацієнтів похилого віку значно частіше зумовлюють смерть, аніж у молодших осіб. Отже, оптимальне лікування гіперглікемії має балансувати між компенсацією діабету та ризиком гіпоглікемії.
Оцінка глікемії у хворих на діабет, які приймають інсулін, окрім визначення рівня HbA1c, має включати частий моніторинг глюкози в капілярній крові за допомогою глюкометра й тестових смужок і/або тривалий моніторинг глюкози.
Модифікація способу життя вважається терапією першої лінії амбулаторного лікування діабету.
Харчування. В усіх пацієнтів рекомендовано оцінювати харчовий статус для виявлення та корекції порушень, використовуючи перевірені методи оцінки, як-от Короткий опитувальник для оцінки харчового статусу. Слабким пацієнтам пропонується дієта, збагачена білком та енергією, щоб запобігти недоїданню та втраті маси тіла. За неможливості досягнення цільових рівнів глікемії шляхом МСЖ рекомендовано обмежити споживання простих вуглеводів, але уникати будь-яких інших типів обмежувальних дієт, особливо в разі порушень харчового статусу. Слід ретельно контролювати реакцію глікемії на будь-які зміни харчування як у пацієнтів, які проживають удома, так і в тих, які перебувають у соціальних закладах догляду.
Для поліпшення загального стану здоров’я, нормалізації маси тіла, досягнення цільових рівнів глікемії, АТ і ліпідів крові та зменшення ризику діабетичних ускладнень потрібно забезпечити здорове збалансоване харчування та високоякісні харчові продукти. Прикладами здорового харчування є середземноморська дієта чи дієта DASH (дієтичні підходи для припинення гіпертензії). Хворим на ЦД рекомендовано збільшити споживання клітковини з 25 до 35 г/добу за рахунок збільшення кількості овочів, фруктів, бобових і цільнозернових злаків у раціоні, за винятком пацієнтів із гастропарезом. Для запобігання закрепам і каловій інтоксикації особам старшого віку важливо споживати достатньо рідини. Хворим на ЦД рекомендовано обмежити споживання натрію
Фармакотерапія. У більшості хворих на ЦД 2 типу рекомендовано починати терапію з перорального застосування метформіну. Проте його не слід призначати пацієнтам зі значною дисфункцією нирок (ШКФ ≤30 мл/хв/1,73 м2) або в разі поганої переносимості внаслідок розладів із боку шлунково-кишкового тракту.
За відсутності досягнення цільових рівнів глікемії, незважаючи на МСЖ і лікування метформіном, рекомендовано додати інший пероральний або ін’єкційний ГЗЗ з огляду на застереження та протипоказання (табл. 2). Для зменшення ризику гіпоглікемії краще уникати препаратів сульфонілсечовини, глінідів і високих доз інсуліну. Режим застосування ГЗЗ має бути максимально спрощеним.
Лікування ускладнень ЦД
Контроль артеріальної гіпертензії. Для зниження ризику виникнення ССЗ, інсульту та прогресування ХХН рекомендовано забезпечити цільовий рівень АТ 140/90 мм рт. ст. Нижчі показники (130/80 мм рт. ст.) можна розглядати в пацієнтів певних груп високого ризику, як-от із перенесеним інсультом або прогресуючою ХХН (ШКФ ≤60 мл/хв/1,73 м2 і/або альбумінурія), за умови ретельного моніторингу з метою уникнення ортостатичної гіпотензії. У пацієнтів із поганим станом здоров’я (група 3, рис. 4) можна розглядати вищі рівні АТ –
Контроль гіперліпідемії. Рекомендовано щорічний контроль ліпідів крові, на підставі результатів якого приймають рішення щодо потреби та ефективності ліпідознижувальної терапії. Препаратами вибору є статини, котрі мають доведену ефективність знижувати абсолютний ризик ССЗ і смерті від усіх причин. Робочою групою цих настанов не вивчалися докази щодо цільових рівнів холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у цій популяції, тому конкретні цільові рівні не запропоновано. Проте для пацієнтів віком ≥80 років або з короткою очікуваною тривалістю життя цільові рівні ХС ЛПНЩ не мають бути настільки строгими, як для загальної популяції.
Якщо терапія статинами не спроможна забезпечити зниження ХС ЛПНЩ до бажаних рівнів або внаслідок побічних ефектів, альтернативним або додатковим шляхом контролю може бути застосування езетимібу або інгібіторів пропротеїнової конвертази субтилізин-кексинового типу 9.
За умови гіпертригліцеридемії (рівень тригліцеридів натще >500 мг/дл) для зменшення ризику розвитку панкреатиту рекомендовано призначати риб’ячий жир і/або фенофібрат.
Ведення СН. Рекомендовано стандартну терапію відповідно до клінічних настанов щодо лікування СН, опублікованих у 2018 р. У зв’язку з можливістю погіршення перебігу СН треба з обережністю призначати такі ГЗЗ: глініди, розиглітазон, піоглітазон, інгібітори дипептидилпептидази‑4.
Ведення атеросклерозу. Хворим на ЦД із супутніми атеросклеротичними ССЗ рекомендовано малі дози ацетилсаліцилової кислоти (75-162 мг/добу) для вторинної профілактики після ретельної оцінки ризику кровотеч за умови спільного прийняття рішення з пацієнтом, членами родини або опікунами.
Очні ускладнення. Для виявлення захворювань сітківки всім хворим на діабет рекомендовано щорічне комплексне офтальмологічне обстеження. Обстеження та лікування має проводити офтальмолог або окуліст відповідно до сучасних стандартів.
Проблеми, пов’язані з нейропатією, падіннями та нижніми кінцівками. У пацієнтів із хронічною сенсомоторною дистальною полінейропатією рекомендовано застосовувати схеми лікування, що мінімізують ризик падінь. Наприклад, уникати призначень / зменшити дози седативних препаратів або лікарських засобів, які спричиняють ортостатичну гіпотензію та/або гіпоглікемію. Якщо нейропатія призводить до порушення ходьби чи рівноваги, доцільно скеровувати пацієнтів на фізичну терапію чи спеціальну програму зі зменшення ризику падінь для уникнення переломів і пов’язаних із ними ускладнень. Пацієнтів із периферичною нейропатією та/або ураженням периферичних артерій треба скеровувати до ортопедів, спеціалістів із лікування діабетичної стопи чи судинних хірургів для превентивного лікування та зменшення ризику виразок стопи та/або ампутації ноги.
Хронічна хвороба нирок. Пацієнтам, які не перебувають на діалізі, рекомендовано щорічний скринінг ХХН із розрахунком ШКФ і визначенням співвідношення альбумін/креатинін у сечі. Останній показник не обов’язково визначати пацієнтам із поганим станом здоров’я (група 3, рис. 4) або тим, у яких співвідношення альбумін/креатинін у сечі <30 мг/г. Пацієнтам зі зниженою ШКФ рекомендовано обмежити застосування чи зменшити дозу багатьох класів ГЗЗ (табл. 2) із метою мінімізації побічних ефектів та уникнення ускладнень, пов’язаних із ХХН.
Особливі обставини та категорії пацієнтів
Ведення ЦД у лікарнях, соціальних установах і зміни умов догляду. Хворим на діабет, які перебувають у лікарні чи в соціальних закладах догляду, рекомендовано встановлення чітких цільових рівнів глікемії – 5,55-7,77 ммоль/л (100-140 мг/дл) натще та 7,77-10 ммоль/л (140-180 мг/дл) після їди, уникаючи гіпоглікемії. Виписка зі стаціонару має бути чітко спланована для відновлення тривалих терапевтичних цілей і режиму застосування ГГЗ поза стаціонаром. Пацієнтам із тяжкими супутніми чи термінальними хворобами рекомендовано спрощені стратегії лікування та ведення діабету.
За відсутності діагностованого ЦД усім пацієнтам віком ≥65 років під час будь-якої госпіталізації рекомендовано плановий скринінг для виявлення діабету шляхом визначення рівня HbA1c.
* Європейське товариство ендокринологів, Американське геронтологічне товариство, Товариство з проблем ожиріння.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 2 (471), січень 2020 р.