17 лютого, 2020
Предиктори залізодефіцитної анемії в осіб похилого віку на первинній ланці медичної допомоги: європейське мультицентрове дослідження
Вступ
Залізодефіцитна анемія (ЗДА) – поширена причина інвалідизації [1]. У країнах високого рівня достатку головними причинами ЗДА є стани, пов’язані з віком та статтю, наприклад надмірні менструальні кровотечі в жінок фертильного віку та шлунково-кишкові кровотечі в чоловіків та осіб похилого віку [2, 3]. В останніх ЗДА й анемія хронічних хвороб негативно впливають на фізичні та когнітивні функції, а також асоціюються зі збільшенням частоти госпіталізацій і меншою тривалістю виживаності [4, 5]. Відповідно до даних нещодавнього систематичного огляду та метааналізу анемія пов’язана із двократним зростанням частоти значної ослабленості, що, своєю чергою, різко підвищує ризик погіршення стану здоров’я в осіб похилого віку [6]. І анемія, і залізодефіцит продемонстрували несприятливий вплив на асоційовану зі здоров’ям якість життя пацієнтів із кількома хронічними захворюваннями [7-9].
У США залізодефіцит спричинює приблизно 17% випадків анемії в осіб похилого віку [10]. В Італії поширеність ЗДА в пацієнтів первинної ланки медичної допомоги віком ≥65 років становить 8,1 випадку на 1 тис. людино-років [11]. Однак слід зауважити, що ознаки та симптоми анемії можуть бути неспецифічними і часто не привертають уваги лікарів під час огляду пацієнтів похилого віку, оскільки ці ознаки приписують іншим хронічним захворюванням [12].
Отже, розпізнання факторів ризику ЗДА є ключовим у забезпеченні пацієнтів своєчасними діагностичними та лікувальними процедурами, а також у запобіганні середньо- та довготерміновим несприятливим наслідкам цього стану.
Хворий на анемію звертається передусім до лікаря загальної практики – сімейної медицини (ЗПСМ). Ознайомлення сімейного лікаря з достовірною інформацією щодо клінічних предикторів анемії може допомогти йому в процесі диференційного діагнозу та раннього виявлення згаданого стану. Для цього було проведено низку досліджень, зокрема в описуваній роботі проаналізовано чинники, що асоціюються з поширенням ЗДА в пацієнтів похилого віку на первинній ланці медичної допомоги в чотирьох країнах Європи.
Методи
Італійські дані було отримано із загальної бази даних Health Search Database, яка включає електронні записи понад тисячі лікарів ЗПСМ по всій країні. Дані для Бельгії, Іспанії та Німеччини було взято з бази даних IQVIA.
Для оптимізації диференційної діагностики між ЗДА й анемією хронічних захворювань [20] ЗДА визначалася за кодами 280 (Міжнародна класифікація хвороб (МКХ) 9-го перегляду) та D50 (МКХ 10-го перегляду) або, за відсутності кодів, за рівнів гемоглобіну <130 г/л у чоловіків та <120 г/л у жінок у сполученні з умістом феритину <15 нг/мл чи вільних рецепторів трансферину >29,5 нмоль/л або загальної залізозв’язувальної здатності сироватки >3,15 мг/л, що були зафіксовані в межах 6 міс до/після визначення гемоглобіну.
У ролі потенційних предикторів ЗДА розглядалися стать, ознаки та симптоми даної хвороби (слабкість, випадіння волосся), супутні патологічні стани і хвороби (поліпи шлунково-кишкового тракту, рак), ятрогенні чинники (штучні клапани серця, прийом нестероїдних протизапальних препаратів (НПЗП), кортикостероїдів). Загальний тягар коморбідних станів оцінювався за індексом коморбідності Чарлсона (ІКЧ) [21].
Для оцінки предикторів були застосовані метод мультиваріантної регресії Кокса та розрахунок стандартизованих відношень ризиків (сВР) з 95% довірчими інтервалами (ДІ). Статистичний аналіз виконувався за допомогою програмного обладнання STATA 11 (STATA Corp., США).
Результати
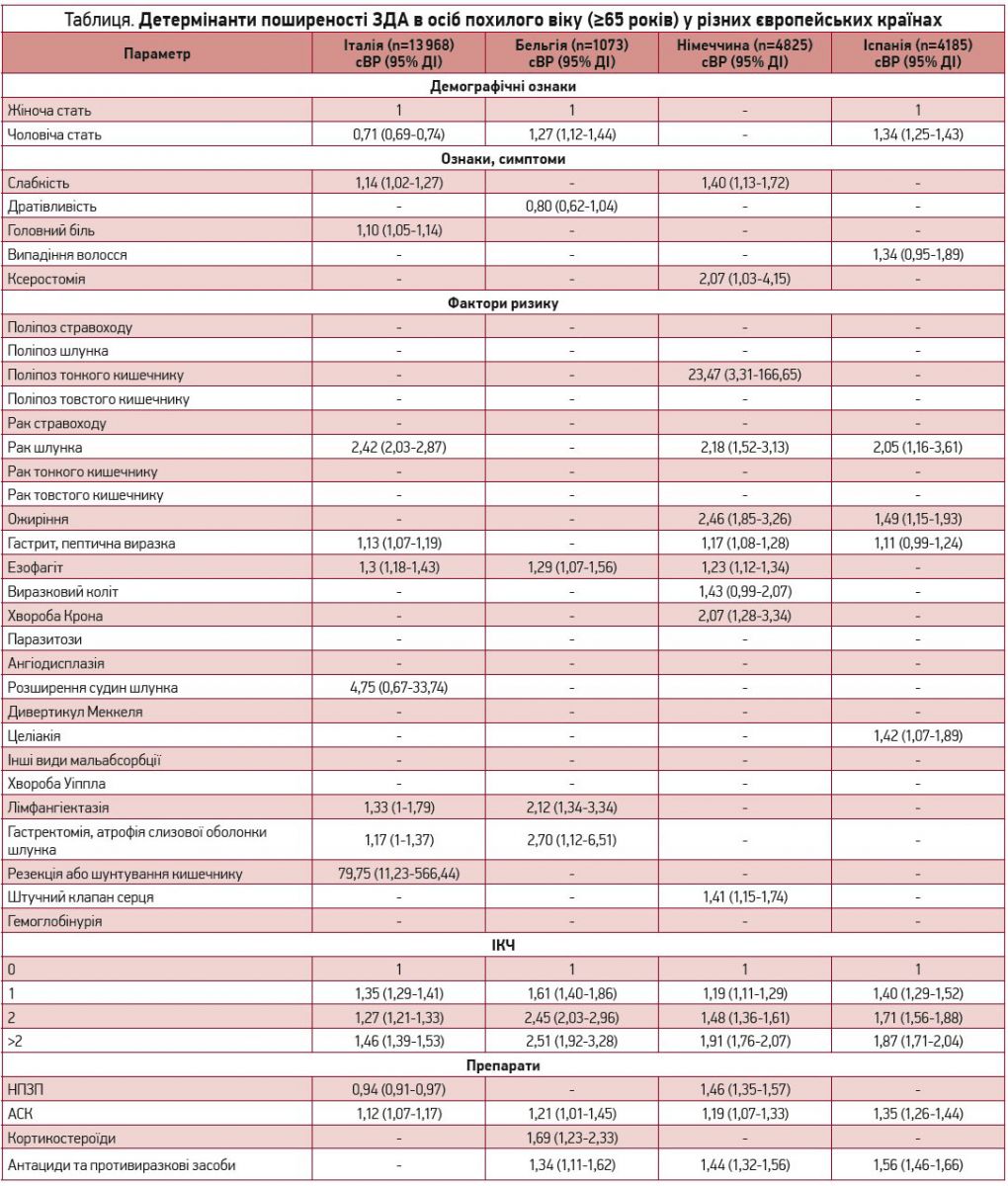
У дослідження було включено 24 051 особу віком ≥65 років (Італія – 13 968, Бельгія – 1073, Німеччина – 4825, Іспанія – 4185). У таблиці показано кореляції поширеності ЗДА з проаналізованими чинниками в різних країнах.
У Бельгії та Іспанії в чоловіків спостерігався на 27 та 34% (p<0,05) відповідно вищий ризик ЗДА, ніж у жінок. І навпаки, в Італії ризик був дещо нижчим (на 29%; p<0,05). З більшою поширеністю ЗДА асоціювалися такі симптоми, як слабкість (діапазон сВР 1,14-1,40), головний біль (сВР 1,10; 95% ДІ 1,05-1,14), ксеростомія (сВР 2,07; 95% ДІ 1,03-4,15), і такі хвороби, як поліпоз тонкого кишечнику (сВР 23,47; 95% ДІ 3,31-166,65) і рак шлунка (діапазон сВР 2,05-2,42). З високою ймовірністю із ЗДА також асоціювалася низка хронічних захворювань, зокрема шлунково-кишкові хвороби, резекції кишечнику в анамнезі, целіакія (сВР 1,42; 95% ДІ 1,07-1,89) та наявність штучних клапанів серця (сВР 1,41; 95% ДІ 1,14-1,74). Вищий ІКЧ також був пов’язаний із більшим ризиком ЗДА у всіх країнах. Крім того, більша частота ЗДА корелювала з уживанням ацетилсаліцилової кислоти (АСК) (діапазон сВР: 1,12-1,35), кортикостероїдів (сВР 1,69; 95% ДІ 1,23-2,33) та антацидних/противиразкових препаратів (діапазон сВР 1,34-1,56). Уживання НПЗП було пов’язано з достовірно більшою частотою ЗДА в Німеччині, але меншою – в Італії.
Обговорення
Дослідження, яке включало понад 24 тис. осіб похилого віку з Італії, Бельгії, Німеччини та Іспанії, показало, що певні хронічні патологічні стани, а також значна кількість коморбідних захворювань, деякі симптоми й види фармакологічного лікування є важливими предикторами ЗДА. Ця інформація може допомогти лікарям ЗПСМ вчасно діагностувати ЗДА в цій когорті пацієнтів.
Нестача заліза – один із найпоширеніших дефіцитів нутрієнтів у світі [22]. Відповідно до даних нещодавнього систематичного огляду та метааналізу, у 24% осіб похилого віку з анемією розвивається слабкість. Ризик останньої за наявності анемії є вдвічі вищим [6]. Це означає, що значна частка осіб похилого віку з анемією знаходиться в групі ризику несприятливих для здоров’я наслідків. Цікаво, що в ослаблених людей похилого віку із ЗДА ризик таких наслідків можна зменшити за умови вчасного початку інтенсивного лікування [23]. Анемія може спричинити низку симптомів, що часто мають місце в осіб цієї вікової когорти, зокрема слабкість, підвищену втомлюваність і задишку. Крім того, анемія може знижувати клінічний поріг, тобто сприяти посиленню проявів таких захворювань, як ішемічна хвороба серця, серцева недостатність та хронічні респіраторні захворювання. Через це анемія асоціюється з підвищенням захворюваності, смертності та використанням медичних ресурсів особами похилого віку, а вчасне розпізнання цього стану здатне допомогти уникнути або відтермінувати численні несприятливі наслідки [24].
Результати дослідження підтверджують вищий ризик ЗДА в пацієнтів із хворобами, які супроводжуються кровотечами або порушенням всмоктування в шлунково-кишковому тракті, на кшталт раку шлунка, гастритів та виразки шлунка, стану після гастректомії, резекції або шунтування кишечнику, атрофії шлунка, езофагіту, хвороби Крона, целіакії, лімфангіектазії та поліпозу тонкого кишечнику [25, 26].
Водночас у ході дослідження було виявлено більшу ймовірність розвитку ЗДА в пацієнтів зі скаргами на слабкість, дратівливість чи ксеростомію, які можуть бути симптомами саме анемії. Власне, вони є проявами явної анемії, недіагностованої в даного контингенту хворих, незважаючи на наявність подібних скарг. Було зафіксовано також більший ризик ЗДА в пацієнтів зі штучними клапанами, що можна пояснити гемолізом – ускладненням після хірургічних втручань на мітральному клапані [27]. Корекція залізодефіциту може сприяти клінічному покращанню в пацієнтів із вищезгаданими станами.
У дослідженні застосування НПЗП супроводжувалося більшим ризиком ЗДА в Німеччині, однак негативно асоціювалося з кількістю анемій в Італії. Перший висновок відповідає добре відомому факту щодо пошкодження шлунка та появи кровотеч унаслідок прийому НПЗП, другий – може бути зумовлений методологічними неточностями [28]. Наприклад, обернену асоціацію можна пояснити тим, що НПЗП призначають хворим із кращим станом здоров’я. Було виявлено цікавий факт: щодо АСК збільшення ризику спостерігалося у всіх проаналізованих країнах, імовірно, як наслідок її тривалого застосування в низьких дозах для вторинної профілактики серцево-судинних захворювань. Оскільки кислота шлункового соку є необхідною для оптимального всмоктування заліза в кишечнику, застосування антацидів і противиразкових засобів супроводжувалося зростанням ризику ЗДА. Крім того, з урахуванням показань до призначення цих препаратів, антациди можуть бути опосередкованим свідченням наявності хвороб, які підвищують ризик шлунково-кишкових кровотеч. Це також може пояснювати тісний зв’язок між ЗДА та вживанням антацидів.
Згідно з результатами попередніх робіт, у ході яких автори виявили очевидну асоціацію ожиріння із залізодефіцитом [29], дане дослідження підтвердило, що ожиріння значуще підвищує ризик ЗДА. Потенційні пояснення цього факту включають низький рівень уживання залізовмісних продуктів, підвищену потребу в залізі та/або порушене його всмоктування, імовірно, унаслідок дії антацидів, які часто призначають пацієнтам з ожирінням для контролю симптомів кислотозалежних захворювань. Крім того, важливу роль може відігравати пов’язане з ожирінням запалення внаслідок активації гепцидину [29].
Той факт, що мультиваріантні моделі включали не всі проаналізовані чинники, може бути пояснений незначною частотою деяких із них, що знижує точність аналізу. Наприклад, дратівливість виступала предиктором ЗДА лише в Бельгії; ксеростомія, поліпоз тонкого кишечнику, хвороба Крона та наявність штучних клапанів – лише в Німеччині; розширення судин шлунка – лише в Італії; випадіння волосся – лише в Іспанії. Проте ці симптоми та захворювання є відомими детермінантами поширеності ЗДА [29].
Головним обмеженням дослідження стала нестача інформації щодо потенційних відмінностей у харчових звичках, які можуть виступати важливим фактором ризику. Наприклад, рівень уживання харчових волокон може впливати на ризик ЗДА та відповідь на препарати заліза [29].
Висновки
Результати описуваного дослідження можуть привернути більше уваги лікарів ЗПСМ до предикторів ЗДА й асоційованих із цією анемією чинників в осіб похилого віку, а також зменшити тягар ЗДА на первинній ланці медичної допомоги. Цей експеримент підтвердив роль шлунково-кишкових захворювань, деяких клінічних ознак і симптомів (ожиріння, слабкість, дратівливість, ксеростомія), застосування певних ліків (НПЗП) як предикторів ЗДА й ознак, асоційованих із цим захворюванням. Це підкреслює важливість обстеження верхніх та нижніх відділів шлунково-кишкового тракту в усіх пацієнтів із підтвердженим діагнозом ЗДА за відсутності інших очевидних причин анемії (явна не шлунково-кишкова кровотеча).
Vetrano D. L., Zuccheli A., Marconi E. et al. Predictors of iron-deficiency anemia in primary care older adults: a real-world European multi-country longitudinal study. Aging Clinical and Experimental Research, 2020.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 2 (471), січень 2020 р.