3 березня, 2020
Ошибки и опасности диагностики и лечения посттравматических грыж диафрагмы
 Посттравматические диафрагмальные грыжи (ПДГ) являются редким, но потенциально смертельным заболеванием, которое развивается в 0,8‑7% случаев закрытой травмы живота и в 10‑15% наблюдений при колото-резаных ранениях.
Посттравматические диафрагмальные грыжи (ПДГ) являются редким, но потенциально смертельным заболеванием, которое развивается в 0,8‑7% случаев закрытой травмы живота и в 10‑15% наблюдений при колото-резаных ранениях.
Впервые диафрагмальная грыжа была описана в 1541 г. Д. Зеннертом, а в 1579 г. А. Паре описал случай развития ПДГ после огнестрельного ранения, который спустя 8 месяцев закончился летальным исходом в результате некроза кишки, ущемленной в диафрагмальной грыже небольших размеров. Первое описание успешного хирургического вмешательства при ПДГ было опубликовано в 1886 г. Ralfi. В России первое сообщение о травматической диафрагмальной грыже было опубликовано в 1852 г. И. В. Буяльским.
Особенности диагностики и лечения диафрагмальных грыж
Развитие ПДГ приводит к сложностям как диагностики, так и хирургического лечения. Это связано, с одной стороны, с множественным характером повреждений органов брюшной и грудной полостей, которые в большинстве случаев сопровождают ПДГ, а с другой – поздним развитием клинических проявлений ПДГ, которые бывают весьма различными. Существующие публикации свидетельствуют о том, что время между получением травмы и диагностикой ПДГ широко варьирует от нескольких недель до нескольких лет (до 50 лет в одном из исследований).
O. Grimes предложил теорию (1974), которая объясняет задержку клинической манифестации заболевания, что связано либо с отсроченным фактическим физическим разрывом диафрагмы, либо с запоздалой точной диагностикой, когда проявления ПДГ воспринимаются как признаки другого заболевания или повреждения. При этом отсроченный разрыв, вероятно, является результатом постоянного прерывистого естественного движения диафрагмы. Несмотря на первичную мышечно-апоневротическую травму, анатомические границы могут сохраняться в течение некоторого времени. Повторные дыхательные экскурсии диафрагмы приводят к постоянным мышечным растяжениям и повторным микротравмам мышечных волокон с возможным разрывом спустя некоторое время (от нескольких дней до нескольких месяцев). Этот основной механизм отсроченного разрыва может быть еще более усугублен или даже ускорен вследствие любых других опасностей, связанных с барометрическими колебаниями, таких как полет на самолете или подводное плавание.
Еще одним возможным вариантом запоздалого клинического проявления ПДГ может быть временное закрытие дефекта либо за счет сокращения мышечных волокон диафрагмы, либо вследствие интерпозиции большого сальника в дефект диафрагмы.
Также необходимо отметить, что в более чем 50% случаев ПДГ не имеют клинических проявлений, их симптомы появляются только при развитии осложнений.
Протективное действие печени приводит к тому, что левосторонние ПДГ встречаются значительно чаще правосторонних, в соотношении 75:25. При этом правосторонние грыжи в большинстве случаев сопровождаются массивными повреждениями органов брюшной и/или грудной полостей, в то время как левосторонние ПДГ могут быть изолированными. Крайне редко дефекты бывают двусторонними. Наличие градиента торакоабдоминального давления приводит к увеличению размеров грыжевого дефекта с дислокацией органов брюшной полости в грудную клетку. Перемещение органов брюшной полости в грудную клетку может приводить к сдавливанию легких и/или сердца, смещению средостения, что, в свою очередь, вызывает развитие дыхательной и сердечно-сосудистой недостаточности разной степени выраженности. Резкое повышение внутрибрюшного давления может приводить к значительному расширению грыжевого дефекта с дислокацией органов брюшной полости в грудную клетку и последующим их ущемлением, возможным развитием перфорации и некроза, а также кишечной непроходимости.
Таким образом, наблюдаемая при ПДГ симптоматика определяется локализацией и величиной дефекта в диафрагме, быстротой перемещения органов, степенью наполнения желудка и кишечника, наличием спаек между перемещаемыми органами, нарушением кровообращения в них, а также уровнем внутрибрюшного давления.
Рентгенологическое исследование является методом выбора первичной диагностики ПДГ с чувствительностью 30‑62%. К рентгенологическим признакам ПДГ относится элевация купола диафрагмы, искажение или затенение края диафрагмы, тень кишечника или наличие уровня «воздух/жидкость» над диафрагмой, наличие назогастрального зонда в плевральной полости грудной клетки, которые сочетаются с плевральным выпотом, коллапсом легкого и смещением средостения.
Компьютерная томография (КТ), обладая большей чувствительностью, позволяет оценить локализацию и размеры дефекта диафрагмы, точно определить дислоцированные органы брюшной полости в грыже, состояние их стенок и наличие их кровоснабжения. Кроме того, для диагностики ПДГ полезными могут быть ультразвуковое исследование (УЗИ), магнитно-резонансная томография (МРТ), а также рентгенконтрастное исследование верхних и нижних отделов желудочно-кишечного тракта.
Лечение ПДГ предполагает только хирургическое вмешательство. Доступы, которые могут быть для этого использованы, разделяются на трансабдоминальные (лапаротомные и лапароскопические), трансплевральные (торакотомные и торакоскопические), а также комбинированные. Существует также широкий ряд методик пластики дефектов диафрагмы. Ушивание дефектов диафрагмы П-образными или узловыми швами с созданием ее дупликатуры возможно при небольших дефектах, в то время как аллопротезирование предпочтительно при значительных повреждениях.
Однако, несмотря на существующие современные методы диагностики и лечения, летальность при ПДГ варьирует от 0% при развитии изолированной грыжи до 25% при наличии осложнений, связанных в первую очередь с ошибками диагностики данного заболевания. В связи с этим интересными будут клинические наблюдения, приведенные ниже.
Клинический случай № 1
Пациент, мужчина, 50 лет, доставлен в клинику Института бригадой скорой медицинской помощи с диагнозом «Острый коронарный синдром». Из анамнеза: за 1 ч до поступления отметил появление выраженной боли в левой половине грудной клетки, некоторое затруднение дыхания, общую слабость. Был сразу госпитализирован в отделение кардиореанимации для проведения ургентной коронарографии, однако по результатам электрокардиографии данных в пользу острого инфаркта миокарда или ишемии миокарда не выявлено. При осмотре у больного отмечалась гематома в области правого плеча, а также ограничение объема активных движений правой верхней конечности. При более детальном опросе пациент отметил, что за 10 сут до поступления был госпитализирован в один из ургентных хирургических стационаров после дорожно-транспортного происшествия – столкновения с неподвижным объектом на скорости около 70 км/ч.
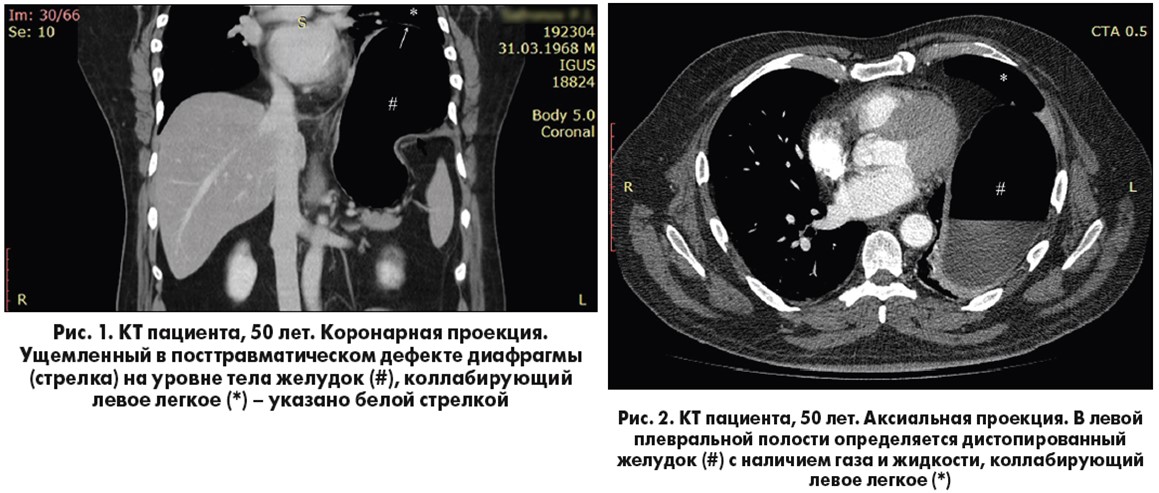
После проведенного обследования больному был установлен диагноз: «Закрытая травма грудной клетки, ушиб грудной клетки. Ушиб мягких тканей правого плеча с формированием его гематомы, травматический плексит». Ввиду отсутствия повреждений внутренних органов, а также удовлетворительного состояния через 2 сут он был выписан из стационара для прохождения амбулаторного лечения. При осмотре была выявлена варикозная болезнь обеих нижних конечностей. С учетом перенесенной травмы, а также для исключения тромбоэмболии легочной артерии пациенту была назначена КТ с болюсным контрастным усилением. Результаты КТ показали наличие ПДГ с транспозицией желудка в плевральную полость и его ущемлением в области тела (рис. 1, 2). Дополнительные лабораторные исследования (клинический анализ крови, мочи, биохимический и коагулологический анализы крови) – без существенных отклонений от нормы.
Больному установлен диагноз «Ущемленная посттравматическая диафрагмальная грыжа с ущемлением желудка на уровне тела», установлены абсолютные показания к ургентному оперативному вмешательству.
После выполнения верхней срединной лапаротомии частично мобилизована левая доля печени путем пересечения треугольной и частично венечной связок печени. При ревизии выявлен дефект левого купола диафрагмы на границе сухожильного центра и реберной ее части до 6 см в диаметре с транспозицией желудка в плевральную полость и его ущемлением на уровне тела. После перевязки и пересечения левой нижней диафрагмальной вены было рассечено ущемляющее кольцо, желудок был перемещен в брюшную полость. После осмотра желудок признан жизнеспособным. Произведена пластика дефекта диафрагмы путем создания дупликатуры. Выполнены установка назогастрального зонда, дренирование левого поддиафрагмального пространства, послойное ушивание раны. Течение послеоперационного периода нормальное. Дренаж удален на 4-е послеоперационные сутки, больной выписан на 10-е послеоперационные сутки. Осмотрен через 6 мес – жалоб не предъявляет. При контрольной рентгенографии органов грудной клетки и брюшной полости, а также при фиброэзофагогастродуоденоскопии патологии не выявлено.
Клинический случай № 2
Пациент, мужчина, 30 лет, доставлен в центральную районную больницу (ЦРБ) по месту жительства ургентно бригадой скорой медицинской помощи 30.11.19 г. с жалобами на боль и вздутие живота, тошноту, повторную рвоту, задержку отхождения стула и газов. Из анамнеза: за несколько месяцев до поступления больной перенес закрытую травму груди и живота в результате удара рогами быка на ферме. При обследовании повреждений внутренних органов груди и живота не выявлено. В результате комплексного клинико-рентгенологического обследования был установлен диагноз «Острая тонкокишечная непроходимость» с показаниями для ургентного хирургического вмешательства. В ходе лапаротомии было выявлено расширение петель тонкой кишки с наличием уровней «газ – жидкость», а также признаки диффузного серозного перитонита. При ревизии органов брюшной полости выявить явную причину кишечной непроходимости не удалось. Операция была завершена назоинтестинальной интубацией, санацией и дренированием брюшной полости.
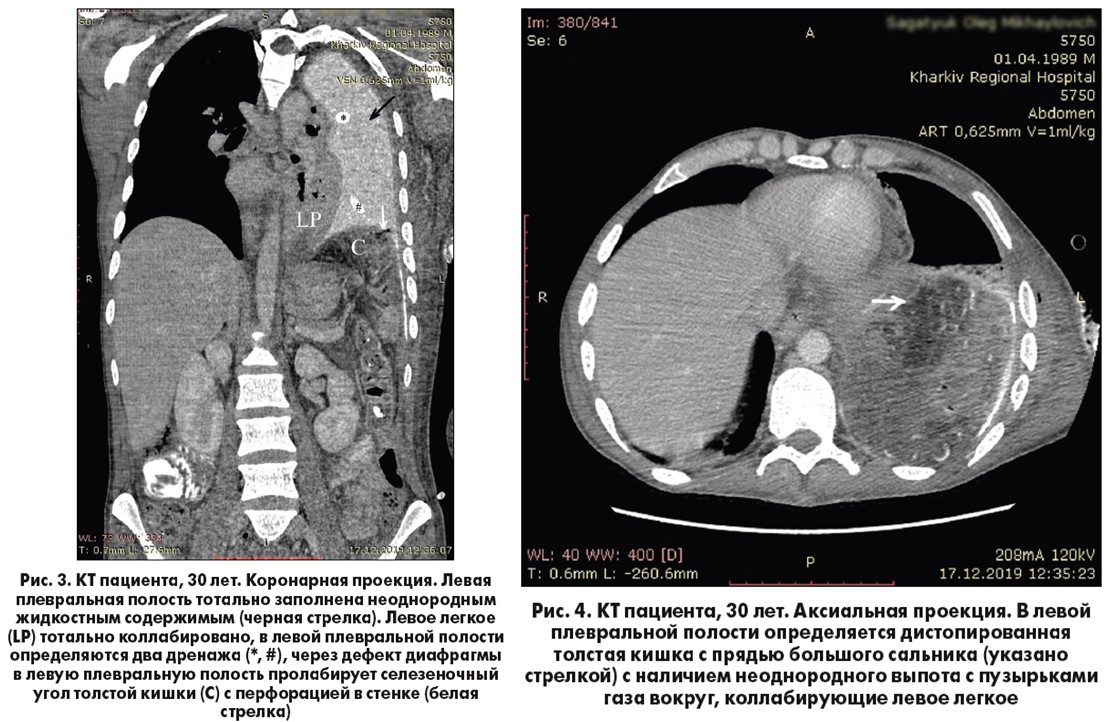
Течение послеоперационного периода было тяжелым, отмечались выраженные явления эндогенной интоксикации, слабая тенденция к восстановлению кишечной перистальтики. 5.12.19 г. состояние пациента ухудшилось: больной жаловался на затруднение дыхания, лабораторно отмечено нарастание лейкоцитоза и нейтрофильного сдвига. Выполнена рентгенография органов грудной клетки, выявленные изменения расценены как левосторонняя пневмония с наличием небольшого количества выпота в левой плевральной полости. Несмотря на проводимое лечение состояние больного продолжало ухудшаться. С 8.12.19 г. вновь отмечено вздутие живота, нарушение отхождения стула и газов, в связи с чем выполнялись очистительные клизмы с незначительным клиническим эффектом. 10.12.19 г. больной отметил резкое усиление боли в левой половине грудной клетки, появление отека и пастозности мягких тканей в области задне-боковой поверхности грудной клетки слева. Лабораторно отмечался лейкоцитоз до уровня 18×109/л, значительный нейтрофильный сдвиг с появлением в периферической крови миелоцитов и метамиелоцитов. При рентгенографии органов грудной клетки – тотальное затемнение левого гемоторакса. При УЗИ плевральных полостей – наличие неоднородного выпота в левой плевральной полости в объеме не менее 2 л. Больному было выполнено дренирование левой плевральной полости по Бюлау в VII межреберье по задней подмышечной линии слева – эвакуировано 2,5 л густого зловонного гноя белого цвета. Отмечена некоторая положительная динамика в виде снижения выраженности проявлений эндогенной интоксикации, а также уменьшение вздутия живота. При контрольной рентгенографии органов грудной клетки от 11.12.19 г. выявлены признаки субтотального пневмоторакса слева, в связи с чем было выполнено дополнительное дренирование левой плевральной полости во II межреберье по среднеключичной линии слева. Состояние больного оставалось стабильным, однако тяжелым. При рентгенографическом контроле расправления легкого не отмечалось, несмотря на активный сброс гноя и воздуха по дренажам плевральной полости. 13.12.19 г. отмечено поступление кишечного отделяемого по дренажу из плевральной полости. Пациенту предложен перевод в областную клиническую больницу (ОКБ), от которого он отказался. В связи с ухудшением состояния, обусловленным нарастанием явлений эндогенной интоксикации, что связано с прогрессированием гнойного процесса в плевральной полости, 16.12.19 г. больной был переведен в ОКБ. По результатам КТ с болюсным контрастным усилением определилась грыжа левого купола диафрагмы с пролабированием селезеночного изгиба толстой кишки с частью брыжейки и большого сальника (грыжевые ворота – 26,5 × 21,5 мм). Стенки дистопированной петли кишки утолщены, с признаками подслизистого отека (что не исключает перфорацию на этом уровне) (рис. 3, 4).
Для дальнейшего лечения больной переведен в клинику Института 18.12.19 г. При поступлении состояние тяжелое. В сознании. Кожа землистого цвета. Грудная клетка правильной формы, асимметрично участвует в акте дыхания за счет отставания левой половины. Слева во II межреберье – дренаж с активным сбросом воздуха, в VII межреберье – дренаж с выделением гноя с толстокишечным отделяемым. Аускультативно справа – жесткое дыхание, рассеянные влажные разнокалиберные хрипы. Слева дыхание не выслушивается. Тоны сердца приглушены, ритмичные. Пульс – 94 уд./мин, АД – 90/60 мм рт. ст. Язык подсушен, обложен белым налетом. Живот правильной формы, участвует в акте дыхания, не вздут. Пальпаторно мягкий, незначительно болезнен в левом подреберье, без перитонеальных знаков. Газы периодически отходят естественным путем, стула не было несколько суток. Диурез через уретральный катетер снижен до 700 мл/сут. Лабораторно: умеренная анемия, незначительный лейкоцитоз до 9,5×109/л с умеренным нейтрофильным сдвигом за счет палочкоядерных нейтрофилов (12%), признаки гипо-, диспротеинемии. Начата предоперационная подготовка, направленная на коррекцию нарушений гомеостаза. 20.12.19 г. больному было предложено оперативное лечение, от которого он категорически отказался и настаивал на переводе в ЦРБ по месту жительства, что и было произведено.
На фоне проводимой терапии состояние больного было без существенной динамики, отмечалась эвакуация по плевральному дренажу до 1,5 гноя с примесью толстокишечного отделяемого, в связи с чем проводились ежедневные фракционные санации левой плевральной полости. Рентгенологически отмечался тотальный коллапс левого легкого. 24.12.19 г. больному в очередной раз было предложено оперативное лечение, на которое он дал согласие. 25.12.19 г. приглашены консультанты из клиники Института.
Больному в условиях ЦРБ было выполнено:
- лапаротомия, ревизия органов брюшной полости;
- торакотомия слева, низведение толстой кишки в брюшную полость, декортикация левого легкого, санация и редренирование левой плевральной полости;
- резекция селезеночного угла толстой кишки, трансверзостомия;
- дренирование брюшной полости.
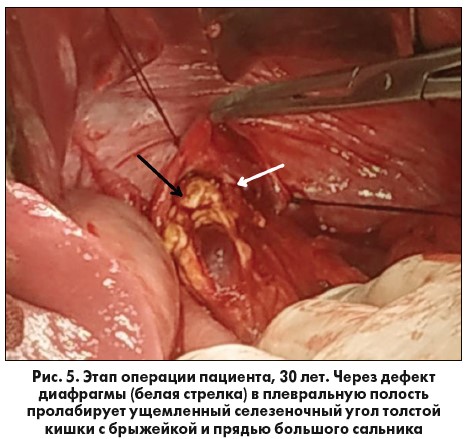 Из протокола операции. Верхнесрединная лапаротомия. В брюшной полости – умеренно выраженный спаечный процесс, произведено рассечение сращений. Также определяется до 0,5 л выпота соломенного цвета без запаха. При ревизии: петли тонкой и толстая кишка не расширены, перистальтируют. В левом поддиафрагмальном пространстве определяется инфильтрат, состоящий из пряди большого сальника, поперечной и нисходящей ободочной кишки с брыжейкой, которые через дефект в левом куполе диафрагмы пролабируют в левую плевральную полость (рис. 5).
Из протокола операции. Верхнесрединная лапаротомия. В брюшной полости – умеренно выраженный спаечный процесс, произведено рассечение сращений. Также определяется до 0,5 л выпота соломенного цвета без запаха. При ревизии: петли тонкой и толстая кишка не расширены, перистальтируют. В левом поддиафрагмальном пространстве определяется инфильтрат, состоящий из пряди большого сальника, поперечной и нисходящей ободочной кишки с брыжейкой, которые через дефект в левом куполе диафрагмы пролабируют в левую плевральную полость (рис. 5).
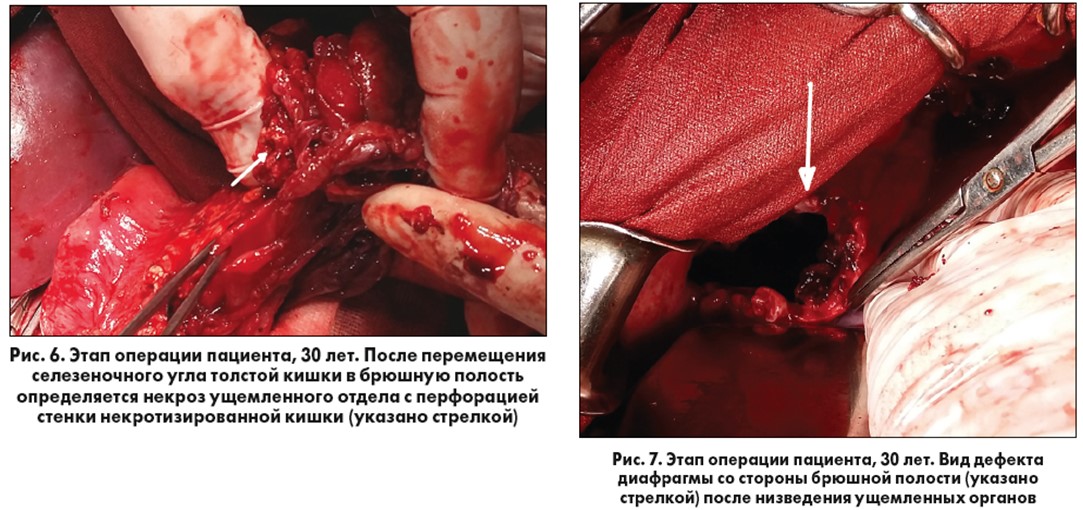
Частично мобилизована левая доля печени путем пересечения ее треугольной и частично венечной связок. Перевязана и пересечена левая нижняя диафрагмальная вена. Выполнена диафрагмотомия. Попытка низвести дистопированную кишку в брюшную полость не представлялась возможной из-за наличия плотных спаек, фиксирующих кишку в плевральной полости и к перикарду. Выполнена передне-боковая торакотомия в VII межреберье слева. Из левой плевральной полости эвакуировано до 1,5 л зловонного гноя серого цвета с толстокишечным отделяемым. Плевральная полость представляет собой полость эмпиемного мешка, к стенкам которого, а также к перикарду плотными сращениями фиксирована дистопированная толстая кишка с участками некроза и перфорацией в зоне ущемления в грыжевом дефекте диафрагмы, из которой поступает толстокишечное отделяемое. Эктопированная петля тонкой кишки мобилизована и перемещена в брюшную полость (рис. 6, 7). Выполнена декортикация левого легкого, санация и редренирование левой плевральной полости по Бюлау (во II межреберье по среднеключичной линии и в VII межреберье по задней подмышечной линии). Торакотомная рана ушита.
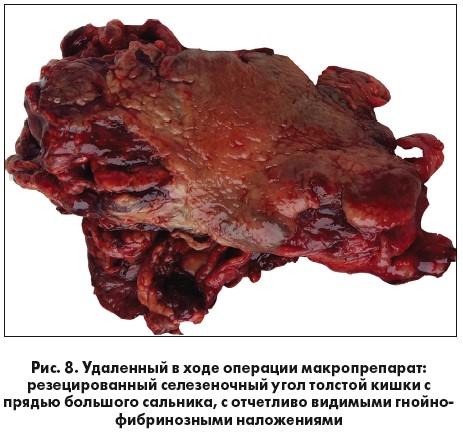
Со стороны брюшной полости произведена резекция селезеночного угла толстой кишки с прядью большого сальника (рис. 8). Дефект диафрагмы ушит с созданием дупликатуры. Сформирована трансверзостома, культя нисходящей ободочной кишки ушита наглухо. Брюшная полость дренирована по Петрову. Лапаротомная рана ушита.
 Диагноз после операции: «Посттравматическая грыжа диафрагмы с ущемлением и некрозом селезеночного угла толстой кишки, формированием толстокишечно-плевро-кожного свища. Тотальная эмпиема плевры справа. Синдром эндогенной интоксикации».
Диагноз после операции: «Посттравматическая грыжа диафрагмы с ущемлением и некрозом селезеночного угла толстой кишки, формированием толстокишечно-плевро-кожного свища. Тотальная эмпиема плевры справа. Синдром эндогенной интоксикации».
Течение послеоперационного периода крайне тяжелое. Отмечалось нагноение торакотомной раны, длительное истечение гноя по дренажу из плевральной полости, а также вялое расправление левого легкого. На фоне местной и общей терапии – состояние с положительной динамикой, легкое расправилось, отмечаются значительные фиброзные изменения в проекции нижней доли левого легкого. Торакотомная рана очистилась, заживает вторичным натяжением. Трансверзостома функционирует с 4-х послеоперационных суток, дренажи из брюшной полости удалены на 5-е послеоперационные сутки, из плевральной полости – на 18-е послеоперационные сутки. Больной выписан для амбулаторного лечения на 19-е послеоперационные сутки.
Обсуждение
Приведенные клинические наблюдения демонстрируют сложность диагностики ПДГ, клиническая манифестация которых может возникать через несколько суток и даже месяцев после перенесенной травмы, что в ряде случаев не позволяет связать развитие «катастрофы» в животе с перенесенной травмой, особенно при отсутствии данных о наличии ПДГ. Клиническая симптоматика при ущемлении ПДГ может имитировать различные заболевания, что может привести не только к неправильной диагностике и интерпретации полученных данных, но и к ошибочной лечебной тактике, включая выполнение нецелесообразных хирургических вмешательств либо операций не в полном объеме. При этом существует вероятность того, что проведение общей анестезии с введением миорелаксантов может привести в результате релаксации диафрагмы к самопроизвольному обратному перемещению ущемленных органов и занятию ими естественной анатомической позиции. При этом недостаточная или затрудненная ревизия не позволит выявить дефект диафрагмы, что может привести к повторному ущемлению (это, по всей вероятности, имело место в клиническом случае № 2 в ходе первой операции). Дальнейшее негативное развитие событий связано с рядом допущенных диагностических ошибок, что связано с отсутствием достаточного материально-технического оснащения учреждения 2-го уровня оказания медицинской помощи (в частности, КТ), а также с отказом пациента от повторных оперативных вмешательств в учреждениях 3-го и 4-го уровней, что привело к истощению больного вследствие гнойной интоксикации. В то же время в клиническом случае № 1 первичное поступление пациента в учреждение 4-го уровня оказания медицинской помощи позволило выявить ущемленную ПДГ уже в первые часы после развития осложнения, что в результате позволило достичь хорошего клинического эффекта и избежать фатальных осложнений.
Выводы
Диагностика ПДГ является непростым заданием для хирурга, требующим не только его осведомленности о возможности развития данной патологии через несколько дней, месяцев и даже лет после перенесенной травмы (закрытой либо колото-резаной) груди и живота, но и соответствующей материально-технической базы. Рентгенологическое исследование груди и живота позволяет с высокой степенью вероятности выявить ПДГ. При исключении других заболеваний, с учетом наличия в анамнезе травмы и при отрицательных результатах рентгенологического исследования следующим этапом диагностики должна быть КТ. При отсутствии компьютерного томографа и принятии решения о необходимости оперативного лечения тщательная ревизия с осмотром диафрагмы у пациентов с травматическим анамнезом позволяет выявить ПДГ и своевременно ликвидировать осложнения, в первую очередь связанные с ущемлением эктопированных органов брюшной полости.
Литература
- Войцеховский В. В., Аникин С. В., Гоборов Н. Д., Яновой В. В., Брегадзе Ю. Е., Глущенко В. В., Хаткеев В. И. Случай диагностики посттравматической грыжи диафрагмы, протекавшей под маской плеврита. Бюллетень физиологии и патологии дыхания. 2017; 65: 104‑110. DOI: 10.12737/article_59adf2402e8e24.08404333.
- Magagi I. A., Habou O., Adamou H., Adakal O., Ada M. O.A., Moustapha H., Abarchi H. Isolated Right-Sided Posttraumatic Diaphragmatic Hernia. Case Reports in Surgery. 2018, Article ID8758021, 3 pages. https://doi.org/10.1155/2018/8758021.
- El-Yakub A., Bello U. M., Sheshe A. A., Naaya H. U. Delayed Presentation of Posttraumatic Diaphragmatic Hernia Masquerading as Recurrent Acute Asthmatic Attack. Case Reports in Medicine. 2017, Article ID5037619, 3 pages. https://doi.org/10.1155/2017/5037619.
- Bhatti U. H., Dawani S. Large bowel obstruction complicating a posttraumatic diaphragmatic hernia. Singapore Med J. 2015; 56(4): e56-e58. doi: 10.11622/smedj.2015061.
- Bhatt N. R., McMonagle M. Recurrence in a Laparoscopically Repaired Traumatic Diaphragmatic Hernia: Case Report and Literature. Review Trauma Mon. 2016 Feb; 21(1): e20421‑25. doi: 10.5812/traumamon.20421.
- Toliczenko-Bernatowicz D., Dębek W., Matuszczak E. Colon volvulus displaced into the chest – right-sided posttraumatic hernia or congenital malformation? Kardiochirurgia i Torakochirurgia Polska. 2016; 13 (2): 159‑161. DOI: 10.5114/kitp.2016.61055.