3 березня, 2020
Актуальні проблеми періопераційного періоду: менеджмент больового синдрому та оптимальна тромбопрофілактика
Адекватний менеджмент періопераційного періоду, зокрема успішний контроль больового синдрому та оптимальна стратегія тромбопрофілактики, сприяє швидкій активізації хворого після оперативного втручання, скороченню терміну його перебування у стаціонарі й покращенню якості життя. Сучасні стратегії аналгезуючої терапії, запобігання розвитку опіоїд-асоційованих побічних ефектів, принципи та терміни оптимальної тромбопрофілактики – цим питанням були присвячені доповіді провідних вітчизняних спеціалістів у рамках Конгресу анестезіологів України, який відбувся 19-21 вересня у Києві.
 Доповідь на тему «Особливості анестезії та періопераційної інтенсивної терапії при операціях в онкогепатології» представив увазі аудиторії головний науковий співробітник ДНУ «НПЦ ПКМ» ДУС (м. Київ), доктор медичних наук, професор Володимир Ілліч Черній.
Доповідь на тему «Особливості анестезії та періопераційної інтенсивної терапії при операціях в онкогепатології» представив увазі аудиторії головний науковий співробітник ДНУ «НПЦ ПКМ» ДУС (м. Київ), доктор медичних наук, професор Володимир Ілліч Черній.
На початку виступу він визначив можливі шляхи прогнозування та мінімізації ризику ускладнень в післяопераційному періоді:
- огляд та підготовка пацієнта у передопераційному періоді;
- визначення показника Revised Cardiac Risk Index – ризику розвитку кардіологічних ускладнень у періопераційному періоді;
- персоніфікований вибір методу анестезії та післяопераційної аналгезії;
- імплементація контрольного списку «Безпека пацієнта в операційній» – простого методу перевірки готовності всіх членів операційної бригади перед втручанням з уточненням усіх даних щодо пацієнта перед проведенням знеболення.
Професор В.І. Черній звернув увагу колег на специфічні особливості хірургічної гепатології. Він зазначив, що проведення двохпідреберного доступу є дуже високотравматичною методикою, тоді як резекція печінки завжди супроводжується вираженою крововтратою. Мобілізація, тракції та компресії печінки, широка лімфодесекція портальних структур супроводжуються потужною аферентною патологічною больовою імпульсацією, активацією симпато-адреналової системи з наступною централізацією кровообігу та гіпоперфузією органів спланхнічної зони. В той же час накладення турнікету на гепатодуоденальну зв’язку дозволяє зменшити інтраопераційну кровотечу, проте спричиняє ішемію гепатоцитів із наступною реперфузією та надходженням у системний кровотік продуктів анаеробного метаболізму.
Доповідач рекомендував наступний план передопераційної підготовки пацієнтів:
- селективна деконтамінація кишечника протягом 3 днів із застосуванням норфлоксацину – 1,5 г/добу, ністатину – 2 г/добу та лактулози;
- прийом антисекреторних препаратів: омепразолу – 40 мг/добу, фамотидину – 20 мг/добу;
- проведення тромбопрофілактики із застосуванням низькомолекулярного гепарину (НМГ): еноксапарин, Цибор® («Берлін-Хемі») – 2500 МО;
- еластична компресія нижніх кінцівок напередодні оперативного втручання.
Професор В.І. Черній зазначив, що ризик розвитку тромботичних ускладнень при проведенні операційних втручань із приводу злоякісних новоутворень печінки є дуже високим, і представив результати дослідження щодо проведення тромбопрофілактики із застосуванням препарату НМГ другого покоління – Цибор®. Згідно з результатами дослідження, застосування препарату Цибор® у якості тромбопрофілактики при проведенні резекції печінки дозволяє підтримувати достатній для профілактики тромбоутворень рівень активності анти-Ха плазми крові. На основі дослідження був розроблений режим тробопрофілактики, представлений у табл. 1.
Таким чином, перше введення антикоагулянту має бути проведене за 12 год напередодні оперативного втручання. Подальше введення антикоагулянтів залежить від ризику розвитку тромботичних ускладнень і проводиться до досягнення повної активізації пацієнта.
Доповідач наголосив, що важливим аспектом лікування даної категорії хворих є забезпечення оптимального менеджменту післяопераційного больового синдрому. Зокрема, застосування режиму мультимодальної аналгезії (ММА) дозволяє впливати на процеси передачі ноцицептивних сигналів. Одним із ключових компонентів ММА є застосування нестероїдних протизапальних препаратів (НПЗП), які сприяють пригніченню активності циклооксигенази‑2 (ЦОГ‑2), що призводить до зниження синтезу простагландинів. Декскетопрофен (Дексалгін®, «Берлін-Хемі») – представник НПЗП, який є правообертаючим ізомером кетопрофену. Ефективність препарату Дексалгін® удвічі перевищує ефективність рацемічного кетопрофену, тоді як ульцерогенний потенціал у нього є значно нижчим. Високий рівень ліпофільності Дексалгіну забезпечує проходження препарату через гематоенцефалічний бар’єр та селективне блокування NMDA[N-метил-D-аспартат]-рецепторів, які беруть безпосередню участь у модуляції больового сигналу. Було зазначено, що впровадження режиму ММА дозволяє мінімізувати застосування опіоїдних препаратів і пов’язаних із ними побічних ефектів: пригнічення дихання та гемодинаміки, надлишкової седації, нудоти та блювання, пригнічення перистальтики, затримки сечі.
У наступній доповіді професор В.І. Черній висвітлив тему «Сучасні тенденції мультимодальної аналгезії в програмах Fast Track-surgery і ERAS». Передусім доповідач підкреслив, що адекватна терапія больового синдрому має виключно важливе значення у менеджменті післяопераційного періоду. Більшість причин післяопераційної летальності в сучасній хірургії мають прямий зв’язок із неадекватним менеджментом больового синдрому. Неконтрольований больовий синдром подовжує перебування пацієнта в стаціонарі й суттєво збільшує витрати на лікування. Неналежний контроль больового синдрому в післяопераційному періоді свідчить про низьку якість медичних послуг, які надаються в даному медичному закладі. Автор доповіді представив увазі аудиторії положення керівництва щодо менеджменту післяопераційного больового синдрому («Guidelines on the Management of Postoperative Pain»), згідно з яким оптимальне післяопераційне знеболення забезпечується за ініціації аналгезуючої терапії ще в передопераційному періоді. Експерти рекомендують застосовувати мультимодальні схеми лікування, проте компоненти терапії мають обиратися залежно від особливостей пацієнта та різновиду оперативного втручання. Професор В.І. Черній зазначив, що застосування опіоїдів є «наріжним каменем» менеджменту післяопераційного періоду впродовж багатьох років. Механізм впливу опіоїдів на ноцицепцію є парадоксальним: аналгезія, що розвивається й домінує на початковому етапі, у подальшому змінюється розвитком гіпералгезії. Таким чином, опіоїд-індукована гіпералгезія – це стан ноцицептивної сенситизації, який розвивається внаслідок застосування опіоїдів. Надмірне застосування опіоїдів протягом останніх десятиліть сприяло поширенню «епідемій» опіоїдної залежності у США.
Сучасні стратегії запобігання розвитку опіоїд-індукованої гіпералгезії передбачають наступне:
- проведення раціональної опіатної терапії;
- застосування антагоністів NMDA-рецепторів;
- застосування габапентиноїдів;
- застосування альфа‑2-агоністів (клонідину, дексмедетомідину);
- застосування регіонарних технік знеболення;
- застосування НПЗП.
Сучасні принципи ERAS (Enhanced Recovery after Surgery – «Покращене одужання після операції») включають у себе застосування стандартизованої ММА з неопіоїдними агентами, дозволяють мінімізувати застосування опіоїдів у післяопераційному періоді й пов’язані з ними негативні наслідки. Типовий мультимодальний режим аналгезії у післяопераційному періоді передбачає застосування ацетамінофену, НПЗП та габапентиноїдів. Завданням ММА є досягнення адекватного знеболення завдяки синергічній взаємодії різних аналгезуючих препаратів. Синергічна взаємодія анальгетиків дозволяє призначати їх у мінімальних дозах і тим самим сприяє зниженню ризику розвитку побічних ефектів. Типовий режим ММА передбачає ініціацію її проведення у передопераційному періоді й включає застосування комбінації парацетамолу та НПЗП/інгібітора ЦОГ‑2. Це є найбільш оптимальним варіантом режиму ММА, який має проводитися на регулярній основі, а не за вимогою.
Разом із тим доповідач зазначив, що слід пам’ятати про побічні ефекти НПЗП:
- гастроінтестинальні:
- пептичні виразки, гастроінтестинальні геморагії;
- розвиток езофагіту, стриктур;
- ерозивні ураження тонкого й товстого кишечника;
- гематологічні:
- пригнічення агрегації тромбоцитів;
- підвищення ризику розвитку кровотеч;
- кардіоренальні:
- зворотна гостра ниркова недостатність;
- порушення обміну рідини та електролітів, набряки;
- хронічна ниркова недостатність, інтерстиціальний фіброз;
- інтерстиціальний нефрит;
- нефротичний синдром;
- погіршення перебігу застійної серцевої недостатності, гіпертензія.
Відомо, що ЦОГ‑1 відіграє важливу роль у захисті слизової оболонки шлунка від дії пошкоджуючих факторів (зокрема, соляної кислоти). Неселективні НПЗП, які інгібують не лише ЦОГ‑2, а й ЦОГ‑1, можуть призводити до підвищення ризику розвитку уражень слизової оболонки шлунково-кишкового тракту. Тому первинна профілактика гастроінтестинальної токсичності НПЗП передбачає застосування останніх із найменшою гастротоксичністю. Прикладом такого НПЗП є Дексалгін® («Берлін-Хемі») – препарат, який володіє потужним антиноцицептивним потенціалом та є (S+)-ізомером кетопрофену. У свою чергу, кетопрофен також відомий вираженим антиноцицептивним потенціалом і складається з двох стереоізомерів: правообертаючого (S+) та лівообертаючого (S–) ізомерів. Встановлено, що правообертаючий ізомер кетопрофену відповідає за розвиток антиноцицептивного ефекту, тоді як лівообертаючий не має виражених аналгезуючих властивостей, проте асоціюється з високим ризиком розвитку побічних ефектів. Виділення правообертаючого ізомеру (декскетопрофену) та виключення з препарату «непотрібного» лівообертаючого ізомеру дозволило зберегти виражені антиноцицептивні властивості з одночасною мінімізацією ризику розвитку побічних ефектів препарату.
Професор В.І. Черній представив результати дослідження F. Miralles et al. (2001), згідно з якими декскетопрофен не збільшує ризик розвитку кровотеч під час операції та у ранньому післяопераційному періоді після проведення ортопедичних і великих абдомінальних втручань. Таким чином, декскетопрофен – діюча речовина препарату Дексалгін®, представляє собою правообертаючий ізомер кетопрофену, який характеризується вираженою аналгезуючою дією та хорошим профілем безпеки. Дексалгін® має два механізми впливу на ноцицептивну систему: центральний (блокування утворення простагландинів у ЦНС) та периферичний (блокування утворення простагландинів у місці ураження). Застосування Дексалгіну сприяє швидкому гальмуванню утворення больового імпульсу, запобігає формуванню «больової пам’яті» та процесу хронізації больового синдрому.
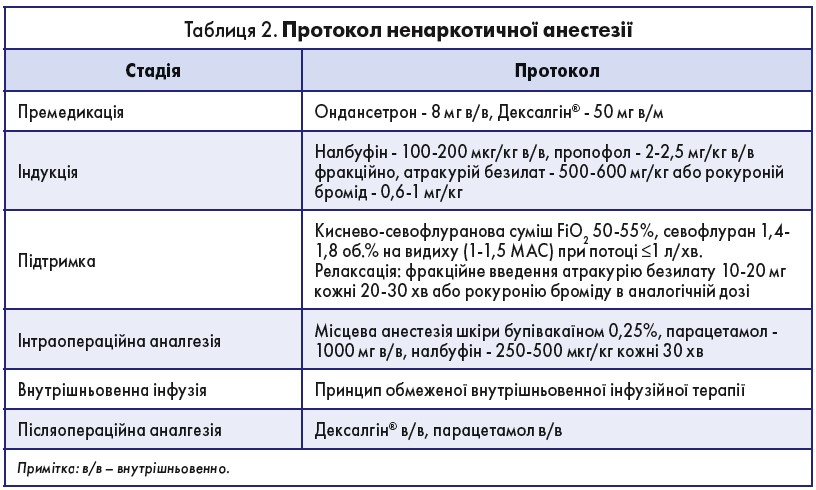
Наприкінці виступу доповідач зазначив, що НПЗП є ключовим компонентом ММА, який сприяє мінімізації застосування опіоїдів і запобігає розвитку пов’язаних із ними побічних явищ, а також представив увазі аудиторії протокол ненаркотичної анестезії (табл. 2).
 Темі «Мультимодальна аналгезія: данина традиції чи сучасний підхід до адекватного знеболення та попередження когнітивної післяопераційної дисфункції?» присвятив свою доповідь доцент кафедри хірургії, анестезіології та інтенсивної терапії Інституту післядипломної освіти Національного медичного університету ім. О.О. Богомольця (м. Київ), доктор медичних наук Іван Іванович Лісний.
Темі «Мультимодальна аналгезія: данина традиції чи сучасний підхід до адекватного знеболення та попередження когнітивної післяопераційної дисфункції?» присвятив свою доповідь доцент кафедри хірургії, анестезіології та інтенсивної терапії Інституту післядипломної освіти Національного медичного університету ім. О.О. Богомольця (м. Київ), доктор медичних наук Іван Іванович Лісний.
На початку виступу він навів наступне визначення ММА: це застосування різних анальгетичних препаратів та технік (у тому числі нефармакологічних) із відмінними механізмами впливу на периферичну й/або центральну нервову систему, які в сукупності проявляють синергічну або адитивну дію та сприяють розвитку більш якісного знеболення порівняно із застосуванням цих препаратів окремо. Режим ММА може включати застосування великої кількості препаратів, зокрема опіоїдних анальгетиків, НПЗП, парацетамолу, метамізолу, місцевих анестетиків тощо. Разом із тим, зазначив доповідач, згідно із програмою ERAS, три наступних її пункти незалежно асоціюються зі зниженням тривалості лікування, зокрема:
- мультимодальна профілактика післяопераційної нудоти та блювання;
- періопераційне застосування НПЗП;
- післяопераційне застосування опіоїдів згідно із протоколом.
Режим ММА має бути індивідуалізованим, оскільки різні препарати можуть бути неоднаково ефективними у різних пацієнтів. Протокол ММА може змінюватися відповідно до потреб хворого. При цьому застосування ММА у передопераційному періоді сприяє зменшенню потреби в застосуванні опіоїдів після проведення операції. Ключовим компонентом ММА, який дозволяє зменшити застосування опіоїдів, є НПЗП. Доповідач зазначив, що застосування НПЗП у комбінації з парацетамолом дозволяє досягнути кращого ефекту знеболення, ніж при застосуванні цих препаратів окремо.
І.І. Лісний зауважив, що одним із побічних ефектів НПЗП, який обмежує їх застосування у передопераційному періоді, є підвищення ризику розвитку кровотеч в інтра- та післяопераційному періодах. Він представив увазі аудиторії результати досліджень, згідно з якими застосування декскетопрофену (Дексалгін®) не сприяє збільшенню крововтрати під час операції та у ранньому післяопераційному періоді при проведенні ортопедичних і великих абдомінальних втручань. Крім того, застосування декскетопрофену одночасно із супутнім прийомом НМГ не збільшує ризик розвитку кровотеч. Таким чином, щодо ризику розвитку шлунково-кишкових кровотеч Дексалгін® є одним із найбільш безпечних представників НПЗП.
Доповідач представив увазі аудиторії результати власного дослідження, в якому порівнювалась ефективність застосування Дексалгіну та омнопону при періопераційному знеболенні в онкохірургічній практиці. Згідно з результатами дослідження, швидкість відновлення імунітету (зокрема, кількості CD16+-лімфоцитів, цитотоксичної активності НК[натуральних кілерів]-клітин) була вищою у пацієнтів, які приймали Дексалгін®. Також І.І. Лісний навів результати іншого дослідження, в якому порівнювалася ефективність двох варіантів аналгезії із застосуванням НПЗП при виконанні передньої резекції прямої кишки. Один варіант передбачав застосування Дексалгіну та парацетамолу за 30 хв до проведення оперативного втручання (1-ша група дослідження), тоді як інший – їх застосування перед зашиванням операційної рани (2-га група). Згідно з результатами дослідження, у 1-й групі відзначали зменшення потреби в застосуванні опіоїдного анальгетика фентанілу, більш стабільний рівень глікемії та кортизолу у плазмі. Таким чином, застосування препарату Дексалгін® напередодні операційного втручання в якості превентивної аналгезії має значні переваги.
Наприкінці виступу І.І. Лісний підкреслив, що всі стратегії та методи післяопераційного знеболення мають бути спрямовані на досягнення адекватної аналгезії та попередження побічних ефектів неадекватного менеджменту гострого післяопераційного болю (зокрема, порушення дихання, гемодинаміки, когнітивних функцій, імуносупресії). Він зазначив, що застосування регіонарних технік знеболення, ММА, а також обмеження прийому опіоїдів (у тому числі за рахунок застосування анальгетиків без опіоїдного ефекту) дозволяють досягнути адекватної аналгезії без порушення когнітивних функцій.
 Наступну доповідь на тему «Фармакологічна тромбопрофілактика: переваги та ризики» представив доктор медичних наук, професор Юрій Леонідович Кучин.
Наступну доповідь на тему «Фармакологічна тромбопрофілактика: переваги та ризики» представив доктор медичних наук, професор Юрій Леонідович Кучин.
На початку виступу він зосередив увагу на аспектах проведення тромбопрофілактики у сфері пластичної хірургії та згадав про ризики розвитку тромботичних ускладнень при проведенні пластичних і реконструктивних хірургічних втручань. Неадекватна тромбопрофілактика з метою мінімізації ризиків розвитку косметичних дефектів, наприклад геморагій та синців, може призвести до розвитку тяжких тромботичних ускладнень, зокрема ТЕЛА (тромбоемболії легеневої артерії). Для стратифікації ризику тромботичних ускладнень необхідно застосовувати шкалу Caprini. Крім того, згідно з рекомендаціями «Practical guidelines for venous thromboembolism chemoprophylaxis in elective plastic surgery» (Практичні рекомендації щодо проведення профілактики тромбоемболічних ускладнень в елективній пластичній хірургії) існує спеціальна шкала для визначення ризику тромботичних ускладнень при проведенні пластичних операцій. Ця шкала аналогічна шкалі Caprini, але й також враховує вид оперативного втручання. Професор Ю.Л. Кучин зазначив, що за наявності показань має застосовуватися фармакологічна профілактика. Застосування НМГ є важливим аспектом тромбопрофілактики при проведенні оперативних втручань, у тому числі й у сфері естетичної медицини.
Далі у ході виступу доповідач представив результати дослідження щодо безпечності одночасного застосування НПЗП та НМГ. Згідно з результатами дослідження, не було виявлено інтеракцій між НМГ (Цибор®) та НПЗП (Дексалгін®), які б мали значний вплив на показники коагуляції. Разом із тим одночасне застосування НМГ та НПЗП може підвищувати ризик розвитку малих кровотеч, проте це не стосується великих та клінічно значущих кровотеч у післяопераційному періоді. Було зазначено, що за необхідності застосування НПЗП препаратом вибору має бути НПЗП із найменшою гастротоксичністю, наприклад Дексалгін®.
 Велику зацікавленість аудиторії викликала доповідь «Сучасні технології підвищення рівня безпеки періопераційного періоду в акушерстві та гінекології», з якою виступив доктор медичних наук, професор Олексій Миколайович Нестеренко.
Велику зацікавленість аудиторії викликала доповідь «Сучасні технології підвищення рівня безпеки періопераційного періоду в акушерстві та гінекології», з якою виступив доктор медичних наук, професор Олексій Миколайович Нестеренко.
Насамперед він підкреслив значення імплементації контрольного списку «Безпека пацієнта в операційній», спрямованого на зниження потенційних ризиків, пов’язаних із проведенням операційного втручання. «Безпека пацієнта в операційній» – це перелік основних позицій та положень щодо оперативного втручання, який оголошується в присутності пацієнта та всієї операційної бригади до початку знеболення хворого. Метою контрольного списку є перевірка готовності пацієнта та медиків до проведення оперативного втручання з метою мінімізації можливих потенційних ризиків. Імплементація контрольного списку в поєднанні з передопераційним оглядом та передопераційною підготовкою пацієнта, а також персоніфікованим вибором методу анестезії сприяє прогнозуванню й запобіганню можливим ускладненням у післяопераційному періоді. Таким чином, контрольний список є інструментом, який дозволяє стандартизувати догляд за пацієнтом, покращити професійну комунікацію та оптимізувати роботу команди медичних працівників.
Далі доповідач зосередив увагу аудиторії на принципах проведення періопераційної тромбопрофілактики. Зокрема, механічна та фізична тромбопрофілактика включає наступні аспекти:
- рання іммобілізація;
- фізичні вправи;
- дихальна гімнастика;
- застосування компресійного трикотажу з дозованою компресією;
- переміжна пневматична компресія.
Професор О.М. Нестеренко зауважив, що вибір методу анестезії (регіонарної або загальної) також відіграє важливу роль у профілактиці тромбозу глибоких вен та тромбоемболічних ускладнень. При цьому застосування ендотрахеального наркозу асоціюється з розвитком тробмозу глибоких вен та тромбоемболічних ускладнень у близько 11% випадків, тоді як епідуральної анестезії – у 4% випадків. З метою мінімізації ризику розвитку тромботичних ускладнень застосовуються специфічні та неспецифічні методики прискорення венозного кровотоку:
- неспецифічні методики – адекватна гідратація, підтримка нормоволемічної гемодилюції, лікування дихальної та циркуляторної недостатності;
- специфічні методики – застосування нефракціонованого та фракціонованого гепаринів, НМГ, інгібіторів фактору Ха (фондапаринуксу, ривароксабану, апіксабану).
Доповідач зазначив, що препарат Цибор® – єдиний представник другого покоління НМГ із найнижчою молекулярною масою. Беміпарин, діюча речовина Цибору, швидко всмоктується після підшкірного введення та характеризується 96% біодоступністю. Суттєвою перевагою препарату Цибор® є можливість його застосування один раз на добу завдяки тривалому періоду напіввиведення. Дослідження продемонстрували, що беміпарин сприяє 3-5-кратному зростанню рівня вільного інгібітора шляху тканинного фактору.
Автор доповіді представив увазі колег аспекти проведення планових операцій в акушерсько-гінекологічній практиці. Він наголосив, що пацієнтки з потенційно травматичними, об’ємними гінекологічними втручаннями та високим ризиком крововтрати потребують персоніфікованого підходу до вибору тактики інфузійно-трансфузійної терапії, анестезії, післяопераційного знеболення й тромбопрофілактики. Було зазначено, що оптимальний об’єм інфузії збалансованих розчинів кристалоїдів становить 15-20 мг/кг і застосовується з метою досягнення центрального венозного тиску 8-15 см вод. ст. Експерти рекомендують застосовувати розчини кристалоїдів при проведенні нетривалих гінекологічних оперативних втручань. Разом із тим при проведенні об’ємних, травматичних операцій рекомендованим є застосування цілеспрямованого інфузійного режиму, який включає колоїди та розчини електролітів.
Далі доповідач зосередив увагу на особливостях менеджменту післяопераційного больового синдрому. Однією з основних проблем, пов’язаних із застосуванням опіоїдів, є розвиток післяопераційної опіоїдної гіпералгезії, що загрожує хронізацією післяопераційного больового синдрому. Саме ця обставина змусила медичну спільноту переглянути догму про необхідність обов’язкового періопераційного застосування опіоїдів. Професор О.М. Нестеренко зазначив, що вірогідність розвитку гіпералгезії залежить від загальної дози опіоїдів, яку отримав пацієнт. Натомість застосування неопіоїдних анальгетичних препаратів (НПЗП, габапентиноїдів, дексаметазону та ін.) дозволяє мінімізувати потребу в опіоїдах та ризик розвитку їх побічних ефектів шляхом впливу на альтернативні ноцицептивні сайти. Застосування неопіоїдних анальгетичних препаратів із різним механізмом дії формує основу концепції ММА, одним із найважливіших інструментів якої є застосування НПЗП. Доповідач зауважив, що препарат Дексалгін® – сучасний представник НПЗП, який є правообертаючим ізомером кетопрофену. Щодо здатності блокування ЦОГ, то Дексалгін® має вдвічі вищу активність порівняно з кетопрофеном й у 100 разів вищу – порівняно з його лівообертаючим ізомером.
Таким чином, Дексалгін® – це сучасний представник НПЗП, застосування якого в режимі ММА дозволяє суттєво зменшити потребу в опіоїдах і досягнути оптимального аналгезуючого ефекту за мінімального ризику розвитку НПЗП-асоційованих побічних ефектів. Адекватний менеджмент больового синдрому в післяопераційному періоді має важливе значення для прискорення активації хворого та скорочення часу перебування у стаціонарі. Дотримання оптимальної стратегії тромбопрофілактики із застосуванням сучасних безпечних антитромботичних засобів, наприклад препарату Цибор®, дозволяє запобігти розвитку тромботичних ускладнень. Застосування сучасних стратегій анестезіологічного забезпечення, імплементація контрольних списків та вдосконалення професійної комунікації дозволяє мінімізувати ризики, пов’язані з періопераційним періодом.
Підготувала Анастасія Козловська
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 4 (38), грудень 2019 р.