10 березня, 2020
Райзодег® ФлексТач®: нові можливості інтенсифікації інсулінотерапії у пацієнтів із цукровим діабетом 2 типу
 Із 31 жовтня по 2 листопада в Одесі, у рамках щорічного циклу регіональних заходів, відбулося засідання науково-освітнього проекту «Школа ендокринолога». Ця подія, як і завжди, виявилася дуже актуальною не лише для сімейних лікарів і ендокринологів, але й для хірургів і неврологів, які частіше стикаються з пацієнтами вже на етапі лікування ускладнень. У присутніх була нагода прослухати лекції провідних фахівців у галузі ендокринології, взяти участь у майстер-класах, практичних розборах, дискусіях та відчути атмосферу неформального спілкування. Значна частина засідання була присвячена інноваціям в галузі діабетології. Керівник відділу діабетології Інституту ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України, доктор медичних наук Любов Костянтинівна Соколова у своїй доповіді навела найновіші дані про застосування препарату Райзодег® ФлексТач® (RYZODEG® FlexTouch®), представлений на ринку України компанією «Ново Нордіск» (Данія).
Із 31 жовтня по 2 листопада в Одесі, у рамках щорічного циклу регіональних заходів, відбулося засідання науково-освітнього проекту «Школа ендокринолога». Ця подія, як і завжди, виявилася дуже актуальною не лише для сімейних лікарів і ендокринологів, але й для хірургів і неврологів, які частіше стикаються з пацієнтами вже на етапі лікування ускладнень. У присутніх була нагода прослухати лекції провідних фахівців у галузі ендокринології, взяти участь у майстер-класах, практичних розборах, дискусіях та відчути атмосферу неформального спілкування. Значна частина засідання була присвячена інноваціям в галузі діабетології. Керівник відділу діабетології Інституту ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України, доктор медичних наук Любов Костянтинівна Соколова у своїй доповіді навела найновіші дані про застосування препарату Райзодег® ФлексТач® (RYZODEG® FlexTouch®), представлений на ринку України компанією «Ново Нордіск» (Данія).
– Цей лікарський засіб є універсальним серед аналогових інсулінів, оскільки поєднує в одному шприці базальний інсулін деглюдек (70%) та інсулін ультракороткої дії аспарт (30%). Така комбінація дає можливість впливати на всі ланки патогенезу цукрового діабету (ЦД) завдяки поєднанню переваг кожної з форм аналогового інсуліну.
Деглюдек
- Тривалість дії понад 42 години.
- Безпека застосування у хворих із серцево-судинними захворюваннями, підтверджена результатами контрольованих клінічних досліджень.
- Знижений ризик гіпоглікемії.
- Можливість введення в зручний для пацієнта час, що напряму впливає на комплаєнс.
- Дозволений у дітей із першого року життя.
- Міжнародний досвід застосування становить 7 років.
Аспарт
- Діє вдвічі швидше та за коротший час, ніж людський інсулін.
- Знижує ризик виникнення гіпоглікемії.
- Може вводитися як до, так і після прийому їжі.
- Дозволений у дітей із 2 років.
- Міжнародний досвід застосування становить 20 років.
Позитивне співвідношення ефективності та безпеки препарату Райзодег® ФлексТач® було підтверджене в клінічних дослідженнях за участю пацієнтів із ЦД 1 та 2 типу. Призначення інсулінотерапії та її наступна інтенсифікація саме в пацієнтів із ЦД 2 типу є особливо дискутабельним та проблематичним питанням лікування діабету.
Прогресування ЦД 2 типу, крім стійкої інсулінорезистентності, зумовлене такими патогенетичними механізмами [1]:
- зниженням функції β-клітин та секреції інсуліну;
- зростанням гіперглікемії як натще, так і у відповідь на прийом їжі.
У дослідженні EU-TREAT вивчалася потреба в болюсному та базальному інсуліні в пацієнтів із ЦД 1 та 2 типу. У пацієнтів з ЦД 1 типу співвідношення було практично однаковим, тоді як у пацієнтів з ЦД 2 типу потреба в болюсному інсуліні, порівняно з базальним, була значно вищою [2].
Це пояснюється патофізіологічними особливостями гіперглікемії при ЦД 2 типу. Постпрандіальна гіперглікемія в цій категорії пацієнтів зумовлена втратою першої фази секреції. При цьому, на відміну від здорових людей, у пацієнтів із ЦД 2 типу у відповідь на вуглеводне навантаження продовжується синтез ендогенної глюкози, а рівень глюкагону залишається високим, що й спричиняє резистентність гіперглікемії [3].
У дослідженні DECODE, яке тривало 10 років і в яке було включено 25 тис пацієнтів, було встановлено асоціацію між рівнем глікемії і серцево-судинною смертністю. Woerle H.J. зі співавторами вивчали вплив цільової глікемії натще чи постпрандіальної глікемії на частоту досягнення цільового рівня глікованого гемоглобіну (HbA1с). Рівня HbA1с ≤7% досягали 94% пацієнтів із рівнем глюкози після прийому іжі ≤7,8 ммоль/л, тоді як нормоглікемія натще корелювала з цільовим рівнем HbA1с лише в третини пацієнтів [4,5].
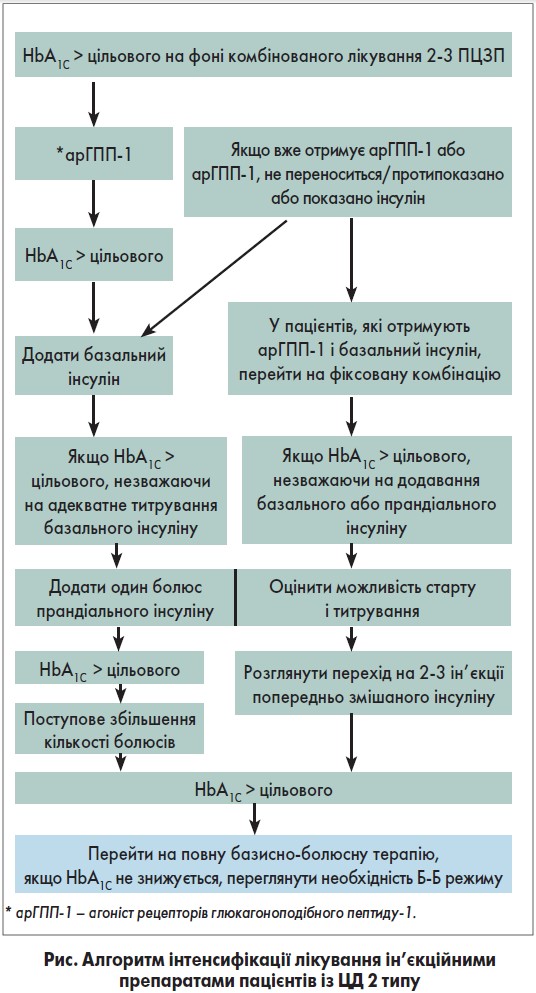 Таким чином, контроль постпрандіальної глікемії є ключовим у досягнені цілей лікування. У разі якщо рівень HbA1с у пацієнтів із ЦД 2 типу вище цільового, незважаючи на комбіновану терапію 2-3 пероральними цукрознижувальними препаратами (ПЦЗП), необхідно інтенсифікувати лікування ін’єкційними препаратами відповідно до алгоритму (рис.) [6].
Таким чином, контроль постпрандіальної глікемії є ключовим у досягнені цілей лікування. У разі якщо рівень HbA1с у пацієнтів із ЦД 2 типу вище цільового, незважаючи на комбіновану терапію 2-3 пероральними цукрознижувальними препаратами (ПЦЗП), необхідно інтенсифікувати лікування ін’єкційними препаратами відповідно до алгоритму (рис.) [6].
Згідно з консенсусом ADA/EASD інтенсифікація інсулінотерапії необхідна всім пацієнтам із ЦД 2 типу, які отримують базальний інсулін (зазвичай із ПЦЗП) за відсутності контролю HbA1C; незважаючи на досягнення цільового рівня глюкози натще (або дозі інсуліну >0,5 од/кг/день), необхідно знижувати постпрандіальну глікемію за допомогою прандіального інсуліну або арГПП‑1. Є два способи зробити це [7]:
- Перейти на 2 ін’єкції комбінованого інсуліну.
- Додати 1 ін’єкцію болюсного інсуліну перед найбільшим прийомом їжі, а в разі неефективності – додати ≥2 ін’єкції болюсного інсуліну (базально-болюсний режим – Б-Б режим).
Препарат Райзодег® ФлексТач® є ідеальним засобом на кожному етапі інтенсифікації інсулінотерапії, незважаючи на обрану лікувальну тактику. Пацієнти можуть бути переведені на Райзодег® ФлексТач® у тій самій добовій дозі базального інсуліну, яку вони отримали напередодні. Титрування дози також не викликає труднощів. Основою є показник середнього рівня глюкози натще за результатами 3 вимірювань:
- показник вище цілі – + 2 ОД;
- ціль досягнута – доза не змінюється;
- показник нижче цілі – - 2 ОД.
Запорукою успішної інтенсифікації інсулінотерапії препаратом Райзодег® ФлексТач® є розуміння того, що саме мається на увазі, коли йдеться про найбільший прийом їжі. Із клінічної точки зору – це страва, яка містить найбільшу кількість вуглеводів. У різні дні найбільший прийом їжі може припадати на різні періоди доби, тому в пацієнта має бути змога самому обирати час введення інсуліну та змінювати його. Таку можливість надає препарат Райзодег® ФлексТач®.
Ефективність і безпека комбінації деглюдеку та інсуліну аспарт у пацієнтів із ЦД 2 типу вивчалася в рандомізованому контрольованому відкритому паралельному дослідженні, де Райзодег® ФлексТач® порівнювався з інсуліном гларгін (IGlar). Учасники були випадковим чином розділені на 2 групи, перша з яких (n=266) отримувала Райзодег® ФлексТач® (IDegAsp), а друга (n=264) – IGlar. Потім учасники розпочали 26-тижневу фазу додаткового лікування (IDegAsp, n=192; IGlar, n=221).
Первинною кінцевою точкою була зміна показників HbA1C від вихідних на 26-й тиждень лікування. Через 26 і 52 тижні середнє значення HbA1C знизилося до аналогічних рівнів в обох групах. Через 52 тижні середня оціночна різниця в лікуванні становила -0,08% (95% ДІ; -0,26, 0,09), що підтверджувало не меншу ефективність IDegAsp проти IGlar, оцінену на 26-му тижні. Через 52 тижні в обох групах лікування спостерігалося однакове зниження середнього рівня глюкози плазми натще. Частота підтверджених гіпоглікемічних епізодів була на 86% вищою (р<0,0001), а частота нічної гіпоглікемії – на 75% нижчою (р<0,0001) для учасників групи IDegAsp порівняно з групою IGlar. Частота підтвердженої нічної гіпоглікемії була вищою в групі IGlar, тоді як загальна та добова гіпоглікемія була вищою в групі IDegAsp – це пояснювалося тим, що засіб використовували не під час основного прийому їжі, без урахування індивідуальних потреб пацієнта [8].
У ще одному масштабному 26-тижневому мультицентровому дослідженні в Азії вивчали ефективність і безпеку IDegAsp у порівнянні з двофазним інсуліном аспарт 30 (BIAsp 30) у дорослих пацієнтах з ЦД 2 типу, який недостатньо контролювався базальним інсуліном, що використовувався 1 або 2 рази на добу [9].
Учасники (середній вік становив 59,8 року, HbA1C – 8,4%, рівень глюкози натще – 7,9 ммоль/л, індекс маси тіла (ІМТ) – 25,4 кг/м2) були рандомізовані у співвідношенні 2:1 у 2 групи. Перша група (n=282) отримувала 2 рази на день IDegAsp, друга (n=142) – BIAsp 30. Учасники обох груп продовжували лікування метформіном.
Інсуліни вводили одночасно зі сніданком та основним вечірнім прийомом їжі, титруючи дозу кожен раз на основі цільового рівня глюкози плазми крові 4-5 ммоль/л. Рівень глюкози пацієнти вимірювали самостійно.
Учасники групи IDegAsp досягли первинної кінцевої точки (середньої зміни HbA1C) аналогічно з групою BIAsp 30 (розрахункова різниця між методами лікування (ETD) IDegAsp-BIAsp 30: 0,05%; 95% ДI -0,10; 0,20). IDegAsp ефективніше знижував рівень глюкози в плазмі натще (ETD -1,06 ммоль/л, 95% ДІ -1,43; -0,70; р<0,001), з меншою середньодобовою дозою інсуліну (0,79 ОД/кг у порівнянні з 0,99 U/кг, розрахунковий відносний ризик (RR) 0,79; 95% ДІ 0,73; 0,85; р<0,0001). Рівні загальної підтвердженої та симптомної гіпоглікемії були зіставні для обох режимів лікування, тоді як частота підтвердженої нічної гіпоглікемії чисельно (p=ns) виявилася нижчою в пацієнтів групи IDegAsp. Протягом підтримувального періоду лікування спостерігалася тенденція (p=ns) до зниження ризику гіпоглікемії в учасників групи IDegAsp.
Отже, було підтверджено, що IDegAsp у дорослих пацієнтів із ЦД 2 типу ефективно покращує тривалий глікемічний контроль порівняно з BIAsp 30 та забезпечує більш ефективне зниження рівня глюкози плазми натще при використанні меншої дози інсуліну, а також рідше викликає нічні гіпоглікемії [9].
Аналогічні результати було отримано в ході метааналізу 5 контрольованих рандомізованих 26-тижневих відкритих досліджень (фаза ІІІ), в яких IDegAsp двічі на день (n=1111) порівнювали з одним із двох препаратів: двофазним інсуліном аспарт 30 (BIAsp 30) двічі на день (n=561) або інсуліном деглюдек (IDeg) 1 раз на день + IAsp (n=136). Дані пацієнтів були стратифіковані відповідно до початкового рівня HbA1C або глюкози плазми крові натще, а також за тривалістю діабету або ІМТ [10].
Рівні HbA1C були аналогічними для IDegAsp і препаратів порівняння за всіма початковими характеристиками (HbA1C, тривалість діабету чи ІМТ) та категоріями груп. Значно нижчий рівень глюкози плазми крові натще спостерігався в групі IDegAsp проти препаратів порівняння за всіма початковими характеристиками.
Цільовий рівень глюкози досягався при використанні статистично значуще менших доз інсуліну IDegAsp проти препаратів порівняння. Також у пацієнтів групи IDegAsp набагато рідше реєстрували епізоди загальної підтвердженої та нічної гіпоглікемії.
Таким чином, комбінація аналогових інсулінів, представлена в препараті Райзодег® ФлексТач®, ефективність і безпека якого підтверджені дослідженнями високого ступеня доказовості, дає можливість полегшити процес ініціації та інтенсифікації інсулінотерапії при ЦД 2 типу. Це забезпечується простотою режиму застосування, контролем рівня глікемії як натще, так і після їжі, меншою добовою дозою, точністю дозування та зниженням ризику гіпоглікемій, зокрема й нічних. Усі ці переваги забезпечують можливість індивідуалізувати ведення пацієнта з ЦД і досягти основних цілей лікування – покращання якості життя та зниження частоти розвитку ускладнень.
Література
- Ramlo-Halsted B.A., Edelman S.V. The natural history of type 2 diabetes. Implications for clinical practice. Prim Care. 1999 Dec;26(4):771-89.
- Thorsten Siegmund, Nikolaos Tentolouris, Sоren T. Knudsen, Annunziata Lapolla et al. and for the EU-TREAT study group. A European, multicentre, retrospective, non-interventional study (EU-TREAT) of the effectiveness of insulin degludec after switching basal insulin in a population with type 1 or type 2 diabetes. Diabetes Obes Metab. 2018 Mar; 20(3):689-697.
- Asimina Mitrakou, David Kelley, Thiemo Veneman et al. Contribution of Abnormal Muscle and Liver Glucose Metabolism to Postprandial Hyperglycemia in NIDDM. Diabetes 1990 Nov; 39(11):1381-1390.
- Woerle H.J., Neumann C., Zschau S., Tenner S. et al. Impact of fasting and postprandial glycemia on overall glycemic control in type 2 diabetes Importance of postprandial glycemia to achieve target HbA1c levels. Diabetes Res Clin Pract. 2007 Aug;77(2):280-5. Epub 2007 Jan 22.
- Melanie J. Davies, David A. D’Alessio, Judith Fradkin et al. Management of Hyperglycemia in Type 2 Diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2018 Sep; dci180033.
- Silvio E. Inzucchi, Richard M. Bergenstal, John B. Buse et al. Management of Hyperglycemia in Type 2 Diabetes, 2015: A Patient-Centered Approach: Update to a Position Statement of the American Diabetes Association and the European Association for the Study of Diabetes.
- Ajay Kumar, Edward Franek, Jonathan Wise et al. Efficacy and Safety of Once-Daily Insulin Degludec/Insulin Aspart versus Insulin Glargine (U100) for 52 Weeks in Insulin-Naive Patients with Type 2 Diabetes: A Randomized Controlled Trial. PLoS One. 2016; 11(10): e0163350.
- Kaneko S., Chow F., Choi D.S., Taneda S. et al. BOOST: Intensify All Trial Investigators. Insulin degludec/insulin aspart versus biphasic insulin aspart 30 in Asian patients with type 2 diabetes inadequately controlled on basal or pre-/self-mixed insulin: a 26-week, randomised, treat-to-target trial. Diabetes Res Clin Pract. 2015 Jan;107(1):139-47.
- Martin Haluzik, Greg Fulcher, Thomas R. Pieber et al. The co-formulation of insulin degludec and insulin aspart lowers fasting plasma glucose and rates of confirmed and nocturnal hypoglycaemia, independent of baseline glycated haemoglobin levels, disease duration or body mass index: A pooled meta-analysis of phase III studies in patients with type 2 diabetes. Diabetes Obes Metab. 2018 Jul; 20(7):1585-1592.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (47) жовтень 2019 р.


