10 березня, 2020
Новини Європейської ендокринної хірургії
За матеріалами 8-ї конференції ESES-2019
.jpg) У травні в м. Гранада (Іспанія) відбулася чергова конференція Європейського товариства ендокринних хірургів, тема якої звучала дещо незвично – «Volume, outcomes and quality standards in endocrine surgery» («Обсяг, результати лікування та стандарти якості в ендокринній хірургії»). Лейтмотивом робочої програми заходу став пошук оптимальних шляхів до забезпечення високоякісної допомоги пацієнтам у галузі ендокринної хірургії з мінімальним ризиком ускладнень. Основний акцент був зроблений на питанні необхідного досвіду ендокринних хірургів, їх навчання та технологічного забезпечення операцій. Розробка оптимальних рішень проводилась із залученням досягнень і думок авторитетних фахівців з усього світу та результатів метааналізу спеціальної літератури.
У травні в м. Гранада (Іспанія) відбулася чергова конференція Європейського товариства ендокринних хірургів, тема якої звучала дещо незвично – «Volume, outcomes and quality standards in endocrine surgery» («Обсяг, результати лікування та стандарти якості в ендокринній хірургії»). Лейтмотивом робочої програми заходу став пошук оптимальних шляхів до забезпечення високоякісної допомоги пацієнтам у галузі ендокринної хірургії з мінімальним ризиком ускладнень. Основний акцент був зроблений на питанні необхідного досвіду ендокринних хірургів, їх навчання та технологічного забезпечення операцій. Розробка оптимальних рішень проводилась із залученням досягнень і думок авторитетних фахівців з усього світу та результатів метааналізу спеціальної літератури.
Ще за рік до події було визначено основні сектори відповідно напрямам ендокринної хірургії та, окремо, питань акредитації установ.
За кожним напрямом працювала робоча група з 4-5 відомих європейських фахівців, які здійснювали масштабний огляд сучасної літератури та систематизацію інформації щодо шляхів досягнення найкращих результатів в ендокринній хірургії. Так, группу з питань тиреоїдної хірургії очолювала Kerstin Lorenz, хірургії прищитоподібних залоз – Maurizio Iacobone, надниркових залоз – Radu Mihai, стажування та тренінгу – liver Gimm, акредитації установ (відділень) ендокринної хірургії – Thomas Musholt.
Програма конференції охоплювала всі розділи хірургічної ендокринології, фахівці з різних країн Європи та світу розповідали про свої клінічні спостереження та результати досліджень і випробувань. Принципово нових розробок представлено не було – подальшого розвитку зазнали питання інтраопераційного електронейромоніторингу гортанних нервів (досліджувався негативний вплив міорелаксантів і пропонувалося проводити рекураризацію, передусім у пацієнтів із надмірною вагою); флюоресценції прищитоподібних залоз в інфрачервоному спектрі після опромінення ультрафіолетовим спектром та введення індоціану зеленого (цей метод був застосований також для виявлення екстраадреналової інвазії та метастазів у лімфатичні вузли воріт нирки під час операції у хворих на адренокортикальний рак). Були також оприлюднені систематизовані дані щодо розподілу моторних і сенсорних волоконець у передній та задній гілках поворотного гортанного нерва (80-100% моторних волоконець складають передню гілку), надано обнадійливу інформацію про високу ефективність радіонуклідної терапії метастазуючих нейроендокринних пухлин гастро-ентеро-панкреатичної зони (застосовують метод зв’язування з пептидними соматостатиновими рецепторами нових речовин та ізотопів – 177Lu-DOTATATE), переглянуто схему передопераційного лабораторного підтвердження наявного медулярного раку з сумнівним підвищенням кальцитоніну крові (50-100 пг/мл) шляхом проведення стимуляційної проби з кальцієм (наголошується, що у випадках незначного підвищення кальцитоніну після проби – до 100 пг/мл слід не покладатися виключно на результати тесту, а враховувати комплекс клінічних даних через низьку специфічність цієї проби).
Присутні на заході ознайомилися також із результатами клінічних випробувань новітніх апаратів для електротермічного роз’єднання тканин та коагуляції з позицій можливої шкоди для гортанних нервів: було доведено безпечність найбільш популярного девайсу «Ligasure» Small Jaw за його використання на відстані понад 2 мм від нервів. Демонструвалися результати та технічні аспекти нових напрямів ендоскопічних операцій на щитоподібній залозі (ЩЗ), насамперед так званого безслідного доступу через слизову оболонку вестибулярного відділу ротової порожнини – цей спосіб набуває популярності в країнах Сходу, у Туреччині, в Італії, у США (так званий метод TOETVA – Transoral Endoscopic Thyroidectomy Vestibular Approach, який сьогодні не можна ще вважати альтернативою традиційному доступу внаслідок деяких труднощів та можливих ускладнень, у тому числі косметичного та інфекційно-запального характеру).
Але, без сумніву, найцікавішими були дискусії щодо пропозицій робочих груп, які готували матеріали стосовно критеріїв акредитації ендокринних хірургів, центрів ендокринної хірургії, безпечних засад ефективного хірургічного лікування ендокринних захворювань.
Причиною, за якою було обрано тему 8-ї конференції ESES, стало занепокоєння лідерів світової хірургічної ендокринології постійним ростом числа відповідних хірургічних операцій, кількості хірургів та лікарень, де виконуються такі операції, з одночасним зменшенням частки медичних установ і фахівців із достатнім досвідом в ендокринній хірургії. Так, за даними регістру Франції, щороку виконується майже 1600 адреналектомій (за період 2012-2017 рр. – 9820) у 538 центрах, але в більшості з них (283) проводиться щонайбільше 1 операція щороку, а понад 1 операції на місяць – тільки в 32 (6%) центрах. Така сама картина спостерігається у Великій Британії: 795 адреналектомій за 2013-2014 рр. було виконано 222 хірургами, з яких 186 роблять менше 6 (в середньому по 1) подібних операції за рік. У США за період з 1998 по 2000 рік було виконано 13 229 адреналектомій, з яких 50% – хірургами з щорічною практикою менше 2 таких операцій.
Схожа ситуація склалася і в тиреоїдній та паратиреоїдній хірургії. Приблизно 80% усіх операцій у тиреоїдній хірургії в США та Канаді виконують хірурги з практикою менше 5 операцій на рік.
 Саме тому Європейське товариство ендокринних хірургів, з метою уніфікації та посилення вимог до виконання операцій на ендокринних органах задля отримання оптимальних результатів у пацієнтів, запланувало розробити чіткі та конкретні «правила гри» для акредитації хірургів (персонально) та установ (клінік, центрів, відділень). Першим кроком на цьому шляху стало введення сертифікації ендокринних хірургів Європейським бюро медичних спеціальностей (розділ «Хірургія», підрозділ – «Ендокринна хірургія»). Тобто допуск до роботи в цілісній ендокринній хірургії (або тільки ендокринній хірургії шиї) отримували фахівці – члени ESES, які беруть активну участь у роботі асоціації, мають практичний досвід виконання фіксованого мінімуму хірургічних утручань (персонально та асистенцій), успішно склали усний іспит із загальної ендокринної або тиреоїдної-паратиреоїдної хірургії. Вони мусять отримати сертифікат – Fellow of European Board of Surgery / Endocrine Surgery (or Neck Endocrine Surgery). Водночас питання ліцензування таких хірургів та акредитації установ, де вони працюють, залишилося без належної регламентації. Треба також зазначити, що багато хто з європейських хірургів відмовляються складати іспит з ендокринної хірургії, бо працюють загальними хірургами, або отоларингологами, або урологами тощо. Утім ендокринна хірургія – це не просто різновид хірургії, це симбіоз фундаментальних знань та хірургічної досконалості, і це усвідомлюють лише справжні професіонали, яким їхнє сумління не дозволяє віддати на поругу свою професію-мистецтво! Тому й взялися за надскладну задачу – окреслити та регламентувати вимоги. Але ж в спільну Європу також ніхто спочатку не вірив…
Саме тому Європейське товариство ендокринних хірургів, з метою уніфікації та посилення вимог до виконання операцій на ендокринних органах задля отримання оптимальних результатів у пацієнтів, запланувало розробити чіткі та конкретні «правила гри» для акредитації хірургів (персонально) та установ (клінік, центрів, відділень). Першим кроком на цьому шляху стало введення сертифікації ендокринних хірургів Європейським бюро медичних спеціальностей (розділ «Хірургія», підрозділ – «Ендокринна хірургія»). Тобто допуск до роботи в цілісній ендокринній хірургії (або тільки ендокринній хірургії шиї) отримували фахівці – члени ESES, які беруть активну участь у роботі асоціації, мають практичний досвід виконання фіксованого мінімуму хірургічних утручань (персонально та асистенцій), успішно склали усний іспит із загальної ендокринної або тиреоїдної-паратиреоїдної хірургії. Вони мусять отримати сертифікат – Fellow of European Board of Surgery / Endocrine Surgery (or Neck Endocrine Surgery). Водночас питання ліцензування таких хірургів та акредитації установ, де вони працюють, залишилося без належної регламентації. Треба також зазначити, що багато хто з європейських хірургів відмовляються складати іспит з ендокринної хірургії, бо працюють загальними хірургами, або отоларингологами, або урологами тощо. Утім ендокринна хірургія – це не просто різновид хірургії, це симбіоз фундаментальних знань та хірургічної досконалості, і це усвідомлюють лише справжні професіонали, яким їхнє сумління не дозволяє віддати на поругу свою професію-мистецтво! Тому й взялися за надскладну задачу – окреслити та регламентувати вимоги. Але ж в спільну Європу також ніхто спочатку не вірив…
Найважливішими питаннями всіх трьох вищезазначених робочих груп було:
- розробка критеріїв оцінки «якісної» хірургічної допомоги ендокринним пацієнтам (тобто за якими параметрами можна на наступному етапі розрахувати мінімально достатню кількість персональних і загальних госпітальних операцій на щитоподібній, прищитоподібних, надниркових залозах для забезпечення оптимального рівня ефективності). Ці критерії стосуються передусім частоти специфічних ускладнень, а також розподілу втручань на операції звичайного та підвищеного ризику;
- визначення кількості хірургічних втручань на певному ендокринному органі, яку можна було б назвати мінімально достатньою для отримання прийнятних показників специфічних хірургічних ускладнень, а також кількості певних операцій для визначення найбільш досвідчених хірургів, які мають оперувати складні випадки захворювань;
- визначення кількості операцій на ендокринних органах для диференціації центрів ендокринної хірургії з недостатнім і великим досвідом;
- визначення критеріїв, необхідних для акредитації центрів ендокринної хірургії як «центрів компетентності» та «референс-центрів».
Щоби виконати всі ці дуже складні завдання, члени робочих груп та запрошені фахівці провели величезну аналітичну роботу: окрім огляду численних літературних джерел та мобілізації особистого інтелектуального потенціалу і професійних знань були проаналізовані великі національні й міжнародні комп’ютерні бази даних. Створення та підтримка функціонування таких баз (наприклад, загальноєвропейської бази даних реєстрації операцій в ендокринній хірургії та їх результатів «EUROCRINE») є головною запорукою можливості об’єктивного аналізу результатів діяльності як окремих ендокринних хірургів, так і медичних закладів. До сьогодні входження та підключення до таких баз було добровільним і регулювалося тільки національним законодавством, але планується визнання в найближчому майбутньому такого методу статистики та аналізу обов’язковим для установ ендокринної хірургії країн ЄС.
Питання достовірності та правдивості результатів хірургічного лікування ендокринних захворювань неодноразово піднімалося протягом конференції. Було визнано, що найбільш надійними є результати, отримані за допомогою статистики страхових кампаній, а також перехресного дослідження шляхом «накладання» даних двох баз. Справа в тому, що у своїх хірургічних звітах клініки й окремі лікарі зазвичай занижують реальні показники післяопераційних ускладнень, а дійсно об’єктивними можуть бути дані щодо повторної госпіталізації протягом 30-90 діб, смертності протягом 90 діб після операцій, рецидивів захворювання, безрецидивного виживання при злоякісних пухлинах, утрати працездатності пацієнтів, уживання певних медикаментів через рік після операції тощо.
Останній приклад виявився дуже показовим щодо частоти постійного гіпопаратиреозу та гіпокальціємії після тотальної тиреоїдектомії. Унікальна за своїм дизайном робота, проведена молодими дослідниками (Anneback М. et al.) з Упсальського університету в Швеції, показала, наскільки можуть відрізнятися дані хірургічних звітів, зареєстрованих у Національному регістрі якості в тиреоїдній, паратиреоїдній та наднирковій хірургії Швеції – SQRTPA, а також у Шведському національному регістрі пацієнтів – NPR, та дані Шведського регістру призначених медикаментів (SPDR). Після відокремлення з більш як 12 400 пацієнтів, прооперованих за 10 років в обсязі тотальної тиреоїдектомії, 4500 пацієнтів із раком ЩЗ (РЩЗ) або ускладненими випадками захворювання для подальшого аналізу залишилося 7850 хворих. Частота постійного гіпопаратиреозу, за першими двома базами даних (відомості надані хірургами та ендокринологами), складала 3%, а за даними регістру призначених ліків (постійне вживання препаратів кальцію та активного вітаміну D через 1-5 років після операції), вона виявилася більш як у 4 (!) рази вищою – 12,5%. Протягом першого року після операції частота гіпокальціємії складала 42,2%, а впродовж наступних 5 років практично не змінювалась (11,9-12,8%). Нагадаємо, що йдеться лише про доброякісні неускладнені захворювання ЩЗ без дисекції шиї.
Таким чином, у дослідників виникатиме багато питань навіть щодо оцінки якості роботи ендокринних хірургів за частотою основних специфічних ускладнень. Попри все це, робочі групи конференції визначилися з критеріями професіоналізму ендокринних хірургів.
Так, для тиреоїдної хірургії обрані: частота ушкоджень поворотного гортанного нерву, гіпопаратиреозу та гіпокальціємії, кровотеч, а для злоякісних пухлин ЩЗ – частота рецидивів раку.
Для паратиреоїдної хірургії – загальний рівень ускладнень, частота персистенції гіперпаратиреозу, частота рецидивів.
Для операцій на надниркових залозах визначальними обрані такі показники: смертність упродовж 90 діб, повторні операції, повторна госпіталізація протягом 90 діб, тривалість перебування в реанімації та стаціонарі.
Метааналіз сучасної літератури та результати останніх проспективних досліджень однозначно довели, що персональний досвід ендокринного хірурга відіграє вирішальну роль у зниженні частоти ускладнень та досягненні найкращих результатів лікування. У тиреоїдній хірургії було доведено, що разом зі збільшенням кількості щорічних операцій достовірно (майже лінійно) знижується частота ускладнень, насамперед парезу гортанних нервів, аж до досвіду 25 тиреоїдектомій на рік, а далі (до 100 операцій на рік) крива зменшення ризику ускладнень повільно переходить у плато (Adam М.А. et al., 2017). Найбільший ризик пошкодження гортанних нервів виникає під час операцій із приводу раку та аутоімунних захворювань ЩЗ, які мають виконувати найбільш досвідчені хірурги в профільних центрах із кількістю втручань понад 100 операцій на рік. В аспекті профілактики парезів гортані після тиреоїдектомій продовжується обговорення ролі застосування інтраопераційного нейромоніторингу гортанних нервів у різних його технічних варіантах. Результати масштабного метааналізу частоти парезу гортані після операцій із візуальним контролем нервів та апаратним нейромоніторингом, який нараховує майже 100 тис нервів у ризику, надав дещо суперечливі дані – тільки 5 із 8 досліджень підтвердили деяку статистично значиму перевагу нейромоніторингу над візуальним контролем нервів. Цифри вказують на збереження високого ризику пошкодження гортанних нервів навіть у Німеччині, де нейромоніторинг є обов’язковим елементом тиреоїдних операцій. В окремих дослідженнях перевага надається все ж таки нейромоніторингу, передусім у пацієнтів із підвищеним ризиком (2,5 проти 4,5%) та повторними операціями (4,45 проти 7,61%). Водночас саме досвід хірурга та його щоденна практика є більш вагомими аргументами запобігання післяопераційним парезам гортані, частота яких коливається в межах 1,5-3%.
Щодо ризику післяопераційних гіпокальцемій, різниця між досвідченими та малодосвідченими хірургами ще більш разюча: потрібно не менше 50 операцій на рік, аби досягти задовільного рівня цього специфічного в тиреоїдній хірургії ускладнення (50 проти 6% через 6 міс та 19 проти 2% через 1 рік після операції відповідно). Така сама залежність прослідковувалась окремо для хірургії хвороби Грейвза, а також для оцінки ризику кровотеч після операцій.
Кровотечі – це окрема тема в хірургії ЩЗ через щонайменше 2-кратне зростання частоти пошкодження гортанних нервів, 20-кратне збільшення ризику трахеостомії та 50-кратне – поопераційної смертності. З метою зменшення ризику кровотеч дослідниками визначено ще більшу кількість персональних операцій для отримання найкращих показників – 100.
При цьому вважається, що 1% кровотеч, які вимагали повторних операцій, є надзвичайно позитивним результатом, а менше 2% – припустимим. Госпітальний рівень активності в тиреоїдній хірургії також є важливим фактором зниження ризику ускладнень (приблизно дорівнює 2-кратному мінімальному обсягу операційної активності 1 хірурга), що свідчить на користь командної роботи в цій галузі ендокринної хірургії.
Дуже цікавим аспектом впливу досвіду хірурга на результати операції було дослідження частоти рецидиву РЩЗ за умови виконання втручання досвідченим і малодосвідченим хірургом. Адже заради зменшення частоти ушкоджень гортанних нервів та прищитоподібних залоз дехто з хірургів йде на свідомо нерадикальні варіанти резекції ЩЗ, що неминуче призведе до зростання частоти рецидивів. Подібних досліджень в літературі було небагато. Останнє масштабне вивчення цього питання на підставі оцінки 31 тис операцій в «Samsung Center» у Південній Кореї (Kim Н.І. et al., 2018) показало, що кількість рецидивів, частота позитивних границь резекції пухлини, залишення резидуальних метастазів у лімфовузли латеральних колекторів шиї зворотно корелює з щорічною практикою, а остання може вважатися достатньою після досягнення межі в 100 операцій на рік.
У питанні забезпечення оптимальної якості операцій на прищитоподібних залозах на першому місці серед оціночних критеріїв стоїть ефективне вилікування первинного гіперпаратиреозу з першої спроби, тобто відсутність персистенції захворювання після операції та незначна кількість рецидивів. Для оцінки цього ускладнення в лікуванні первинного гіперпаратиреозу навіть ввели таке поняття, як «помилка, якій можна було б запобігти» («preventable failures»): за даними Chen (2010), хірург із досвідом ≥50 операцій на рік припустить таких помилок у рази менше (13 проти 89%). Менш категоричний Mitchel (2008): 75 проти 15-30% після досягнення хірургом порогової межі в 20 операцій на рік. На відміну від тиреоїдних операцій виключно персональний досвід хірурга відіграє вирішальну роль в ефективному лікуванні, а роль клініки залишається другорядним фактором. Висновок: досвідчений паратиреоїдний хірург однаково результативно працюватиме в будь-якій клініці. Цікавим було спростування усталеної думки, що досвідчений тиреоїдний хірург буде нібито таким же досвідченим у паратиреоїдній хірургії. Результати окремого дослідження показали, що паратиреоїдна хірургія вимагає виключно специфічного багажу знань та вмінь.
Ще один оціночний параметр – частота операційних ускладнень у паратиреоїдній хірургії – також напряму залежить від персонального досвіду хірурга. Відсоток ризику основних ускладнень у первинних та повторних операціях на прищитоподібних залозах у разі виконання втручань справжнім професіоналом (>50 операцій на рік) або хірургом, який виконує <15 операцій на рік, буде складати 0,9 та 1,49% проти 1,89 та 3,77% відповідно. Інтегруючи дані різних дослідників за останні 20 років, робоча група дійшла висновку, що маркером високого рівня активності та досвіду є ≥40 операцій на прищитоподібних залозах на рік, а показником недостатнього досвіду – <15 операцій на рік. При цьому пропонується поділяти випадки первинного гіперпаратиреозу на «стандартні» та «ускладнені» (без чіткої локалізації), мультигляндулярні, спадкові, рецидивні. Саме останні вимагатимуть проведення операції найбільш досвідченим хірургом.
Питання перегляду ставлення до первинного гіперпаратиреозу як до ретельно вивченої медичної проблеми з відомим передбачуваним результатом лікування стало темою лекції президента ESES Девіда Скотта-Кумбса (David Scott-Coombes). Філософське високопрофесійне переосмислення нових парадигм проблеми дозволило йому накреслити певні характерні особливості сучасного стану діагностики та лікування захворювання:
- сформувалася тенденція до виконання малоінвазивних «націлених» операцій із приводу первинного гіперпаратиреозу, що призвело до зменшення досвіду виконання традиційних операцій з експлорацією всіх 4 прищитоподібних залоз;
- кількість випадків персистенції та рецидивів гіперпаратиреозу поступово зростає зі збільшенням частки «націлених» втручань;
- розмір і вага аденом прищитоподібних залоз поступово зменшуються («вимивання тяжких форм»), що ускладнює їх інтраопераційний пошук та візуалізацію перед операцією;
- зростає частка пацієнтів із подвійно-негативною візуалізацією (МІВІ-сцинтиграфія та сонографія), що ускладнює операцію та вимагає проведення тонкозрізової комп’ютерної томографії з довенним контрастуванням, а від ендокринного хірурга – великого персонального досвіду;
- звичним стає парадоксальний хибний принцип, яким усе частіше стали керуватися ендокринологи та малодосвідчені хірурги: немає візуалізації – немає показів до операції (!).
Професор С.М. Черенько (справа) з президентом ESES Девідом Скоттом-Кумбсом (David Scott-Coombes) біля стендового докладу на конференції в м. Гранада (Іспанія)
Відомий американський хірург-паратиреоїдолог J.Norman (2012) вирішив навіть відмовитися від «націлених» операцій при первинному гіперпаратиреозі, коли побачив поступове погіршання віддалених результатів спостереження з 99,4 до 94% на масиві з 15 тис прооперованих пацієнтів. Отже, вимоги до персонального досвіду хірурга в лікуванні первинного гіперпаратиреозу стають дедалі більш визначальними. Будь-які випадки підозри на мультигляндулярне ураження, спадковість, ектопію прищитоподібних залоз (це часто корелює з подвійно-негативною передопераційною візуалізацією) потребують направлення хворого до референс-центру з великим власним досвідом лікарів.
Третя робоча група працювала над питанням безпеки операцій на надниркових залозах та адекватного досвіду хірургів, які виконують адреналектомію.
Складність цієї проблеми визначається відносною рідкісністю патології надниркових залоз, яка потребує хірургічного лікування, обмеженою кількістю центрів для стажування та тренінгу, наявністю різних методик виконання адреналектомії (відкрита, лапароскопічна, задня ретроперитонеоскопічна, роботизована) та різноманітністю фахівців, які беруться за таку операцію (ендокринні, загальні хірурги, урологи).
Так, за даними літератури, серії адреналектомій залежно від клінік варіюють за кількістю від 35 до 560 за 12 років. Потенційна кількість операцій, яку зможе зробити кожен із двох хірургів (на півмільйона населення), дорівнює 2 інціденталомам, 2 альдостеромам та 1 феохромоцитомі (малоймовірно – 1 синдрому Кушинга). Тільки 5 британських хірургів стикаються з принаймні одним випадком адренокортикального раку щороку. Крива досягнення достатньої майстерності виконання адреналектомії налічує не менш ніж 30-40 операцій. Тому раціональні вимоги до мінімально необхідного навантаження ендокринного хірурга в британських і французьких авторитетних експертів відрізняються більш ніж удвічі. Так, британці вважають достатнім 6 адреналектомій для нетяжких випадків та 12 для адрено-кортикальних карцином (для референс-центрів – понад 20), у той час як, на думку французьких фахівців, оптимальний маркер ефективного та безпечного виконання адреналектомії – це 32 операції на рік. Показник післяопераційної летальності за 90 діб теж відрізнявся вдвічі (0,9 проти 1,8% відповідно). Пацієнтів із високим ризиком (який розраховується на підставі багатьох факторів, передусім віку, наявності супутніх хвороб, відсутності секреції та підозри на малігнізацію) мають оперувати найбільш досвідчені хірурги.
З огляду на вищенаведені факти, стає зрозумілою зацікавленість присутніх результатами 15-річного досвіду професора С.М. Черенька (фото), який представив інтегровані дані персонального виконання більш як 1 тис адреналектомій, проведених переважно за лапароскопічною методикою.
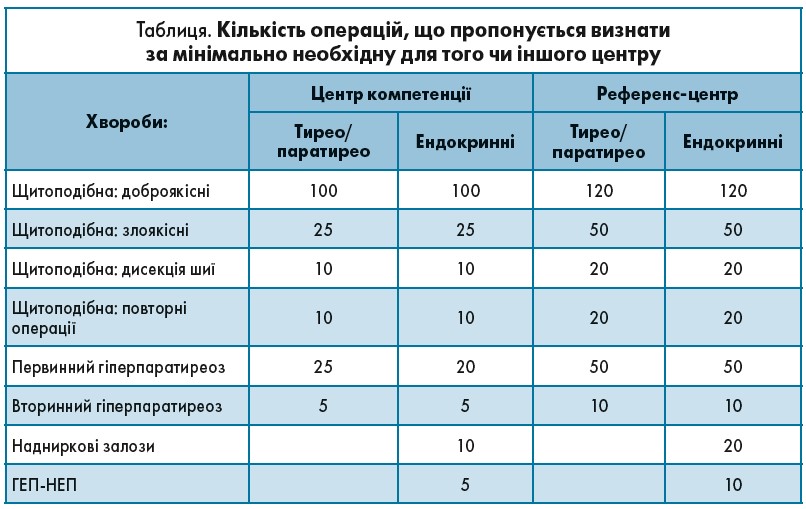
Останні засідання конференції були присвячені розробці та обґрунтуванню акредитаційних вимог до медичних закладів, де мають виконуватись операції на ендокринних органах. Усі учасники мали змогу долучитися до дискусії. Обговоренню цих питань під час роботи заходу передувало електронне опитування членів ESES напередодні зустрічі. Члени робочої групи та делегати дійшли згоди, що центри ендокринної хірургії мають бути розподілені на дві категорії: центри компетенції (Competence center) та референс-центри (Reference center). Діяльність кожного з них має бути сконцентрована тільки на проблемі щитоподібної та прищитоподібних залоз або охоплювати весь комплекс питань ендокринної хірургії (включно із захворюваннями надниркових залоз та гастро-ентеро-панкреатичними нейро-ендокринними пухлинами – ГЕП-НЕП) (табл.).
В якості критеріїв належної хірургічної майстерності визнано доцільним вважати такі показники, як частота післяопераційного парезу гортанних нервів (<5% від нервів у ризику) при операціях із приводу багатовузлового зоба; частота кровотеч після операцій на ЩЗ, які потребували повторного втручання (<2%); частота відновлення нормального рівня паратгормону після операцій із приводу первинного гіперпаратиреозу (>92%).
Додатковими критеріями акредитації стали вимоги до персоналу: 2 акредитованих за Європейськими вимогами ендокринних хірурги для центру компетенції та 3 хірурги – для референс-центру. Хірурги мають брати активну участь у міжнародних та національних конференціях, курсах, дослідженнях та набирати за рік не менш ніж 16 кредитів.
Перелік необхідного обладнання акредитованих центрів включає прилади для інтраопераційного нейромоніторингу гортанних нервів, інтраопераційного визначення паратгормону крові, периопераційної ларингоскопії, експрес-біопсії заморожених зрізів, для виконання стернотомії, а також – залучення методів променевого та радіоізотопного лікування. Обов’язковим вважається робота в кооперації з мультидисциплінарною командою, у складі якої є ендокринолог, патолог (у тому числі з експрес-біопсією та імуногістохімією), отоларинголог, радіолог (КТ, МРТ, радіонуклідне лікування та діагностика, у тому числі сонографія та ендоскопічна сонографія), а для референс-центрів, додатково, – променевий терапевт, онколог, інтервенційний радіолог, торакальний, судинний, серцево-судинний хірург, клінічний генетик, служба лабораторного тестування.
Лікарі мають брати участь у наукових дослідженнях, публікаціях, виступах на конференціях, їх організації, навчанні студентів/резидентів.
Дуже важливим елементом контролю та самоконтролю є внесення даних щодо хірургічного лікування ендокринних захворювань до єдиної комп’ютерної бази (в Європі – це EUROCRINE), хоча, звісно, це потребує високої самодисципліни, залучення додаткових коштів та часу. Але саме так формується справжнє підґрунтя для постійної аналітичної роботи, порівняння власних результатів з іншими, з різних країн та центрів. Єдине застереження та єдина вимога – це чесність: без правдивих даних, які дають уявлення про реальну ситуацію в цій галузі медицини, все це не варто навіть починати.
Всі пропозиції робочих груп щодо акредитації ендокринних хірургів та центрів ендокринної хірургії будуть опрацьовані та представлені на затвердження на наступному конгресі ESES.
Ми віримо, що для українських колег ці високі вимоги (які на сьогодні, звичайно, не є обов’язковими для виконання в нашій багатостраждальній країні з жебрацьким фінансуванням медицини) стануть дороговказом і стимулом для подальшого професійного вдосконалення попри всі соціальні негаразди.
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (47) жовтень 2019 р.