17 березня, 2020
Кардиоваскулярная токсичность ингибиторов тирозинкиназы BCR-ABL при хроническом миелоидном лейкозе
Методы профилактики и принципы ведения пациентов
 Хронический миелоидный лейкоз (ХМЛ) – это миелопролиферативное заболевание, возникающее вследствие реципрокной транслокации, при которой часть хромосомы 9, содержащая онкоген c-abl, транслоцируется на хромосому 22 и соединяется с геном BCR. Объединенный ген кодирует белок BCR-ABL с активностью тирозинкиназы (ТК). В результате происходит гиперпродукция гранулоцитов – главным образом, в костном мозге, а также в экстрамедуллярных очагах (селезенка, печень). Нормальные стволовые клетки сохраняются и могут активизироваться после медикаментозной супрессии опухолевого клона.
Хронический миелоидный лейкоз (ХМЛ) – это миелопролиферативное заболевание, возникающее вследствие реципрокной транслокации, при которой часть хромосомы 9, содержащая онкоген c-abl, транслоцируется на хромосому 22 и соединяется с геном BCR. Объединенный ген кодирует белок BCR-ABL с активностью тирозинкиназы (ТК). В результате происходит гиперпродукция гранулоцитов – главным образом, в костном мозге, а также в экстрамедуллярных очагах (селезенка, печень). Нормальные стволовые клетки сохраняются и могут активизироваться после медикаментозной супрессии опухолевого клона.
Малые молекулы ингибиторов TK (ИТК) произвели революцию в лечении ХМЛ. У пациентов, у которых достигается ответ на терапию ИТК, продолжительность жизни стала сопоставима с таковой в популяции без ХМЛ.
ИТК радикально изменили естественное течение ХМЛ и многих других видов рака, но в некоторых случаях их использование может приводить к развитию кардиоваскулярных и/или метаболических осложнений.
TK принимают участие в эукариотической клеточной передаче сигналов, и нарушение их регуляции связано с многими типами рака, включая ХМЛ. ТК также играют важную роль в функционировании сердечно-сосудистой системы, включая сосудистые, метаболические и миокардиальные физиологические процессы. Поэтому закономерно, что ингибирование определенных ТК может нарушать работу сердечно-сосудистой системы и вызывать клинические осложнения.
На сегодняшний день достигнут значительный прогресс в выявлении повышенного риска возникновения сердечно-сосудистых событий (ССС), связанных с воздействием ИТК у пациентов с ХМЛ. Однако следует отметить, что механизмы развития осложнений до конца не изучены, а стратегии их профилактики и лечения нуждаются в дальнейшей разработке. Тем не менее, врачи имеют достаточно инструментов для профилактики, своевременного выявления и вмешательств с целью коррекции кардиоваскулярных осложнений.
В настоящем обзоре представлены современные данные, касающиеся профилей безопасности ИТК BCR-ABL по влиянию на сердечно-сосудистую систему, предложены стратегии ведения пациентов, оценка факторов риска сердечно-сосудистых осложнений и их модификация во время лечения пациентов с ХМЛ.
Факторы риска ССС у больных ХМЛ
Эпидемиологические исследования и анализ регистров, проведенные в последние годы, внесли существенный вклад в знания о важности факторов риска (ФР), помогли разработать методы оценки и прогнозирования индивидуального риска ССС. Риск развития ишемической болезни сердца, заболеваний периферических артерий, инсульта и сердечно-сосудистой смерти может быть оценен с учетом совокупности традиционных ФР: дислипидемия, артериальная гипертензия, курение, возраст, пол, этническая принадлежность, ожирение, семейный анамнез и отсутствие физической активности. Важное значение имеют также «нетрадиционные» факторы, в частности факторы атеротромботического риска, такие как аномалии воспаления или тромбоза.
Существующие на сегодня данные свидетельствуют о том, что комбинация ФР со стороны сердечно-сосудистой системы и кардиальных побочных эффектов ИTK может способствовать возникновению ССС у больных ХМЛ. Тот факт, что ССС более распространены у пациентов с ХМЛ, у которых уже есть ФР, подтверждает это мнение. Кроме того, в Украине большинство пациентов с ХМЛ относятся к старшей возрастной группе, а риск развития ССС с возрастом существенно повышается (рис. 1).
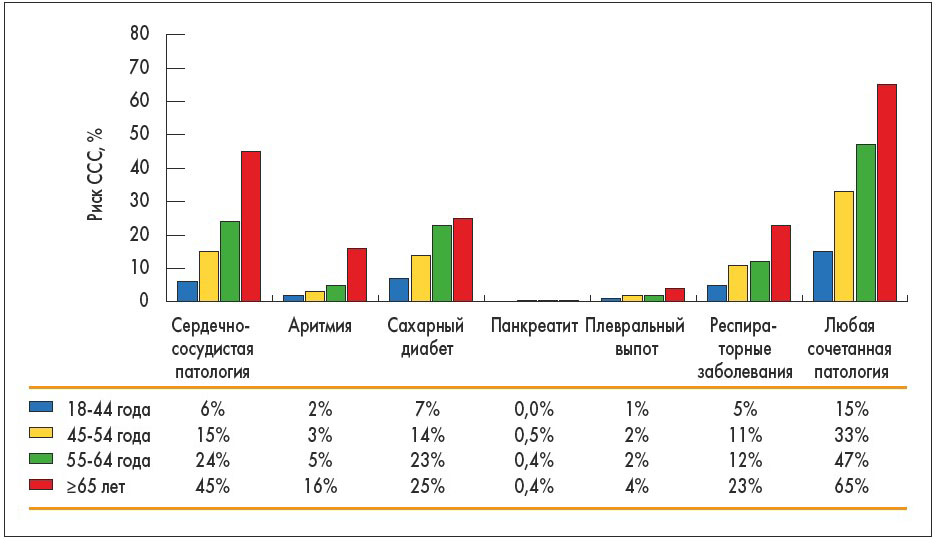 Рис. 1. Риск наступления ССС у пациентов разных возрастных групп (адаптировано по Jabbour E. et al. Clin Lymphoma Myeloma Leuk. 2015; 15(12): 797-802)
Рис. 1. Риск наступления ССС у пациентов разных возрастных групп (адаптировано по Jabbour E. et al. Clin Lymphoma Myeloma Leuk. 2015; 15(12): 797-802)
Ингибиторы BCR-ABL
Первым ИTK для лечения больных ХМЛ был иматиниб. Препарат кардинально изменил подходы к лечению этого заболевания. С разработкой и одобрением препаратов второго поколения (2G), таких как дазатиниб, нилотиниб и бозутиниб, клиническая эффективность терапии существенно повысилась.
Хотя все ИTK, одобренные для лечения ХМЛ, обладают активностью против BCR‑ABL1, они различаются по степени активности и влиянию на другие киназы, включая вовлеченные в физиологические процессы сердечно-сосудистой системы. Это может объяснить причину разнообразия кардиотоксических эффектов разных ИТК. Следовательно, профили безопасности относительно сердечно-сосудистой системы у каждого ИTK должны рассматриваться отдельно.
Иматиниб
Иматиниб – ингибитор тромбоцитарного фактора роста (PDGFR), ABL1 и ТК. Был одобрен для лечения ХМЛ в 2001 г. В 2006 г. появилось первое сообщение о серии случаев кардиотоксичности иматиниба как в клинической практике, так и в экспериментальных исследованиях. Тем не менее, проспективные клинические исследования (КИ), проводимые с участием большого количества пациентов в течение длительного времени, не показали повышенного риска развития ССС и кардиотоксичности. В частности, результаты 11-летнего наблюдения пациентов, принимавших иматиниб в исследовании IRIS (международное рандомизированное исследование по изучению применения интерферона и STI571), показали, что ССС были редкими. Ретроспективный анализ 6 исследований по использованию иматиниба, включивший данные 2327 пациентов со средней длительностью лечения 2,4 года, показал, что сердечная недостаточность (СН) регистрировалась всего в 0,2% случаев.
В другом исследовании с участием 103 пациентов с ХМЛ при использовании иматиниба в среднем в течение 28 мес не выявлено существенных различий в фракции выброса левого желудочка у пациентов, принимавших иматиниб, и в контрольной группе (68 (65-74) против 69% (64-73); р=0,67). В еще одном исследовании у 59 больных ХМЛ после лечения иматинибом средней продолжительностью 3,4±1,8 года не обнаружено признаков дисфункции миокарда с помощью эхокардиографии (ЭхоКГ), за исключением пациентов с заболеванием сердца в анамнезе. На основании имеющихся данных можно заключить, что иматиниб практически не оказывает негативного влияния на функцию сердца.
Однако, поскольку прием препарата в отдельных случаях вызывает задержку жидкости (гидроторакс, гидроперикард, асцит, отеки), рекомендуется уменьшение дозы до максимально переносимой, применение диуретиков и оценка систолической функции левого желудочка с помощью ЭхоКГ.
Нилотиниб
Несмотря на обнадеживающие результаты применения иматиниба при ХМЛ, почти у 20% пациентов не достигается полный цитогенетический ответ, а в ряде случаев со временем возникали непереносимые побочные явления или лекарственная устойчивость. Нилотиниб является препаратом с большей эффективностью и селективностью в отношении BCR‑ABL, чем иматиниб. Нилотиниб был одобрен и успешно используется у пациентов с ХМЛ.
Первое сообщение относительно сосудистой токсичности нилотиниба было опубликовано в 2011 г.: извещалось о 3 случаях заболеваний периферических артерий (ЗПА) у пациентов, принимавших нилотиниб. Согласно ретроспективному анализу данных 179 пациентов, у 11 (6,2%) пациентов развился периферический атеросклероз с вовлечением нижних конечностей, 8 больных нуждались в инвазивной терапии (ангиопластика и стентирование), а 4 пациентам потребовалась ампутация.
В рандомизированном исследовании ENESTnd через 5 лет наблюдения была выявлена более высокая частота кардиоваскулярных осложнений у больных, применявших нилотиниб, по сравнению с иматинибом. В данном исследовании было показано, что терапия нилотинибом ассоциируется с повышенным риском развития ССС, предикторами которых могут быть сердечно-сосудистые ФР в анамнезе. Применение иматиниба связано с более низкой частотой кардиоваскулярных осложнений, ему предписывают потенциальный кардиозащитный эффект. Согласно ретроспективному анализу исследований IRIS, TOPS и ENESTnd, выявлена более низкая частота развития ЗПА у пациентов, получавших иматиниб, чем у получавших нилотиниб.
По данным электрокардиографии (ЭКГ), выполняемой во время I фазы КИ по использованию нилотиниба, отмечалось удлинение интервала QTс на 5-15 мс. Однако в ходе исследования ENESTnd ни у одного пациента не зафиксировано удлинение интервала QTс >500 мс. При длительном наблюдении также не было зарегистрировано угрожающих жизни аритмий сердца.
Тем не менее, существуют следующие рекомендации по применению нилотиниба:
- если QTc >480 мс и присутствуют электролитные нарушения, необходимо провести коррекцию содержания электролитов (калия и магния) и отменить прием сопутствующих препаратов, которые могут удлинять QT;
- если QTc >480 мс и концентрация сывороточных электролитов в пределах нормы, можно начать лечение, а через 7 дней провести ЭКГ и повторно оценить уровень сывороточных электролитов.
По истечении этого времени:
- если QTc >480 мс, рекомендуется прекратить лечение;
- если QTc уменьшился до <450 мс, возобновить прием препарата в предыдущей дозе;
- если QTc в пределах 450-480 мс, снизить дозу до 400 мг 1 раз в день;
- если интервал QTc >480 мс после уменьшения дозы до 400 мг 1 раз в день, лечение необходимо прекратить.
ЭКГ следует проводить примерно каждые 7 дней после любой коррекции дозы нилотиниба, необходимо избегать применения ингибиторов CYP3A4, также способствующих удлинению интервала QT.
До начала терапии нилотинибом всем пациентам показано определение концентрации калия и магния в сыворотке крови, при нарушении этих показателей необходимо провести коррекцию. Принципы ведения пациентов с удлинением интервала QT представлены на рисунке 2.
При применении нилотиниба отмечалось повышение содержания в крови уровня глюкозы и холестерина. Это может составлять основу механизма повышения риска ССС у пациентов, принимающих нилотиниб. Поэтому рекомендуется определять уровень глюкозы и холестерина до лечения и мониторировать в процессе лечения.
Подводя итог, следует отметить, что применение нилотиниба может представлять потенциальный риск у пациентов с ХМЛ и сочетанной сердечно-сосудистой патологией. Учет ФР ССС, контроль ЭКГ, а также уровня глюкозы и холестерина крови могут способствовать предотвращению возможного неблагоприятного влияния нилотиниба на сердечно-сосудистую систему больного ХМЛ.
Дазатиниб
Дазатиниб угнетает многие устойчивые к иматинибу формы BCR-ABL и обладает в 325 раз большей эффективностью, чем иматиниб, при ингибировании BCR-ABL. Он также подавляет некоторые другие киназы, включая семейство Src.
Самой распространенной побочной реакцией/побочным явлением (ПР/ПЯ), связанной с приемом дазатиниба, является плевральный выпот, который выявляют у 28% пациентов. Механизм плеврального выпота недостаточно ясен, но этиологически он не связан с сердечно-сосудистой патологией. На основании сообщений о высоком количестве лимфоцитов в плевральной жидкости предполагается, что это осложнение может быть иммуноопосредованным.
В 2012 г. по данным Французского регистра легочной гипертензии сообщалось о 9 случаях развития легочной артериальной гипертензии (ЛАГ), связанных с использованием дазатиниба. Клинические, функциональные и гемодинамические улучшения наблюдались после прекращения приема дазатиниба. На основании данных регистра было подсчитано, что ЛАГ развивается, по меньшей мере у 0,45% лиц, которые длительно принимают дазатиниб. В 7-летнем исследовании по применению дазатиниба у 670 больных ХМЛ с резистентностью к иматинибу или его непереносимостью зафиксировано развитие ЛАГ у <3% пациентов.
Дазатиниб также может удлинять интервал QT. Принципы мониторинга и дозирования препарата при удлинении интервала QT аналогичны таковым при применении нилотиниба (рис. 2).
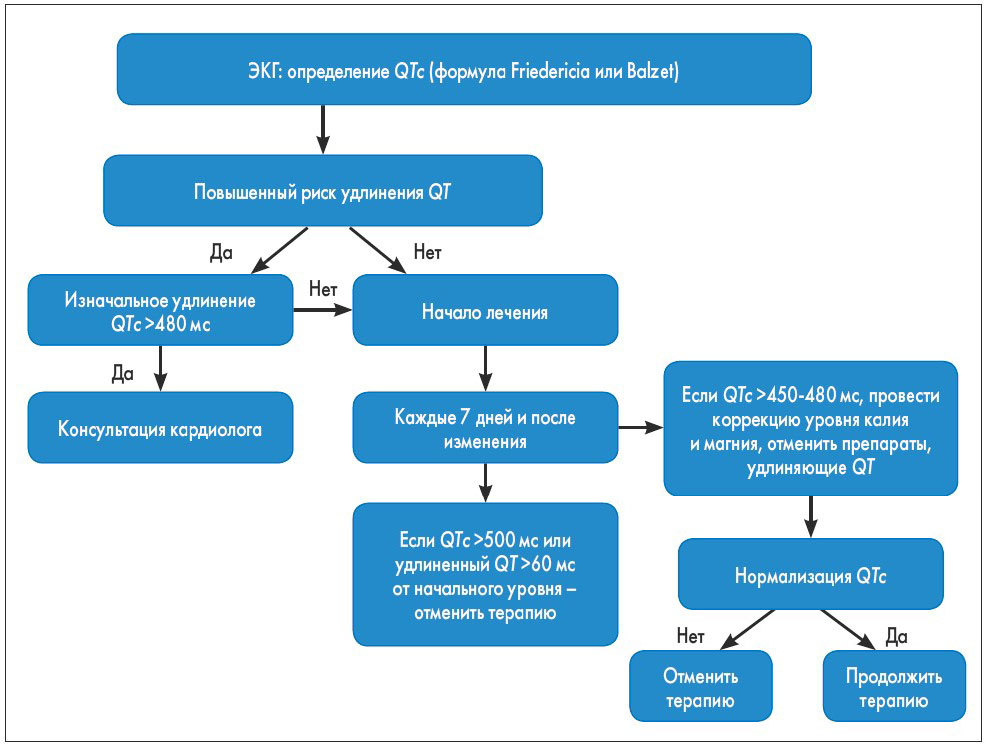 Рис. 2. Схема оценки риска и ведения пациентов с удлинением интервала QTc
Рис. 2. Схема оценки риска и ведения пациентов с удлинением интервала QTc
Бозутиниб
Бозутиниб является двойным (Src и ABL) 2G ИTK с минимальной активностью в отношении PDGFR или c-KIT. В проспективных КИ препарат продемонстрировал эффективность в качестве второй и третьей линии терапии у больных ХМЛ с резистентностью к другим ИTK или их непереносимостью. В ретроспективном анализе 2 крупных КИ по использованию бозутиниба не выявлено значимых различий в общей частоте ССС между группами бозутиниба и иматиниба. Частота ССС во время длительной терапии бозутинибом в качестве первой (исследование III фазы), второй и третьей линии (исследование I/II фазы) была относительно низкой. Следует отметить, что пациенты с ССС, принимавшие бозутиниб, получали сопутствующие препараты без необходимости прекращения или прерывания лечения по поводу ХМЛ.
В отличие от нилотиниба, побочные явления при приеме бозутиниба в основном связаны с желудочно-кишечным трактом и включают диарею, тошноту, рвоту и т.д.
Оценка кардиоваскулярного риска и скрининг
ССС атеросклеротического генеза достаточно распространены в общей популяции пациентов с ХМЛ. Для идентификации риска у пациентов, у которых может развиться ССС в течение определенного периода, используют разные модели, например Фремингемскую модель 10-летнего риска ССС. Разработан ряд моделей многомерного риска (табл.) для оценки риска возникновения ССС у здоровых лиц без симптомов. Необходимо отметить, что некоторые из этих моделей риска не учитывают такие тяжелые сердечно-сосудистые заболевания, как инсульт, СН или развитие симптоматических ЗПА.
В последнее время все эти модели риска использовали для прогнозирования ССС у пациентов с ХМЛ, получающих нилотиниб. Важно отметить, что кардиоваскулярные конечные точки, выбранные для этих исследований, весьма отличались от того, что можно было бы прогнозировать при помощи модели риска SCORE. Шкала риска SCORE, по сути, оценивает риск наступления сердечно-сосудистой смерти, а риск нефатальных событий не может быть спрогнозирован. В результате эти модели риска не были должным образом протестированы у больных ХМЛ. Поэтому перед началом лечения пациентов такими ИTK, как нилотиниб, рекомендуется провести скрининг на наличие симптоматической ишемической болезни сердца, ЗПА или CH. Если ССС в анамнезе отсутствуют, то применение шкал оценки риска для пациентов с ХМЛ может помочь онкологам в стратификации риска перед началом лечения ИTK (рис. 3). Выбор наиболее подходящей модели оценки риска зависит от исследуемой группы и ожидаемых результатов (табл.). Общий риск развития ССС должен быть установлен для каждого пациента, и модифицируемые ФР должны быть откорректированы согласно рекомендациям. У пациентов с повышенным риском развития ЗПА следует выполнить мультифакторную оценку наличия симптомов, связанных с физической нагрузкой на ногу, включая хромоту или другие нарушения ходьбы, ишемическую боль в покое и незаживающие раны. Для таких пациентов до начала терапии ИTK необходимо измерить лодыжечно-плечевой индекс (ЛПИ).
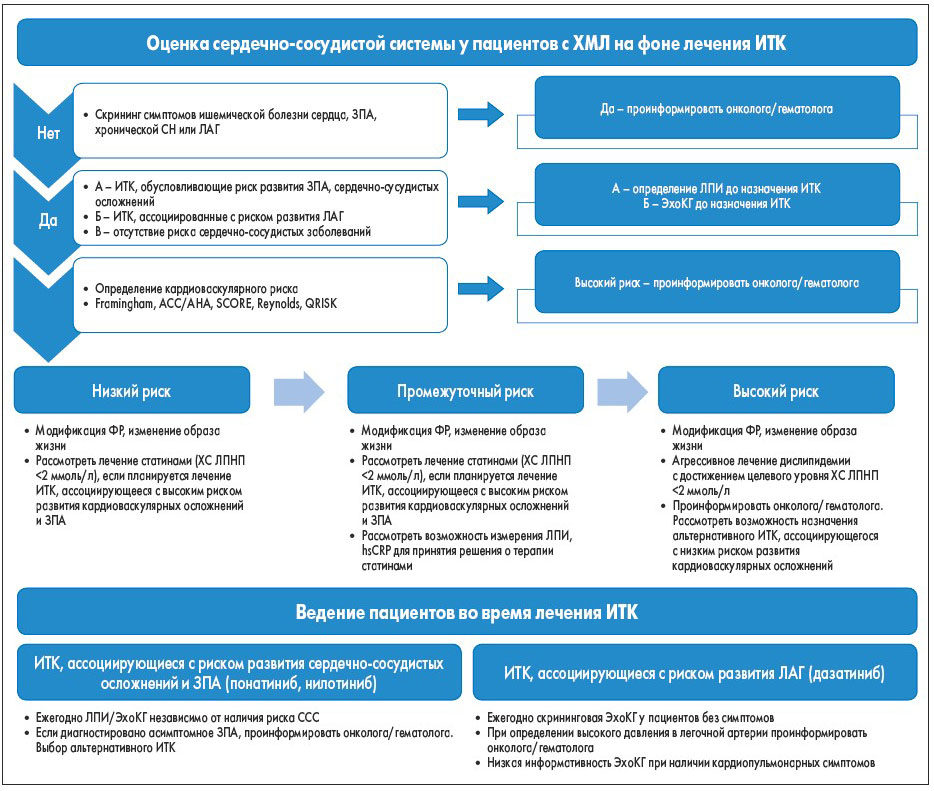 Рис. 3. Оценка функции сердечно-сосудистой системы и ведение больных ХМЛ, принимающих ИТК. ХС ЛПНП – холестерин липопротеидов низкой плотности; hsCRP – high-sensitivity C-reactive protein
Рис. 3. Оценка функции сердечно-сосудистой системы и ведение больных ХМЛ, принимающих ИТК. ХС ЛПНП – холестерин липопротеидов низкой плотности; hsCRP – high-sensitivity C-reactive protein
ЛПИ – это тест, который используется для диагностики ЗПА. Для этого измеряют артериальное давление (АД) на плече и лодыжке. Математическое отношение этих двух значений и составляет показатель ЛПИ:
ЛПИ = АД (на уровне лодыжки)/АД (на уровне плеча)
Отношение от 0,90 до 1,30 считается нормой для взрослых, показатели менее 0,8 свидетельствуют о наличии ЗПА. Более низкие показатели (<0,7) позволяют предположить высокую степень тяжести ЗПА.
В новом руководстве по лечению ЗПА в общей популяции рекомендуется (класс IIa) рутинное определение ЛПИ для пациентов с повышенным риском развития ЗПА: 1 – возраст ≥65 лет; 2 – возраст 50‑64 года и наличие ФР развития атеросклероза; 3 – возраст <50 лет и наличие сахарного диабета, а также 1 дополнительного ФР; 4 – пациенты с атеросклеротическим заболеванием в другом сосудистом русле. Эти рекомендации также могут быть применены к пациентам с ХМЛ для комплексной оценки риска наступления ССС перед началом терапии ИTK.
Как сказано выше, у пациентов, которым назначают дазатиниб, повышается риск развития ЛАГ. У таких пациентов следует тщательно изучать анамнез и проводить клиническую оценку на предмет изначального наличия высокого давления в легочной артерии, например у лиц с заболеваниями легких или тромбоэмболией легочной артерии в анамнезе, патологией соединительной ткани и врожденными пороками сердца. ЭхоКГ с доплеровским исследованием обеспечивает неинвазивную оценку давления в легочной артерии перед приемом дазатиниба.
Целесообразно выполнять ЭКГ перед началом терапии ИTK, поскольку прием всех их может быть связан с удлинением QT. Электролитные нарушения следует откорректировать и избегать одновременного приема лекарственных средств, которые удлиняют QT.
Профилактика кардиоваскулярных осложнений
Ключевым элементом в профилактике ССС в целом является модификация ФР ССС. Для пациентов с ХМЛ характерна высокая распространенность как ранее существовавших, так и вновь приобретенных ФР сердечно-сосудистых осложнений. Однако среди больных ХМЛ общий сердечно-сосудистый риск не может быть сопряжен исключительно с соответствующими ФР, так как лечение ИТК также может увеличить вероятность развития ССС.
Ингибиторы киназы BCR-ABL воздействуют также на другие киназы, отличные от мишени, что может привести к нецелевой кардиоваскулярной токсичности. Она может представлять собой комбинацию побочных эффектов ИTK как на мишени, так и за их пределами. Однако при использовании одного и того же ИTK у разных пациентов существует вариабельность сердечно-сосудистой токсичности. Это говорит о том, что сердечно-сосудистая токсичность ИTK может быть результатом совокупного влияния ФР ССС, генетической предрасположенности и определенных мишеней, на которые воздействуют ИTK.
Профилактика ССС у больных ХМЛ является важной составляющей ведения таких пациентов. От нее может зависеть эффективность терапии, полнота ее проведения и как результат – полное излечение. Поэтому у всех пациентов перед началом терапии следует индивидуализированно оценивать риск наступления возможных ССС. В случае повышенного риска необходимо принять меры по агрессивному управлению модифицируемыми сердечно-сосудистыми ФР. При использовании скрининговых моделей риска следует руководствоваться принципом, что даже у пациентов с низким риском необходимо управлять ФР и откорректировать образ жизни.
Некоторые ИTK, такие как нилотиниб, могут повышать риск возникновения ССС у пациентов с ХМЛ, и это продемонстрировано в ряде КИ. Поскольку нет специфических рекомендаций по профилактике ССС у больных ХМЛ, нужно руководствоваться общими принципами: поддерживать уровень липидов в пределах нормы, нормализовать массу тела, обеспечивать контроль АД, сахарного диабета, отказаться от курения и злоупотребления алкоголем.
Наблюдение и терапевтические стратегии
У пациентов с ХМЛ и ФР, предрасполагающими к развитию ССС, которые длительно принимают ИTK, точная частота возникновения таких осложнений неизвестна. В настоящее время невозможно провести разграничение между ССС, вызванными применением лекарственного средства и возникающими в результате воздействия ФР. Точная патофизиология сосудистых событий также остается неясной.
Для выявления кардиотоксичности был изучен потенциал сердечных биомаркеров, таких как BNP, NT-proBNP и тропонинов. В настоящее время определение этих биомаркеров дает возможность идентифицировать пациентов, подвергающихся риску возникновения сердечно-сосудистых осложнений. Одышка, усталость, периферические отеки и плевральный выпот могут быть ПР/ПЯ лечения ИТК, а также и симптомами СН. Например, плевральный выпот является распространенным побочным эффектом, обусловленным приемом дазатиниба, а задержка жидкости – иматиниба. Учитывая общие симптомы и признаки как у пациентов с ХМЛ, которые получают ИТК, так и у пациентов с СН, вполне можно предположить, что натрийуретические пептиды имеют клиническое значение при скрининге, и исключать СН как причину этих симптомов и признаков.
Относительно пациентов, которые получают нилотиниб, сегодня существует экспертное мнение изначально определять ЛПИ и мониторировать данный показатель в процессе лечения. Эксперты European LeukemiaNet рекомендуют проводить мониторинг ЛПИ (или дуплексное ультразвуковое исследование) каждые 6-12 мес у пациентов, применяющих нилотиниб. ЭхоКГ рекомендована пациентам, которые получают дазатиниб, для мониторинга ЛAГ. Сегодня продолжаются исследования для уточнения интервалов проведения ЭхоКГ. Пациентам, которые получают дазатиниб, Европейское общество кардиологов рекомендует выполнять ЭхоКГ каждые 3 мес; оптимальные интервалы между исследованиями также уточняются.
В настоящее время тактика ведения пациентов, у которых развиваются сердечно-сосудистые осложнения при приеме ИTK, предусматривает изменение плана лечения: прерывание терапии, снижение дозы или использование альтернативных ИTK. Раннее распознавание осложнений и соответствующее вмешательство по их коррекции может дать возможность большему количеству пациентов получить пользу от долгосрочного лечения ИТК. Это еще раз подчеркивает важность в клинической практике первичной профилактики, которая поможет предотвратить сердечно-сосудистые осложнения и даст возможность продолжать терапию до полного излечения.
В стратегии лечения необходимо учитывать лекарственные взаимодействия между ИTK и некоторыми кардиологическими препаратами. ИTK BCR-ABL являются ингибиторами CYP3A4 и могут повышать концентрации препаратов, метаболизируемых этим ферментом, в плазме крови, например дилтиазема, верапамила, симвастатина и аторвастатина. Эти лекарственные средства могут повышать концентрацию в плазме крови иматиниба, дазатиниба и нилотиниба путем ингибирования P-гликопротеина. Правастатин, розувастатин, атенолол, рамиприл, кандесартан, фуросемид и гидрохлортиазид не имеют негативного взаимодействия с иматинибом и нилотинибом и могут безопасно использоваться одновременно с этими ИTK.
Дазатиниб может вызывать ЛАГ – редкое заболевание вследствие прогрессирующего ремоделирования дистальных легочных артерий. Однако повышение давления в легочной артерии является распространенным явлением и может быть вызвано разными причинами, такими как заболевания левых отделов сердца, легких и хронические тромбоэмболические заболевания. ЛАГ характеризуется повышением легочного сосудистого сопротивления и давления в легочной артерии, что в конечном итоге может стать причиной правожелудочковой недостаточности. Дазатиниб может вызывать прекапиллярную ЛАГ, что связано с первичным повышением давления в системе легочной артерии. Пациентов с предполагаемым наличием ЛАГ вследствие приема дазатиниба следует направить к кардиологу для подтверждения ЛАГ, оценки состояния, а также выявления/исключения других потенциальных причин увеличения давления в легочной артерии. Обследование с целью оценки степени увеличения давления в легочной артерии следует начинать с выполнения ЭхоКГ, хотя для окончательного диагноза ЛАГ требуется выполнение катетеризации правых отделов сердца, а в случае подтверждения дазатиниб-индуцированной ЛАГ прием препарата следует отменить.
Лечение по поводу индуцированного дазатинибом плеврального выпота включает временное прерывание его приема, снижение дозы или полное прекращение применения препарата. В этом случае можно использовать диуретики и кортикостероиды. Большинство пациентов, принимающих дазатиниб, у которых развилась ЛАГ, имели сопутствующий плевральный выпот. Поэтому у пациентов с возникшим плевральным выпотом необходимо выполнять ЭхоКГ для оценки наличия ЛАГ.
Разработаны рекомендации по мониторингу функции сердечно-сосудистой системы у пациентов, получающих лечение ИTK. Основными рекомендуемыми вмешательствами являются агрессивное управление модифицируемыми ФР и мониторинг функции сердечно-сосудистой системы во время лечения с учетом профиля ПР/ПЯ конкретного ИTK. Клиницистам рекомендуется тщательно собирать анамнез (а именно – о наличии сердечно-сосудистых ФР, перенесенных ССС) и учитывать прием сопутствующих лекарственных средств, которые могут взаимодействовать с ИTK. Следует выбирать те ИТК, которые не будут утяжелять сопутствующие заболевания. Однако если необходимо выбрать ИТК с заведомо известным риском возникновения ПР/ПЯ, контроль над сопутствующим заболеванием может снизить риск развития осложнений.
Выводы
Сочетание кумулятивных сердечно-сосудистых эффектов ИTK (нилотиниб) и ФР ССС у пациентов с ХМЛ в ряде случаев приводит к возникновению ПР/ПЯ. Оценка профиля сердечно-сосудистой безопасности различных ИTK перед началом лечения является важной задачей. Понимание механизмов кардиоваскулярной токсичности имеет решающее значение для обоснования профилактических стратегий. Учитывая повышенный риск ССС у больных ХМЛ и осложнения, с которыми эти пациенты сталкиваются, тщательная стратификация сердечно-сосудистого риска и наблюдение в динамике должны быть неотъемлемой частью их ведения.
Список литературы находится в редакции.
Статья опубликована при поддержке компании Pfizer.
PP-BOS-UKR‑0016
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 5 (61), 2019 р.