18 березня, 2020
Ефективність і переносимість лейпрореліну ацетату (Елігард) у рутинній практиці у Німеччині
Узагальнені дані двох проспективних неінтервенційних досліджень із застосуванням депо-форм препарату для введення 1 раз на 3 або 6 місяців у пацієнтів із поширеним раком передміхурової залози
У Німеччині рак передміхурової залози є найпоширенішим типом раку у чоловіків. Так, у 2016 р. виявлено 66 900 нових випадків цієї пухлини [1]. Рак передміхурової залози також є третьою за частотою причиною смерті від раку у чоловіків [1]. Оскільки рак передміхурової залози є андрогензалежним новоутворенням [2-4], андрогенна депривація (АД), спрямована на зниження сироваткового рівня тестостерону, протягом кількох десятиліть є стандартним методом лікування поширених гормоночутливих пухлин, а також рекомендується у випадках резистентності до кастрації [5, 6].
АД все частіше використовується у пацієнтів з більш ранніми стадіями захворювання та осіб із повторним підвищенням рівня простатичного специфічного антигену (ПСА) після радикальної простатектомії чи променевої терапії. АД можна призначати як монотерапію або як складову мультимодального підходу [5, 6].
Досягти АД можна шляхом застосування агоністів лютеотропін-рилізинг-гормону (ЛРГ) тривалої дії на кшталт лейпрореліну ацетату (ЛА), бусереліну ацетату, гозереліну ацетату чи триптореліну ацетату [5, 6]. Ці синтетичні аналоги ЛРГ стимулюють відповідні рецептори у гіпофізі, індукуючи секрецію лютеїнізувального та фолікулостимулювального гормонів. Останні, у свою чергу, стимулюють вироблення тестостерону яєчками, що на початку лікування може призводити до минущого зростання рівня цього гормону. Тривалий вплив агоністів ЛРГ запускає механізм негативного зворотного зв’язку, що призводить до зниження відповіді рецепторів ЛРГ та зменшення виділення лютеїнізувального та фолікулостимулювального гормонів, і, відповідно, зумовлює зниження секреції тестостерону. Впродовж 2-4 тиж лікування у більшості пацієнтів досягається рівень тестостерону, що відповідає посткастраційному (традиційно визначається як <50 нг/дл, хоча останнім часом пропонуються показники <20 нг/дл), тобто після двобічної орхіектомії [5, 6].
Раніше лікування агоністами ЛРГ передбачало щоденні підшкірні ін’єкції, однак сьогодні наявні депо-форми, дія яких триває упродовж 1, 2, 3, 4, 6 та 12 міс. Елігард («Астеллас Фарма», Німеччина) є депо-формою, що містить діючу речовину ЛА та біодеградувальну полімерну матрицю (систему доставки Atrigel®).
Оскільки дані клінічних досліджень обмежені суворими критеріями включення та виключення, існує потреба в отриманні інформації з щоденної клінічної практики. Тому автори цього аналізу узагальнили дані двох неінтервенційних досліджень, проведених з метою оцінювання ефективності та переносимості депо-форм ЛА для застосування через 3 та 6 міс, у гетерогенній популяції пацієнтів. Загалом у включених до цього аналізу дослідженнях взяли участь 1906 пацієнтів, що робить цей аналіз найбільш масштабним із проведених у рутинній клінічній практиці на даний момент.
Матеріали та методи
У цьому огляді представлено узагальнені дані двох проспективних відкритих неінтервенційних досліджень ЛА, проведених у Німеччині з січня 2007 р. по грудень 2009 р. У цих дослідженнях пацієнти протягом 12 міс отримували лікування депо-формами ЛА із введенням через 3 міс (n=633) або 6 міс (n=1273). У дослідження були включені дорослі пацієнти (віком від 18 років) із поширеним гормоночутливим раком передміхурової залози, яким була показана АД. Критеріїв виключення та обмежень за часом після встановлення діагнозу, ступенем чи стадією розвитку пухлини не було. Пацієнти отримували депо-форми ЛА (Елігард) у дозі 22,5 мг (введення 1 раз на 3 міс) або 45 мг (1 раз на 6 міс). Спостереження тривало 12 міс.
Як первинна кінцева точка розглядався рівень сироваткового ПСА через 12 міс лікування. Цей показник визначали на початку дослідження та через кожні 3 міс (у пацієнтів, що отримували ЛА у дозі 22,5 мг) чи 6 міс (45 мг) протягом 12 міс.
Результати
Були проаналізовані дані 1906 пацієнтів. Медіана віку склала 75 років, медіана часу після встановлення діагнозу – 11,2 міс. Метастази у кістках були у 8% учасників, інші віддалені метастази – у 1,3%, метастази у лімфатичних вузлах – у 2%. У 58,5% учасників діагностували коморбідні стани, у більшості випадків – кардіоваскулярні захворювання.
Попередньо гормональну терапію отримували 43,2% учасників дослідження. Клінічно значущих відмінностей між пацієнтами, що раніше не зазнавали АД, хворими, які вже лікувалися ЛА, та особами, що приймали інші агоністи ЛРГ, не зафіксовано.
Основним показанням до призначення депо-форм ЛА у цьому дослідженні був місцевопоширений рак передміхурової залози (42,1%), іншими – неможливість проведення радикальної простатектомії чи променевої терапії (28,2%), підвищення вмісту ПСА після радикальної простатектомії (13,5%) чи променевої терапії (8,1%), наявність віддалених метастазів (12,9%) або метастазів у лімфатичних вузлах (5,6%). У 58,4% пацієнтів ЛА призначали як монотерапію, 34,3% хворих отримували комбіноване лікування ЛА та антиандрогенним препаратом (бікалутамідом – 14,7%; флутамідом – 12,2%; ципротерону ацетатом – 4,7%; золедроновою кислотою – 8%) або хіміотерапевтичним агентом (естрамустином – 0,7%, доцетакселом – 0,4%).
12-місячний курс лікування не закінчили 129 (6,8%) пацієнтів, 28 з яких померли, 22 не з’явилися на контрольний візит, 15 відзначили недостатній терапевтичний ефект, а 4 припинили терапію у зв’язку з побічними ефектами. В інших випадках причини припинення лікування залишилися невідомими.
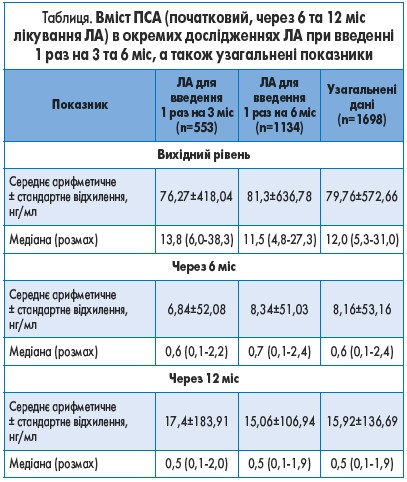 Таким чином, відомості про рівень ПСА у повному обсязі були отримані у 1698 пацієнтів. Упродовж періоду спостереження медіана сироваткового ПСА знизилася на 96% – з 12,0 до 0,5 нг/мл. Це зниження було зіставним у групах ЛА при введенні 1 раз на 3 та 6 міс (з 13,8 до 0,5 нг/мл та з 11,5 до 0,5 нг/мл відповідно; табл.). Аналіз зниження вмісту ПСА також не виявив залежності від попереднього лікування.
Таким чином, відомості про рівень ПСА у повному обсязі були отримані у 1698 пацієнтів. Упродовж періоду спостереження медіана сироваткового ПСА знизилася на 96% – з 12,0 до 0,5 нг/мл. Це зниження було зіставним у групах ЛА при введенні 1 раз на 3 та 6 міс (з 13,8 до 0,5 нг/мл та з 11,5 до 0,5 нг/мл відповідно; табл.). Аналіз зниження вмісту ПСА також не виявив залежності від попереднього лікування.
Побічні ефекти відзначали у 167 (8,8%) пацієнтів. Нетяжкі побічні ефекти розвинулися у 109 (5,7%) учасників; найчастішими з них були біль у місці ін’єкції (2,3%) та відчуття припливу жару (1,6%). Побічні ефекти були визнані лікарем як точно або імовірно пов’язані з лікуванням ЛА в 1,3% учасників. Тяжкі побічні реакції виявляли у 3,0% хворих. У пацієнтів із цими реакціями було зафіксовано 14 смертей, переважно пов’язаних з основним захворюванням та розвитком поліорганної недостатності. Кардіоваскулярні тяжкі побічні реакції включали цереброваскулярні події (n=6), серцеву недостатність (n=5), колапс (n=4) тощо. Однак достовірно пов’язаним із лікуванням ЛА було визнано лише один випадок тяжкої побічної реакції.
Обговорення
Це дослідження становить собою найбільший наявний на сьогодні аналіз ефективності та переносимості ЛА при раку передміхурової залози у рутинній клінічній практиці. Цей аналіз узагальнює дані двох неінтервенційних досліджень, що включали 1906 пацієнтів.
З часу виведення ЛА на фармацевтичний ринок було опубліковано результати трьох неінтервенційних досліджень, присвячених застосуванню агоністів ЛРГ у щоденній клінічній практиці: французького дослідження ELIRE (форми для введення через 3 та 6 міс) [11], бельгійського дослідження MANTA (введення через 1 та 3 міс) [12] та німецького неінтервенційного дослідження (введення через 6 міс) [10].
Результати зазначеного узагальненого аналізу продемонстрували істотне зниження медіани ПСА (на 96%) через 12 міс регулярного введення депо-форм ЛА 1 раз на 3 та 6 міс (табл.).
Тоді як клінічні дослідження демонструють ефективність і переносимість ліків у однорідних популяціях пацієнтів, що відповідають чітким критеріям включення та виключення, дослідження рутинної клінічної практики охоплюють набагато ширше коло хворих. Порівняно з учасниками ключових випробувань ЛА, популяція пацієнтів цього аналізу була значно більш гетерогенною і характеризувалася відмінностями у властивостях пухлин, показаннях до призначення ЛА, коморбідних станах. Така гетерогенність віддзеркалена також у верхній межі рівня ПСА у хворих, включених у це дослідження (0,02-17300 нг/мл), порівняно з базисними випробуваннями (форма для введення через 3 міс: 0,2-5270 нг/мл; через 6 міс: 0,19-2284 нг/мл) [7, 8].
На відміну від клінічних досліджень, значна кількість пацієнтів отримувала ЛА у поєднанні з антиандрогеном, бісфосфонатом чи хіміотерапевтичним препаратом. Також не було жодних обмежень стосовно попереднього проведення гормонотерапії, тоді як у клінічних дослідженнях вимагалося ≥3 міс перерви після попереднього лікування [7, 8]. До цього аналізу було включено хворих, яким виконували АД раніше або на момент початку дослідження. Нижчий початковий рівень ПСА у пацієнтів, які раніше отримували лікування, ніж у хворих, які ніколи не лікувалися, свідчить, що перерва між попередньою терапією та призначенням депо-форм ЛА була порівняно нетривалою.
Середні показники та медіана рівня ПСА у цьому аналізі різко відрізнялися, що зумовлено значною варіабельністю початкових даних. Оскільки у базисних дослідженнях депо-форм ЛА [7, 8] представлено середні значення, а у цьому аналізі – медіани, безпосередньо порівнювати отримані результати неможливо. Однак результати цього аналізу демонструють, що у більшості пацієнтів депо-форми ЛА для введення 1 раз на 3 та 6 міс здатні ефективно знижувати рівень ПСА незалежно від статусу попереднього лікування агоністами ЛРГ.
Побічні реакції у цьому дослідженні фіксували рідше, ніж у попередніх клінічних випробуваннях [7, 8]. Передусім була зареєстрована менша кількість припливів жару та реакцій у місці ін’єкції. Потенційними поясненнями цього факту можуть бути одночасне призначення антиандрогенів, які здатні знижувати частоту припливів [5, 6], приблизно у третині випадків; застосування інших гормоновмісних препаратів на початку лікування депо-формами ЛА; менша кількість повідомлень про подібні реакції, оскільки у рутинній клінічній практиці лікарі вважають такі прояви нормою.
У зв’язку з тим, що до цього аналізу було включено неінтервенційні дослідження, отримані дані не є такими всеохоплюючими, як результати рандомізованих контрольованих досліджень, однак аналіз застосування ЛА у широкій популяції пацієнтів може краще відображати ефекти цього препарату у щоденній клінічній практиці.
Висновки
У цьому дослідженні виявлено високу ефективність (за сироватковим рівнем ПСА) та хорошу переносимість депо-форм ЛА для введення через 3 та 6 міс у широкій популяції пацієнтів, у тому числі у хворих, що раніше не лікувалися, та пацієнтів, котрі раніше проходили терапію агоністами ЛРГ.
Список літератури знаходиться в редакції.
Ohlmann C. – H., Gross-Langenhoff M. Efficacy and Tolerability of Leuprorelin Acetate (Eligard®) in Daily Practice in Germany: Pooled Data from 2 Prospective, Non-Interventional Studies with 3- or 6-Month Depot Formulations in Patients with Advanced Prostate Cancer. Urol Int; DOI: 10.1159/000479187.
Переклала з англ. Лариса Стрільчук
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 5 (61), 2019 р.


